Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку Спирты
Содержание
- 1. Презентация к уроку Спирты
- 2. Цели урока: 1.Сформировать представление о классификации спиртов.
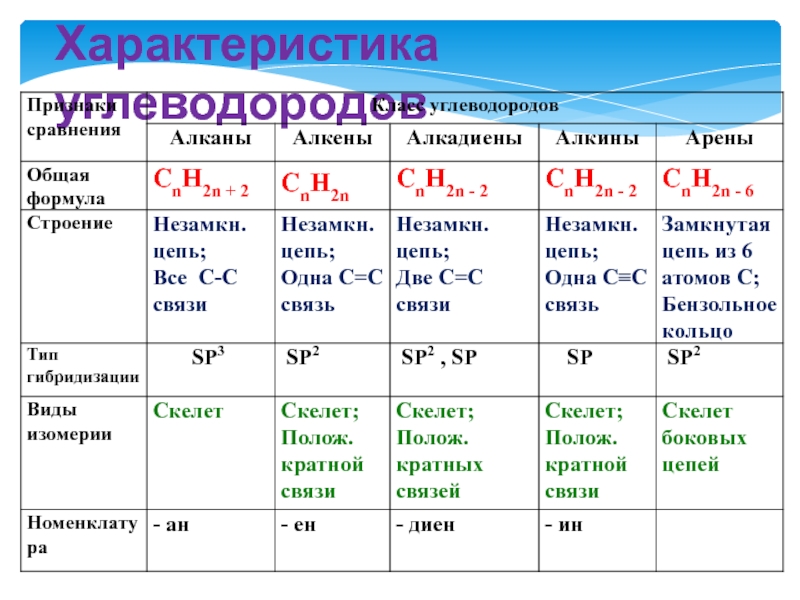
- 3. Характеристика углеводородов
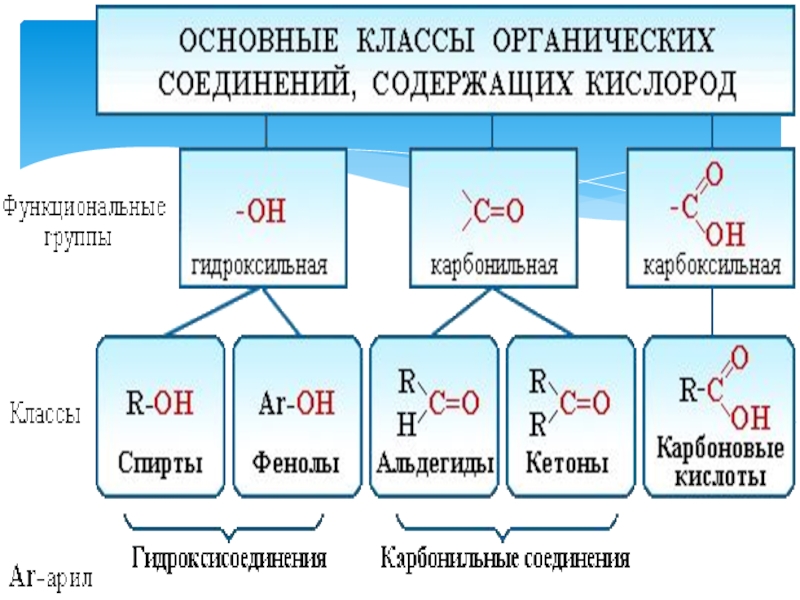
- 4. Слайд 4
- 5. Какие вещества называются спиртами?По каким признакам классифицируют
- 6. Исторические данные.
- 7. Спирты (алканолы) – это органические вещества,
- 8. По числу гидроксильных группОдноатомные (СН3-CH2-ОН)ДвухатомныеНО-СН2-СН2-ОНТрехатомные СН2-СН-СН2
- 9. По характеру атома углерода, с которым связана
- 10. 1.При образовании названия спиртов к названию углеводорода,
- 11. Слайд 11
- 12. Слайд 12
- 13. Виды изомерии спиртов-изомерия положения ОН- группы,
- 14. Получение.Общие способы:1) Взаимодействие галогеналканов с растворами щелочей:
- 15. Получение Частные способы.Метанол получают из синтез – газа.
- 16. Температура кипения спиртов выше температуры кипения соответствующих
- 17. R -
- 18. Этиловый спирт пагубно влияет на клетки головного мозга СПАСИБО ЗА УРОК
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1СПИРТЫ: состав, строение,
классификация, изомерия,
номенклатура, физические свойства.
СПИРТЫ: состав,
строение,
классификация, изомерия,
номенклатура.
Слайд 2Цели урока:
1.Сформировать представление о классификации спиртов. 2.Познакомиться с отдельными
представителями спиртов, их строение, физическими свойствами, номенклатурой, изомерией, рассмотреть влияние
спиртов на живые организмы.3.Рассмотреть влияние водородной связи на физические свойства спиртов
Слайд 5Какие вещества называются спиртами?
По каким признакам классифицируют спирты?
3. Какие виды
изомерии характерны для спиртов?
4. Номенклатура спиртов?
5. Физические свойства характерные для
спиртов?6. Где нашли применение спирты?
Основные вопросы урока
Слайд 7 Спирты (алканолы) – это органические вещества, в молекулах которых
алкильный радикал связан с гидроксильной группой. R – OH Группа -ОН обусловливает
свойства спиртов, поэтому данную группу атомов называют функциональной группойСлайд 8
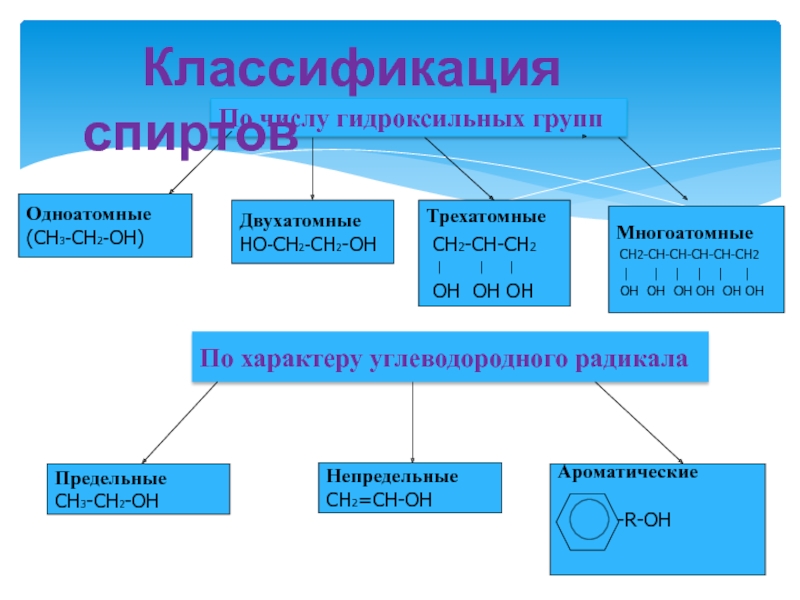
По числу гидроксильных групп
Одноатомные
(СН3-CH2-ОН)
Двухатомные
НО-СН2-СН2-ОН
Трехатомные
СН2-СН-СН2
|
| |
ОН ОН ОН
По характеру
углеводородного радикалаПредельные
СН3-СН2-ОН
Непредельные
СН2=СН-ОН
Ароматические
-СН2-О-R-OН
Классификация спиртов
Многоатомные
СН2-СН-СН-CH-CH-СН2
| | | | | |
ОН ОН ОН ОН OH OH
Слайд 9
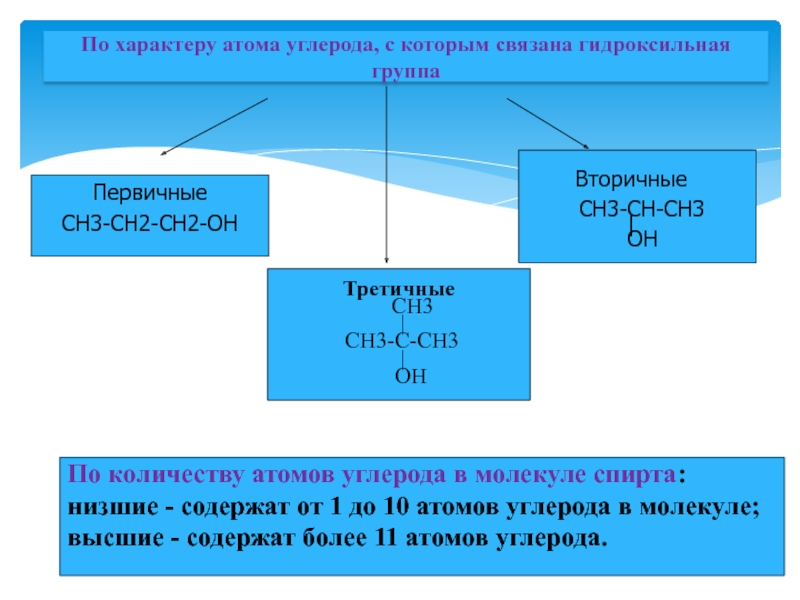
По характеру атома углерода, с которым связана гидроксильная группа
Первичные
СН3-СН2-СН2-ОН
Вторичные
СН3-СН-СН3
|ОН
Третичные
СН3
|
СН3-C-CН3
|
ОН
По количеству атомов углерода в молекуле спирта: низшие - содержат от 1 до 10 атомов углерода в молекуле; высшие - содержат более 11 атомов углерода.
Слайд 101.При образовании названия спиртов к названию углеводорода, соответствующего спирту, добавляют
суффикс – ОЛ.
2.Цифрами после суффикса указывают положение ОН- группы в
главной цепи, а префиксами ДИ-, ТРИ-, ТЕТРА- и т. д. – их число.Предельные одноатомные спирты
CnH2n+1OH – общая формула алканолов
Номенклатура спиртов
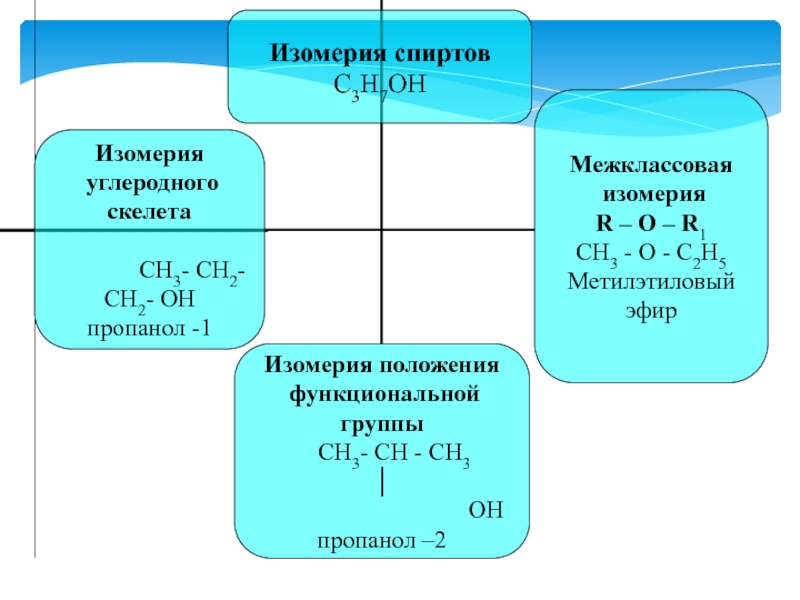
Слайд 13Виды изомерии спиртов
-изомерия положения ОН- группы, (начиная с С3)
CH3-CH2-CH2-OH
CH3-CHOH-CH3пропанол-1 и пропанол-2 ;
-углеродного скелета, (начиная с С4 );
CH3-CH2-CH2-CH2-OH бутанол-1
CH3-CH-CH2-OH 2-метилпропанол-1
|
CH3
-межклассовая изомерия с простыми эфирами, (начиная с С2 )
СН3-CH2–OH и CH3–O–CH3
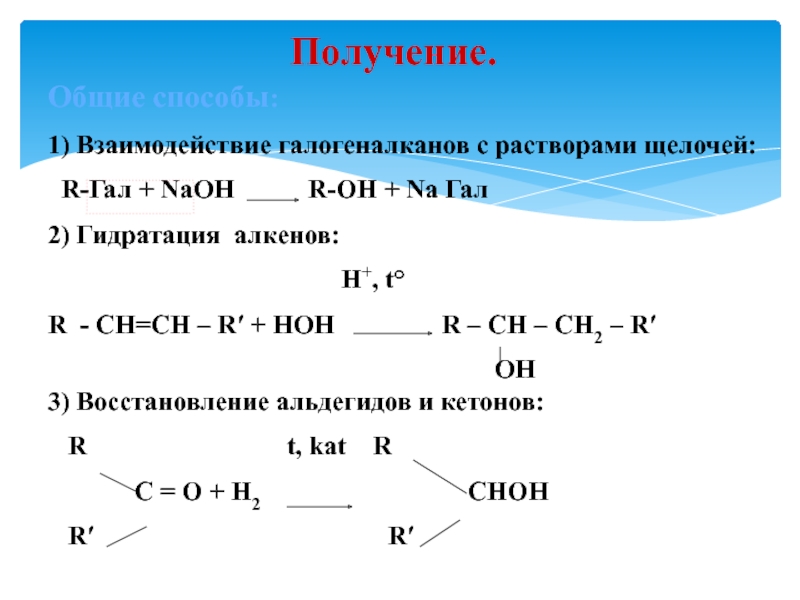
Слайд 14Получение.
Общие способы:
1) Взаимодействие галогеналканов с растворами щелочей:
R-Гал + NaOH
R-OH + Na Гал
2) Гидратация
алкенов:H+, t°
R - CH=CH – R′ + HOH R – CH – CH2 – R′
ОH 3) Восстановление альдегидов и кетонов:
R t, kat R
C = O + H2 CHOH
R′ R′
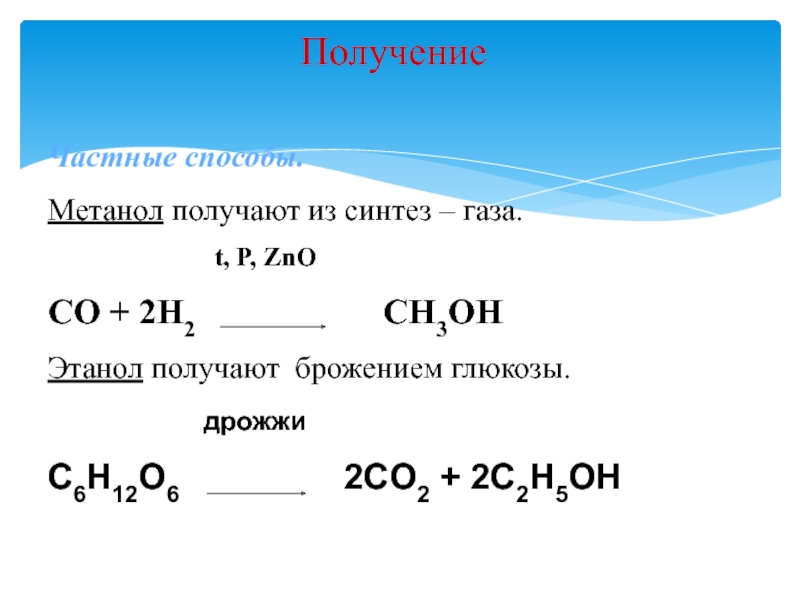
Слайд 15Получение
Частные способы.
Метанол получают из синтез – газа.
t,
P, ZnOCO + 2H2 CH3OH
Этанол получают брожением глюкозы.
дрожжи
C6H12O6 2CO2 + 2C2H5OH
Слайд 16Температура кипения спиртов выше температуры кипения соответствующих углеводородов.
Среди спиртов нет газов.
С увеличением относительной молекулярной
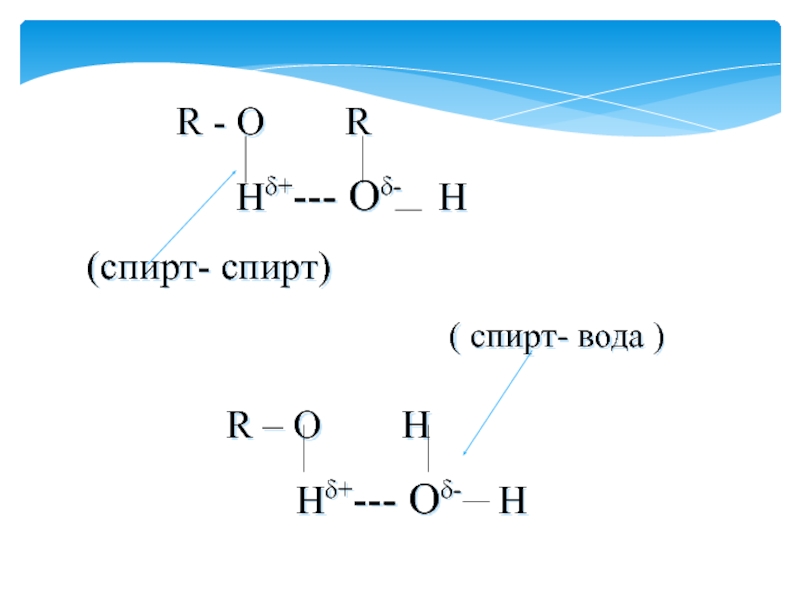
массы спиртов повышаются их температуры кипения, уменьшается растворимость в воде.Это объясняется наличием межмолекулярной водородной связи, которая может образовываться как между молекулами спиртов, так и между молекулами спиртов и воды.
Это влияет на физические свойства спиртов: повышает температуру кипения, снижает летучесть, способствует хорошей растворимости в воде, не позволяет перегонкой получить 100% спирт из его водного раствора.
Физические свойства.
Агрегатное состояние:
С1- С11- жидкости
С12 - С…- твердые вещества