Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация по химии "Основания" 8 класс
Содержание
- 1. Презентация по химии "Основания" 8 класс
- 2. Классы веществОснования – сложные вещества, состоящие из атомов металла и гидроксильных групп.Ме+n(ОН)nNaOHKOHCu(OH)2Назовите основные классынеорганических веществ
- 3. Ca(OH)2CuOHClNaHSO4Fe(OH)3HNO3LiOHNH4OHAl(NO3)3ОснованияОпределите основания
- 4. ОснованияЗапишите уравнения диссоциации веществ:NaOH
- 5. ОснованияПризнак классификациирастворимыенерастворимыесильныеслабыеоднокислотныедвухкислотныеКоличественно распад электролита на ионы определяется
- 6. Выберите указанные понятияЩелочиСлабые основанияОднокислотныеМолодецОшибкаМолодецМолодецМолодецОшибкаМолодецОшибкаМолодецОшибкаМолодецМолодецОшибкаМолодецОшибкаМолодецМолодецМолодецОшибкаОшибкаМолодецОшибкаМолодецОшибкаNaOHCsOHBa(OH)2Mg(OH)2LiOHCu(OH)2Ca(OH)2Ba(OH)2KOHFe(OH)3LiOHZn(OH)2NH4OHCsOHBe(OH)2Fe(OH)2KOHAl(OH)3Fe(OH)2Cr(OH)3RbOHNaOHSn(OH)2Pb(OH)2
- 7. Химические свойства оснований1.Основание + кислота = соль
- 8. Реакции ионного обменаCa(OH)2 + 2HNO3 = Ca(NO3)2
- 9. Реакции ионного обмена6KOH + P2O5 = 2K3PO4
- 10. Реакции ионного обмена2NaOH + CuSO4 = Na2SO4 + Cu(OH)22Na++2OH-+Cu2++SO42-=2Na++SO42-+Cu(OH)2Cu2+ +2OH- = Cu(OH)2Cu(OH)2 - нерастворимое вещество
- 11. Химические свойства основанийЗадание: выпишите номера клеток с
- 12. +CuSO4Na2SO4H2O+=H2SO4+H2O++=CuSO4+2NaOH=Cu(OH)2+Na2SO4 Cu(OH)2 CuO + H2OCuO
- 13. ЩелочьФ-ФКислотаЩелочьФенолфталеинКислотаОтветРеакция нейтрализацииЗадание: просмотрите опыт. Определите вещества, тип реакции.Опыт
- 14. LiOHKOHNaOHCa(OH)2Ba(OH)2Применение оснований
- 15. Гидроксид литияLiOH электролит в щелочных аккумуляторах; поглотитель углекислого газа в противогазах, подводных
- 16. KOHГидроксид калияВ качестве пищевой добавки (Е525) (изготовлении
- 17. производство бумаги, картона Производство мыла, шампуня.Для изготовления биодизельного топлива.Зарегистрирован в качестве
- 18. Для приготовления известкового строительного раствора. Известковая вода.
- 19. Ba(OH)2Гидроксид бария как реактив на SO42− и CO32− (сульфат- и карбонат-ионы);
- 20. 1.Тест включает в себя 10 вопросов.2. Для
- 21. Тест1.Нерастворимые в воде основания можно получить при
- 22. Интернет - ресурсыИзображение стаканаhttp://primelux.ru/published/publicdata/ALEXBOROVKPRLUX/attachments/SC/products_pictures/e375f117-f61e-11df-a398-0015174d425c_enl.jpgИзображение кристаллов гидроксида натрияhttp://kurs-on.ru/images1/57a79d2931c46.pngИзображение
- 23. Интернет - ресурсыИзображение аккумулятораhttp://electroshemi.ru/_nw/0/64666780.jpgИзображение керамической посудыhttp://www.ua.all.biz/img/ua/catalog/2388351.jpegИзображение космической
- 24. Интернет - ресурсыИзображение. Сахар.http://dachnaya-zhizn.ru/images/dacha/svekolnyiy-sahar1.jpegИзображение. Известь гашеная.http://sezon.com.ua/image/sredstva-zashchity-rasteniy/fungitsidy-dlya-zashchity-ot-bolezney/izvest-pushonka-184405mf.jpgИзображение. Растительные
- 25. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Основания
Химия 8 класс
Автор: Ширяева Екатерина Константиновна, учитель МБОУ «СОШ №31»
п. Восток Красноармейского муниципального района Приморского края
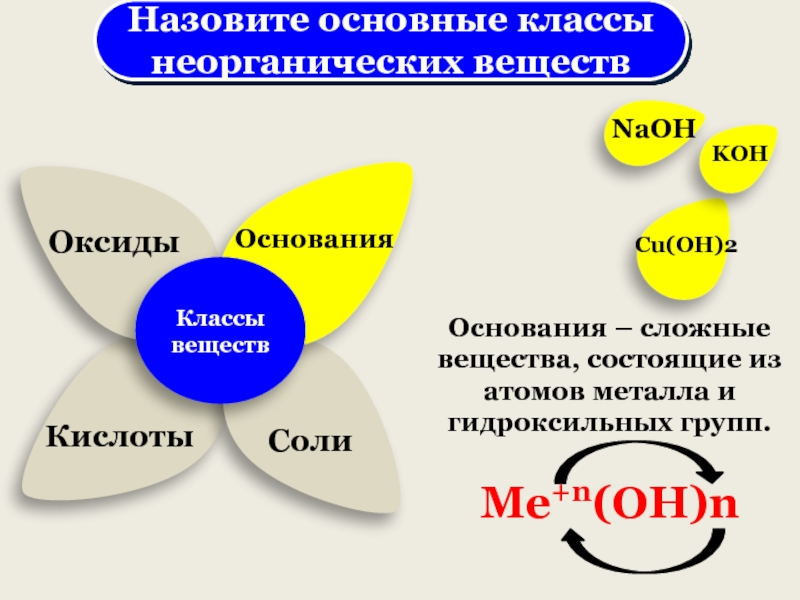
Слайд 2Классы веществ
Основания – сложные вещества, состоящие из атомов металла и
гидроксильных групп.
Ме+n(ОН)n
NaOH
KOH
Cu(OH)2
Назовите основные классы
неорганических веществ
Слайд 4Основания
Запишите уравнения диссоциации веществ:
NaOH
Ca(OH)2
LiOH
Ba(OH)2
Na+
OH-
+
Ca2+
2 OH-
Li+
OH-
Ba2+
2 OH-
+
+
+
Основаниями называют электролиты,
которые при диссоциации образуют
катионы металла и анионы гидроксогрупп ОН-
Слайд 5Основания
Признак классификации
растворимые
нерастворимые
сильные
слабые
однокислотные
двухкислотные
Количественно распад электролита на ионы
определяется степенью
диссоциации -
= . 100%
Сильные электролиты
1IА IIА
LiOH Ca(OH)2
NaOH Sr(OH)2
KOH Ba(OH)2
RbOH
CsOH
n
N
Слабые основания
0
1.Нерастворимые основания
2.Водный раствор аммиака
NH3 . H2O
Однокислотные Двухкислотные
LiOH Mg(OH)2
NaOH Sr(OH)2
KOH Ba(OH)2
RbOH Cu(OH)2
Слайд 6Выберите указанные понятия
Щелочи
Слабые основания
Однокислотные
Молодец
Ошибка
Молодец
Молодец
Молодец
Ошибка
Молодец
Ошибка
Молодец
Ошибка
Молодец
Молодец
Ошибка
Молодец
Ошибка
Молодец
Молодец
Молодец
Ошибка
Ошибка
Молодец
Ошибка
Молодец
Ошибка
NaOH
CsOH
Ba(OH)2
Mg(OH)2
LiOH
Cu(OH)2
Ca(OH)2
Ba(OH)2
KOH
Fe(OH)3
LiOH
Zn(OH)2
NH4OH
CsOH
Be(OH)2
Fe(OH)2
KOH
Al(OH)3
Fe(OH)2
Cr(OH)3
RbOH
NaOH
Sn(OH)2
Pb(OH)2
Слайд 7Химические свойства оснований
1.Основание + кислота = соль + вода
2.Щелочь+кислотный оксид=соль+вода
3.Щелочь
+ соль1 = основание + соль2
4.Основание оксид +
водаCa(OH)2 + HNO3
KOH + P2O5
NaOH + CuSO4
Fe(OH)3
2
6
2
2
t
РИО
РИО
РИО
Ca(NO3)2 + 2H2O
2 K3PO4 + 3H2O
Na2SO4 + Cu(OH)2
Fe2O3 + 3H2O
Слайд 8Реакции ионного обмена
Ca(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O
Ca2+ +2OH-
+2H+ +2NO3- =Ca2+ +2NO3- +2H2O
2OH- +2H+ =2H2O
H2O – малодиссоциирующее
веществоСлайд 9Реакции ионного обмена
6KOH + P2O5 = 2K3PO4 + 3H2O
6K++6OH- +
P2O5 = 6K+ + 2PO43- + 3H2O
6OH- + P2O5 =
2PO43- + 3H2O P2O5 - оксид
H2O - малодиссоциирующее вещество
Слайд 10Реакции ионного обмена
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2
2Na++2OH-+Cu2++SO42-=2Na++SO42-+Cu(OH)2
Cu2+ +2OH-
= Cu(OH)2
Cu(OH)2 - нерастворимое вещество
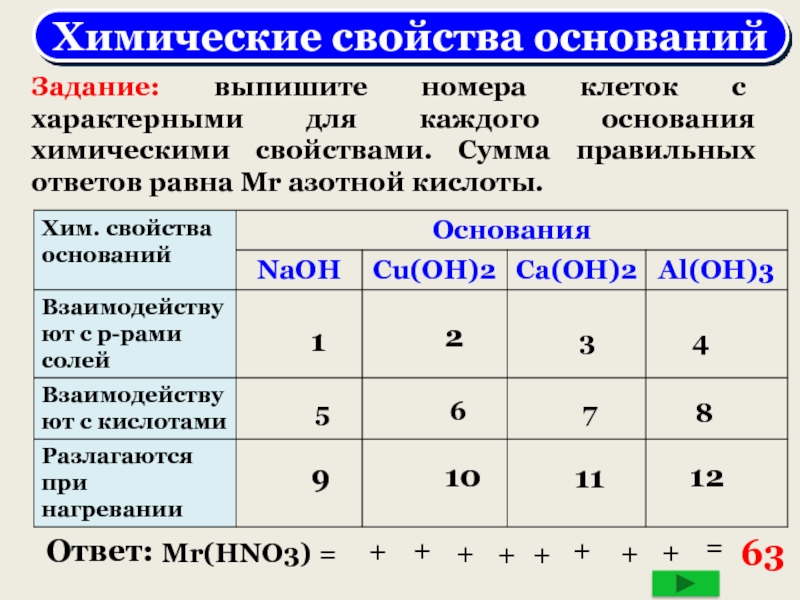
Слайд 11Химические свойства оснований
Задание: выпишите номера клеток с характерными для каждого
основания химическими свойствами. Сумма правильных ответов равна Мr азотной кислоты.
1
2
3
4
5
6
7
8
9
10
11
12
Ответ:
Мr(HNO3)
=+
+
+
+
+
+
+
+
=
63
Слайд 12+
CuSO4
Na2SO4
H2O
+
=
H2SO4
+
H2O
+
+
=
CuSO4+2NaOH=Cu(OH)2+Na2SO4
Cu(OH)2 CuO + H2O
CuO + H2SO4 =
CuSO4 + H2O
Ответ
Заполните пустые клетки формулами веществ,
расставляя необходимые коэффициенты,
чтобы получить уравнения реакций
Си(ОН)2
NaOH
CuO
CuSO4
Слайд 13Щелочь
Ф-Ф
Кислота
Щелочь
Фенолфталеин
Кислота
Ответ
Реакция
нейтрализации
Задание: просмотрите опыт.
Определите вещества, тип реакции.
Опыт
Слайд 15Гидроксид лития
LiOH
электролит в щелочных аккумуляторах;
поглотитель углекислого газа в противогазах, подводных лодках и космических
кораблях;
в стекольной и керамической промышленности.
Слайд 16KOH
Гидроксид калия
В качестве пищевой добавки (Е525) (изготовлении какао, шоколада).
Производство мыла
и шампуней, отбеливателей.
Электролит в щелочных батарейках.
В строительстве: для изготовления штукатурки,
гипсовых растворов, побелка.Для очистки сточных вод.
Слайд 17 производство бумаги, картона
Производство мыла, шампуня.
Для изготовления
биодизельного топлива.
Зарегистрирован в качестве
пищевой добавки E524.
В гражданской обороне - для
дегазации и нейтрализации
отравляющих веществ.
NaOH
Гидроксид натрия
Слайд 18Для приготовления известкового строительного раствора.
Известковая вода. Для обнаружения углекислого
газа.
Известковое молоко.
При производстве сахара и
приготовления смесей для борьбы с болезнями растений, побелки стволов.Гидроксид кальция
Ca(OH)2
Слайд 19Ba(OH)2
Гидроксид бария
как реактив на SO42− и CO32− (сульфат- и карбонат-ионы);
Для очистки растительных
масел и животных жиров;
в нефтеперерабатывающей промышленности для производства присадок к маслам;
в
производстве элементов питания постоянных источников тока.Слайд 20
1.Тест включает в себя 10 вопросов.
2. Для начала работы
перейдите к следующему слайду.
3.Выберите 1 правильный ответ из предложенных
вариантов и щелкните по нему. 4.При правильном ответе появляется ,
при неправильном – .
5.Для перехода к следующему вопросу используйте кнопку
6.По окончании работы подсчитайте количество набранных баллов.
Тест
Химические свойства оснований
Инструкция
Слайд 21Тест
1.Нерастворимые в воде основания можно получить при взаимодействии:
А) металла с
водой;
Б) оксида металла с водой;
В) растворимой в воде соли данного
металла с щелочью.2.Какое из нижеприведенных свойств характерно только для нерастворимых в воде оснований:
А) взаимодействие с кислотами;
Б) взаимодействие с солями;
В) разложение при нагревании.
3.Взаимодействие между кислотными и основными оксидами относится к реакции:
А) соединения;
Б) замещения;
В) обмена.
4.При какой реакции образуется нерастворимое основание:
А) металла с водой;
Б) любого основного оксида с водой;
В) щелочи с растворимой в воде солью.
5.Реакцией нейтрализации называется реакция:
А) кислоты с основным оксидом;
Б) кислоты с растворимым основанием;
В) кислотного оксида с основным оксидом.
6.Какой тип химической реакции не характерен для оснований:
А) реакция разложения;
Б) реакция замещения;
В) реакция обмена.
7.Гидроксид кальция реагирует с
А) оксидом бария;
Б) хлоридом калия;
В) соляной кислотой;
Г) гидроксидом натрия.
8.В реакцию с раствором гидроксида натрия вступает каждое из двух веществ:
А) CuO и Ba(OH)2;
Б) P2O5 и H2SO4;
В) H2S и Cu;
Г) HCl и H2.
9.В результате разложения гидроксида меди(II) образуются:
А) CuO и H2;
Б) Cu и H2O;
В) CuOH и H2;
Г) CuO и H2O.
10.С гидроксидом калия не реагирует:
А) HNO3;
Б) Cu2O;
В) CO2;
Г) H2S.
Подсчитайте количество правильных ответов
0 - 5 баллов – оценка «2»
6 - 7 баллов – оценка «3»
8 - 9 баллов – оценка «4»
10 баллов – оценка «5»
Слайд 22Интернет - ресурсы
Изображение стакана
http://primelux.ru/published/publicdata/ALEXBOROVKPRLUX/attachments/SC/products_pictures/e375f117-f61e-11df-a398-0015174d425c_enl.jpg
Изображение кристаллов гидроксида натрия
http://kurs-on.ru/images1/57a79d2931c46.png
Изображение кристаллов гидроксида калия
http://d13z1xw8270sfc.cloudfront.net/origin/309891/1414136183955_koh.jpg
Изображение
кристаллов гидроксида кальция
http://images.ua.prom.st/327640990_w640_h640_gidroksid_kaltsiya.jpg
Изображение кристаллов гидроксида меди
http://chemistry-chemists.com/N8_2013/P1/Schweizer's_reagent-5.jpg
Изображение кристаллов гидроксида железа
http://polpoz.ru/umot/klassi-neorganicheskih-veshestv-diblenko-s-yu/36.jpg
Изображение пипетки
http://www.web-shpargalka.ru/icons/medical/48.png
Изображение
склянкиhttps://pcgroup.ru/files/products/Sklajanka_temnaja_uzkoe_gorlo_3.175x200.jpg?08fd64603cd1b42f5c6566d79a721e07
Слайд 23Интернет - ресурсы
Изображение аккумулятора
http://electroshemi.ru/_nw/0/64666780.jpg
Изображение керамической посуды
http://www.ua.all.biz/img/ua/catalog/2388351.jpeg
Изображение космической станции
http://politikus.ru/uploads/posts/2015-02/1424813990_655180285.jpg
Изображение очистки сточных
вод
http://kanalizacia-pro.ru/wp-content/uploads/2014/07/22.jpg
Изображение отбеливателей
http://www.kanztrend.ru/img/catalogue/products/080916143416.1.jpg
http://www.kazanopttorg.ru/img/small/627242.jpg
Изображение плитки шоколада
http://s57.radikal.ru/i155/1102/9d/0af36a711ae7.jpg
Изображение щелочной батарейки
http://www.instrument-43.ru/published/publicdata/DEEMERDS3DB26/attachments/SC/products_pictures/SV-59018.jpg
Изображение .Производство бумаги.
http://printbusiness.su/wp-content/uploads/2012/02/paper.jpg
Изображение завода
биодизельного топливаhttp://www.avtika.ru/uploads/news/610/3a3402e14ba74ffeed96f68336ec2064.jpg
Графические объекты (слайды 14,2,5)
http://mypresentation.ru/presentation/2051_prezentaciya_804