Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Растворы
Содержание
- 1. Растворы
- 2. Растворы – это гомогенные (однородные) системы, состоящие
- 3. Растворы подразделяются:Молекулярные – водные растворы неэлектролитов
- 4. Растворение – физико – химический процесс, в
- 5. Растворимость – свойство вещества растворяться в воде
- 6. Влияние различных факторов на растворимость. Растворимость Температура Давление Природа растворенных веществПрирода растворителя
- 7. Концентрация раствора – это содержание вещества в определенной массе или объеме раствора.
- 8. Выражение концентраций растворов. Массовая доля растворенного вещества
- 9. Выражение концентраций растворов. Молярность - число молей
- 10. Выражение концентраций растворов.Эквивалентная концентрация (нормальность) –
- 11. Выражение концентраций растворов.Моляльная концентрация (моляльность) – число молей растворенного вещества на 1000 г растворителя.
- 12. Природные растворы.Минеральная вода.Кровь животных.Морская вода.
- 13. Практическое применение растворов.Продукты питания.Лекарственные препараты.Минеральные столовые воды.Сырье промышленности.Биологическое значение растворов.
- 14. http://tdtka.ru/wpcontent/uploads/2012/10/aneclab_banky.jpghttp://www.chemicalnew.com/images/main.jpghttps://encryptedtbn3.gstatic.com/images?q=tbn:ANd9GcTgTDZ65NpmSQPa3OSKckFCyY9nXOZDwdz6cToSB0BYlKEeridtgwhttp://polnota.3dn.ru/Kartinki2/ximia.jpghttp://images.ua.prom.st/23326677_w200_h200_chemistry17070901.jpghttp://associationplus.kz/ru/wpcontent/themes/association/images/pic1.jpghttp://images.myshared.ru/408824/slide_2.jpghttp://www.provisor.com.ua/archive/2008/N02/img/vitro_208r2.jpghttp://3.bp.blogspot.com/-lZSv3fbm0Y8/Tws3W8giKBI/AAAAAAAAABM/u2J7b3Ywkag/s758/a3584d36.jpghttp://vsuet.ru/school-y-chemist/dictionary/8.jpghttp://www.syl.ru/misc/i/ai/179232/706080.jpghttp://www.syl.ru/misc/i/ai/66594/62790.jpgМатериалы, используемые для оформления
- 15. Информация для педагога.Ресурс предназначен для учащихся 11
- 16. Скачать презентанцию
Растворы – это гомогенные (однородные) системы, состоящие из двух и более компонентов и продуктов их взаимодействия.Точное определение раствора ( 1887 год Д.И.Менделеев):Раствор – гомогенная (однородная) система, состоящая из частиц растворенного вещества,
Слайды и текст этой презентации
Слайд 2Растворы – это гомогенные (однородные) системы, состоящие из двух и
более компонентов и продуктов их взаимодействия.
Точное определение раствора ( 1887
год Д.И.Менделеев):Раствор – гомогенная (однородная) система, состоящая из
частиц растворенного
вещества, растворителя
и продуктов
их взаимодействия.
Справочник.
Справочник.
Слайд 3
Растворы подразделяются:
Молекулярные – водные растворы неэлектролитов
(
спиртовой раствор иода, раствор глюкозы).
Молекулярно-ионные – растворы слабых электролитов (
азотистая и угольная кислоты, аммиачная вода).Ионные растворы –
растворы
электролитов.
Справочник.
Слайд 4
Растворение –
физико – химический процесс, в котором наряду с
образованием обычной механической смеси веществ идет процесс взаимодействия частиц растворенного
вещества с растворителем.Справочник.
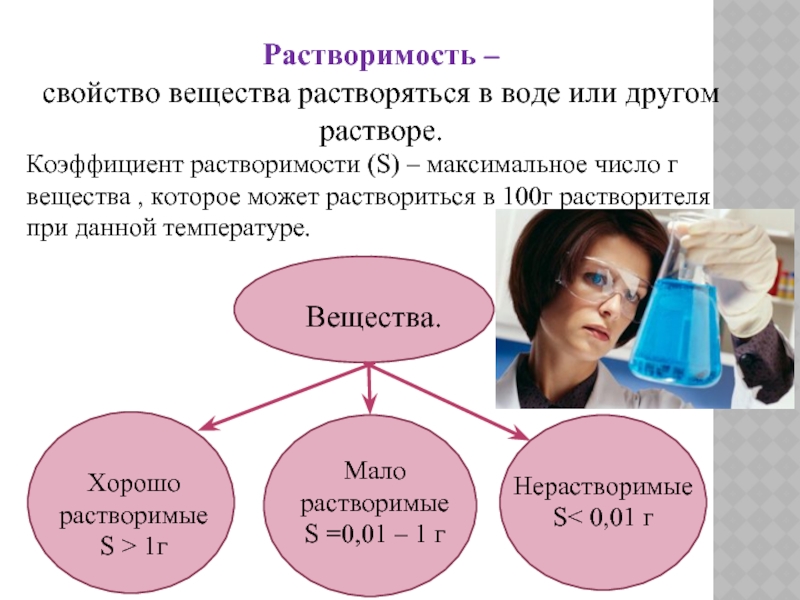
Слайд 5Растворимость –
свойство вещества растворяться в воде или другом растворе.
Коэффициент
растворимости (S) – максимальное число г вещества , которое может
раствориться в 100г растворителя при данной температуре.
Хорошо растворимые
S > 1г
Мало растворимые
S =0,01 – 1 г
Вещества.
Нерастворимые
S< 0,01 г
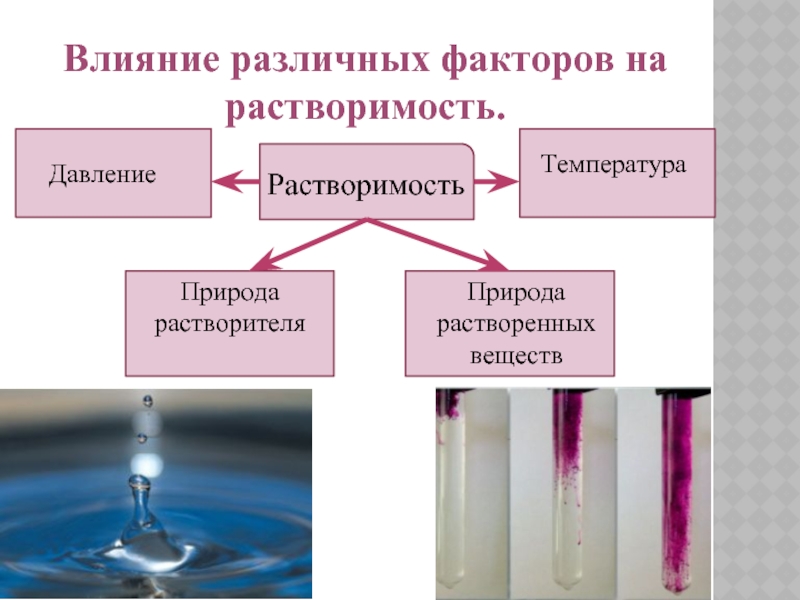
Слайд 6Влияние различных факторов на растворимость.
Растворимость
Температура
Давление
Природа
растворенных веществ
Природа растворителя
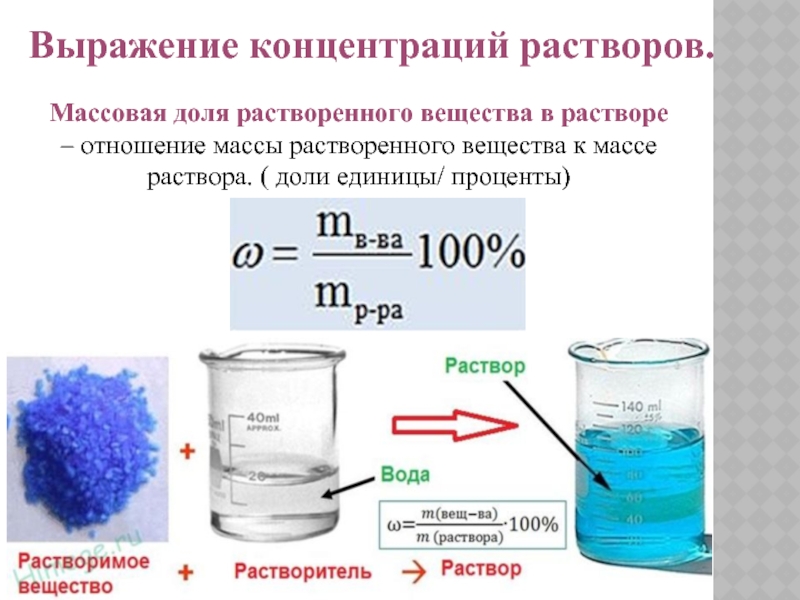
Слайд 8Выражение концентраций растворов.
Массовая доля растворенного вещества в растворе –
отношение массы растворенного вещества к массе раствора. ( доли единицы/
проценты)Слайд 9Выражение концентраций растворов.
Молярность - число молей растворенного вещества в
1 л раствора.
ʋ - количество вещества (моль);
V –
объем раствора (л);Слайд 10 Выражение концентраций растворов.
Эквивалентная концентрация (нормальность) – число эквивалентов растворенного
вещества в 1л раствора.
ʋ экв. - количество эквивалентов;
V – объём
раствора, л.Слайд 11Выражение концентраций растворов.
Моляльная концентрация (моляльность) – число молей растворенного вещества
на 1000 г растворителя.
Слайд 13Практическое применение растворов.
Продукты питания.
Лекарственные препараты.
Минеральные столовые воды.
Сырье промышленности.
Биологическое значение растворов.
Слайд 14
http://tdtka.ru/wpcontent/uploads/2012/10/aneclab_banky.jpg
http://www.chemicalnew.com/images/main.jpg
https://encryptedtbn3.gstatic.com/images?q=tbn:ANd9GcTgTDZ65NpmSQPa3OSKckFCyY9nXOZDwdz6cToSB0BYlKEeridtgw
http://polnota.3dn.ru/Kartinki2/ximia.jpg
http://images.ua.prom.st/23326677_w200_h200_chemistry17070901.jpg
http://associationplus.kz/ru/wpcontent/themes/association/images/pic1.jpg
http://images.myshared.ru/408824/slide_2.jpg
http://www.provisor.com.ua/archive/2008/N02/img/vitro_208r2.jpg
http://3.bp.blogspot.com/-lZSv3fbm0Y8/Tws3W8giKBI/AAAAAAAAABM/u2J7b3Ywkag/s758/a3584d36.jpg
http://vsuet.ru/school-y-chemist/dictionary/8.jpg
http://www.syl.ru/misc/i/ai/179232/706080.jpg
http://www.syl.ru/misc/i/ai/66594/62790.jpg
Материалы, используемые для оформления
Слайд 15Информация для педагога.
Ресурс предназначен для учащихся 11 класса. Является иллюстрацией
при освоении темы «Растворы. Количественные характеристики растворов».
В презентации рассматриваются основные
понятия темы, формулы количественных выражений концентраций растворов.Материал может быть
фрагментарно использован на
уроках химии в 8 – 9 классах.
Ресурс рассчитан на
использование УМК
О.С.Габриеляна.