Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Решение задач с использованием понятия «доля»
Содержание
- 1. Решение задач с использованием понятия «доля»
- 2. Задачи из вариантов ЕГЭОпределите массу воды, которую
- 3. Задачи из вариантов ЕГЭКусок сплава меди с
- 4. Доля Доля - обыкновенная дробь,
- 5. ПроцентыПроцент – одна сотая часть чего-либо.Перевод доли в проценты:0,5560,6340,762Перевод процентов в доли :34%45,89%23,6%
- 6. Растворы Растворы – однородные смеси двух или большего числа веществ (компонентов).
- 7. Бесцветное вещество, без вкуса и запаха, плотность
- 8. Вода – хороший растворитель. В ней растворяются
- 9. СплавыСплавы – это системы из двух или
- 10. Сталь –
- 11. Слайд 11
- 12. Бронза – сплав меди и олова
- 13. Бронзовые предметы обихода
- 14. Дюралюминий – сплав алюминия с небольшими добавками меди, магния, марганца и кремния
- 15. Золото используется в сплавах, обычно с серебром или медью
- 16. Томпак – ”поддельное золото” – сплав меди и цинка, часто используемый для имитации золота
- 17. Латунь – сплав меди и цинка
- 18. Сплав Вуда (висмут, свинец, олово, кадмий) используется при пайке
- 19. Монель-металл (медно-никелевый сплав) используется для изготовления химического
- 20. ОловоПластинки из бронзыМедь
- 21. Теоретические основы решения задач
- 22. При решении задач о смесях, сплавах, растворах
- 23. Определения и обозначенияМассовая доля растворенного вещества в
- 24. Определения и обозначенияВведем обозначения:ω1(в-ва) - массовая доля
- 25. Слайд 25
- 26. С помощью расчетной формулыМасса полученного при смешивании
- 27. С помощью расчетной формулыТаким образом, массовая доля растворенного вещества вполученном растворе равна:
- 28. «Правило смешения»Исходя из формулы:
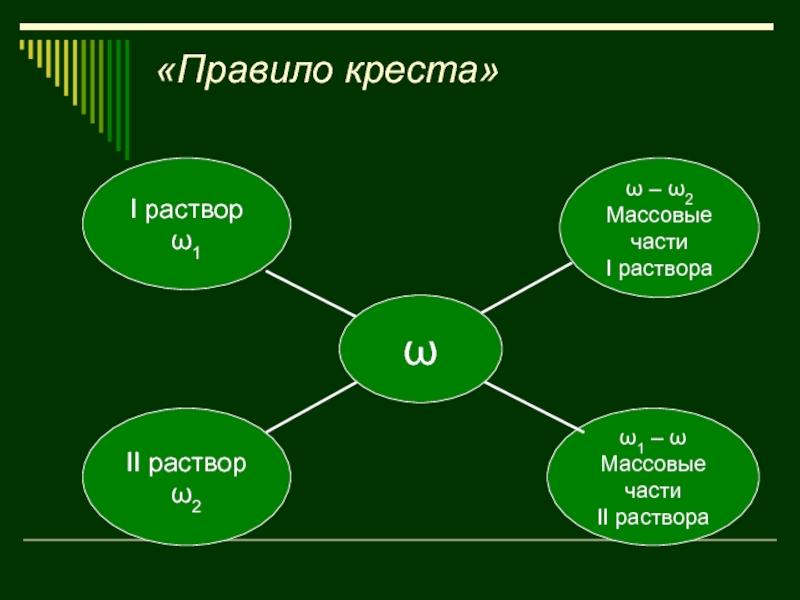
- 29. «Правило креста»
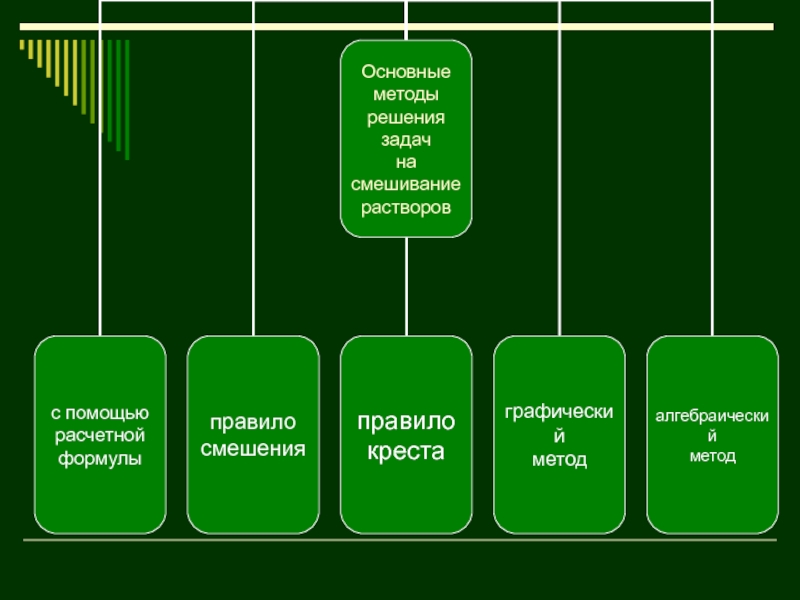
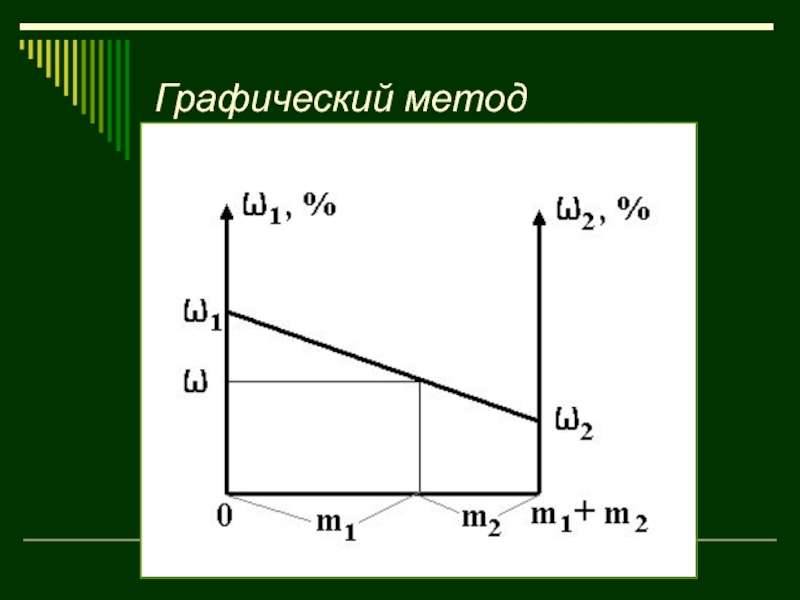
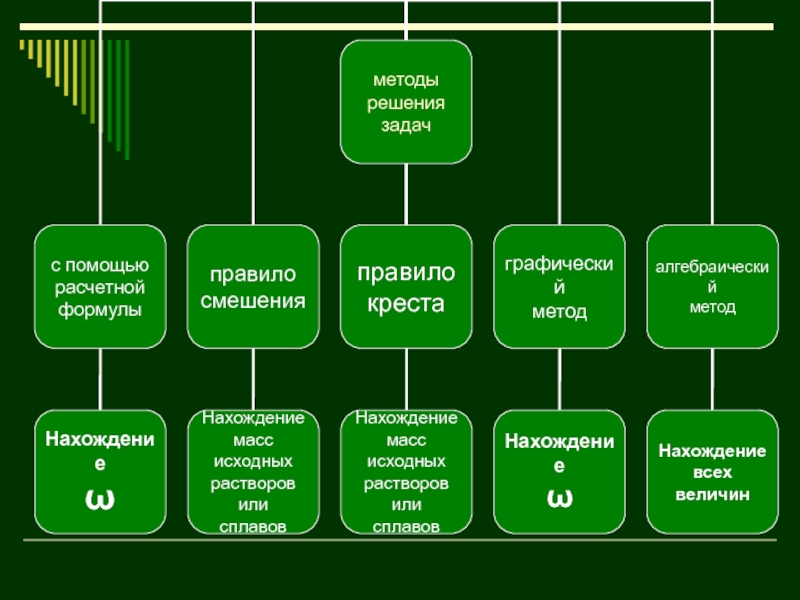
- 30. Грaфuческий метод
- 31. Алгебраический метод Задачи на смешивание
- 32. Слайд 32
- 33. Решение задач Приготовление растворов или сплавовВ воде
- 34. Решение задач Приготовление растворов или сплавовКакую массу
- 35. Решение задач Сложные процентыЗадача 1
- 36. Решение Алгебраический методm1(р-ра) = 100 гm2(р-ра) =
- 37. Решение С помощью расчетной формулыm1(р-ра) = 100
- 38. Решение Графический способm1(р-ра) = 100 гm2(р-ра) = 300 гω1(в-ва) = 0,2ω2(в-ва) = 0,1ω(в-ва) - ?Ответ: 12,5%
- 39. Решение задач Сложные процентыЗадача 2
- 40. Решение Алгебраический методω1(в-ва) = 0,1ω2(в-ва) = 0,25m(р-ра)
- 41. Решение Графический способω1(в-ва) = 0,1ω2(в-ва) = 0,25m(р-ра)
- 42. Решение «Правило смешения»ω1(в-ва) = 0,1ω2(в-ва) = 0,25m(р-ра)
- 43. Решение «Правило креста»ω1(в-ва) = 0,1ω2(в-ва) = 0,25m(р-ра)
- 44. Решение задач Сложные процентыК 300 г раствора,
- 45. «Правило креста»
- 46. Решение задач Сложные процентыИмеется сталь двух сортов
- 47. Решение Алгебраический методm1(сп-ва) = 20 кгω1(Ag) =
- 48. Решение «Правило смешения»m1(сп-ва) = 20 кгω1(Ag) =
- 49. Решение «Правило креста»m1(сп-ва) = 20 кгω1(Ag) =
- 50. Решение задач Сложные процентыИмеются два слитка сплава
- 51. Спасибо за работу!!!
- 52. Скачать презентанцию
Задачи из вариантов ЕГЭОпределите массу воды, которую надо добавить к 20 г раствора уксусной кислоты с массовой долей 70% для получения раствора уксуса с массовой долей 3%. Смешали 120 г раствора
Слайды и текст этой презентации
Слайд 1Решение задач с использованием понятия «доля»
Бинарный урок по химии и
алгебре и началам анализа
Слайд 2Задачи из вариантов ЕГЭ
Определите массу воды, которую надо добавить к
20 г раствора уксусной кислоты с массовой долей 70% для
получения раствора уксуса с массовой долей 3%.Смешали 120 г раствора серной кислоты с массовой долей 20% и 40 г 50%-ного раствора того же вещества. Массовая доля кислоты в Полученном растворе равна ________% .
Какая масса азотной кислоты содержится в 1 л ее 20%-ного раствора с плотностью 1,05 г/мл?
К 120 г раствора, содержащего 80% соли, добавили 480 г раствора, содержащего 20% той же соли. Сколько процентов соли содержится в получившемся растворе?
Слайд 3Задачи из вариантов ЕГЭ
Кусок сплава меди с оловом массой 15
кг содержит 20% меди. Сколько чистой меди необходимо добавить к
этому сплаву, чтобы новый сплав содержал 40% олова?Первый сплав меди содержит 70 г меди, а второй сплав - 210 г серебра и 90 г меди. Взяли 225 г первого сплава и кусок второго сплава, сплавили их и получили 300 г сплава, который содержит 82% серебра. Сколько граммов серебра содержалось в первом сплаве?
В каждую из нескольких пробирок налили по две щелочи. Первую щелочь наливали по 1,2 мл в каждую пробирку. Вторую щелочь наливали по такой схеме: 0,8 мл в первую пробирку, а в каждую следующую пробирку на 0,8 мл больше, чем в предыдущую. Всего разлили 56 мл щелочей. Сколько миллилитров щелочи налили в последнюю пробирку?
Первый сплав серебра и меди содержит 430 г серебра и 70 г меди, а второй сплав - 210 г серебра и какое-то количество меди. Сплавили кусок первого сплава с куском массой 75 г второго сплава и получили 300 г сплава, который содержит 82% серебра. Определите массу (в граммах) второго сплава.
Слайд 4Доля
Доля - обыкновенная дробь, числитель которой равен
единице.
доля – дробь (прикладные науки)
ω = 0,4Слайд 5Проценты
Процент – одна сотая часть чего-либо.
Перевод доли в проценты:
0,556
0,634
0,762
Перевод процентов
в доли :
34%
45,89%
23,6%
Слайд 7Бесцветное вещество, без вкуса и запаха, плотность 1 г/см3, температура
кипения 1000С , температура плавления (замерзания) – 00С.
Вода – единственное
вещество в природе, которое в земных условиях существует в трех агрегатных состояниях: жидком, газообразном и твёрдом.Слайд 8Вода – хороший растворитель. В ней растворяются твёрдые, жидкие и
газообразные вещества.
Вода – хороший растворитель для многих веществ
Слайд 9Сплавы
Сплавы – это системы из двух или нескольких металлов (или
металлов и неметаллов), обладающие по сравнению с чистыми металлами как
общими металлическими, так и новыми ценными свойствами.Количество сплавов намного больше, чем чистых металлов. Применение их разнообразно.
Слайд 10 Сталь – сплав железа с
добавками углерода, кремния и других металлов и неметаллов (до 2,5%)
Слайд 19Монель-металл (медно-никелевый сплав) используется для изготовления химического оборудования, а также
в промышленности, например в паровых турбинах
Слайд 22При решении задач о смесях, сплавах, растворах используют следующие допущения:
все
полученные смеси, сплавы, растворы считаются однородными;
не делается различия между литром
как мерой вместимости сосуда и литром как мерой количества жидкости (или газа);смешивание различных растворов происходит мгновенно;
объем смеси равен сумме объемов смешиваемых растворов;
объемы растворов и массы сплавов не могут быть отрицательными.
Слайд 23Определения и обозначения
Массовая доля растворенного вещества в растворе - это
отношение массы этого вещества к массе раствора.
где ω(в-ва) - массовая
доля растворенного вещества в растворе;m(в-ва) - масса растворенного вещества в растворе;
m(р-ра) - масса раствора.
Слайд 24Определения и обозначения
Введем обозначения:
ω1(в-ва) - массовая доля растворенного вещества в
первом растворе;
ω2(в-ва) - массовая доля растворенного вещества во втором растворе;
ω(в-ва)
- массовая доля растворенного вещества в новом растворе, полученном при смешивании первого и второго растворов;m1(в-ва), m2(в-ва), m(в-ва) – массы растворенных веществ в соответствующих растворах;
m1(р-ра), m2(р-ра), m(р-ра) - массы соответствующих растворов.
Слайд 26С помощью расчетной формулы
Масса полученного при смешивании раствора равна:
т(р-ра) = т1(р-ра) + т2(р-ра)
массы растворенных веществ в первом
и втором растворах:т1(в-ва) = ω1(в-ва)·т1(р-ра),
т2(в-ва) = ω2(в-ва)·т2(р-ра)
масса растворенного вещества в полученном растворе вычисляется как сумма масс веществ в исходных раствopax:
т(в-ва) = m1(в-ва) + т2(в-ва) = ω1(в-ва)·т1(р-ра) + ω2(в-ва)·т2(р-ра)
Слайд 27С помощью расчетной формулы
Таким образом, массовая доля растворенного вещества в
полученном
растворе равна:
Слайд 31Алгебраический метод
Задачи на смешивание растворов решают с
помощью составления уравнения или системы уравнений.
Слайд 33Решение задач
Приготовление растворов или сплавов
В воде массой 400 г растворили
50 г серной кислоты. Какова массовая для серной кислоты в
полученном растворе?Найти массу воды и соли, необходимых для приготовления 500 г 25%-ного раствора этой соли.
Сплавили 60 г серебра и 240 г меди. Найти массовую долю серебра в полученном сплаве.
Слайд 34Решение задач
Приготовление растворов или сплавов
Какую массу алюминия и магния необходимо
взять, чтобы приготовить образец сплава массой 300 г, содержащий 45%
алюминия?Массовая доля солей в морской воде достигает 3,5%. Определите массу соли, остающейся после выпаривания морской воды объемом 8,93 л с плотностью 1,12 г/мл.
Какая масса карбоната натрия потребуется для приготовления 0,5 л 13%-ного раствора плотностью 1,13 г/мл?
Слайд 35Решение задач
Сложные проценты
Задача 1
К 100
г 20%-ного раствора соли добавили 300 г её 10%-ного раствора.
Определите процентную концентрацию полученного раствора.Слайд 36Решение
Алгебраический метод
m1(р-ра) = 100 г
m2(р-ра) = 300 г
ω1(в-ва) = 0,2
ω2(в-ва)
= 0,1
ω(в-ва) - ?
Первый раствор:
m1(р-ра) = 100 г, m1(в-ва)
= 100.0,2 = 20 (г) Второй раствор :
m2(р-ра) = 300 г, m2(в-ва) = 300.0,1 = 30 (г)
Полученный раствор :
m(р-ра) = 100 + 300 = 400 (г), m(в-ва) = 20 + 30 =50 (г)
Тогда,
Ответ: 12,5%.
Слайд 37Решение
С помощью расчетной формулы
m1(р-ра) = 100 г
m2(р-ра) = 300 г
ω1(в-ва)
= 0,2
ω2(в-ва) = 0,1
ω(в-ва) - ?
Используем формулу:
Получаем:
Ответ: 12,5%
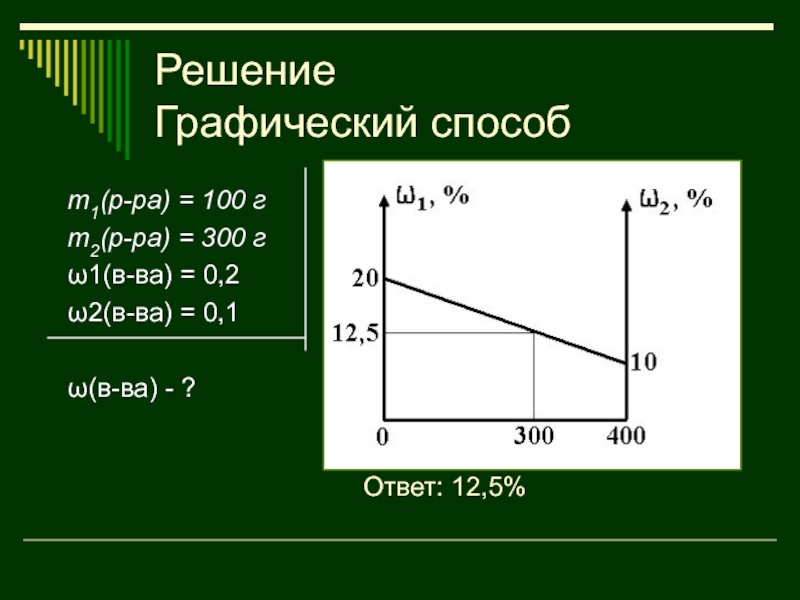
Слайд 38Решение
Графический способ
m1(р-ра) = 100 г
m2(р-ра) = 300 г
ω1(в-ва) = 0,2
ω2(в-ва)
= 0,1
ω(в-ва) - ?
Ответ: 12,5%
Слайд 39Решение задач
Сложные проценты
Задача 2
Смешали 10%-ный и
25%-ный растворы соли и получили 3 кг 20%-ного раствора. Какое
количество каждого раствора в килограммах было использовано?Слайд 40Решение
Алгебраический метод
ω1(в-ва) = 0,1
ω2(в-ва) = 0,25
m(р-ра) = 3 кг
ω(в-ва) =
0,2
m1(р-ра) - ?
m2(р-ра) - ?
Первый раствор:
m1(р-ра) = x кг,
m1(в-ва) = 0,1.x (кг) Второй раствор :
m2(р-ра) = (3 – x) кг, m2(в-ва) = (0,25.(3 – x)) кг
Полученный раствор :
m(р-ра) = 3 кг, m(в-ва) = 3.0,2 = 0,6 (кг)
Так как масса вещества в полученном растворе
0,6 кг, можно составить уравнение:
0,1x + 0,25(3 - x) =0,6
0,1x + 0,75 – 0,25x =0,6
0,1x – 0,25x =0,6 - 0,75
- 0,15x = - 0,15
X=1
Масса первого раствора 1 кг, масса второго раствора 3 -1 = 2 (кг)
Ответ: 1 кг, 2 кг.
Слайд 41Решение
Графический способ
ω1(в-ва) = 0,1
ω2(в-ва) = 0,25
m(р-ра) = 3 кг
ω(в-ва) =
0,2
m1(р-ра) - ?
m2(р-ра) - ?
Ответ: 1 кг, 2 кг.
Слайд 42Решение
«Правило смешения»
ω1(в-ва) = 0,1
ω2(в-ва) = 0,25
m(р-ра) = 3 кг
ω(в-ва) =
0,2
m1(р-ра) - ?
m2(р-ра) - ?
Воспользуемся формулой:
Получаем:
m1 = 0,5m2
m1 +
m2 = 3, следовательно, m1 = 1 кг, m2 = 2 кг.Ответ: 1 кг, 2 кг.
Слайд 43Решение
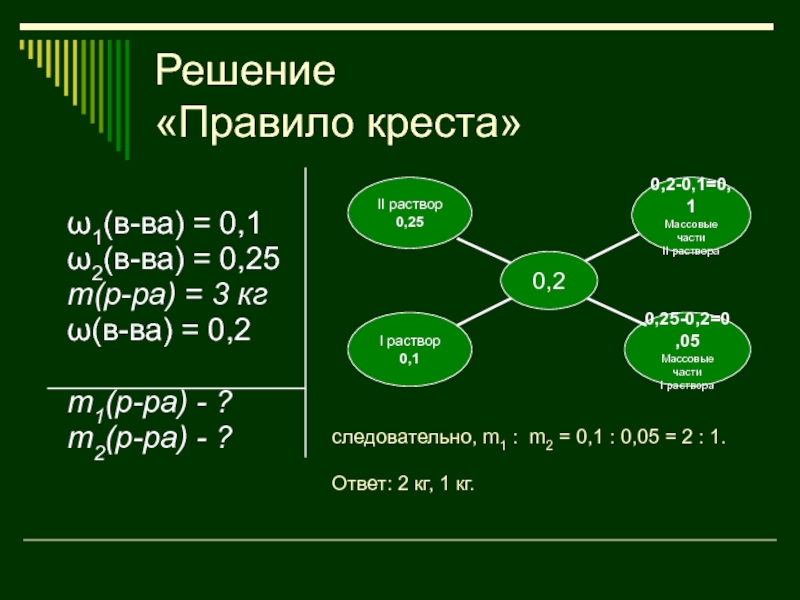
«Правило креста»
ω1(в-ва) = 0,1
ω2(в-ва) = 0,25
m(р-ра) = 3 кг
ω(в-ва) =
0,2
m1(р-ра) - ?
m2(р-ра) - ?
следовательно, m1 : m2 = 0,1
: 0,05 = 2 : 1.Ответ: 2 кг, 1 кг.
Слайд 44Решение задач
Сложные проценты
К 300 г раствора, содержащего 10% соли, добавили
некоторое количество раствора, содержащего 30% той же соли. Получили раствор,
содержащий 15% соли. Какую массу второго раствора взяли?Имеются два слитка сплава серебра и олова. Первый слиток содержит 360 г серебра и 40 г олова, а второй слиток - 450 г серебра и 150 г олова. От каждого слитка взяли по куску, сплавили их и получили 200 г сплава, в котором оказалось 81 % серебра. Определите массу (в граммах) куска, взятого от второго слитка.
Слайд 46Решение задач
Сложные проценты
Имеется сталь двух сортов с содержанием никеля 5%
и 40%. Сколько тонн стали первого сорта нужно взять, чтобы
в смеси со вторым сортом получить при плавке 140 т стали с содержанием никеля 30%?Имеются два сплава, в первом из которых содержится 40%, а во втором - 20% серебра. Сколько килограммов второго сплава необходимо добавить к 20 кг первого сплава, чтобы получить сплав, содержащий 30% серебра?
Проверить
Дальше
Слайд 47Решение
Алгебраический метод
m1(сп-ва) = 20 кг
ω1(Ag) = 0,4
ω2(Ag) = 0,2
ω(Ag) =
0,3
m2(сп-ва) - ?
Первый сплав:
m1(сп-ва) = 20 кг, m1(Ag) =
20.0,4 = 8 (кг) Второй сплав:
m2(сп-ва) = x кг, m2(Ag) = (x.0,2) кг
Полученный сплав:
m(сп-ва) = (20 + x) кг, m(Ag) = (8 + 0,2x) кг
Так как ω(Ag) = 0,3, то
8 + 0,2x = 6 + 0,3x
0,2x – 0,3x = 6 - 8
-0,1x = -2
x=20
Ответ: 20 кг.
Слайд 48Решение
«Правило смешения»
m1(сп-ва) = 20 кг
ω1(Ag) = 0,4
ω2(Ag) = 0,2
ω(Ag) =
0,3
m2(сп-ва) - ?
Воспользуемся формулой:
Получаем:
m1 = m2 = 20 кг.
Ответ:
20 кг.Слайд 49Решение
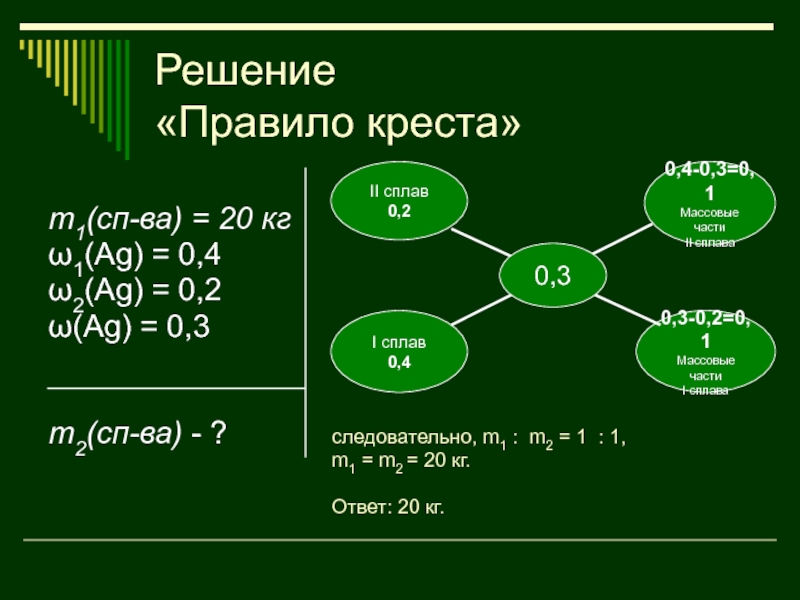
«Правило креста»
m1(сп-ва) = 20 кг
ω1(Ag) = 0,4
ω2(Ag) = 0,2
ω(Ag) =
0,3
m2(сп-ва) - ?
следовательно, m1 : m2 = 1 : 1,
m1
= m2 = 20 кг.Ответ: 20 кг.
Слайд 50Решение задач
Сложные проценты
Имеются два слитка сплава золота с медью. Первый
слиток содержит 230 г золота и 20 г меди, а
второй слиток - 240 г золота и 60 г меди. От каждого слитка взяли по куску, сплавили их и получили 300 г сплава, в котором оказалось 84% золота. Определите массу (в граммах) куска, взятого от первого слитка.К 120 г раствора, содержащего 80% соли, добавили 480 г раствора, содержащего 20% той же соли. Сколько процентов соли содержится в получившемся растворе.