Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Сложные эфиры. Жиры
Содержание
- 1. Сложные эфиры. Жиры
- 2. Что такое сложные эфиры и жиры?R1, R2,
- 3. НоменклатураНазвания сложных эфиров производят от названия углеводородного
- 4. ИзомерияИзомерия углеродной цепи начинается по кислотному остатку
- 5. 2. Изомерия положения сложноэфирной группировки —СО—О—Этот вид
- 6. 3. Межклассовая изомерия -например, метилацетату изомерна пропановая кислота.СН3―СО―О―СН3 метилацетат С2Н5―СО―ОН пропионовая кислотаИзомерия
- 7. 4. Для сложных эфиров, содержащих непредельную кислоту
- 8. Физические свойства сложных эфировСложные эфиры низших карбоновых
- 9. Физические свойства жировЖиры широко распространены в природе.
- 10. Химические свойства сложных эфировПроцесс расщепления сложного эфира
- 11. Химические свойства сложных эфировРеакция присоединения. Сложные эфиры,
- 12. Одно из важнейших свойств жиров ― их
- 13. Химические свойства жировЕсли на выделяющуюся карбоновую кислоту
- 14. Химические свойства жировТвердые животные жиры более ценны
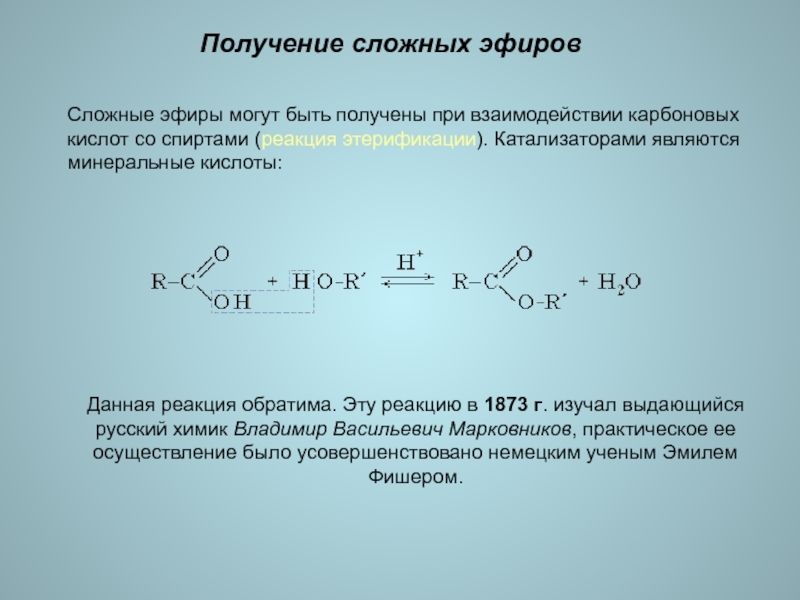
- 15. Получение сложных эфиров
- 16. Получение жировПолучить Жиры можно реакцией этерификации, в
- 17. Применение сложных эфировлаки краскиПищевая промышленностьпарфюмерная промышленностьСложные эфирытекстильная промышленность
- 18. Применение жировЖирыЛаки ОлифаКондитерская промышленность Получение мылаПищевая промышленность
- 19. Интересное о жирахЖиры являются одной из трех
- 20. ЛитератураНесмеянов А. Н., Несмеянов Н. А., Начала
- 21. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Что такое сложные эфиры и жиры?
R1, R2, R3-углеводородные радикалы (для
сложных эфиров) и углеводородные радикалы карбоновых кислот (для жиров)
Слайд 3
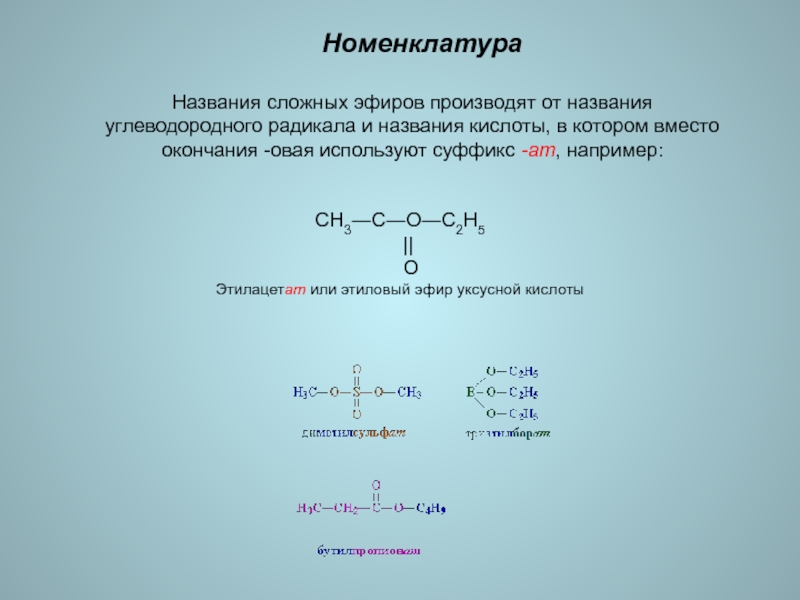
Номенклатура
Названия сложных эфиров производят от названия углеводородного радикала и названия
кислоты, в котором вместо окончания -овая используют суффикс -ат, например:
CH3―С―O―C2H5
|| О
Этилацетат или этиловый эфир уксусной кислоты
Слайд 4Изомерия
Изомерия углеродной цепи начинается по кислотному остатку с бутановой кислоты,
по спиртовому остатку — с пропилового спирта, например, этилбутирату изомерны
этилизобутират, пропилацетат и изопропилацетат.СН3―СН2―СН2―СН2―С―О―С2Н5
||
О
Этилбутират
СН3―СН―СН2―C―О―С2Н5
| ||
CH3 O
Этилизобутират
СН3―С―O―СН2―СН2―СН3
||
О
Пропилацетат
СН3―С―O―СН―СН3
|| |
O CH3
Изопропилацетат
Слайд 52. Изомерия положения сложноэфирной группировки
—СО—О—
Этот вид изомерии начинается со
сложных эфиров, в молекулах которых содержится не менее 4 атомов
углерода, например этилацетат и метилпропионат.Изомерия
СН3―СО―О―С2Н5
этилацетат
С2Н5―СО―О―СН3
метилпропионат.
Слайд 63. Межклассовая изомерия
-например, метилацетату изомерна пропановая кислота.
СН3―СО―О―СН3
метилацетат
С2Н5―СО―ОН
пропионовая кислота
Изомерия
Слайд 74. Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт,
возможны еще два вида изомерии:
изомерия положения кратной связи
цистрансизомерия
Изомерия
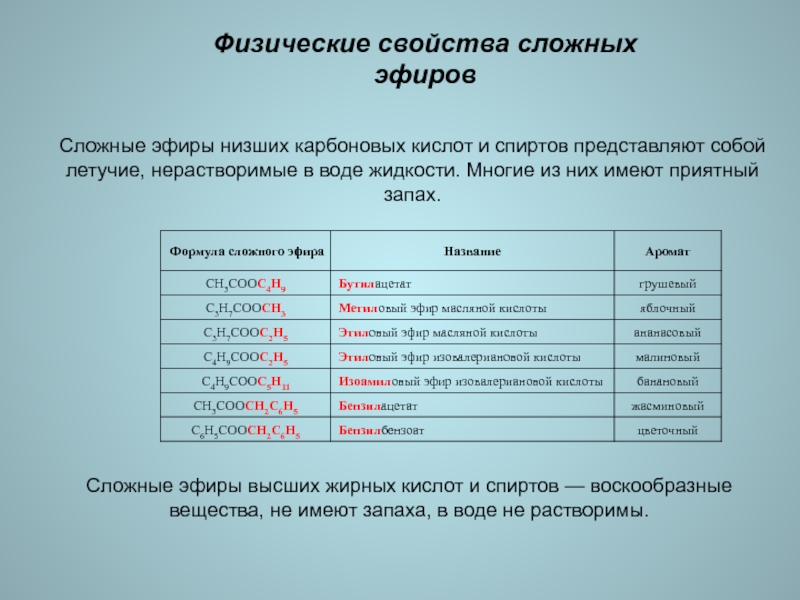
Слайд 8Физические свойства сложных эфиров
Сложные эфиры низших карбоновых кислот и спиртов
представляют собой летучие, нерастворимые в воде жидкости. Многие из них
имеют приятный запах.Сложные эфиры высших жирных кислот и спиртов — воскообразные вещества, не имеют запаха, в воде не растворимы.
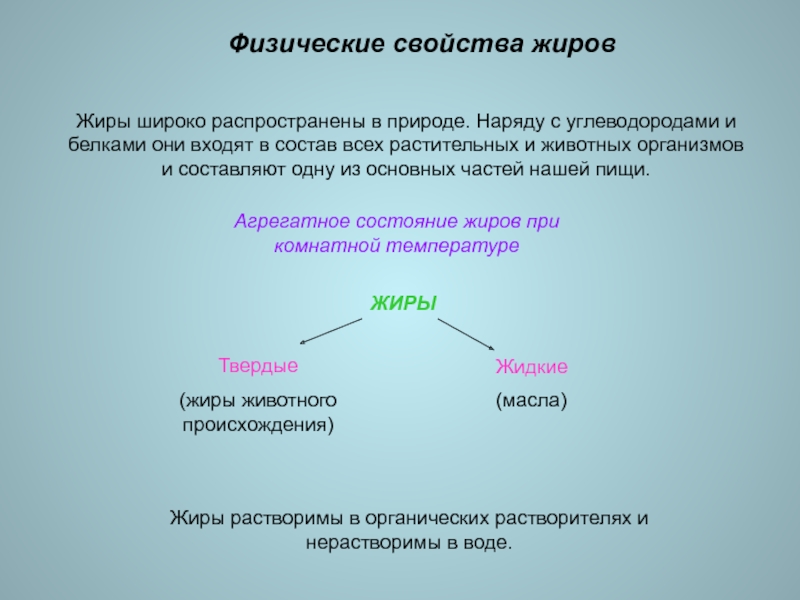
Слайд 9Физические свойства жиров
Жиры широко распространены в природе. Наряду с углеводородами
и белками они входят в состав всех растительных и животных
организмов и составляют одну из основных частей нашей пищи.Агрегатное состояние жиров при комнатной температуре
Жиры растворимы в органических растворителях и нерастворимы в воде.
Слайд 10Химические свойства сложных эфиров
Процесс расщепления сложного эфира при действии воды
с образованием карбоновой кислоты и спирта называют гидролизом сложного эфира:
СН3―СО―О―С2Н5
+ H2O ↔ СН3―СООН + С2Н5ОНРеакция этерификации (с помощью которой можно получить сложные эфиры) ― обратимый процесс. Прямая реакция ― образование сложного эфира, обратная ― его кислотный гидролиз. Для того чтобы сдвинуть равновесие вправо, необходимо удалять из реакционной смеси воду.
Гидролиз в присутствии щелочи протекает необратимо (т. к. образующийся отрицательно заряженный карбоксилат-анион RCOO– не вступает в реакцию с нуклеофильным реагентом ― спиртом).
Эта реакция называется омылением сложного эфира.
Слайд 11Химические свойства сложных эфиров
Реакция присоединения. Сложные эфиры, имеющие в своем
составе непредельную кислоту или спирт, способны к реакциям присоединения. Например,
при каталитическом гидрировании они присоединяют водород.Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:
R'―CO―OR" + [H]→ R'―CH2―OH + R"OH
Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты
R'―CO―OR" + NH3 → R'―CO―NH2 + R"OH
Слайд 12Одно из важнейших свойств жиров ―
их способность расщепляться на
составляющие:
глицерин и карбоновые кислоты.
Если такая реакция осуществляется под
действием воды в присутствии кислот, она называется гидролизом (гидро ― вода, лиз ― разрушение):
Химические свойства жиров
Приведенная выше реакция является обратимой. Но как сместить равновесие вправо? Один из способов ― удаление одного из конечных продуктов, например, превратить его в другое вещество (см. след. слайд)
Слайд 13Химические свойства жиров
Если на выделяющуюся карбоновую кислоту действовать щелочью ―
она превратится в соль:
C17H35COOH + NaOH → C17H35COONa + H2O
Если
объединить две реакции в одну, т. е. нагревать раствором щелочи, то разложение будет необратимым и пройдет до конца:СН2―О―СО―С17Н35 CH2―OH
| |
СН―О―СO―С17H35 + 3NaOH → CH―OH + 3C17H35COONa
| |
СН2―О―СО―С17Н35 CH2―OH
Эта реакция называется омылением, поскольку образующиеся соли щелочных металлов и высших карбоновых кислот являются мылами.
Слайд 14Химические свойства жиров
Твердые животные жиры более ценны и дорогостоящи, чем
растительные масла. Способ превращения непредельных жиров в предельные ― присоединение
по двойной связи молекулы водорода.Такая реакция называется реакцией гидрирования.
Например, реакция гидрирования триолеата глицерина до тристеарата:
CH2―O―CO―C17H33 CH2―O―CO―C17H35
| |
CH―O―CO―C17H33 + 3H2 → CH―O―CO―C17H35
| |
CH2―O―CO―C17H33 CH2―O―CO―C17H35
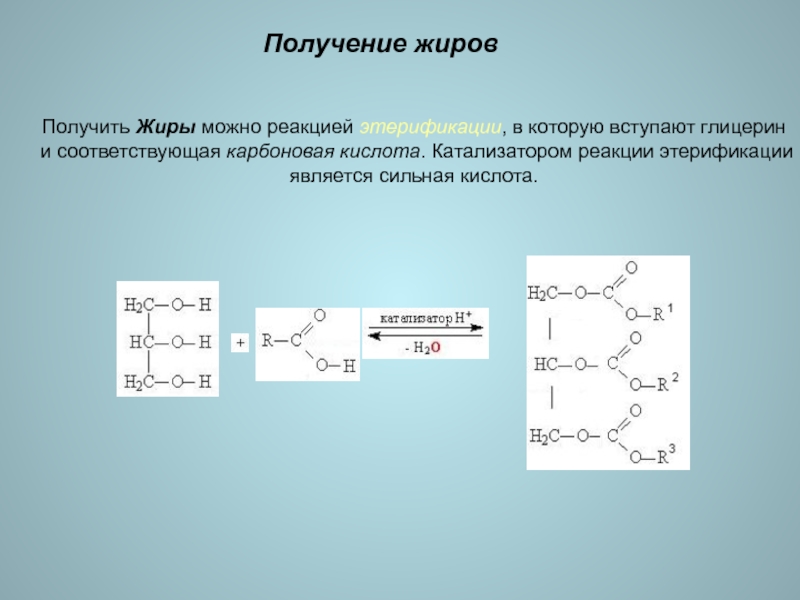
Слайд 16Получение жиров
Получить Жиры можно реакцией этерификации, в которую вступают глицерин
и соответствующая карбоновая кислота. Катализатором реакции этерификации является сильная кислота.
Слайд 17Применение сложных эфиров
лаки
краски
Пищевая
промышленность
парфюмерная
промышленность
Сложные эфиры
текстильная
промышленность
Слайд 18Применение жиров
Жиры
Лаки
Олифа
Кондитерская
промышленность
Получение мыла
Пищевая
промышленность
Слайд 19
Интересное о жирах
Жиры являются одной из трех главных составляющих пищи
человека и животных , наряду с углеводами и белками. При
их окислении в организме выделяется энергия, необходимая для поддержания постоянной температуры тела и протекания других физиологических процессов (калорийность чистого жира 3770 кДж (900 ккал/100 г). Поступающие с пищей жиры в процессе пищеварения расщепляются на глицерин и жирные кислоты; эти вещества всасываются в кишечнике, затем из них вновь синтезируются жиры. Кроме того, жиры накапливаются в подкожных тканях и тканях, окружающих внутренние органы, и выполняют терморегулирующую и защитную функцию в организме.жиры