Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
СОЛИ
Содержание
- 1. СОЛИ
- 2. Определения и классификацияНоменклатура Физические свойстваСпособы полученияХимические свойствасоли
- 3. Общяя классификацияПростыеСложныеМеталлыНеметаллыОрганическиеНеорганическиеОСНОВАНИЯОКСИДЫСОЛИКИСЛОТЫ
- 4. Классификация солейсолисредниекислыеосновныедвойныесмешанныекомплексныегидратные
- 5. Структура кристалла хлорида натрияСолиэто в основном твердые
- 6. Определения типов солейСоли состоят из атомов металла
- 7. Примеры солейСредние соли: Ca(NO3)2; K2SO4; Al(NO3)3.
- 8. а) К основным солямб) К смешанным солямв) К комплексным солямг) К двойным солям
- 9. Номенклатура солейНазвание солей образуется из названия аниона,
- 10. Как правильно назвать соль: KCl?а) Хлор калияб) Хлорид калияв) Хлорат калияг) Хлорит калия
- 11. Физические свойства солейОсновное свойство солей- это то,
- 12. +
- 13. Способы получения солейСоли получают разнообразными способами. Вот
- 14. Химические свойства солейСоли обладают общими химическими свойствами
- 15. С каким из металлов будет взаимодействовать соль MgS?а) Caб) Mnв) Zn г) Ni
- 16. Гидролиз солейСуществуют четыре типа гидролиза:Соль образована ионом
- 17. План составления гидролиза:1) Проверить соль на растворимость
- 18. Первый тип гидролизаПример:
- 19. Второй тип гидролизаПример:
- 20. Третий тип гидролизаВ этом случае гидролиз необратим.Примеры:
- 21. Четвертый тип гидролизаNaClРастворимые соли, образованные сильной кислотой
- 22. Факторы, влияющие на гидролиз1) Повышение температуры приводит
- 23. КОНЕЦ!P.S. Надеюсь, Вам понравилось.
- 24. ВЕРНО
- 25. Не верно
- 26. Не верно
- 27. ВЕРНО
- 28. ВЕРНО
- 29. Не верно
- 30. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Определения и классификация
Номенклатура
Физические свойства
Способы получения
Химические свойства
соли
Слайд 3Общяя классификация
Простые
Сложные
Металлы
Неметаллы
Органические
Неорганические
ОСНОВАНИЯ
ОКСИДЫ
СОЛИ
КИСЛОТЫ
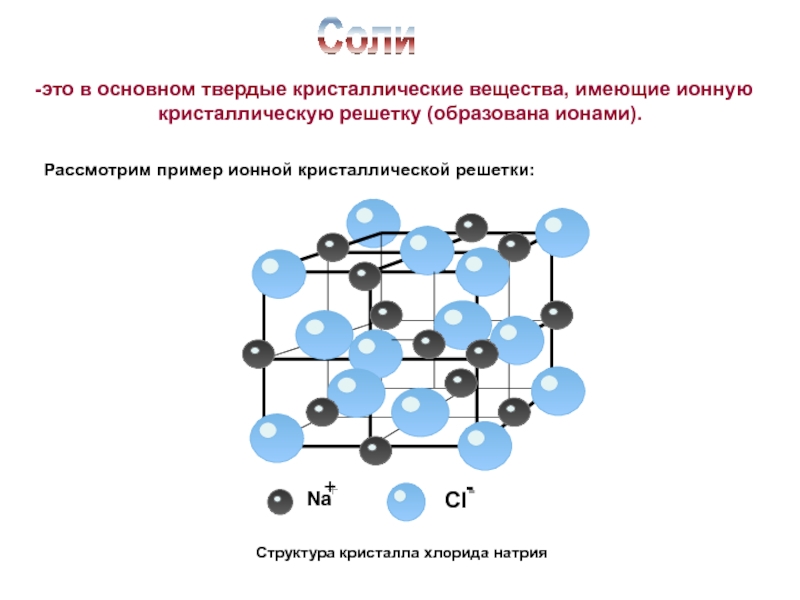
Слайд 5Структура кристалла хлорида натрия
Соли
это в основном твердые кристаллические вещества, имеющие
ионную
кристаллическую решетку (образована ионами).
Рассмотрим пример ионной кристаллической решетки:
Слайд 6Определения типов солей
Соли
состоят из атомов металла и атомов кислотного
остатка.
Основные типы солей это:
комплексные, кислые и основные.
Средние соли
-это соли,
в которых все атомы водорода соответствующей кислоты замещены на атомы металла.
Кислые соли
- это соли, в которых атомы водорода замещены только частично.
Основные соли
это соли, в которых группы ОН соответствующего основания
частично замещены на кислотные остатки.
Двойные соли
- это соли, в которых содержится два разных катиона и один анион.
Смешанные соли
- это соли, в которых содержится один катион и два разных аниона.
Комплексные соли
- это соли, в состав которых входит комплексный йон.
Слайд 7Примеры солей
Средние соли: Ca(NO3)2; K2SO4; Al(NO3)3.
Кислые соли: KHSO4; MgHPO4; NaSO3.
Основные соли: LiOHPO4; CaOHP2O 7; MnSiO4.
Двойные соли: KAl(SO4)2
Смешанные соли: CaOCl2
Комплексные соли: K4[Fe(CN)6]
Слайд 9Номенклатура солей
Название солей образуется из названия аниона, за
которым следует
название катиона.
Для солей бескислородных кислот к названию неметалла добавляется
суффикс - ид. Например: MgS- сульфид магния.При наименовании солей кислородосодержащих кислот к латинскому корню
названия элемента добавляется окончание- ат для высших степеней
окисления. Например: MgSO4- сульфат магния.
Для более низких степеней окисления прибавляется окончание- ит.
Например: MgSO4- сульфит натрия.
Кислые и основные соли можно рассматривать как продукт неполного прев-
ращения кислот и оснований. Атом водорода, входящий в состав кислой
соли, обозначается приставкой гидро.
Например: NaHS- гидросульфид натрия.
В основных же солях группа ОН обозначается приставкой гидрокси.
Например: Mg(OH)Cl- гидроксихлорид магния.
Слайд 11Физические свойства солей
Основное свойство солей- это то, что они являются
электролитами.
Электролиты- это вещества, растворы или
расплавы которых проводят электрический
ток.Рассмотрим опыт, доказывающий это :
Слайд 13Способы получения солей
Соли получают разнообразными способами. Вот примеры
некоторых из
них:
а) Взаимодействием двух простых веществ:
б) Взаимодействием двух сложных веществ:
в) Взаимодействием
простого и сложного вещества:(железо при нагревании с серой образует сульфид железа (II)).
(Соли вступаю друг с другом в обменные
реакции в водном растворе, если
образуется соль слабый электролит).
(соли образуются при растворении металлов
в кислотах).
Слайд 14Химические свойства солей
Соли обладают общими химическими свойствами
за счет сходного
иона.
Пример:
Взаимодействие солей с солями.
Взаимодействие соли с щелочью.
Взаимодействие соли с кислотой.
Взаимодействие
солей с металлами.Каждый левее стоящий металл вытесняет правее стоящий металл из его соли:
Fe + CuSO4 = FeSO4 + Cu
Слайд 16Гидролиз солей
Существуют четыре типа гидролиза:
Соль образована ионом сильного основания и
ионом
слабой кислоты.
2)Соль образована ионом слабого основания и ионом
сильной кислоты.
3)
Соль образована ионом слабого основания и иономслабой кислоты.
4) Соль образована ионом сильного основания и ионом
сильной кислоты.
Слайд 17План составления гидролиза:
1) Проверить соль на растворимость по таблице
растворимости.
2)
Определить, есть ли в составе соли ионы слабого
электролита.
4) Записать
краткое ионное уравнение гидролиза.5) Записать полное молекулярное уравнение гидролиза.
3) Определить количество ступеней гидролиза
( количество ступеней численно = заряду иона, по
которому ведется расчет).
Слайд 21Четвертый тип гидролиза
NaCl
Растворимые соли, образованные сильной
кислотой и сильным основанием,
в воде не гидролизируются.
Их растворы имеют нейтральную среду.
Слайд 22Факторы, влияющие на гидролиз
1) Повышение температуры приводит к смещению
равновесия
в сторону продуктов реакции.
2)Увеличение концентрации в сторону исходных
веществ приводит к смещению равновесия в сторону продуктов реакции.
3)Увеличение концентрации продуктов реакции
приводит к подавлению гидролиза и смещению
равновесия в сторону исходных веществ.