Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Вода как растворитель
Содержание
- 1. Вода как растворитель
- 2. Мы хотим выяснить:Что называется раствором? Какие вещества
- 3. Слайд 3
- 4. Слайд 4
- 5. Слайд 5
- 6. Слайд 6
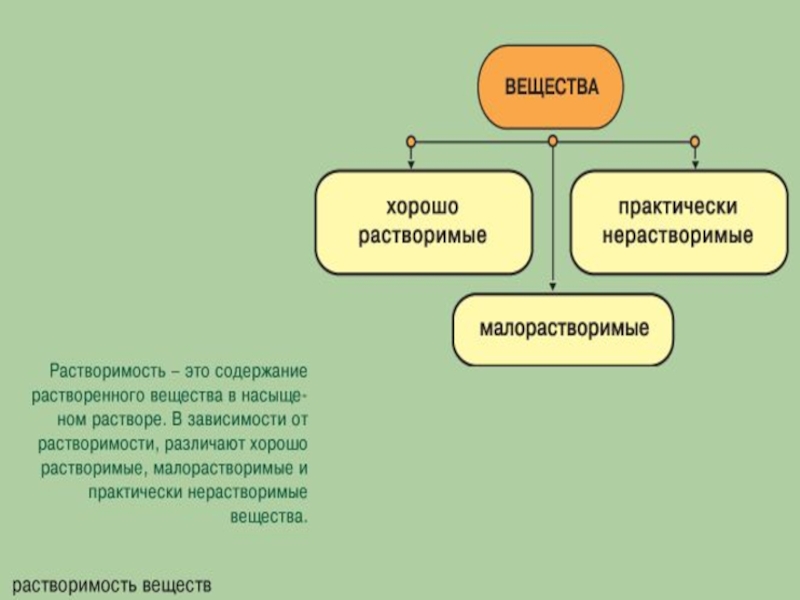
- 7. Растворимость вещества показывает, сколько вещества в граммах
- 8. Растворимость веществ зависит от природы растворяемого вещества
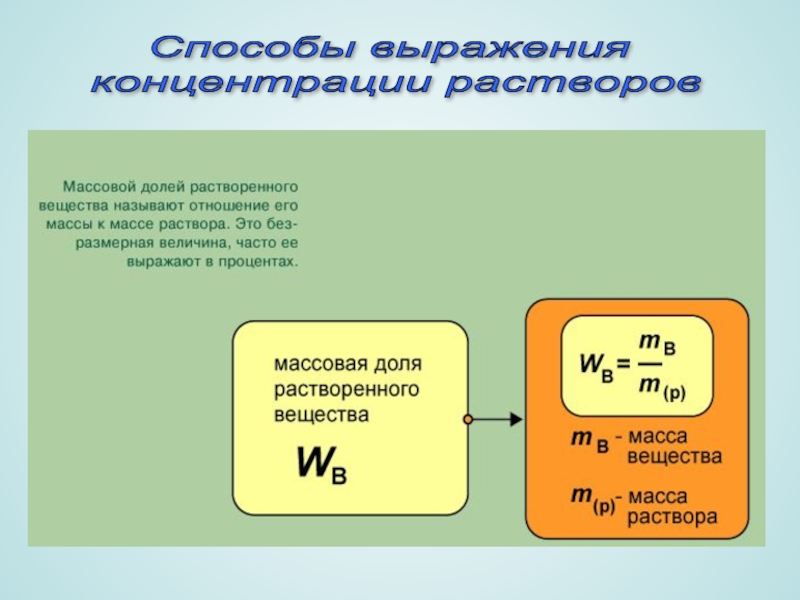
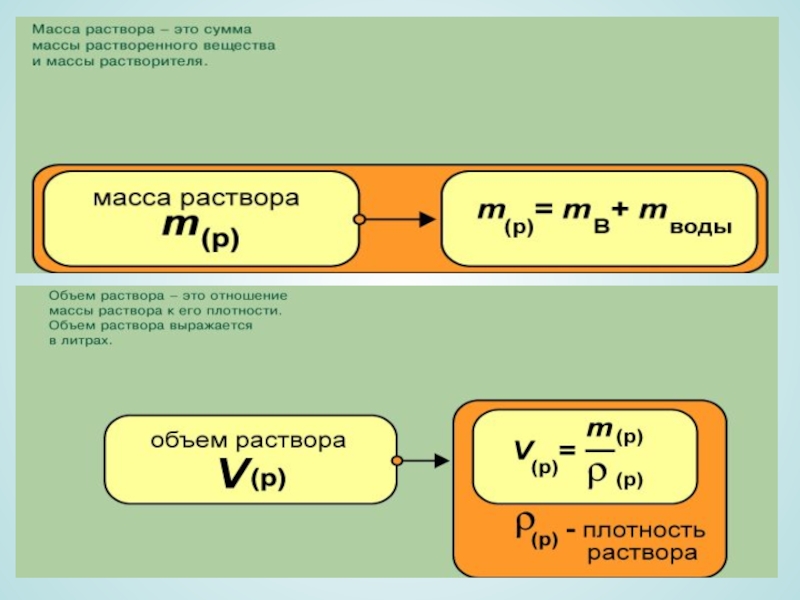
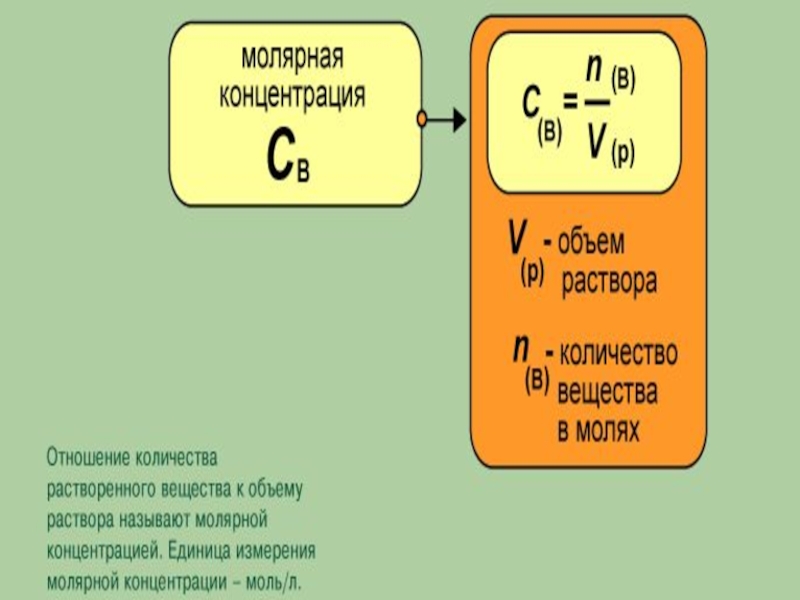
- 9. Способы выражения концентрации растворов
- 10. Слайд 10
- 11. Слайд 11
- 12. 1. Мы выяснили, что раствор – это
- 13. ЛитератураКрицман В.А. Книга для чтения по неорганической
- 14. Скачать презентанцию
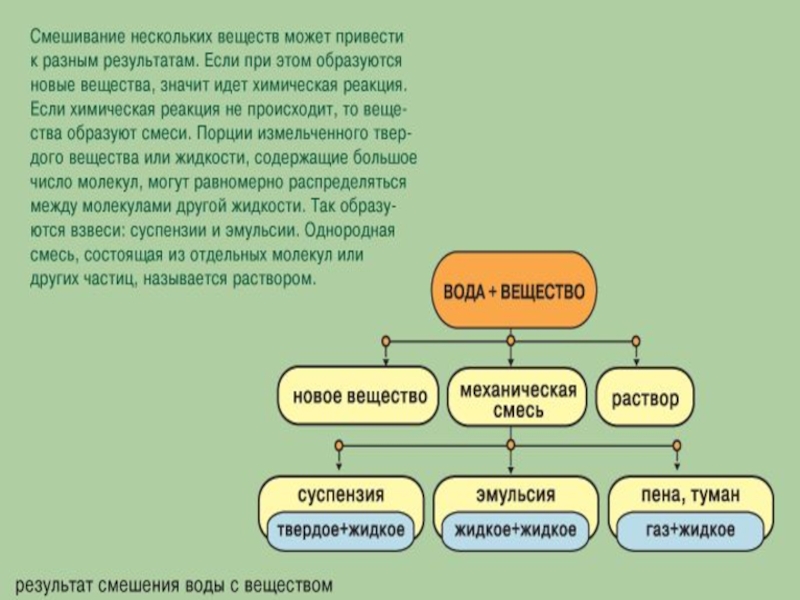
Мы хотим выяснить:Что называется раствором? Какие вещества встречаются в природе при взаимодействии с водой?От чего зависит растворимость (эксперимент) ?Как и в чем выражается концентрация растворов?
Слайды и текст этой презентации
Слайд 1Вода как растворитель
Презентация учеников 8 «Б» класса
Анучин Артем, Голубев Миша
Колеганова
Аня, Коваленко Женя
Слайд 2Мы хотим выяснить:
Что называется раствором?
Какие вещества встречаются в природе
при взаимодействии с водой?
От чего зависит растворимость (эксперимент) ?
Как и
в чем выражается концентрация растворов?Слайд 7Растворимость вещества показывает, сколько вещества в граммах может раствориться в
1 л воды или сколько вещества в граммах может раствориться
в 100 г растворителя.Отношение массы вещества, образующего насыщенный раствор при данной температуре, к объему растворителя называется растворимостью этого вещества или коэффициентом растворимости.
Слайд 8Растворимость веществ зависит от природы растворяемого вещества и растворителя, температуры
и давления. Причины различной растворимости веществ пока точно не установлены,
их связывают с характером взаимодействия молекул растворителя и растворенного вещества. Поэтому точно установить растворимость вещества в некотором растворителе можно только экспериментальным путем. Однако замечено, что вещества, состоящие из полярных молекул и вещества с ионным типом связи лучше растворяются в полярных растворителях, а неполярные вещества – в неполярных растворителях. Или иначе: подобное растворяется в подобном.Перманганат калия хорошо растворяется в воде, а растительное масло – не растворяется
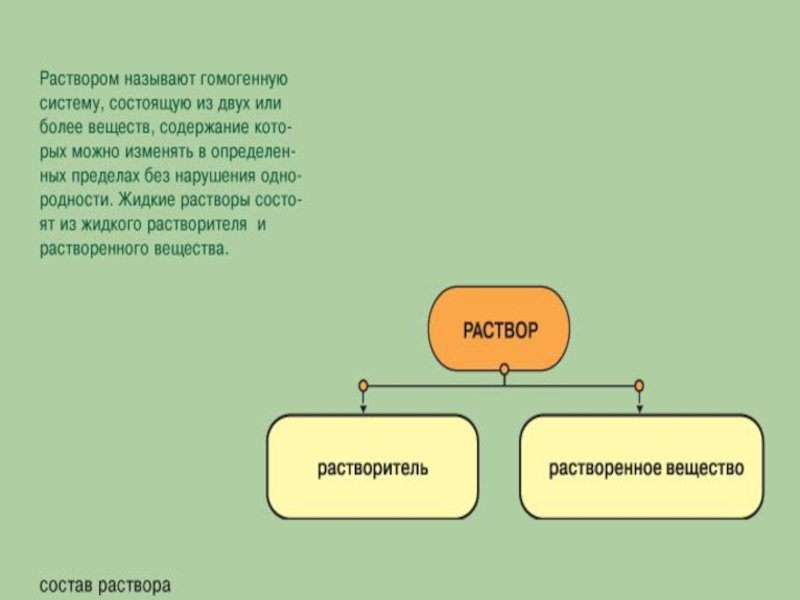
Слайд 121. Мы выяснили, что раствор – это неоднородная масса, состоящая
из растворителя и растворенного вещества.
2. Вещества бывают растворимыми и нерастворимыми,
поэтому и сами растворы отличаются по насыщенности.3.Из природных водных растворов образовались громадные толщи многих минералов, например каменной соли.
4. Растения берут из почвы необходимые им соли только в виде растворов. Поэтому своевременное поступление воды из почвы – одно из главных условий высокого урожая.
5. Процессы усвоения пищи животными и человеком также осуществляется через превращение ее в органах пищеварения в соединения, растворимые в воде, и переход этих соединений в водные растворы.
6. Изучая химию, мы часто пользуемся водными растворами веществ. Предварительное растворение веществ в воде обеспечивает быстрое протекание химических реакций между
ними.
Выводы
Слайд 13Литература
Крицман В.А. Книга для чтения по неорганической химии. М: Просвещение,1993.
Мартыненнко
Б.В. Кислоты – основания. М: Просвещение, 1998.
Орлик Ю.Г. Химия после
уроков. Минск, 1979.Габриелян О.С. Химия 8 класс. М: Дрофа, 2001.
Теги