Слайд 1Демиелинизирующие заболевания ЦНС
Слайд 2Определения истинной демиелинизации
Заболевания с преимущественным поражением миелина и относительной
интактностью клетки и аксона
Отсутствует вторичная валлеровская дегенерация
Инфильтрация воспалительными клетками
периваскулярных участков
Околовенозный характер распространения демиелинизации
Вероятно аутоиммунный характер патологии
Слайд 3Демиелинизирующие заболевания
Рассеянный склероз
Диффузный церебральный склероз (диффузный периаксиальный энцефалит) Шильдера и
концентрический склероз Бало
Острый рассеянный энцефаломиелит (ОРЭМ) (в т.ч. постинфекционный) и
миелит
Острый и подострый некротический геморрагический энцефаломиелит
Слайд 4Демиелинизирующие заболевания неаутоиммунной (доказанной) этиологии
Подострая комбинированная дегенерация спинного мозга (В12
дефицитная) («фуникулярный миелоз»)
Демиелинизация коры при гипоксической энцефалопатии
Прогрессирующая мультифокальная лейкоэнцефалопатия (HIV)
Слайд 5Этиология
Этиология истинных демиелинизирующих заболеваний неизвестна
Иммунопатология
Патогенез
Возможности ремиелинизации
Эфаптическая передача
Слайд 6Рассеянный склероз
Синонимы: Множественный склероз (Multiple Sclerosis), склероз в бляшках
(Sclerosis in Plaque)
Слайд 7Определения
Рассеянный склероз — хроническое прогрессирующее заболевание, характеризующееся множественными очагами поражения
в центральной и периферической нервной системе («бляшками») и множественными симптомами
поражения, а также течением с атаками и ремиссиями (Sharcot, 1865).
Слайд 8Эпидемиология
РС – самое распространенное демиелинизирующее заболевание
Частота заболеваемости – от
3 до 80 на 100000 населения
В США в 2004 г.
– около 400000 пациентов
Ежегодные затраты в США – около 65000$ на 1 пациента в год
Слайд 9Эпидемиология РС
Заболевание в основном регистрируется в странах с холодным климатом,
гораздо реже — в жарких странах (правило «северно-южного» градиента).
Женщины
болеют несколько чаще (60%).
В 80% случаев дебют –в возрасте от 20 до 40 лет
В США, Канаде, Австралии, странах Западной Европы частота рассеянного склероза составляет 30—80 случаев на 100 тыс. населения;
в странах Азии, Центральной Америки, Африки — не более 5 случаев на 100 тыс. населения.
В Армении – 3,75 на 100 тыс. населения (В.Дарбинян, 1982)
Слайд 10Эпидемиология РС
Изучение миграции (Израиль) показало, что лица, переехавшие из зоны
высокого риска в зону низкого риска до 15-летнего возраста, болеют
рассеянным склерозом значительно реже, чем это имеет место на их родине. Напротив, лица, мигрировавшие в возрасте старше 15 лет, сохраняют такую же возможность заболеть РС, как и на родине.
Комбинация экзогенных и эндогенных факторов:
Экзогенные (вирусы, географический фактор)
Эндогенные (генетическая предрасположенность)
Слайд 11Рассеянный склероз - мультифакториальная болезнь:
Экзогенные фак-ры
Вирусы
Корь
Миксавирусы
Пикарновирусы
Прионы (?)
Радиация
Микроэлементы почвы и воды
Эндогенные
фак-ры
Генетическая предрасположенность
HLA-B7
HLADR3
Daffy
Kidd-Chellano
Комбинация экзогенных и эндогенных факторов
Слайд 12Гипотеза патогенеза демиелинизации
вирусная инфекция
активация аутореактивных Т-клеток
Атака на антигены миелина
Демиелинизация
HLA-опосредованный
дефект
Слайд 13Гипотеза патогенеза демиелинизации
Активизированные Т-клетки проникают через ГЭБ и атакуют антиген-представляющие
клетки, в качестве которых выступают макрофаги и клетки глии. Последние
поглощают антигены на своей мембране в комплексе с HLA-молекулами 2-го комплекса, которые, соединяясь с рецептором Т-клетки, служат главным звеном в развитии аутоиммунного процесса при рассеянном склерозе. Происходит еще большая активация Т-клеток и их миграция в очаг поражения.
Слайд 14Гипотеза патогенеза демиелинизации
Этот процесс сопровождается выделением цитокинов провоспалительного характера —
фотоксина, интерферона, фактора некроза опухоли (ФНО). Нарушается проницаемость гематоэнцефалического барьера
(ГЭБ), активируются В-клетки и составляющие гуморального иммунитета, система комплемента, а также макрофаги. Результатом этой воспалительной реакции является разрушение миелина и олигодендроглиоцитов, в процессе которого и происходит формирование бляшки.
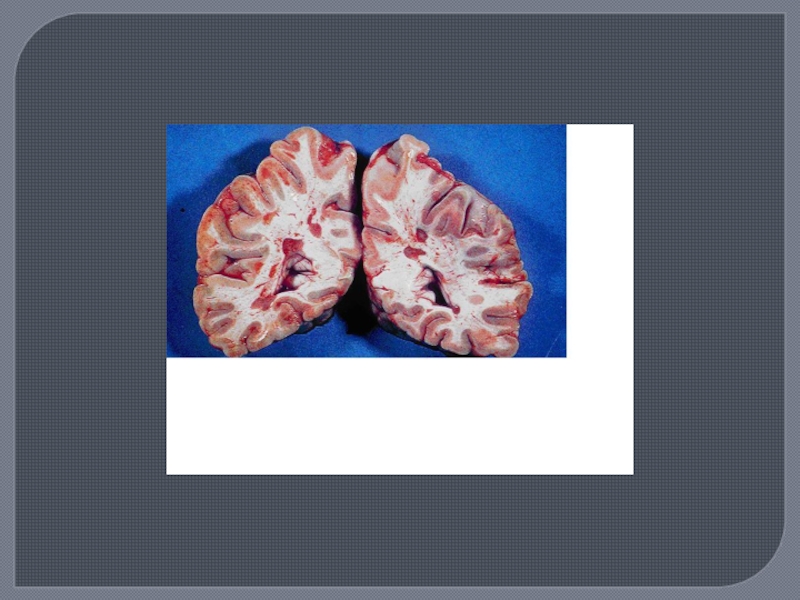
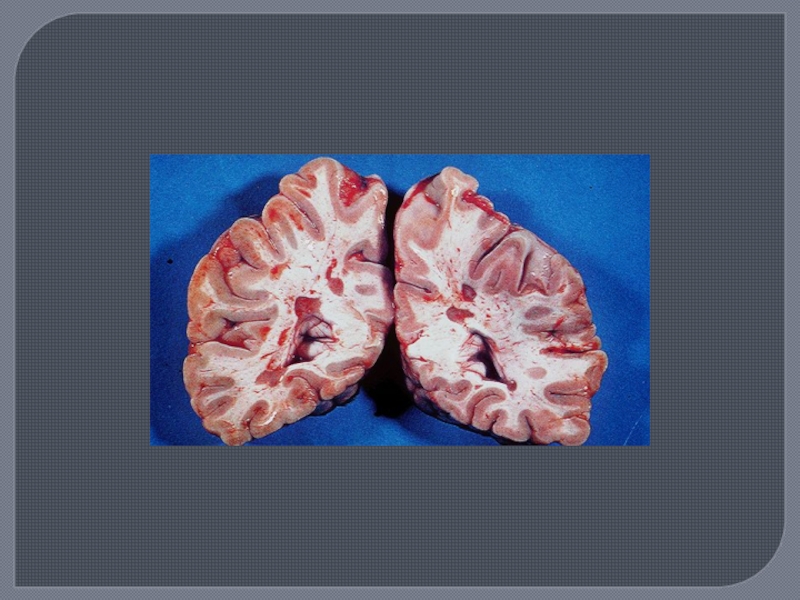
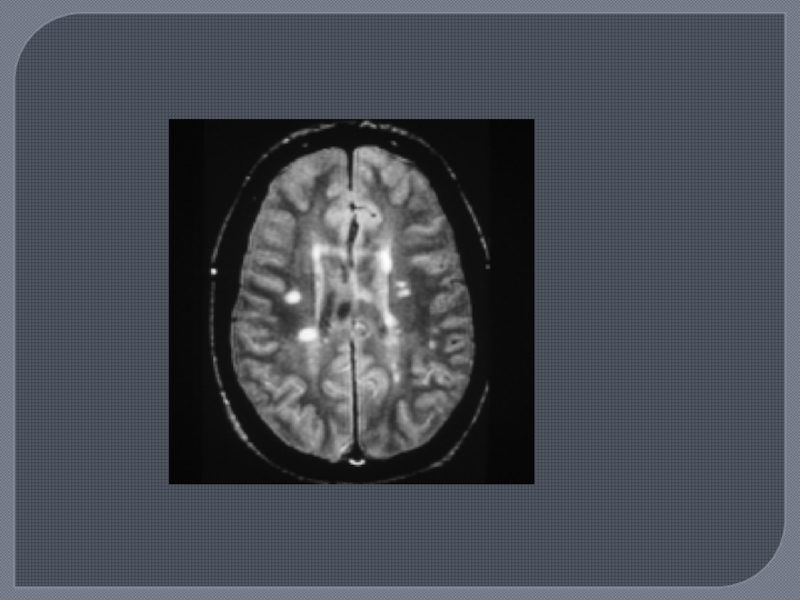
Слайд 15Патологоанатомическая картина РС
Множественные очаговые повреждения различных отделов ЦНС, в основе
которых лежат процессы демиелинизации в сочетании с гибелью олигоглиоцитов при
длительной сохранности осевого цилиндра нервного волокна. Сочетание демиелинизации с реактивными изменениями других элементов — пролиферацией волокнистых астроцитов приводит к образованию своеобразных очагов, которые называют «бляшками» рассеянного склероза.
Реже в процесс вовлекается периферическая нервная система (менее 5%).
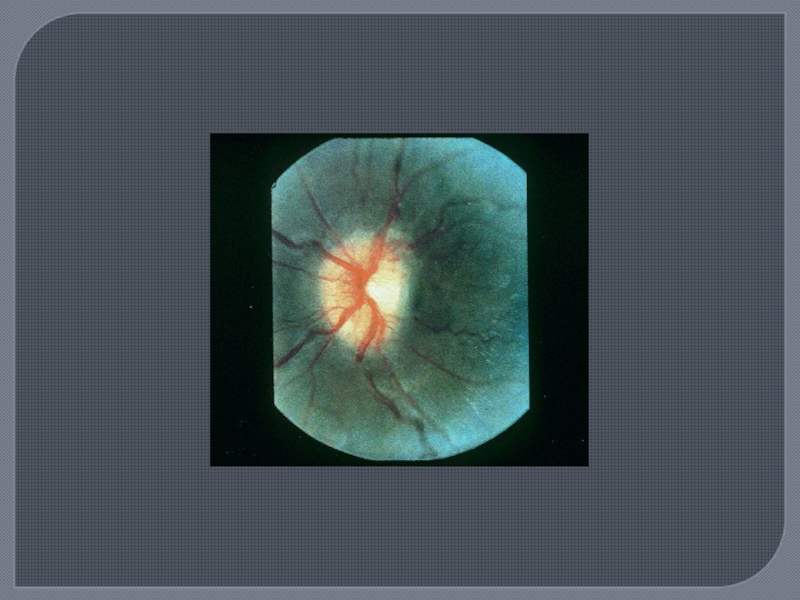
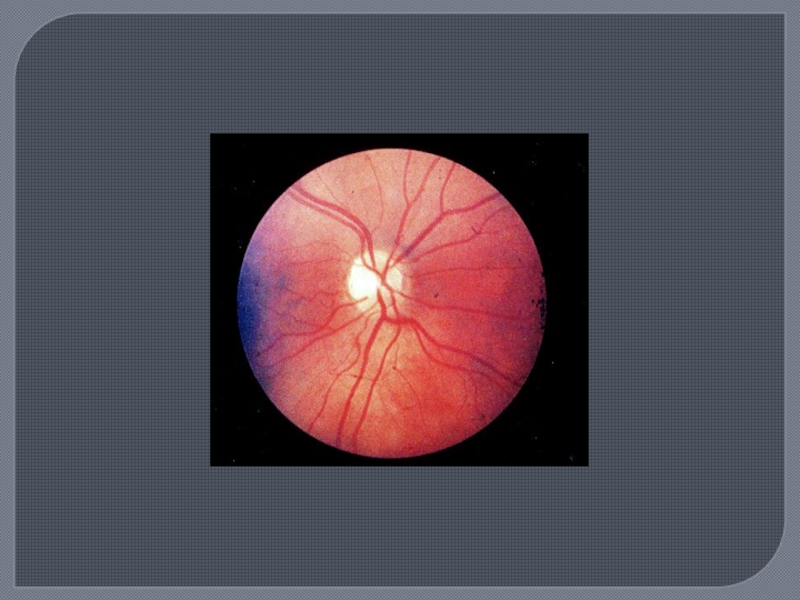
Слайд 16Демиелинизация оптического перекреста
Слайд 20Патофизиология РС
Основной патофизиологический механизм, вызывающий клинический «феномен расщепления» - механизм
эфаптической передачи импульса
Нормальная синаптическая передача
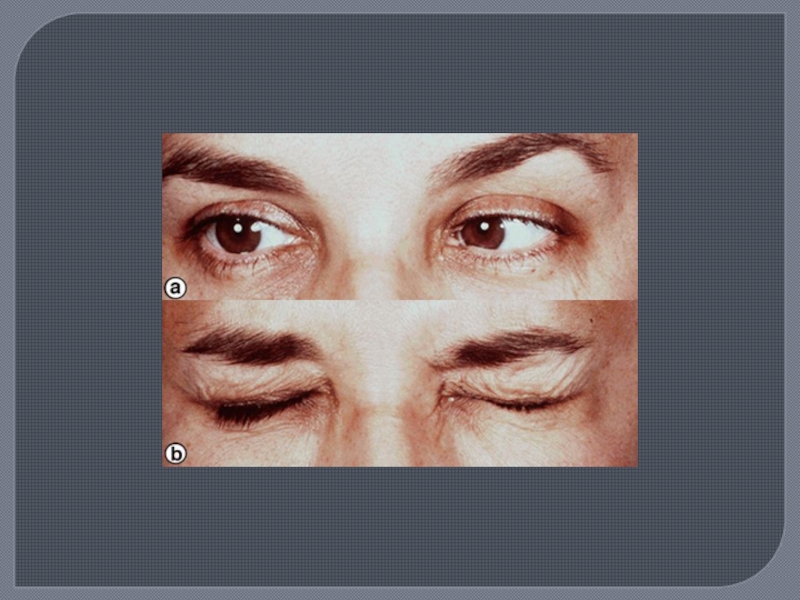
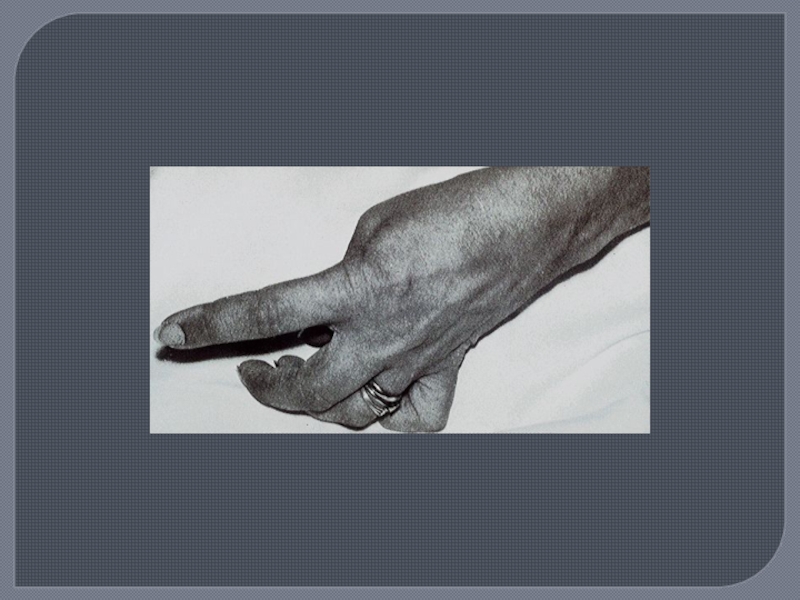
Слайд 21Клиническая картина
Чрезвычайный полиморфизм объясняется случайностью распределения демиелинизации. Дебют заболевания одинаково
часто бывает поли- и моносимптомным. Наиболее частые проявления в дебюте:
Моторные
нарушения (слабость в ногах);
Парестезии.
Координаторные нарушения (шаткая походка, головокружение, рвота, нистагм).
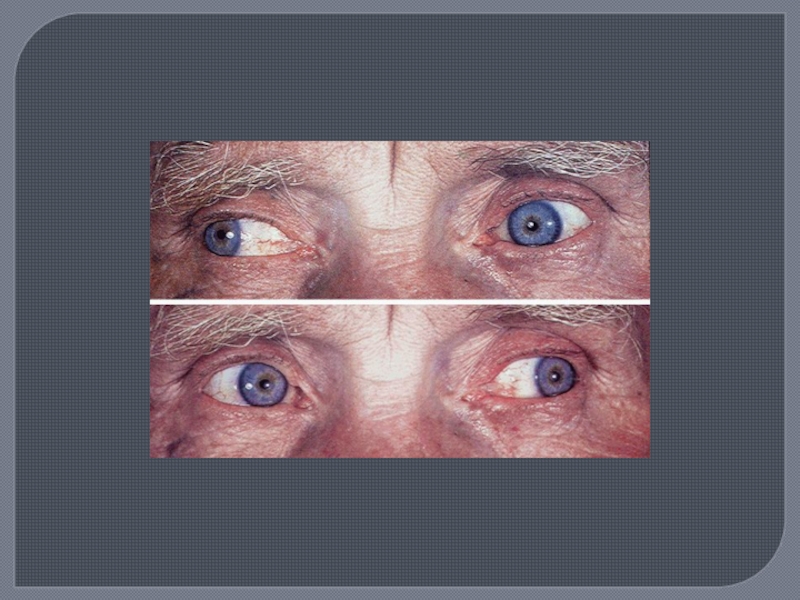
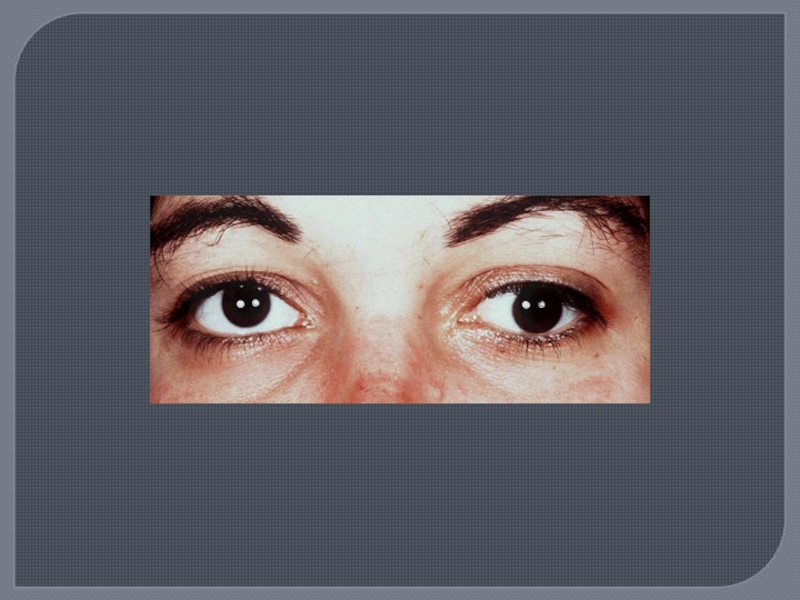
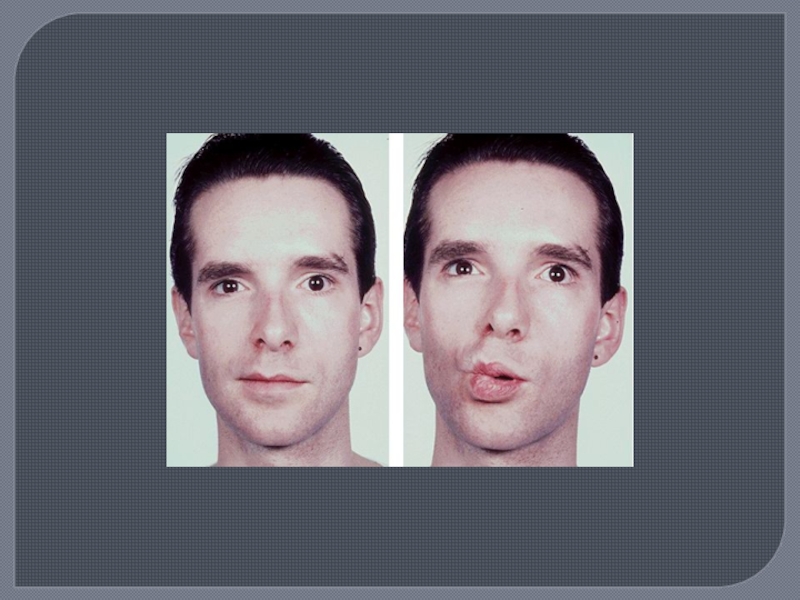
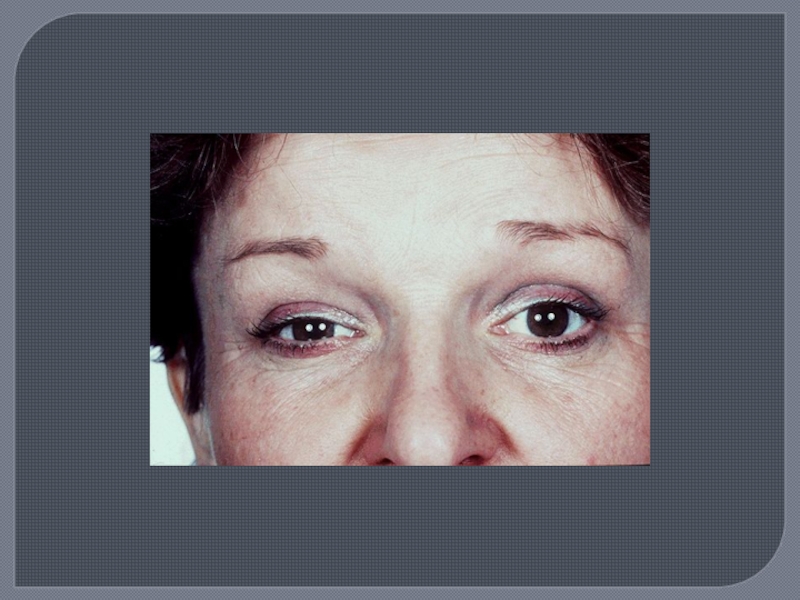
Поражение ЧМН, ( особенно часто зрительный нерв - ретробульбарный неврит, скотомы); отводящий нерв, глазодвигательный, что проявляется диплопией. В начале заболевания часты поражения лицевого и тройничного нервов.
Часто уже в начале заболевания может быть нарушена функция тазовых органов.
Слайд 22Клиническая картина
У многих больных при длительном течении болезни развиваются когнитивные
нарушения. Наблюдаются также эмоциональная лабильность, эйфория, некритичное отношение к своему
состоянию. Реже определяются тяжелые психические расстройства.
Слайд 23Типичные формы РС
Цереброспинальная форма характеризуется выраженными симптомами поражения как головного,
так и спинного мозга;
Церебральная форма рассеянного склероза характеризуется в основном
глазодвигательными, зрительными, мозжечковыми и стволовыми нарушениями;
При спинальной форме чаще наблюдается нижний спастический парапарез с нарушением функции тазовых органов, реже отмечаются расстройства чувствительности на ногах.
Слайд 31Клинические варианты рассеянного склероза
Острый рассеянный склероз
Хронический рецидивирующий энцефаломиелитический вариант
Оптикомиелит (болезнь
Девик)
Рецидивирующий ретробульбарный неврит
Слайд 32Клинические «формы» рассеянного склероза
Классическая цереброспинальная форма
Церебральная
Спинальная
Мозжечковая
«Проскакивающая»
«Высокая» форма
И т.д.
Понятие «Атипичная
форма РС»
Слайд 34Диагноз РС
Остается клиническим (Критерии комиссии Shumaker and McAlpin, 1985)
Дебют заболевания
от 15 до 50 лет
Наличие не менее 3 атак и
ремиссии
Наличие не менее чем самостоятельных 3 очагов поражения
Исключение других заболеваний (васкулиты, накопительные заболевания, факоматозы и др.)
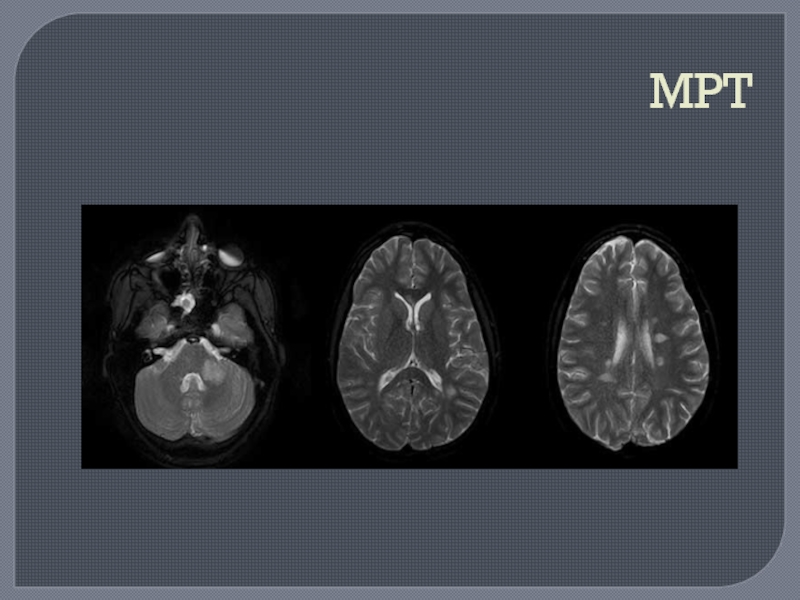
Лабораторные методы диагностики:
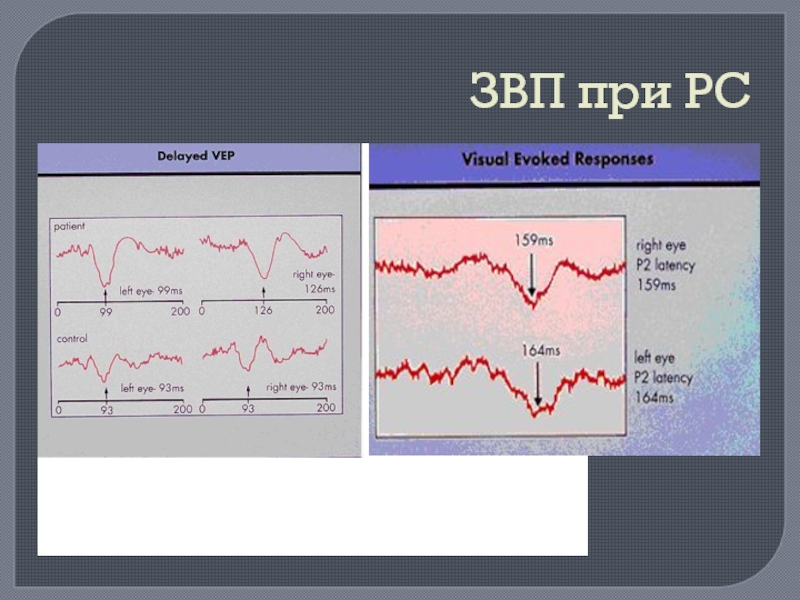
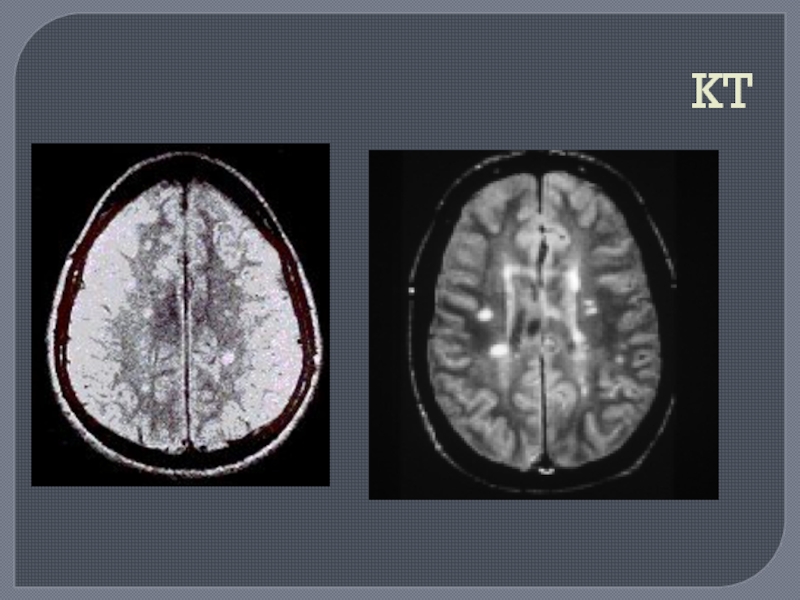
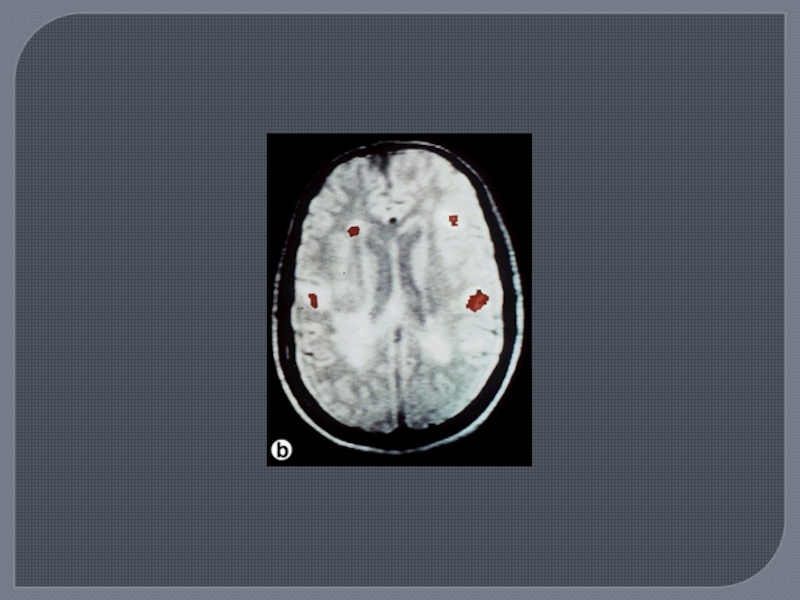
методы выявления субклинических очагов демиелинизации (МРТ, КТ, ВП);
методы, позволяющие судить об активности патологического процесса (олигоклониальные иммуноглобулины G в СМЖ).
Слайд 44Poser’s criteria for the diagnosis of
MS
Clinically definite MS
A1: 2 Attacks
2 lesions on examination
A2: 2 Attacks 1 lesion on examination
1 paraclinical
lesion
Laboratory-supported definite MS
B1: 2 Attacks 1 lesion on examination or 1 paraclinical
lesion abnormal CSF
B2: 1 Attack 2 lesions on examination abnormal CSF§
B3: 1 Attack 1 lesion on examination 1 paraclinical
lesion‡ abnormal CSF
Clinically probable MS
C1: 2 Attacks 1 lesion on examination
C2: 1 Attack 2 lesions on examination
C3: 1 Attack 1 lesion on examination 1 paraclinical
lesion
Слайд 45Diagnostic considerations in patients with suspected
MS or MRI white matter
abnormalities
Age-related white matter changes
Acute disseminated encephalomyelitis
Behc~et disease
Bacterial infections (syphilis, Lyme
disease)
Cerebral autosomal dominant arteriopathy, subcortical infarcts,and leukoencephalopathy
Cervical spondylosis or stenosis
HIV infection
Human T-lymphotrophic virus I/II
Ischemic optic neuropathy (arteritic and nonarteritic)
Leukodystrophies (e.g., adrenoleukodystrophy, metachromatic
leukodystrophy)
Слайд 46Diagnostic considerations in patients with suspected
MS or MRI white matter
abnormalities
Neoplasms (e.g., lymphoma, glioma, meningioma)
Migraine
Sarcoid
Sjo¨gren syndrome
Stroke and ischemic cerebrovascular disease
Systemic
lupus erythematosus, antiphospholipid antibody syndromes, and related collagen vascular disorders
Unidentified bright objects
Vascular malformations
Vasculitis (primary CNS or other)
Vitamin B12 deficiency
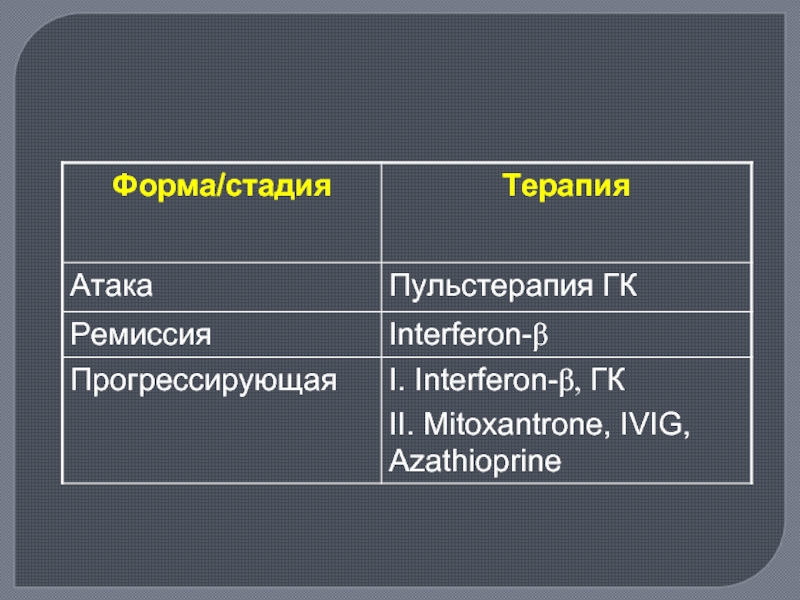
Слайд 47Лечение
Этиотропной терапии нет
Патогенетическая терапия
Иммуносупрессия
Глюкокортикостероиды
Цитостатики
Плазмаферез
Иммуномодуляция
Интерферон (копаксон и бетаферон)
Симптоматическая терапия
Слайд 50Glucocorticoids:
1. On the basis of several and generally consistent Class
I and
Class II studies, glucocorticoid treatment has been demonstrated
to have
a short-term benefit on the speed of functional
recovery in patients with acute attacks of MS. It is
appropriate, therefore, to consider for treatment with glucocorticoids
any patient with an acute attack of MS (Type A
recommendation).
2. There does not appear, however, to be any long-term functional
benefit after the brief use of glucocorticoids in this
clinical setting (Type B recommendation).
3. Currently, there is not compelling evidence to indicate that
these clinical benefits are influenced by the route of glucocorticoid
administration, the particular glucocorticoid prescribed,
or the dosage of glucocorticoid, at least at the doses
that have been studied to date (Type C recommendation).
4. On the basis of a single Class II study, it is considered possible
that regular pulse glucocorticoids may be useful in the
long-term management of patients with RRMS (Type C
recommendation)
Слайд 51Interferon beta:
1. On the basis of several consistent Class I
studies, IFN has
been demonstrated to reduce the attack rate (whether
measured clinically or by MRI) in patients with MS or with
clinically isolated syndromes who are at high risk for developing MS (Type A recommendation). Treatment of MS with IFN produces a beneficial effect on MRI measures of disease severity such as T2 disease burden and probably also slows sustained disability progression (Type B recommendation).
2. As a result, it is appropriate to consider IFN for treatment
in any patient who is at high risk for developing CDMS, or
who already has either RRMS or SPMS and is still experiencing relapses (Type A recommendation). The effectiveness of IFN in patients with SPMS but without relapses is uncertain
(Type U recommendation).
Слайд 523. It is possible that certain populations of MS patients
(e.g.,those with more attacks or at earlier disease stages) may
be better candidates for therapy than others, although, at the moment, there is insufficient evidence regarding these issues (Type U Recommendation)
4. On the basis of Class I and II studies and several pieces of consistent Class III evidence, it is considered probable that there is a dose-response curve associated with the use of IFN for the treatment of MS (Type B recommendation). It is possible, however, that a portion of this apparent dose-effect instead may be due to differences in the frequency of IFN administration (rather than dose) between studies.
Слайд 535. On the basis of several Class II studies, the
route of administration
of IFN is probably not of clinical importance,
at least with regard to efficacy (Type B recommendation). The side-effect profile, however, does differ between routes of administration. There is no known clinical difference between the different types of IFN, although this has not been thoroughly studied (Type U recommendation).
6. On the basis of several Class I studies, treatment of patients with MS with IFN is associated with the production of Nab (Type A recommendation). The rate of NAb production, however, is probably less with IFN-1a treatment than with IFN-1b treatment (Type B recommendation). The biologic effect of NAb is uncertain, although their presence may be associated with a reduction in clinical effectiveness of IFN treatment (Type C recommendation). Whether there is a difference in immunogenicity between subcutaneous and intramuscular routes of administration is unknown (Type U recommendation). The clinical utility of measuring NAb in an individual on IFN therapy is uncertain