Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
митоз
Содержание
- 1. митоз
- 2. MAVZUNING MAQSADI:Eritmalar nazariyasi bilan tanishtirib, gazlarning suyuqlikda
- 3. KO’RILADIGAN MASALALAR Bioanorganik va fizkolloid
- 4. KO’RILADIGAN MASALALARDiffuziya hodisasiOsmos va osmotik bosimIdeal eritmalarning
- 5. Genri qonuniα= K ⋅ P -
- 6. Eruvchanlikni begona moddalar mavjudligiga bog’liqligi. Sechenov qonuniSechenov
- 7. Eritmalarning kolligativ hossalariEritmalarning osmotik bosimiEritmalarning to’yingan bug’
- 8. Osmos hodisasi yuz berayotgan sistemaErituvchi molekulalarining yarim o’tkazgich membrana orqali bir tomonlana diffuziyasi osmos deyiladi
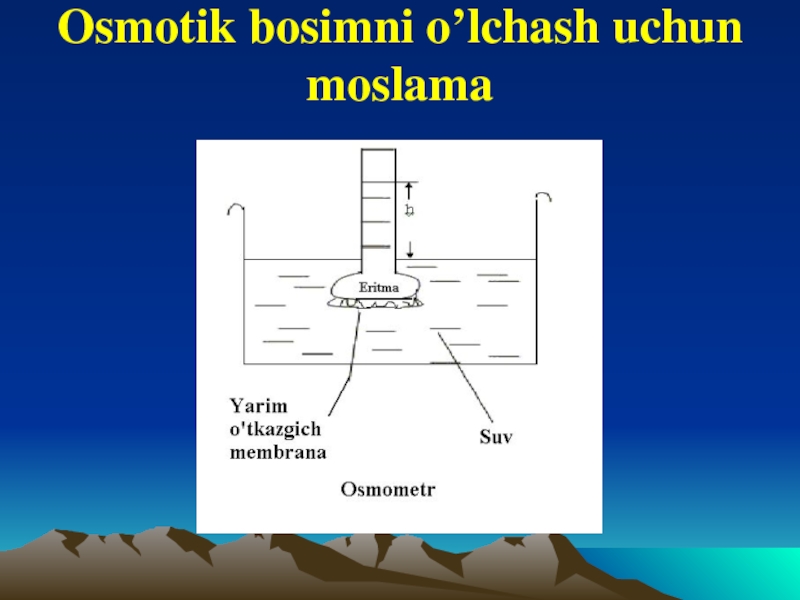
- 9. Osmotik bosimni o’lchash uchun moslama
- 10. Osmotik bosim. Vant-Goff qonuniDiffuziya tufayli erituvchi molekulalarining
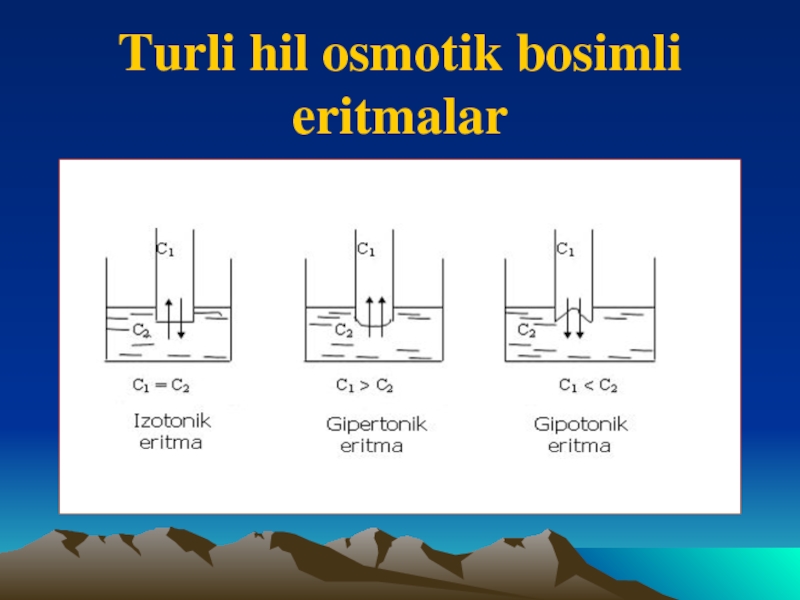
- 11. Turli hil osmotik bosimli eritmalar
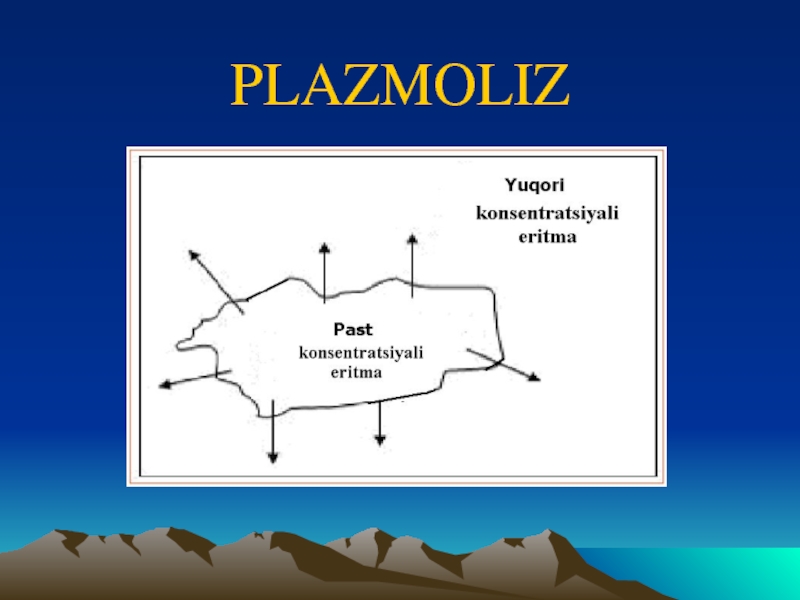
- 12. PLAZMOLIZ
- 13. GEMOLIZ
- 14. Raul qonunlari P0-P
- 15. Ebulioskopiya qonuniEritmaning qaynash haroratini ortishi erigan moddaning
- 16. Krioskopiya qonuniEritmaning muzlash haroratini pasayishi erigan moddaning
- 17. Скачать презентанцию
MAVZUNING MAQSADI:Eritmalar nazariyasi bilan tanishtirib, gazlarning suyuqlikda erishi qanday omillarga bog’liqligini ko’rsatish va shu bog’liqliklarni ifodalash uchun qanday qonunlarga asoslanish kerakligini tushinib yetish. Eritmalar ahamiyatini biologik eritmalar misolida ko’rib chiqish.
Слайды и текст этой презентации
Слайд 2MAVZUNING MAQSADI:
Eritmalar nazariyasi bilan tanishtirib, gazlarning suyuqlikda erishi qanday omillarga
Слайд 3KO’RILADIGAN MASALALAR
Bioanorganik va fizkolloid kimyo fani va
uninng vazifalari
Bioanorganik va fizkolloid kimyo fanining tibbiyotdagi ahamiyati
Eritmalar va
eritmalarning umumiy hossalariEruvchanlik va eruvchanlikka ta’sir etuvchi omillar
Kuchli va kuchsiz elektrolitlarning hossalari
Eritmalarning kolligativ hossalari
Diffuziya hodisasi
Слайд 4KO’RILADIGAN MASALALAR
Diffuziya hodisasi
Osmos va osmotik bosim
Ideal eritmalarning osmotik bosimini Mendeleyev-Klayperon
tenglamasidan foydalanib hisoblash
Onkotik bosim
Eritma ustidagi bug’ bosimi va Raul qonunlari
Kislota
va asoslarning protolitik nazariyasiSuvning ionli ko’paytmasi, vodorod va gidroksid ko’rsatkichlari
Слайд 5Genri qonuni
α= K ⋅ P
- absorbtsiya koeffitsienti
P –
gazning bosimi
K – gazning tabiatiga bog’liq doimiy
Genri-Dalton qonuni αi = Ki ⋅ Pi
αI - absorbtsiya koeffitsienti
Pi– gazning parsial bosimi
Ki – gazning tabiatiga bog’liq doimiy
Слайд 6Eruvchanlikni begona moddalar mavjudligiga bog’liqligi. Sechenov qonuni
Sechenov qonuni: Erigan moddalarning
mavjudligi gazlarning suvdagi eruvchanligini kamaytiradi: N
--------- = n N0
Слайд 7Eritmalarning kolligativ hossalari
Eritmalarning osmotik bosimi
Eritmalarning to’yingan bug’
bosimining pasayishi
Eritmalarning muzlash haroratini
pasayishi
Eritmalarning qaynash haroratini
ko’tarilishi
Слайд 8
Osmos hodisasi yuz berayotgan sistema
Erituvchi molekulalarining yarim o’tkazgich membrana orqali
bir tomonlana diffuziyasi osmos deyiladi
Слайд 10Osmotik bosim. Vant-Goff qonuni
Diffuziya tufayli erituvchi molekulalarining idish devorlariga ko’rsatayotgan
bosimi osmotik bosim deuiladi.
Vant-Goff qonuni: osmotik bosim erigan modda konsentratsiyasiga
to’g’ri proporsionalπ = CRT - noelektrolitlar eritmalari uchun
π = ιCRT - elektrolitlar eritmalari uchun
bu erda: π - osmotik bosim, C - eritma konsentratsiyasi, R -universal gaz doimiysi
T - absolut harorat, ι - izotonik koeffitsient
Слайд 14Raul qonunlari
P0-P n
P0-P
n-------- = -------- yoki --------- = ------
P0 n + N P0 N
Bu erda: P0 - sof erituvchi ustidagi to’yingan bug’ bosimi
P - eritma ustidagi bug’ bosimi
n, N - erigan modda va erituvchining modda
miqdori
Слайд 15Ebulioskopiya qonuni
Eritmaning qaynash haroratini ortishi erigan moddaning molal konsentratsiyasiga to’g’ri
proporsional:
tqayn. = E . mBu yerda: tqayn. - qaynash haroratining
ortishi;
E - ebulioskopik doimiy
m - eritmaning molal
konsentratsiyasi
Слайд 16Krioskopiya qonuni
Eritmaning muzlash haroratini pasayishi erigan moddaning molal konsentratsiyasiga to’g’ri
proporsional:
tmuzlash. = K . mBu yerda: tmuzlash. - muzlash haroratining
pasayishi;
K - krioskopik doimiy
m - eritmaning molal
konsentratsiyasi
Теги