Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биохимия
Содержание
- 1. Биохимия
- 2. 08/12/2019Коваль А. Н. (С)Кафедра биохимии Гомельского государственного
- 3. 08/12/2019Коваль А. Н. (С)Структура курса1-е полугодиеВведение в
- 4. 08/12/2019Коваль А. Н. (С)Лекция 1Введение в биохимию. Значение биохимии для врача. Химия белка.
- 5. 08/12/2019Коваль А. Н. (С)Введение в биохимиюБиохимия -
- 6. 08/12/2019Коваль А. Н. (С)История биохимииПредставления античных философов
- 7. 08/12/2019Коваль А. Н. (С)История развития отечественной биохимии
- 8. 08/12/2019Коваль А. Н. (С)Выдающиеся представители отечественной биохимии
- 9. 08/12/2019Коваль А. Н. (С)Выдающиеся представители отечественной биохимии
- 10. 08/12/2019Коваль А. Н. (С)Предмет и задачи биохимии.Познание
- 11. 08/12/2019Коваль А. Н. (С)Разделы биохимииСтатическая биохимия -
- 12. 08/12/2019Коваль А. Н. (С)Разделы биохимии по
- 13. 08/12/2019Коваль А. Н. (С)Разделы биохимии по объекту
- 14. 08/12/2019Коваль А. Н. (С)Методы биохимических исследований.Исследование на
- 15. 08/12/2019Коваль А. Н. (С)Методы биохимических исследований (продолжение)Изучение
- 16. 08/12/2019Коваль А. Н. (С)Химия белкаБелки - высокомолекулярные
- 17. 08/12/2019Коваль А. Н. (С)20 протеиногенных аминокислотГлицин (гли)Гистидин
- 18. 08/12/2019Коваль А. Н. (С)Отрицательно заряженные аминокислотыАсп Asp, DГлу Glu, EАспарагиновая кислотаГлутаминовая кислота
- 19. 08/12/2019Коваль А. Н. (С)Положительно заряженные аминокислоты АргининГистидинЛизинАрг Arg, RГис His, HЛиз Lys, K
- 20. 08/12/2019Коваль А. Н. (С)Полярные аминокислоты, которые могут приобретать отрицательный зарядЦистеинТирозинЦис Cys, CТир Tyr, Y
- 21. 08/12/2019Коваль А. Н. (С)Объемные модели 11 полярных аминокислотАспГлуТирЦисАргЛизГисСерАснГлн
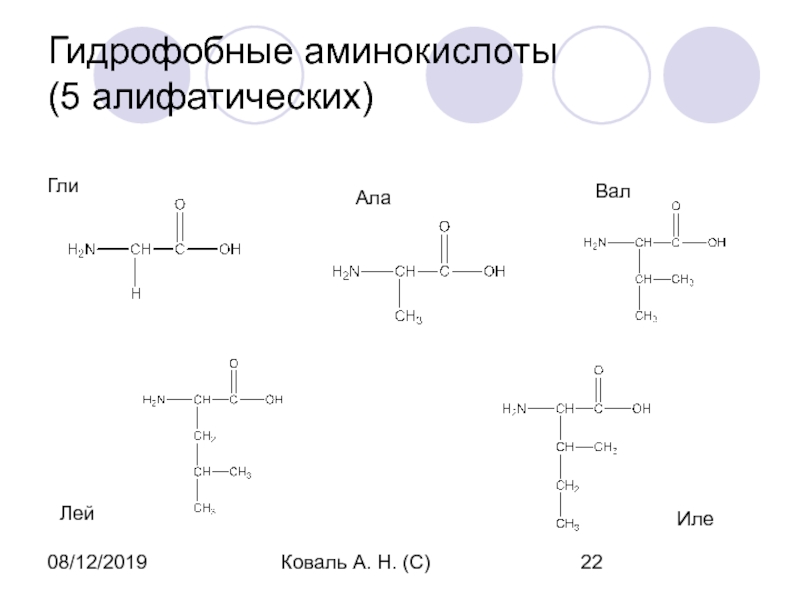
- 22. 08/12/2019Коваль А. Н. (С)Гидрофобные аминокислоты (5 алифатических)ГлиАлаВалЛейИле
- 23. 08/12/2019Коваль А. Н. (С)Гидрофобные аминокислоты (4
- 24. 08/12/2019Коваль А. Н. (С)История химии белка1728 г.
- 25. 08/12/2019Коваль А. Н. (С)Эвристическая идея Э. ФишераБелки
- 26. 08/12/2019Коваль А. Н. (С)Структурная организация белковой молекулыВыделяют
- 27. 08/12/2019Коваль А. Н. (С)Первичная (одномерная, линейная) структурапорядок
- 28. 08/12/2019Коваль А. Н. (С)Пример: пептид ангиотензин-2, повышающий давлениеH2N-asp-arg-val-tyr-ile-his-pro-phe-COOH
- 29. 08/12/2019Коваль А. Н. (С)Особенности пептидной связиНаличие плоской
- 30. 08/12/2019Коваль А. Н. (С)Особенности пептидной связи (продолжение)Атомы,
- 31. 08/12/2019Коваль А. Н. (С)Мезомерия пептидной связиКето- (лактимная)Енол- (лактамная)
- 32. 08/12/2019Коваль А. Н. (С)Конформация полипептидной цепиПептидная связь
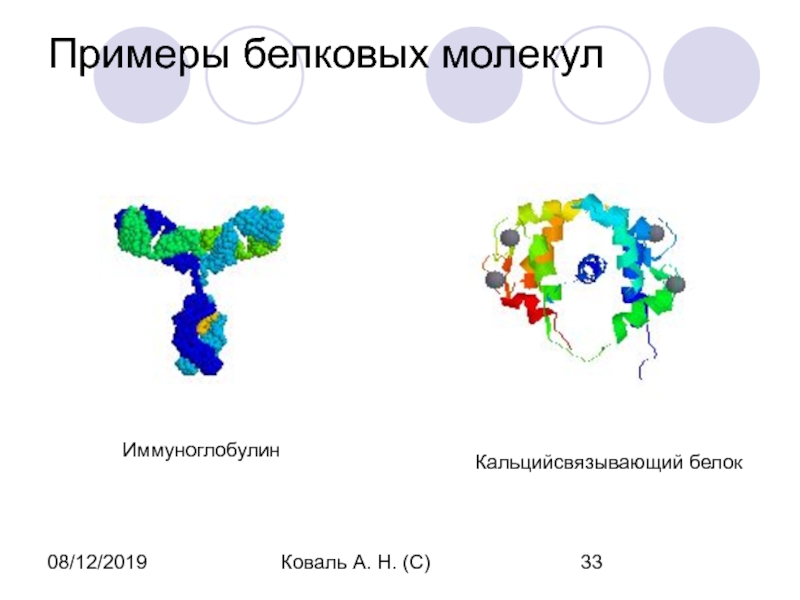
- 33. 08/12/2019Коваль А. Н. (С)Примеры белковых молекулИммуноглобулинКальцийсвязывающий белок
- 34. 08/12/2019Коваль А. Н. (С)Динамика белковой молекулы
- 35. 08/12/2019Коваль А. Н. (С)Вторичная (двухмерная, пространственная) структураα-спиральБета-структура (β–складчатый слой)
- 36. 08/12/2019Коваль А. Н. (С)Характеристика альфа-спиралиВысота витка 0,54
- 37. 08/12/2019Коваль А. Н. (С)Характеристика бета-структурыВытянутые полипептидные цепи
- 38. 08/12/2019Коваль А. Н. (С)Другие разновидности вторичной структурыКроме
- 39. 08/12/2019Коваль А. Н. (С)Соотношение структур в белках α-белки:миоглобин,
- 40. 08/12/2019Коваль А. Н. (С)Третичная структураТретичная структура –
- 41. 08/12/2019Коваль А. Н. (С)Доменная организация белкаДомен -
- 42. 08/12/2019Коваль А. Н. (С)Четвертичная структура белкаЧетвертичная структура
- 43. 08/12/2019Коваль А. Н. (С)Пятый уровень органицации белковой
- 44. 08/12/2019Коваль А. Н. (С)Форма, размеры и масса
- 45. 08/12/2019Коваль А. Н. (С)Конец первой лекции «Введение в биохимию»Следующая лекция: «Ферменты»Спасибо за внимание!
- 46. Скачать презентанцию
Слайды и текст этой презентации
Слайд 108/12/2019
Коваль А. Н. (С)
ГРИЦУК Александр Иванович
д-р мед.наук, профессор,
зав.
каф. биохимии Гомельского государственного медицинского университета
н., доцент каф. биохимииСлайд 208/12/2019
Коваль А. Н. (С)
Кафедра биохимии Гомельского государственного медицинского университета
Грицук Александр
Иванович – заведующий кафедрой биохимии, д. м. н., профессор.
Свергун Валентина
Тимофеевна – доцент,
к. б. н.Коваль Александр Николаевич – доцент, к. б. н.
Сергеенко Сергей Михайлович – ассистент.
Шершнева Екатерина Михайловна – ассистент.
Яськова Надежда Сергеевна – аспирант.
Громыко Марина Владимировна – лаборант 2-й кат.
Безрукова Елена Владимировна – лаборант.
Бордиенко Светлана Олеговна – лаборант 2-й кат.
Даргель Ирина Витальневна – лаборант.
Слайд 308/12/2019
Коваль А. Н. (С)
Структура курса
1-е полугодие
Введение в биохимию
(1 пр.
зан.)
Энзимология и биоэнергетика
(5 пр. зан., + контр.)
Биохимия углеводов
(4
пр. зан. + контр.)Биохимия липидов (3 пр. зан. + контр.)
Зачетное занятие семестра.
2-е полугодие
Биохимия белков и нуклеиновых кислот.
Биохимия витаминов и гормонов.
(8 пр. зан. + контр.)
Биохимия крови, печени, почек. Биохимия мышечной, нервной и соединительной тканей
(7 пр. зан. + контр.)
Зачетное занятие семестра.
Слайд 408/12/2019
Коваль А. Н. (С)
Лекция 1
Введение в биохимию. Значение биохимии для
врача. Химия белка.
Слайд 508/12/2019
Коваль А. Н. (С)
Введение в биохимию
Биохимия - это наука, изучающая
качественный и количественный состав, а также пути, способы, закономерности, биологическую
и физиологическую роль превращения вещества, энергии и информации в живом организме.Термин «биохимия» впервые применил в 1858 г. австрийский врач и химик Винцент Клетцинскй в своей книге «Компендиум по биохимии».
В то же время использовался другой термин – физиологическая химия.
Окончательно термин «биохимия» был введен Карлом Нейбергом в 1903 г.
Слайд 608/12/2019
Коваль А. Н. (С)
История биохимии
Представления античных философов (Аристотель, Платон)
VI-X вв.
– развитие в Европе алхимии
XVI-XVII вв. – ятрохимия (Парацельс), виталистические
взглядыСередина XVII – конец XVIII вв. – эмпирический период
конец ХVIII – середина ХIХ вв. – аналитический период
1828 г. - Ф. Велер впервые синтезировал мочевину
1839 г. – Ю. Либих установил, что в состав пищи входят белки, жиры и углеводы.
1845 г. - Г. Кольбе синтезировал уксусную кислоту
1847 г. – А.И. Ходнев издал первый учебник по физиологической химии
1854 г. - М. Бертло синтезировал жиры.
1861 г. - А.М. Бутлеров синтезировал углеводы.
1864 г.- А.Я. Данилевский основал первую кафедра физиологической химии при Казанском университете.
XX в. – современный период
20-30-е годы – развитие биохимии углеводов и липидов
30-е годы – развитие биохимии гормонов и витаминов.
40-50 годы – биохимия нуклеиновых кислот и белков.
Слайд 708/12/2019
Коваль А. Н. (С)
История развития отечественной биохимии (Россия).
1847 г. –
А.И. Ходнев – первый учебник по физиологической химии
1864 г. –
А.Я. Данилевский – первая кафедра физиологической химии при Казанском университете.1891 г. – М.В. Ненцкий – первая биохимическая лаборатория в Институте экспериментальной медицины (Петербург).
1880 г. – Н.И. Лунин – открытие витаминов.
28 апреля 1883 г. в Санкт-Петербурге было основано первое в мире биохимическое (биолого-химическое) общество, основателями которого было 16 человек: Н.Н. Лунин, Э. Эйхвальд, В. Анреп, К. Дегио, И. Биль, А. Пель, Р. Штерн, Фр. Лесгафт и др.
1896 г. – А.Н. Бах – создание теории перекисного окисления.
1899 г. – И.П. Павлов, Н.П. Шеповальников – открытие проферментов.
1903 г. – М.С. Цвет – открытие метода хроматографии
1912 г. – В.И. Палладин – создание теории биологического окисления.
Слайд 808/12/2019
Коваль А. Н. (С)
Выдающиеся представители отечественной биохимии (Россия)
Российская школа биохимиков
А.Н.
Бах
1921 г. организовал в Москве Научно-исследовательский биохимический институт Наркомздрава.
1935
г. – А.Н. Бах - возглавил в Москве Институт биохимии АН СССР, названный впоследствии его именем.А.И. Опарин - автор первой теории происхождения жизни.
Акад. В.А. Энгельгардт
В 1959 г. – основал Институт молекулярной биологии АН СССР
Автор классических работ по окислительному фосфорилированию, механохимии мышц, углеводному обмену и др.
Акад. Ю.А. Овчинников – работы в области мембранной биологии.
Акад. А.С. Спирин – работы по молекулярным механизмам биосинтеза белка.
Акад. В.П. Скулачев – работы по биоэнергетике.
Слайд 908/12/2019
Коваль А. Н. (С)
Выдающиеся представители отечественной биохимии (продолжение)
Белорусская школа биохимиков
Акад.
Ю.М. Островский – работы в области витаминов (Институт биохимии АН
РБ, г. Гродно).Украинская школа биохимиков
Акад. А.В. Палладин – работы в области нейрохимии и витаминов,
Работы в области биохимии белкового, липидного обмена, возрастной биохимии.
Слайд 1008/12/2019
Коваль А. Н. (С)
Предмет и задачи биохимии.
Познание молекулярных механизмов физиологических,
генетических и иммунологических процессов жизнедеятельности в норме и при патологии
и действии на организм различных факторов.Совершенствование методов профилактики, диагностики и лечения заболеваний.
Разработка новых лекарственных средств, нормализующих обменные процессы.
Разработка научных основ, рационального, сбалансированного питания, здорового образа жизни.
Слайд 1108/12/2019
Коваль А. Н. (С)
Разделы биохимии
Статическая биохимия - исследует качественные и
количественный химический состав живых организмов.
Динамическая биохимия - изучает совокупность превращений
веществ, энергии и информации в живом организме.Функциональная биохимия - изучает химическую основу функций тканей, органов, систем органов и межорганных взаимоотношений.
Слайд 1208/12/2019
Коваль А. Н. (С)
Разделы биохимии
по объекту исследования
общая биохимия
изучает
общие вопросы химических основ жизнедеятельности различных организмов
бионеорганическая химия
изучает роль
и значение в процессе жизнедеятельности комплексов неорганических ионов с органическими соединениямибиоорганическая химия
исследует физико-химические основы функционирования живых систем
биохимия человека и животных, (растений, микроорганизмов)
Слайд 1308/12/2019
Коваль А. Н. (С)
Разделы биохимии по объекту исследования (продолжение)
техническая биохимия
изучает состав пищевых продуктов, химическую основу технологических процессов их хранения,
переработки и т.д.сравнительная (эволюционная) биохимия
исследует биохимические процессы в сравнительном (эволюционном) аспекте
радиационная биохимия
изучает биохимические основы радиационного повреждения и способы его профилактики в живой организме
медицинская (клиническая) биохимия
исследует биохимические основы патологических процессов
физико-химическая биология
объединяет цели и задачи всех вышеназванных направлений биохимии
Слайд 1408/12/2019
Коваль А. Н. (С)
Методы биохимических исследований.
Исследование на уровне целого организма
удаление
органа (гепатэктомия)
изменение диеты (голодание, усиленное питание)
прием лекарств
введение токсинов
наблюдение за животными
со специфическими заболеваниями (сахарный диабет)использование сложным методов (ЯМР-спектроскопия и др.)
Перфузия изолированных органов
наиболее пригодны сердце, печень, почки
Инкубация тканевых срезов
чаще используются срезы печени
Инкубация целых клеток
наиболее пригодны клетки крови и печени
Слайд 1508/12/2019
Коваль А. Н. (С)
Методы биохимических исследований (продолжение)
Изучение гомогенатов
работа с бесклеточными
препаратами
можно удалять или добавлять различные вещества и наблюдать за результатами
можно
фракционировать различные органеллы путем дифференциального центрифугированияИсследование изолированных органелл
широко используются митохондрии, микросомы, рибосомы и др.
Субфракционирование изолированных органелл
например митохондрий для выделение комплексов дыхательной цепи
Выделение и характеристика ферментов и метаболитов
обязательно при описании любой химической реакции и метаболического пути
Клонирование генов, кодирующих ферменты и др. белки
исследование особенностей структуры и регуляции гена и первичной структуры белка, кодируемой этим геном
Слайд 1608/12/2019
Коваль А. Н. (С)
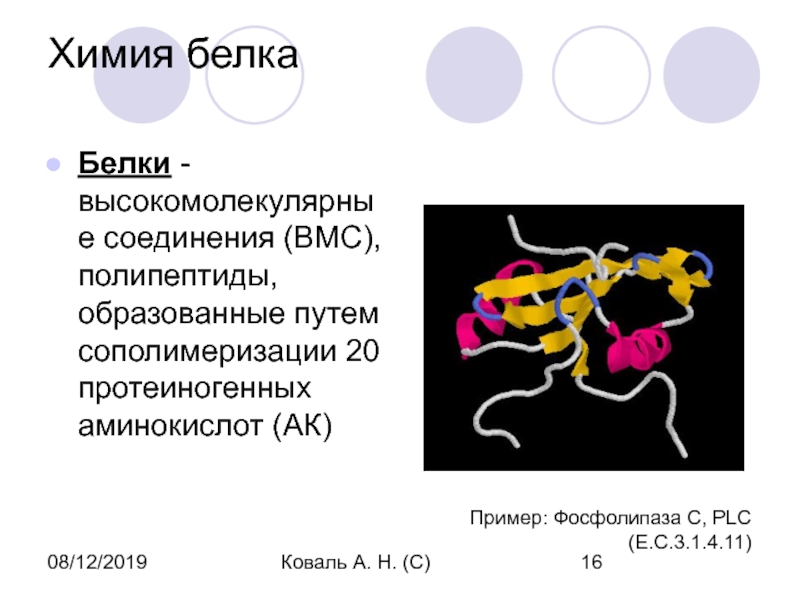
Химия белка
Белки - высокомолекулярные соединения (ВМС), полипептиды,
образованные путем сополимеризации 20 протеиногенных аминокислот (АК)
Пример: Фосфолипаза C, PLC
(E.C.3.1.4.11)Слайд 1708/12/2019
Коваль А. Н. (С)
20 протеиногенных аминокислот
Глицин (гли)
Гистидин (гис)
Аланин (ала)
Серин (сер)
Валин
(вал)
Треонин (тре)
Лейцин (лей)
Цистеин (цис)
Изолейцин (иле)
Метионин (мет)
Пролин (про)
Аспарагин (асп)
Аспарагиновая кислота (асп)
Глутамин
(глу)Глутаминовая кислота (глу)
Фенилаланин (фен)
Лизин (лиз)
Тирозин (тир)
Аргинин (арг)
Триптофан (трп)
Эти аминокислоты можно групппировать по различным свойствам их радикалов, например, полярности:
Неполярные (гидрофобные)
Полярные (гидрофильные)
Нейтральные (незаряженные)
Заряженные
Отрицательно (ала, глу)
Положительно (арг, гис, про)
В зависимости от структуры радикала можно выделить также:
Циклические
Ароматические
Неароматические (гетероциклические)
Ациклические
Алифатические
Серосодержащие (мет, цис)
Иминокислота (про)
По физиологической значимости
Заменимые
Незаменимые
Слайд 1808/12/2019
Коваль А. Н. (С)
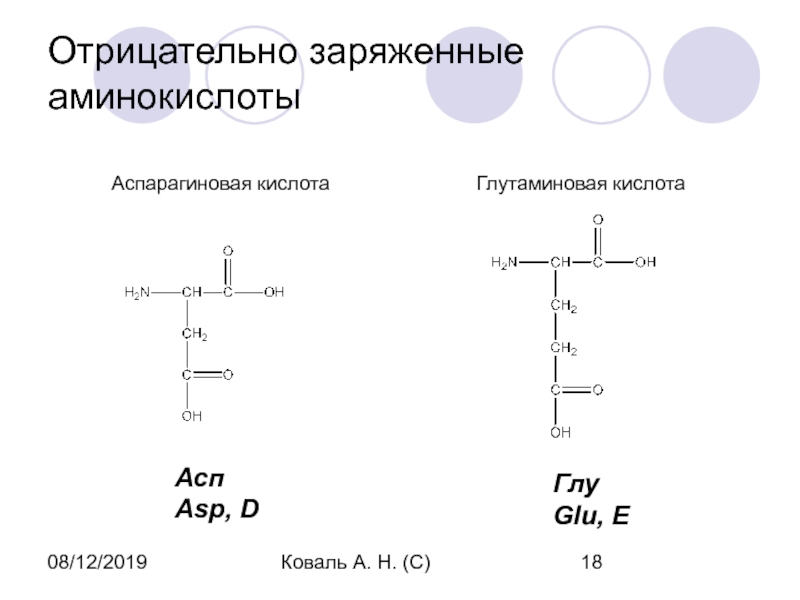
Отрицательно заряженные аминокислоты
Асп
Asp, D
Глу
Glu, E
Аспарагиновая кислота
Глутаминовая кислота
Слайд 1908/12/2019
Коваль А. Н. (С)
Положительно заряженные аминокислоты
Аргинин
Гистидин
Лизин
Арг
Arg, R
Гис
His, H
Лиз
Lys, K
Слайд 2008/12/2019
Коваль А. Н. (С)
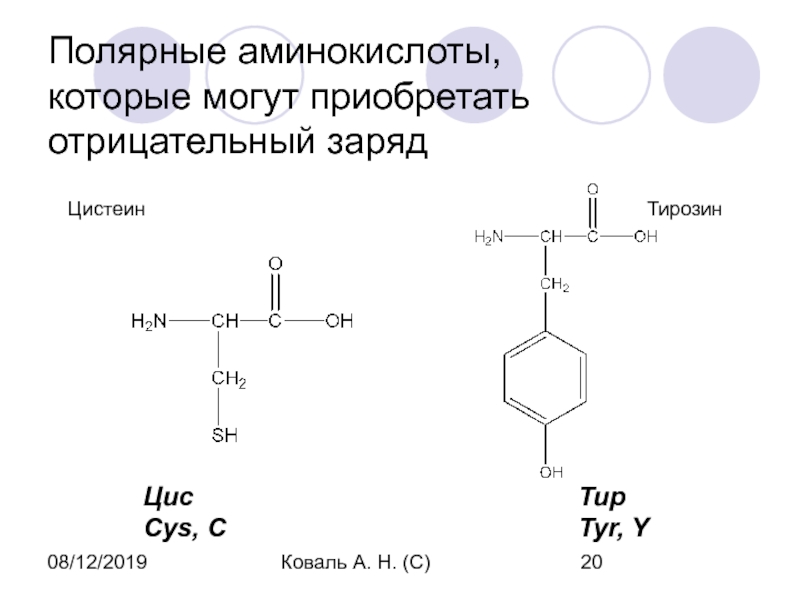
Полярные аминокислоты,
которые могут приобретать отрицательный заряд
Цистеин
Тирозин
Цис
Cys,
C
Тир
Tyr, Y
Слайд 2108/12/2019
Коваль А. Н. (С)
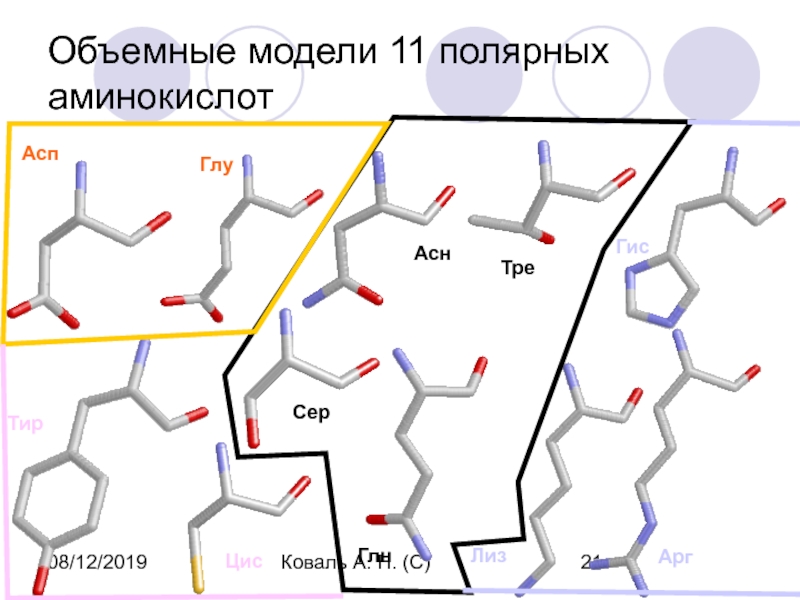
Объемные модели 11 полярных аминокислот
Асп
Глу
Тир
Цис
Арг
Лиз
Гис
Сер
Асн
Глн
Слайд 2308/12/2019
Коваль А. Н. (С)
Гидрофобные аминокислоты
(4 оставшихся)
Фенилаланин – вместе с
Тир и Трп образует группу ароматических АК
Метионин – вместе с
Цис составляет группу серосодержащих АКПролин – единственная иминокислота.
Фен
Трп
Мет
Про
Слайд 2408/12/2019
Коваль А. Н. (С)
История химии белка
1728 г. – Якоп Баккари,
выделил белковый препарат (клейковину) из пшеничной муки
1793 г. - Й.
Жакен – впервые употребил термин «белок»1-я половина ХIХ в – открытие явления ферментативного катализа
2-я половина ХIХ в. – выяснение полимерной природы белков (Ф. Гоппе-Зайлер, А. Хеннингер, А. Вюрц, Р. Харт)
появление структурных гипотез строения белка (П. Шютценберже, А.Я. Данилевский, А. Коссель)
1891 г. - А.П. Сабанеев - определение криоскопическим методов молекулярной массы альбумина
1905 г. – Э.Рейд – определение методом осмотического давления молекулярной массы гемоглобина
Слайд 2508/12/2019
Коваль А. Н. (С)
Эвристическая идея Э. Фишера
Белки состоят только из
α-АК.
(Из всей массы продуктов расщепления белков аминокислоты являются главными составляющими,
а все остальные соединения относятся к вторичным продуктам).АК, входящие в состав белков, относятся к L ряду.
Белковая молекула представляет собой линейный полимер.
α-АК образуют линейный полимер путем образования пептидной связи между карбоксильной группой одной АК и аминогруппой другой.
Слайд 2608/12/2019
Коваль А. Н. (С)
Структурная организация белковой молекулы
Выделяют четыре уровня структурной
организации белковой молекулы (классификация К. Линдерштрема-Ланга):
Первичная
Вторичная
Третичная
Четвертичная
Слайд 2708/12/2019
Коваль А. Н. (С)
Первичная (одномерная, линейная) структура
порядок или последовательность расположения
аминокислотных остатков в пептидной цепи (включая -S-S- связи), ее химическое
строение.Слайд 2808/12/2019
Коваль А. Н. (С)
Пример: пептид ангиотензин-2, повышающий давление
H2N-asp-arg-val-tyr-ile-his-pro-phe-COOH
Слайд 2908/12/2019
Коваль А. Н. (С)
Особенности пептидной связи
Наличие плоской (компланарной) сопряженной системы
в пептидном звене затрудняет вращение вокруг связи С-N
вал
тир
Слайд 3008/12/2019
Коваль А. Н. (С)
Особенности пептидной связи (продолжение)
Атомы, связанные с пептидной
группой, располагаются по разные стороны плоскости в более выгодном транс-положении.
Боковые группы остатков АК в этом случае наиболее удалены друг от друга.вал
тир
Слайд 3208/12/2019
Коваль А. Н. (С)
Конформация полипептидной цепи
Пептидная связь является практически плоской.
Поэтому вращение осуществляется по другим связям.
Угол φ («фи») характеризует поворот
вокруг связи N-Cα, т.е. предшествующей пептидной связи.Угол ψ («пси») – поворот вокруг связи Cα-C, т. е. следующей за пептидной связью.
Слайд 3508/12/2019
Коваль А. Н. (С)
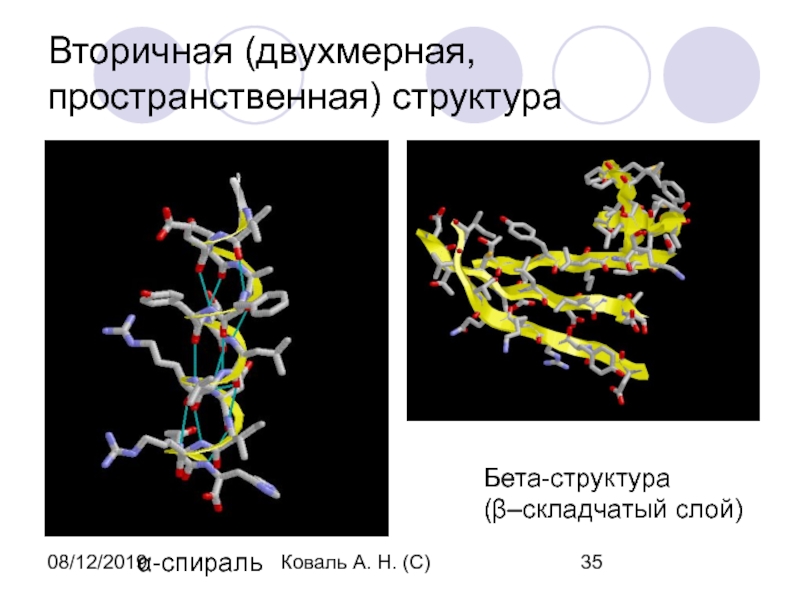
Вторичная (двухмерная, пространственная) структура
α-спираль
Бета-структура
(β–складчатый слой)
Слайд 3608/12/2019
Коваль А. Н. (С)
Характеристика альфа-спирали
Высота витка 0,54 нм (3,6 остатков
АК, 13 атомов),
Диаметр 0,50 нм,
Стабилизируется водородными связями между CO-группой n-го
и NH2-группой n+4-го остатка.0,54 нм
0,50 нм
Слайд 3708/12/2019
Коваль А. Н. (С)
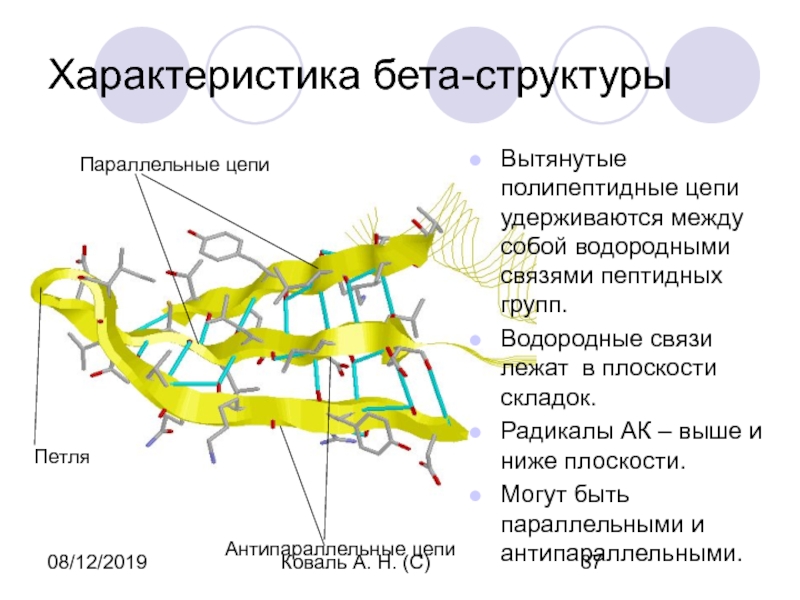
Характеристика бета-структуры
Вытянутые полипептидные цепи удерживаются между собой
водородными связями пептидных групп.
Водородные связи лежат в плоскости складок.
Радикалы АК
– выше и ниже плоскости.Могут быть параллельными и антипараллельными.
Параллельные цепи
Антипараллельные цепи
Петля
Слайд 3808/12/2019
Коваль А. Н. (С)
Другие разновидности вторичной структуры
Кроме α-спирали известны также
310-спираль (на один виток 3 остатка АК, или 10 атомов)
– более закручена, π-спираль (один виток из 4,4 АК, или 16 атомов) – более рыхлая,
αII-спираль (один виток – 4 АК, или 14 атомов) – рыхлая.
Спираль коллагена – ломаная, левозакрученная, растянутая.
В коллагене 1/3 АК глицин, 1/5 – пролин и оксипролин, редко - оксилизин.
Могут также встречаться
петли (в местах изменения направления складчатых структур),
неупорядоченные участки полипептидной цепи.
Слайд 3908/12/2019
Коваль А. Н. (С)
Соотношение структур в белках
α-белки:
миоглобин, гемоглобин, парамиозин, α-кератин.
β-белки:
конканаваллин A (растительные лектины), супероксиддисмутаза, фиброин шелка, паутины.
α+β-белки (одна часть
пептидной цепи представлена α-спиралями, другая – β-структурами) – редкие:термолизин (бакт.),
α/β-белки (α- и β- структуры чередуются) – наиболее часто:
фосфоглицераткиназа, флаводоксин.
без α,β (практически не имеют спиральных и складчатых структур):
ферредоксин (бакт.)
Слайд 4008/12/2019
Коваль А. Н. (С)
Третичная структура
Третичная структура – это общее расположение
в пространстве частей полипептидной молекулы.
третичная структура удерживается за счет
ковалентных
связей, сильных (дисульфидные, псевдопептидные),нековалентных, слабых (электростатические, водородные связи, гидрофобные взаимодействия).
Процесс укладки белковой молекулы (фолдинг белка) контролируется специфическими белками – шаперонами и шаперонинами (белки теплового шока).
ONCOGENE PROTEIN
(C-H-RAS P21 PROTEIN)
Слайд 4108/12/2019
Коваль А. Н. (С)
Доменная организация белка
Домен - обособленная область молекулы
белка, обладающая структурной и функциональной автономией.
В иммуноглобулине G1 (IgG1), различают
12 доменов: 2 легкие цепи по 2 домена (VL, CL)
2 тяжелые цепи по 4 домена (VH, CH1, CH2, CH3).
HUMAN IGG1
Слайд 4208/12/2019
Коваль А. Н. (С)
Четвертичная структура белка
Четвертичная структура – комплекс отдельных
полипептидных цепей (субъединиц, или мономеров);
Удерживается водородными связями и гидрофобными взаимодействиями.
Гемоглобин
A – тетрамерный белокСлайд 4308/12/2019
Коваль А. Н. (С)
Пятый уровень органицации белковой молекулы
Иногда выделяют и
пятый уровень – метаболон, т. е. совокупность ферментов, катализирующих определенный
метаболический путь (например, цикл Кребса).Слайд 4408/12/2019
Коваль А. Н. (С)
Форма, размеры и масса белковых молекул
По форме:
Глобулярные
(альбумин, рибонуклеаза, миоглобин, гемоглобин).
шарообразные, эллипсоидные, вытянутые.
Фибриллярные (кератины, фиброин, коллаген, F-актин,
тропомиозин).нитевидные.
По размерам - от 2,5 до 300 нм.
По массе – от 13 000 до 500 000 Да (дальтон).