Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биохимия печени
Содержание
- 1. Биохимия печени
- 2. Печень – посредник между кишечником и другими
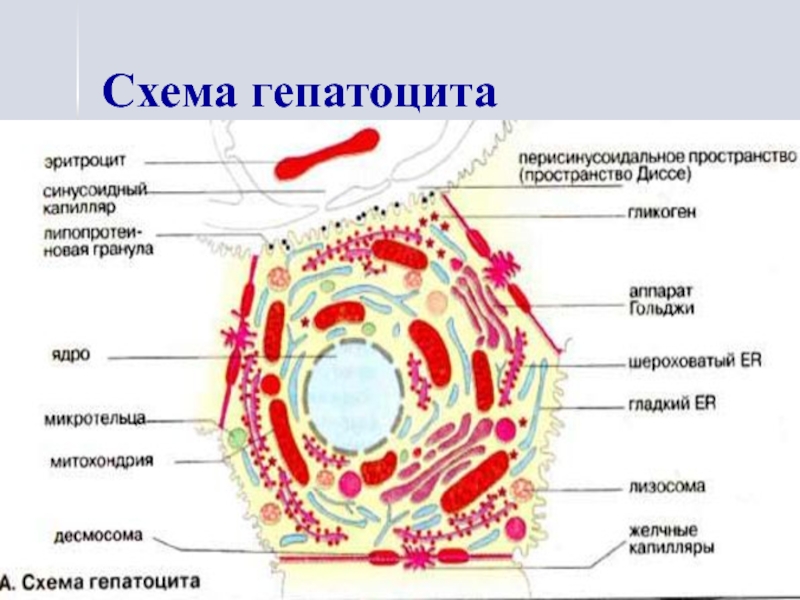
- 3. Схема гепатоцита
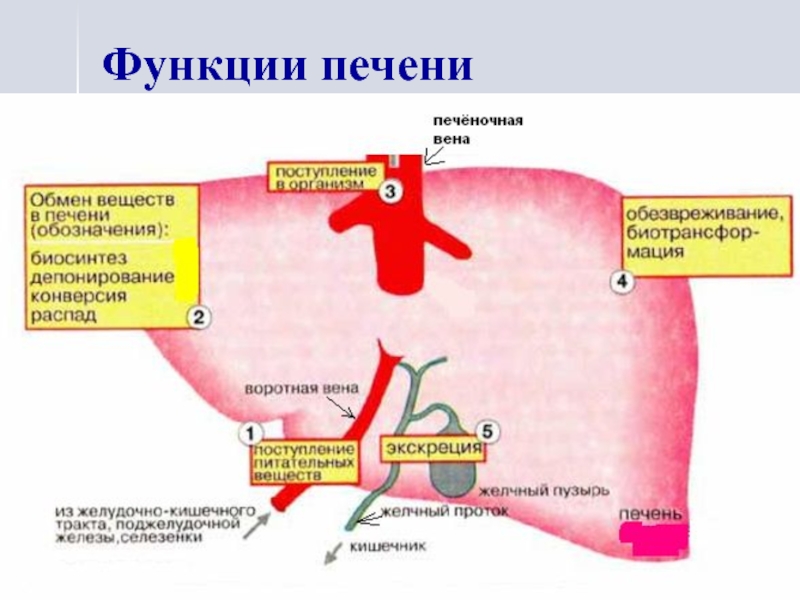
- 4. Функции печени
- 5. Функции печени
- 6. Химический состав печени
- 7. Роль печени в углеводном обмене Печень –
- 8. Регуляция синтеза и распада гликогенаУвеличивают содержание гликогена
- 9. Гликогенолиз Нарушение активности ферментов фосфоролиза приводит к
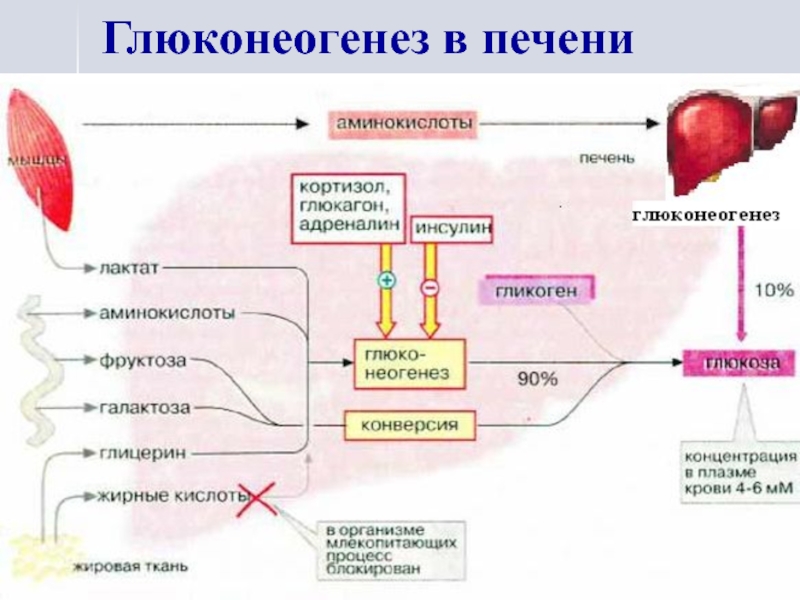
- 10. Глюконеогенез в печени
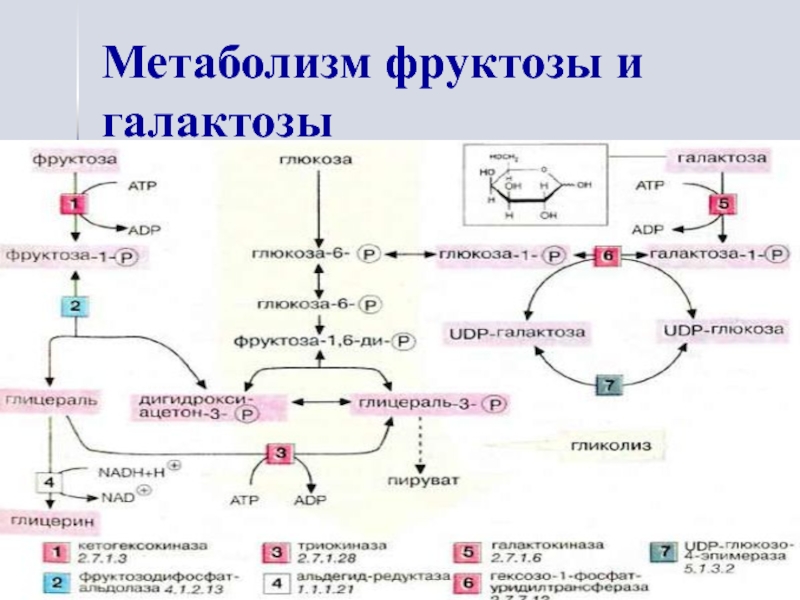
- 11. Метаболизм фруктозы и галактозы
- 12. Роль печени в липидном обмене В печени
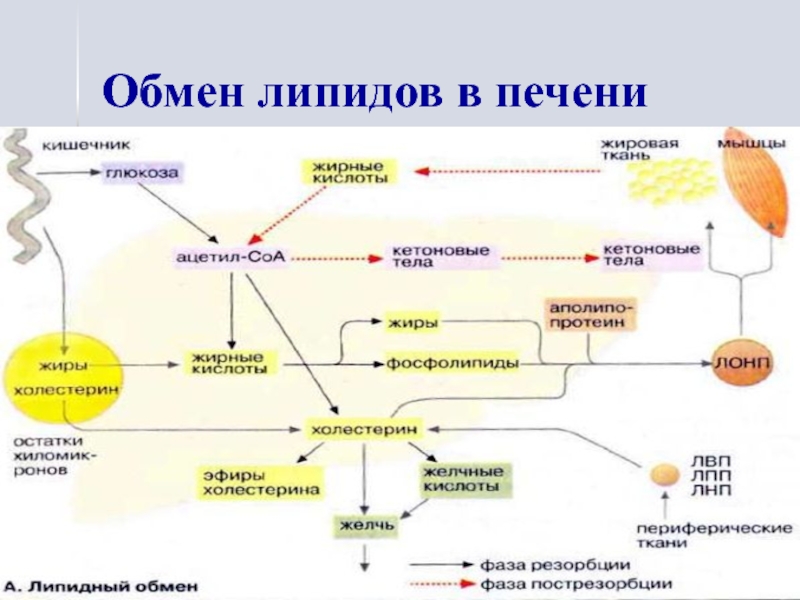
- 13. Обмен липидов в печени
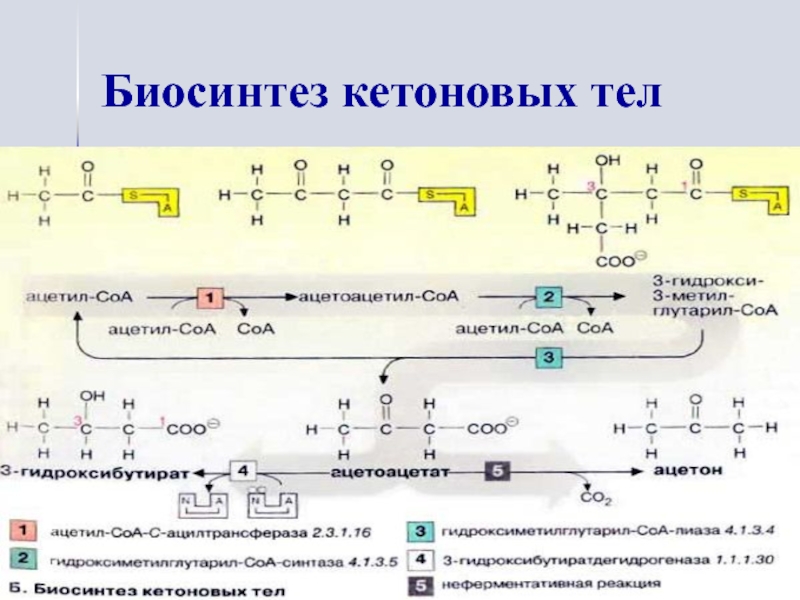
- 14. Биосинтез кетоновых тел
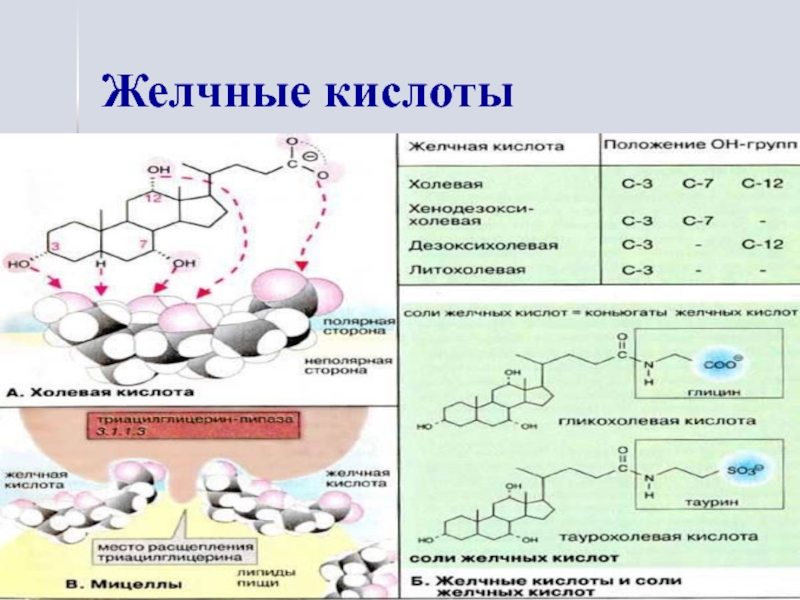
- 15. Желчные кислоты
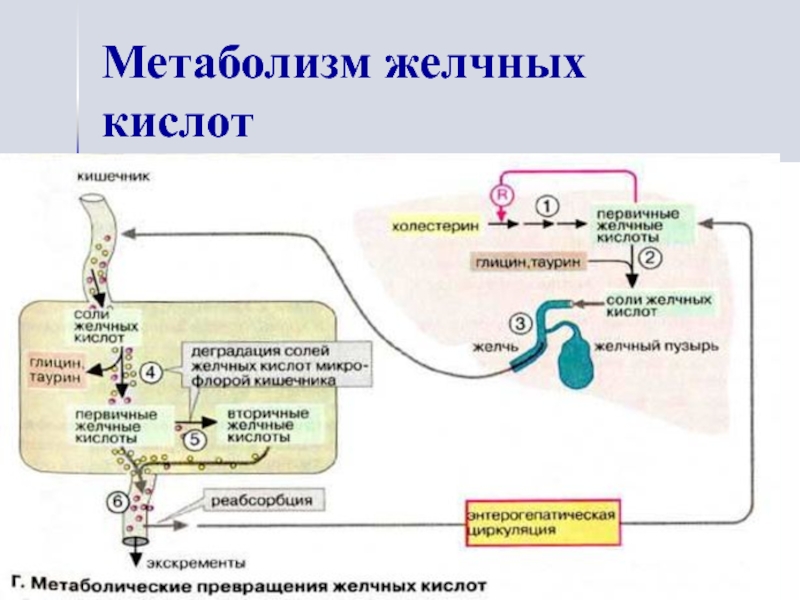
- 16. Метаболизм желчных кислот
- 17. Роль печени в обмене белковВ печени протекает:
- 18. Метаболизм гормонов в печениИнактивация: стероидных гормонов, тироксина, АДГ, альдостерона, эстрогенов, инсулина.Синтез: транскортина, дофамина.
- 19. Печень, витамины, микроэлементыПечень - депо витаминов
- 20. Роль печени в обезвреживании метаболитов и токсических веществОбезвреживание происходит путем: окисления, восстановления, метилирования, ацетилирования, конъюгации.
- 21. Обезвреживание токсических веществ в печениВ печени происходит
- 22. Слайд 22
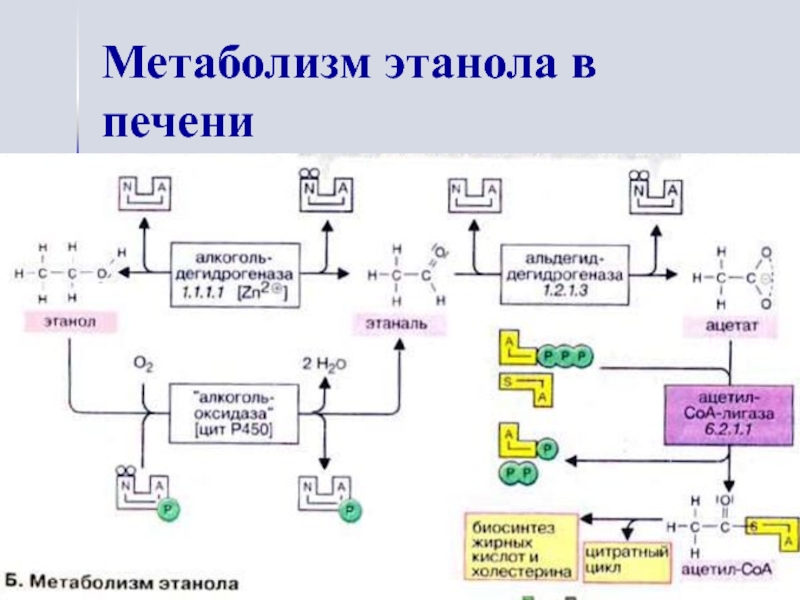
- 23. Метаболизм этанола в печени
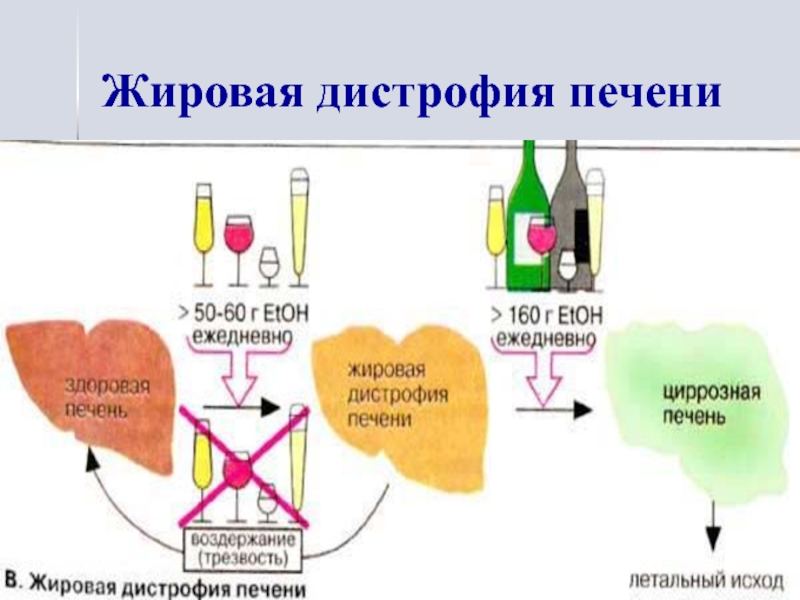
- 24. Жировая дистрофия печени
- 25. Микросомальное окисление Микросомы – морфологически замкнутые везикулы,
- 26. Монооксигеназная система состоит из
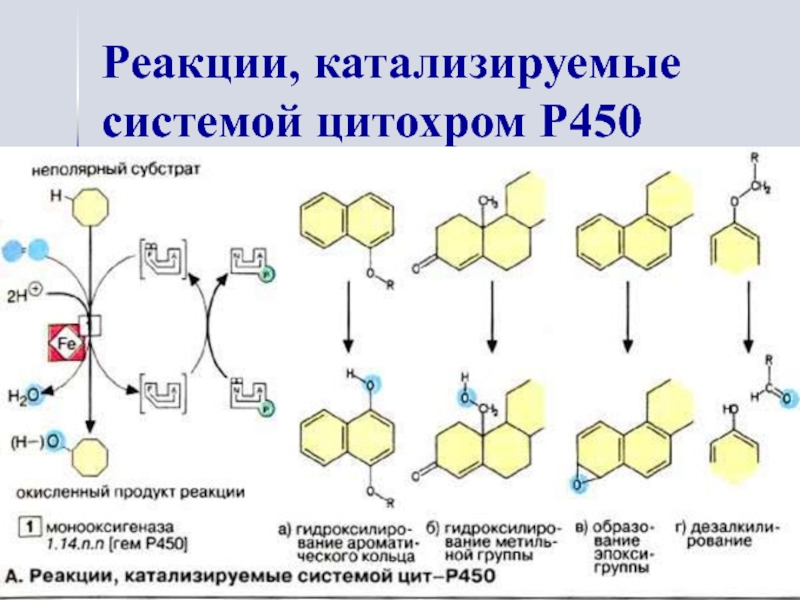
- 27. Реакции, катализируемые системой цитохром Р450
- 28. Слайд 28
- 29. Цитохром Р450 выполняет двойную функцию: цитохром Р450 связывает субстрат гидроксилирования, на нём происходит активация молекулярного кислорода.
- 30. Цепь микросом печени- универсальная биологическая система, окисляющая
- 31. Элиминация. Окисление молекулярным кислородом приводит к
- 32. Микросомальные гидроксилазы могуткатализировать не только гидроксилирование,но и
- 33. Цитохром Р450 инактивируется in vitro окисью углерода
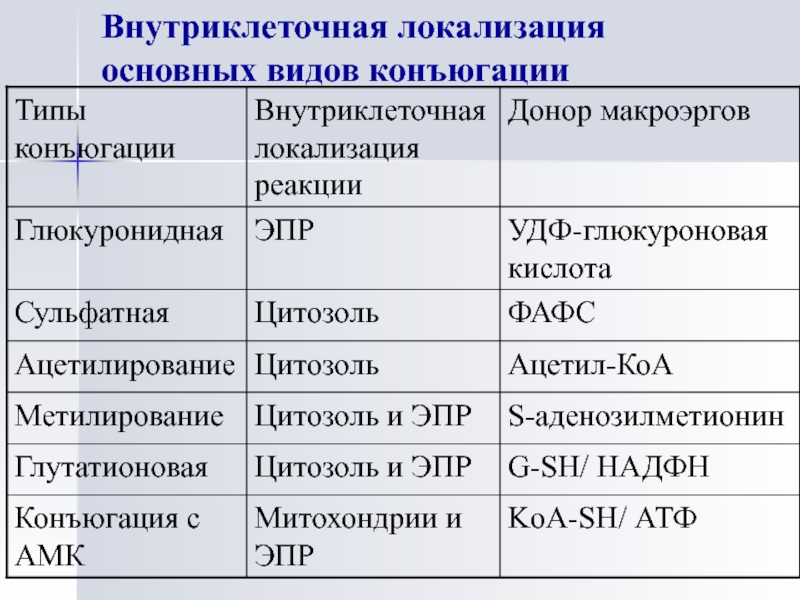
- 34. Внутриклеточная локализация основных видов конъюгации
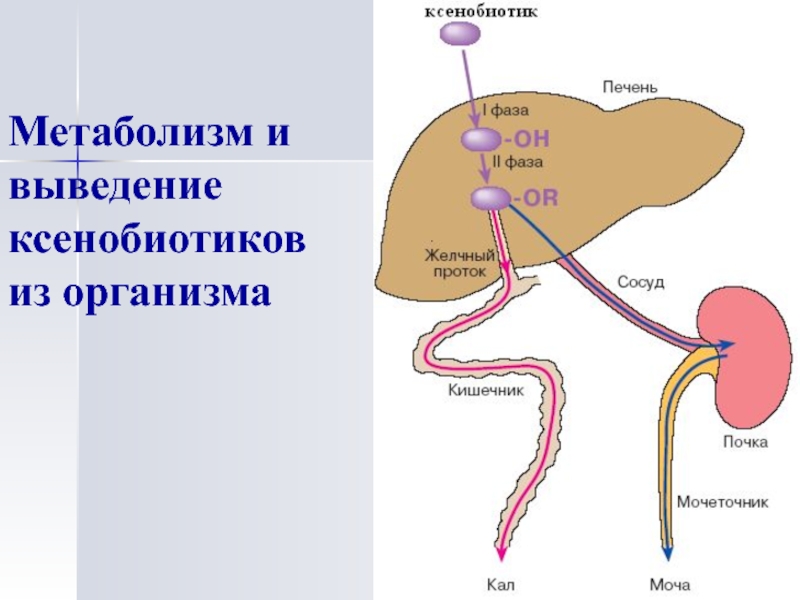
- 35. Метаболизм и выведение ксенобиотиков из организма
- 36. Субклеточная локализация ферментных систем в печениЯдро гепатоцита
- 37. Биохимические показатели при цитолитическом синдромеПовышение в сыворотке
- 38. Соотношение АСТ/АЛТ: АЛТ сосредоточен в цитозоле.
- 39. Повышение активности:щелочной фосфатазы (стимуляция биосинтеза ЩФ на
- 40. Биохимические показатели при мезенхимально-воспалительном синдроме
- 41. Индикаторы гепато-депрессивного синдрома (малой недостаточности печени)Показатели
- 42. Индикаторы гепатодепрессии, связанные с синтезом белка альбумины
- 43. Биохимические показатели при синдроме печеночно-клеточной недостаточности
- 44. Биохимические показатели при синдроме портокавального шунтирования Возникает
- 45. Слайд 45
- 46. Информационный уровень взаимосвязиВ геноме клеток заложена информация
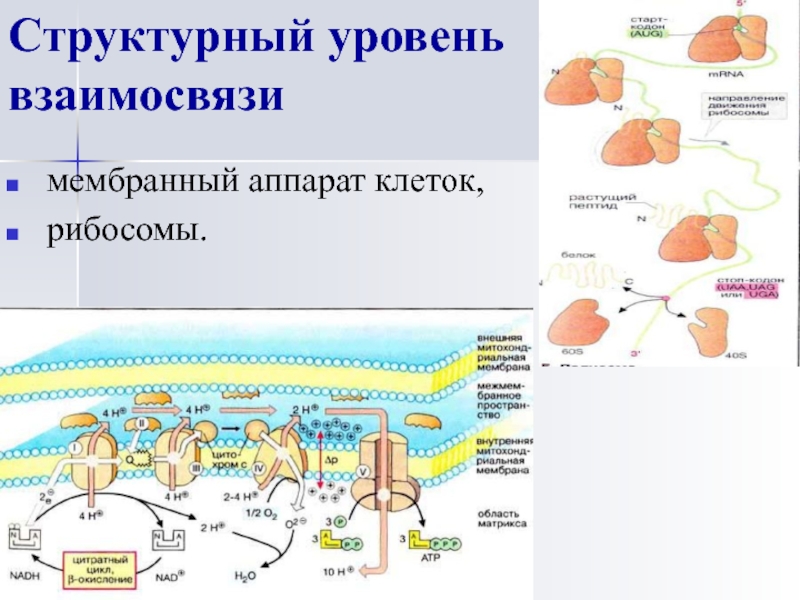
- 47. Структурный уровень взаимосвязи мембранный аппарат клеток, рибосомы.
- 48. Общее энергетическое обеспечениеАТФ – универсальная энергетическая валюта,
- 49. Окисляемые субстратыПродукты окисленияПродукты биосинтезовСубстраты длябиосинтезовНАДФ+НАДФН+Н+НАДН+Н+НАД+2Н+2Н+2Н+анаболизмкатаболизм
- 50. Взаимосвязь на уровне общих метаболитовЦентральные метаболиты: ацетил-КоА, ПВК, ЩУК, ФГА.
- 51. ПВКФГАацетил-КоАЩУКБелкиУглеводыЖирыГлицеринХолестеринЦ.Т.К.Кетоновые телаЖирные кислотыАМКЛактат
- 52. Ацетил-КоА образуется при окислительном декарбоксилировании ПВК, при β-окислении жирных кислот, из аминокислот.
- 53. ПВК + СО2
- 54. Взаимосвязь углеводного и липидного обменов осуществляется черезацетил-КоА,ФГА,НАДФН2
- 55. Взаимосвязь белкового и жирового обменов на уровне ПВК, ацетил-КоА, кетоновых тел.Из белков осуществляется синтез жира.
- 56. Взаимосвязь углеводного и белкового обменов на уровнеПВК,ЩУК,ацетил-КоА,
- 57. Сопряжение на уровне Ц.Т.К. углеродные скелеты
- 58. Связь липидного обмена с Ц.Т.К. осуществляется через
- 59. Взаимосвязь обменов на уровне органов и
- 60. Печень и мозг.Глюкоза из печени с кровью
- 61. Почки и печень.Глюконеогенез происходит в почках и
- 62. Жировая ткань и печень.В обеих тканях
- 63. Скачать презентанцию
Слайды и текст этой презентации
Слайд 7Роль печени в углеводном обмене
Печень – депо гликогена.
Печень обеспечивает
постоянный уровень глюкозы в крови,
регулируя соотношения между синтезом и распадом
гликогена.
В печени протекают:
гликолиз,
гликогенолиз,
глюконеогенез,
гликогеногенез,
превращение фруктозы и галактозы в глюкозу,
синтез гепарина.
Слайд 8Регуляция синтеза и распада гликогена
Увеличивают содержание гликогена в печени:
АКТГ,
глюкокортикоиды,
инсулин.
Стимулируют распад гликогена:
адреналин,
глюкагон,
СТГ, тироксин.
Слайд 9Гликогенолиз
Нарушение активности ферментов фосфоролиза приводит к накоплению гликогена в
печени и далее к гипогликемии.
Это наблюдается при гликогенозах.
Слайд 12Роль печени в липидном обмене
В печени осуществляется:
синтез желчных
кислот (желчь необходима для переваривания и всасывания липидов),
синтез фосфолипидов (при
дефиците АТФ и липотропных факторов фосфатидная кислота используется для синтеза нейтрального жира),синтез холестерина (98%), его этерификация,
синтез ЛПВП,
синтез жирных кислот,
липолиз,
кетогенез,
распад фосфолипидов.
Слайд 17Роль печени в обмене белков
В печени протекает:
синтез белков (за
сутки обновляется около 9 % собственных белков, 1/4 альбуминов плазмы):
альбуминов плазмы,80 % a-глобулинов,
50 % b-глобулинов,
ряда ферментов, аминокислот.
трансаминирование и окислительное дезаминирование аминокислот,
синтез мочевины и мочевой кислоты,
синтез холина, креатинина,
синтез протромбина, фибриногена, проакцелерина.
Слайд 18Метаболизм гормонов в печени
Инактивация:
стероидных гормонов,
тироксина,
АДГ,
альдостерона,
эстрогенов,
инсулина.
Синтез:
транскортина,
дофамина.
Слайд 19 Печень, витамины, микроэлементы
Печень - депо витаминов А, Д, К,
РР.
В большом количестве содержатся витамины
С,
В1,
В2, В12,
фолиевая кислота.
В печени находятся запасы:
железа,
меди,
цинка,
марганца,
молибдена.
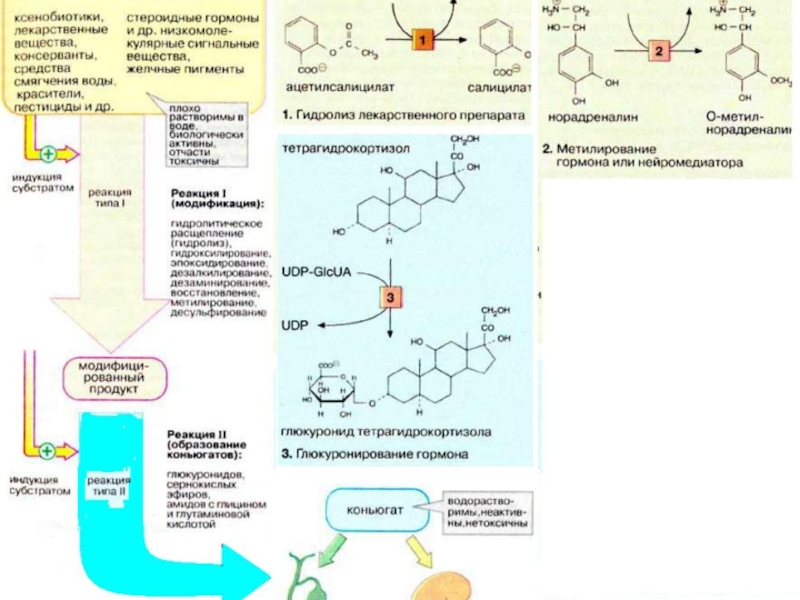
Слайд 20Роль печени в обезвреживании метаболитов и токсических веществ
Обезвреживание происходит путем:
окисления,
восстановления,
метилирования,
ацетилирования,
конъюгации.
Слайд 21Обезвреживание токсических веществ в печени
В печени происходит синтез мочевины (обезвреживание
аммиака).
Путем образования парных соединений с ФАФС или глюкуроновой кислотами обезвреживаются:
продукты гниения аминокислот в кишечнике: индол, скатол, фенол, крезол,билирубин (путем образования моно- и диглюкуронидов),
стероидные гормоны (в виде глюкуронидов).
Образование парных соединений в печени протекает также с участием гликокола и таурина:
желчные кислоты находятся в желчи в виде соединений с гликоколом и таурином,
бензойная кислота, соединяясь с гликоколом, превращается в гиппуровую кислоту.
При участии моно- и диаминоокисидаз (МАО, ДАО) в печени
происходит окислительный распад - адреналина и гистамина.
Слайд 25Микросомальное окисление
Микросомы – морфологически замкнутые везикулы, в которые превращается
эндоплазматический ретикулум при гомогенизации тканей.
Функция микросомального окисления:
использование
кислорода с «пластическими» целями.Микросомальное окисление осуществляется во фракции микросом печени и надпочечников, но может встречаться и в любой другой ткани.
Слайд 26 Монооксигеназная система состоит из трёх компонентов:
НАДФ-специфичного
ФАД - содержащего флавопротеина,
железосерного белка,
цитохрома Р450.
Монооксигеназы
присоединяют к субстрату один из двух атомов кислорода.
НАДФН+Н+ - поставщик атомов водорода для восстановления
второго атома кислорода до воды.
Электрон НАДФН+Н+ переносится на флавопротеин, затем на
белок, содержащий негемовое железо, затем на цитохром Р450.
В цепи микросомального окисления образуются свободные
радикалы.
Fe(2+) от Р450 - радикалообразующий центр.
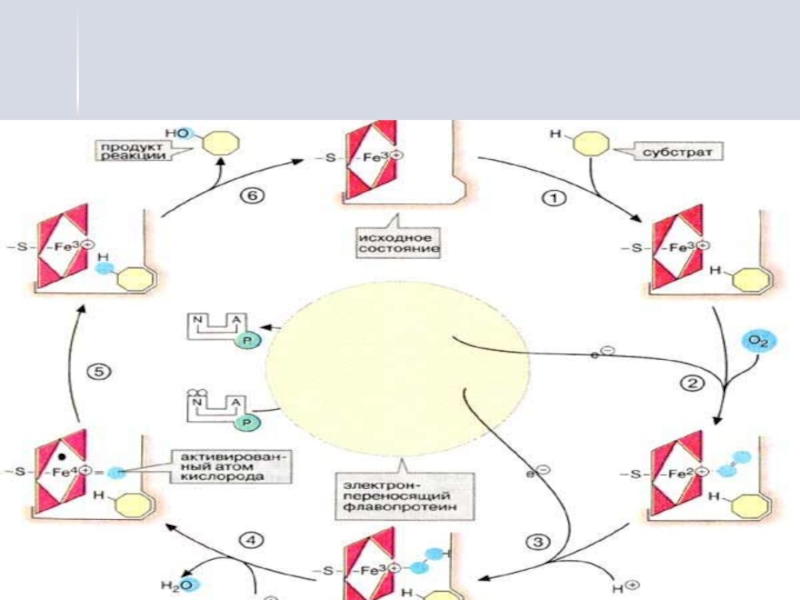
Слайд 29Цитохром Р450 выполняет двойную функцию:
цитохром Р450 связывает субстрат гидроксилирования,
на нём происходит активация молекулярного кислорода.
Слайд 30Цепь микросом печени
- универсальная биологическая система, окисляющая неполярные соединения любого
происхождения:
эндогенные субстраты – стероидные гормоны, холестерин, витамины, ненасыщенные жирные
кислоты.экзогенные субстраты (ксенобиотики) - гидрофобные загрязнители окружающей среды, канцерогены, лекарства, пестициды.
Ключевым ферментом в элиминации, детоксикации и метаболической активации экзогенных субстратов является цитохром Р450.
Слайд 31Элиминация.
Окисление молекулярным кислородом приводит к увеличению гидрофильности чужеродных соединений.
Детоксикация.
Химическая
модификация приводит к потере
молекулой её биологической активности,
токсичности.
Метаболическая активация.
Продукт реакции становится
более активным,чем молекула, из которой он образовался.
Слайд 32Микросомальные гидроксилазы могут
катализировать не только гидроксилирование,
но и другие реакции:
эпоксидирование,
сульфоокисление,
дезалкилирование,
восстановление нитросоединений.
Полиспецифичность микросомального окисления
объясняется тем, что цитохром Р450
существует ввиде различных изоферментов.
Слайд 33Цитохром Р450
инактивируется in vitro окисью углерода и тиоловыми ядами,
реактивируется – тиоловыми антиоксидантами.
В печени обезвреживание веществ заключается в их
химической модификации в две фазы:Вещество окисляется, восстанавливается или гидролизуется. При этом образуется ОН, СООН, SH, NH2.
К этим группам присоединяется глюкуроновая кислота, серная кислота, глицин, глутамин, глутатион, метильная или ацетильная группа (реакции конъюгации).
Слайд 36Субклеточная локализация ферментных систем в печени
Ядро гепатоцита служит хранилищем информации
и может быть источником генетических дефектов и аномалий белков и
ферментов печени или плазмы крови.Цитозоль гепатоцита содержит ферменты гликолиза и пентозного цикла, лейцинаминопептидазу, АЛТ, АСТ, сорбитолдегидрогеназу,ферменты глюконеогенеза.
В митохондриях локализованы ферменты цикла Кребса и окислительного фосфорилирования окисления жирных кислот, карбомоилфосфатсинтетаза, глутаматдегидрогеназа, АСТ.
На рибосомах локализованы ферменты синтеза белков.
На гладкой ЭПС располагаются глюкозо-6-фосфатаза ферменты биотрансформации и конъюгации.
Лизосомы гепатоцитов содержат кислые гидролазы.
Слайд 37Биохимические показатели при цитолитическом синдроме
Повышение в сыворотке крови активности:
АЛТ,
АСТ,
альдолазы,
ГЛДГ,
сорбитолдегидрогеназы,
ЛДГ 5
орнитинкарбомоилтрансферазы,
γ-ГТП.Повышение в крови содержания общего билирубина и прямого билирубина.
Повышение содержания железа в сыворотке крови.
Слайд 38
Соотношение АСТ/АЛТ:
АЛТ сосредоточен в цитозоле.
АСТ –
в цитозоле и митохондриях.
При вирусном гепатите первично поражается мембрана клетки.
В кровь попадает больше АЛТ.При циррозе АСТ выше, чем АЛТ:
Воспалительный тип: АСТ/АЛТ<1,
Некротический тип: АСТ/АЛТ >1.
Соотношение АСТ + АЛТ/ГЛДГ:
при метастазах в печень <10,
при обструктивной желтухе 5-20,
при остром вирусном гепатите >50.
Соотношение ЛДГ/АСТ:
при гемолитической желтухе >12,
при гепатоцеллюлярной желтухе <12.
Слайд 39Повышение активности:
щелочной фосфатазы (стимуляция биосинтеза ЩФ на поверхности гепатоцитов
поступление в синусоиды
проникновение в кровь)лейцинаминопептидазы (ЛАП),
5'-нуклеотидазы,
γ-ГТП.
Повышение содержания фосфолипидов, холестерина, ЛПНП, желчных кислот.
Гипербилирубинемия.
Биохимические показатели при синдроме холестаза (исследование сыворотки крови)
Слайд 40Биохимические показатели при мезенхимально-воспалительном синдроме
(исследование сыворотки крови)
Рост содержания иммуноглобулинов:
IgM при острых воспалениях,
IgG и IgA - при хронических;
Повышение содержания γ-глобулинов,
снижение – альбуминов,
Повышение белков острой фазы:
гаптоглобина, орозомукоида,
Изменение белкового спектра сыворотки крови выявляют
осадочные пробы: тимоловая, сулемовая.
Слайд 41Индикаторы гепато-депрессивного синдрома
(малой недостаточности печени)
Показатели выделительной функции:
Скорость выведения бромсульфолеина
10-16 мг краски/мин.
Тесты на обезвреживающую функцию:
антипириновая проба,
кофеиновая проба.
При
остром гепатите - снижение клиренса до 80%Тесты, связанные с синтезом прокоагулянтов:
При повреждениях печени снижается синтез
витамин К-зависимых факторов свёртывания крови:
II, VII, IX, X.
Холестерин сыворотки крови (3,9-6,5 ммоль/л)
Аммиак (0,1-0,3 мг/л).
Слайд 42Индикаторы гепатодепрессии, связанные с синтезом белка
альбумины (35-50 г/л),
фибронектин (333+8,6 мкг/мл),
церулоплазмин
(0,15-0,6 г/л),
а1-АТ (2-4 г/л),
псевдохолинэстераза
(160 - 340 мкмоль/г*мл).Слайд 43Биохимические показатели при синдроме печеночно-клеточной недостаточности
(исследования сыворотки крови)
понижение
активности холинэстеразы,
гипопротеинемия и диспротеинемия
с понижением содержания альбуминов.снижение концентрации протромбина, фибриногена,
снижение содержания холестерина,
гипербилирубинемия. Повышается содержание неконъюгированного билирубина.
Слайд 44Биохимические показатели при синдроме портокавального шунтирования
Возникает этот синдром за счет
развития мощных венозных коллатералей с поступлением из кишечника в общий
кровоток большого количества веществ, подлежащих в норме преобразованию в печени (аммиак, фенолы, аминокислоты, меркаптены).Определение аммиака в сыворотке крови для выявления портально-печеночной недостаточности.
Биохимические показатели при синдроме регенерации и опухолевого роста печени.
Повышение в сыворотке крови содержания
a-фетопротеина.
Слайд 45 Взаимосвязь обменов осуществляется благодаря
интегрирующим системам:
нервной,
эндокринной,
сосудистой.
Взаимосвязь обеспечивается различными уровнями:
информационный уровень,
структурный уровень,общее энергетическое обеспечение,
на уровне общих метаболитов,
на уровне Ц.Т.К.
.
Слайд 46Информационный уровень взаимосвязи
В геноме клеток заложена информация о структуре и
функциональной активности различных белков , принимающих участие в структурной и
динамической организации живых систем.Слайд 48Общее энергетическое обеспечение
АТФ – универсальная энергетическая валюта, образующаяся при окислении
углеводов, жиров, аминокислот.
НАДФН2 – основной донор электронов в восстановительных реакциях
биосинтеза.Восстановительные эквиваленты, накапливаемые в ходе катаболизма в клетке в виде восстановительных форм НАДФН2 используются в восстановительных реакциях клеточного анаболизма, связывая таким образом, катаболические и анаболические процессы в единую систему.
Синтез одного соединения (жира) происходит за счёт катаболизма другого (глюкозы).
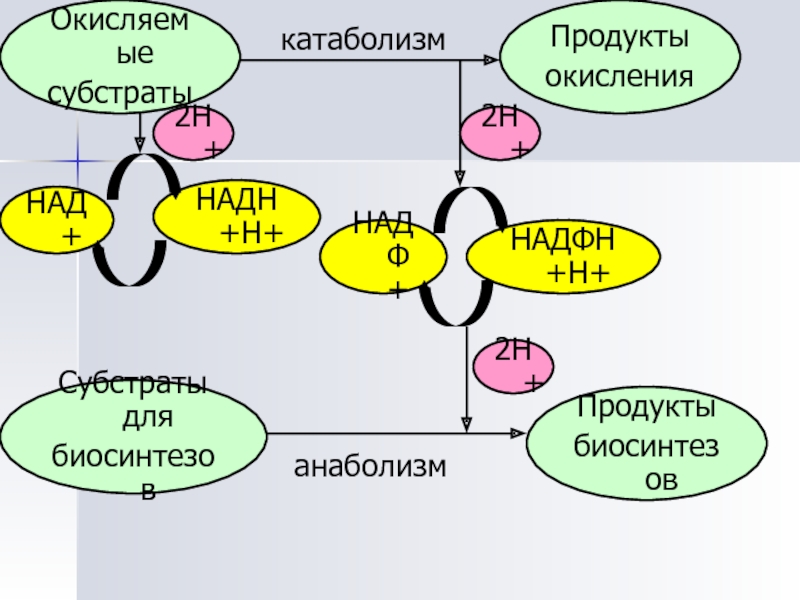
Слайд 49Окисляемые
субстраты
Продукты
окисления
Продукты
биосинтезов
Субстраты для
биосинтезов
НАДФ+
НАДФН+Н+
НАДН+Н+
НАД+
2Н+
2Н+
2Н+
анаболизм
катаболизм
Слайд 51
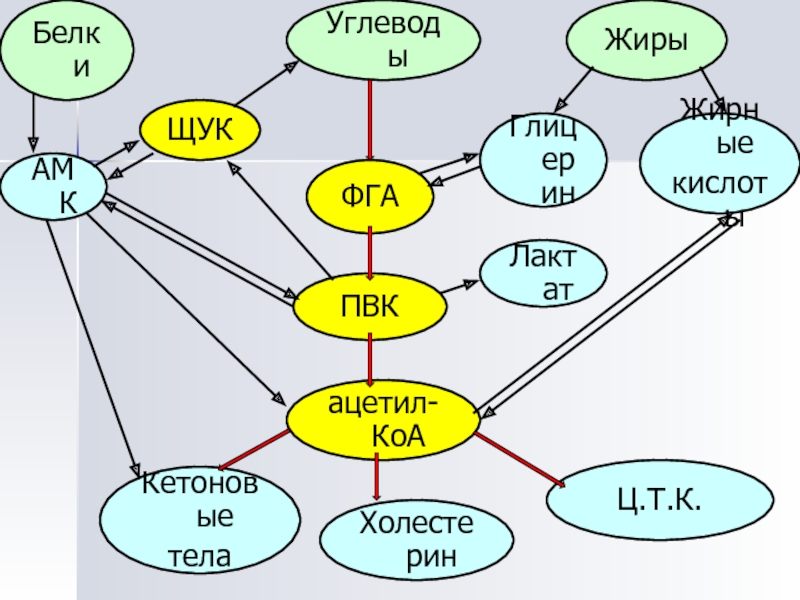
ПВК
ФГА
ацетил-КоА
ЩУК
Белки
Углеводы
Жиры
Глицерин
Холестерин
Ц.Т.К.
Кетоновые
тела
Жирные
кислоты
АМК
Лактат
Слайд 52Ацетил-КоА образуется
при окислительном декарбоксилировании ПВК,
при β-окислении жирных кислот,
из аминокислот.
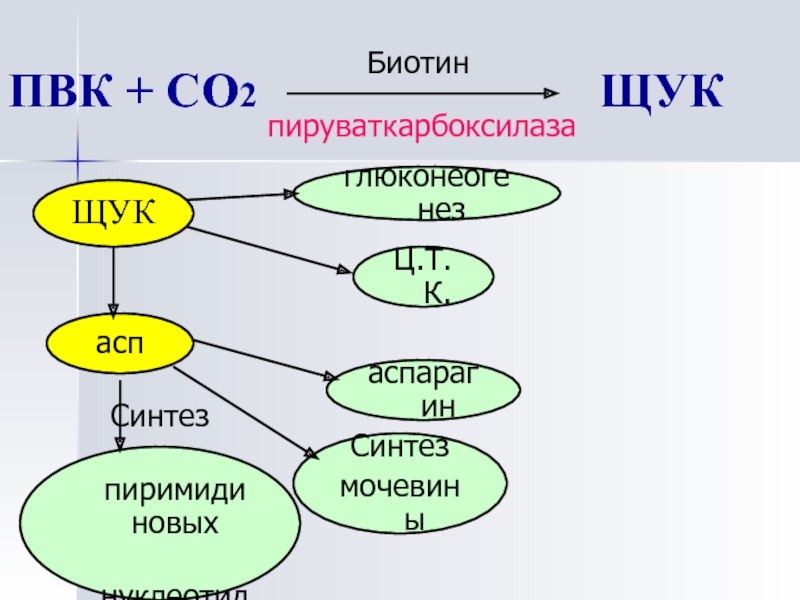
Слайд 53ПВК + СО2
ЩУК
пируваткарбоксилаза
Биотин
ЩУК
асп
глюконеогенез
Ц.Т.К.
аспарагин
Синтез
мочевины
Синтез
пиримидиновых
нуклеотидов
Слайд 54Взаимосвязь углеводного и липидного обменов осуществляется через
ацетил-КоА,
ФГА,
НАДФН2 из пентозного цикла
идёт на синтез жирных кислот,
ЩУК нужен для работы Ц.Т.К.
Жиры
сгорают в пламени углеводов.При избытке в пище углеводов возникает ожирение.
ФГА и ацетил-КоА– источники глицерина и жирных кислот.
При спячке у животных происходит образование
углеводов из жиров.
Слайд 55Взаимосвязь белкового и жирового обменов на уровне
ПВК,
ацетил-КоА,
кетоновых
тел.
Из белков осуществляется синтез жира.
Слайд 56Взаимосвязь углеводного и белкового обменов на уровне
ПВК,
ЩУК,
ацетил-КоА,
пентоз,
глюкопластичных и
кетопластичных аминокислот.
Углеродные скелеты АМК вступают в Ц.Т.К.
Возможно образование углеводов из
белков (ГНГ) и белков из углеводов (из ПВК образуется аланин).
Слайд 57Сопряжение на уровне Ц.Т.К.
углеродные скелеты АМК включаются в Ц.Т.К,
все кислоты Ц.Т.К. превращаются в ЩУК (ГНГ),
взаимосвязь Ц.Т.К. с
синтезом мочевины через фумарат, асп, СО2,ЩУК,
жирные кислоты,
мочевина, азотистые основания.
Ц.Т.К обеспечивает энергией все обмены.
СО2
Слайд 58Связь липидного обмена с Ц.Т.К. осуществляется через
цитрат
- активатор
ацетил-КоА-карбоксилазы,
- перенос в цитоплазму ацетил-КоА,
Сукцинил-КоА
Жирные кислоты с нечётным числом
углеродных атомов через пропионил-КоА превращаются в
сукцинил-КоА.
СО2,
малат
Малик-реакция – источник образования НАДФН2 .
Слайд 59Взаимосвязь обменов
на уровне органов и тканей
Печень и мышцы.
В
покоящихся мышцах субстрат энергетического обмена – свободные жирные кислоты и
кетоновые тела, доставляемые с кровью из печени.При умеренной нагрузке присоединяется аэробный распад глюкозы.
При тяжёлой физической нагрузке источник энергии – гликоген мышц (гликогенолиз). Лактат идёт из мышц в печень, где превращается в глюкозу.
При длительном голодании происходит распад белков мышц. Аммиак переносится на ПВК, образуется аланин, который является источником глюконеогенеза.
Слайд 60Печень и мозг.
Глюкоза из печени с кровью поступает в мозг.
В ткани мозга содержится много АТФ для синтеза нейромедиаторов.
Обезвреживание
аммиака путем синтеза глутамина.При голодании источники глюкозы для мозга сначала – гликоген, затем – белки мышц.
Слайд 61Почки и печень.
Глюконеогенез происходит в почках и печени.
Почки зависят от
поступления из печени глутамина, который служит источником аммиака, необходимого для
нейтрализации экскретируемых ионов водородаПечень отвечает за синтез, а почки за экскрецию мочевины.