Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Раздражимость и возбудимость клеток и тканей. Методы исследования электровозбудимых мембран. Потенциал покоя и механизм его форм
Содержание
- 1. Раздражимость и возбудимость клеток и тканей. Методы исследования электровозбудимых мембран. Потенциал покоя и механизм его форм
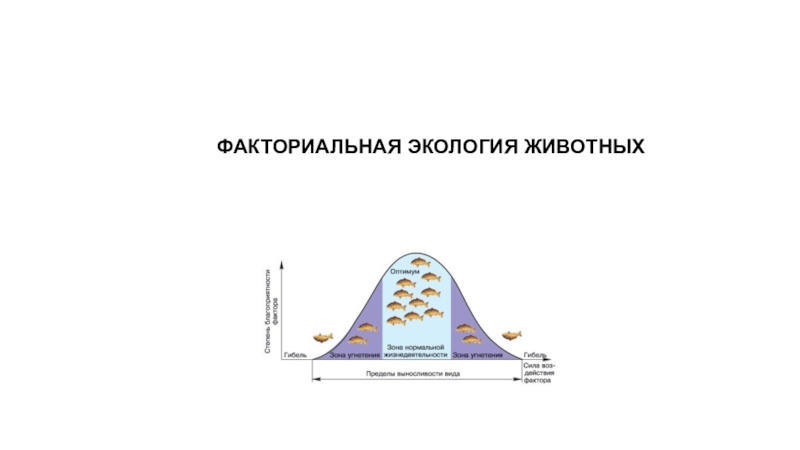
- 2. РАЗДРАЖИМОСТЬ – ОБЩЕЕ СВОЙСТВО ВСЕХ ЖИВЫХ ОРГАНИЗМОВ
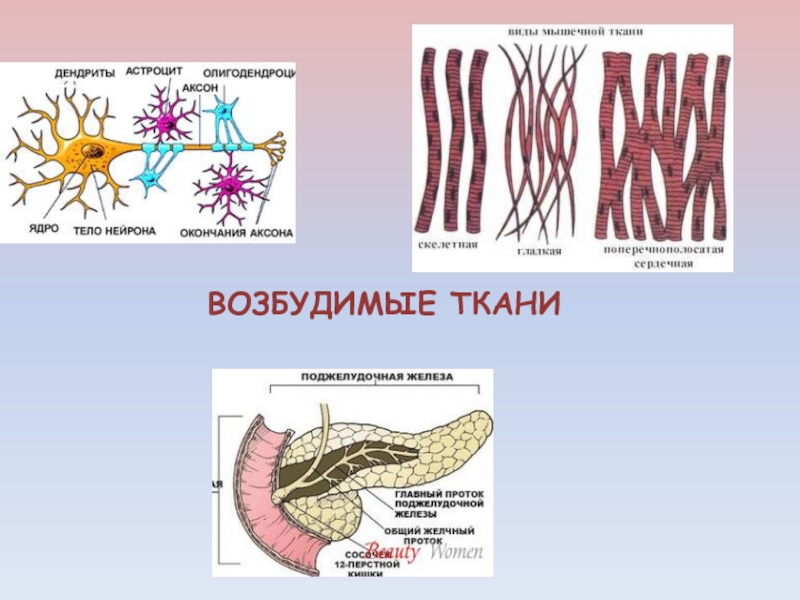
- 3. ВОЗБУДИМЫЕ ТКАНИ
- 4. Мера возбудимости – порог раздражения, т.е. минимальная
- 5. РАЗДРАЖИТЕЛИПОДПОРОГОВЫЕСВЕРХПОРОГОВЫЕПОРОГОВЫЕ
- 6. РАЗДРАЖИТЕЛИФИЗИЧЕСКИЕ (механические, звуковые, световые, температурные, электрические)ХИМИЧЕСКИЕ (щелочи,
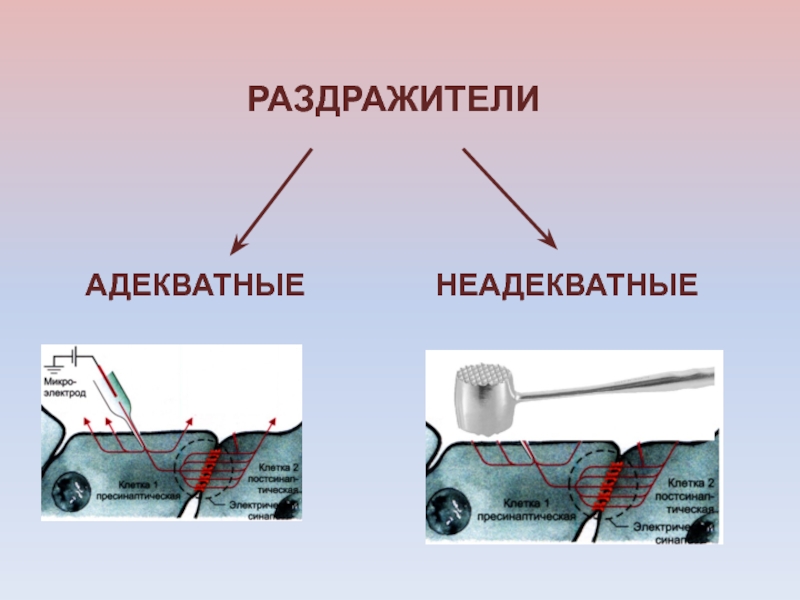
- 7. РАЗДРАЖИТЕЛИНЕАДЕКВАТНЫЕАДЕКВАТНЫЕ
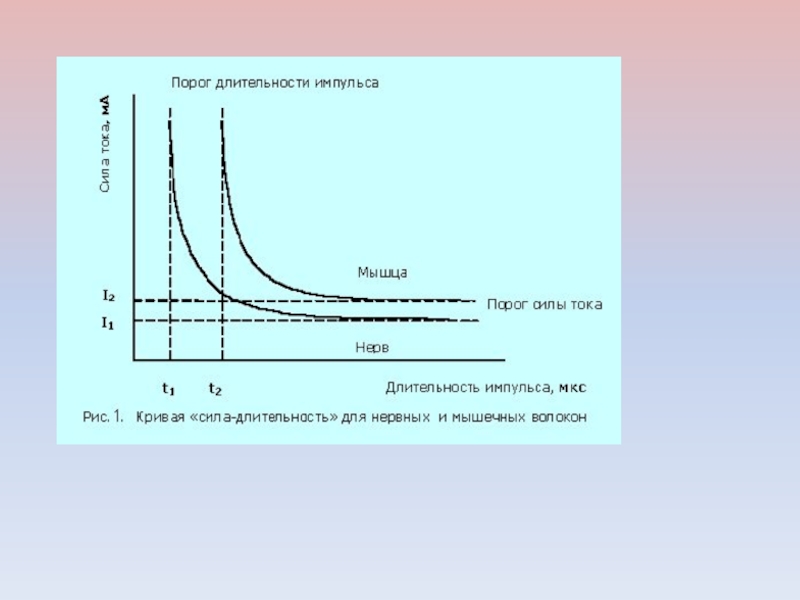
- 8. СООТНОШЕНИЕ МЕЖДУ ПОРОГОВОЙ СИЛОЙ РАЗДРАЖЕНИЯ И ЕГО ДЛИТЕЛЬНОСТЬЮ
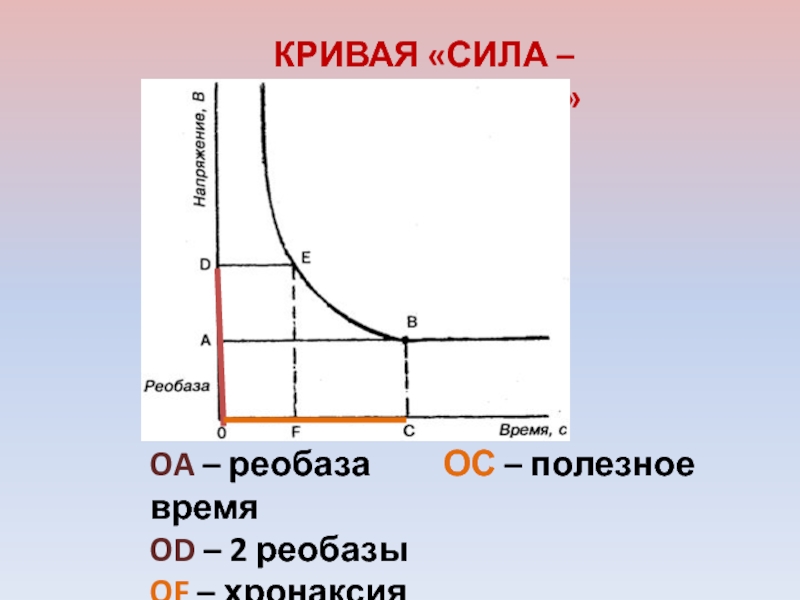
- 9. КРИВАЯ «СИЛА – ДЛИТЕЛЬНОСТЬ» OA – реобаза
- 10. Слайд 10
- 11. МЕТОДЫ ИССЛЕДОВАНИЯ ЭЛЕКТРОВОЗБУДИМЫХ ТКАНЕЙ
- 12. ПРОГРЕСС В ИССЛЕДОВАНИИ БИОПОТЕНЦИАЛОВ ОБЕСПЕЧЕНРАЗРАБОТКОЙ МИКРОЭЛЕКТРОДНОГО МЕТОДА ВНУТРИКЛЕТОЧНОГО ОТВЕДЕНИЯ ПОТЕНЦИАЛОВСОЗДАНИЕ СПЕЦИАЛЬНЫХ УСИЛИТЕЛЕЙ БИОПОТЕНЦИАЛОВВЫБОР УДАЧНЫХ ОБЪЕКТОВ ИССЛЕДОВАНИЯ
- 13. ДИАМЕТР гигантского аксона – 0,5 – 1 мм
- 14. ОСНОВНЫЕ ЭЛЕМЕНТЫ УСТАНОВКИ ДЛЯ ИЗУЧЕНИЯ ВОЗБУДИМЫХ КЛЕТОК
- 15. a - внутриклеточное раздражение и отведение потенциалов
- 16. НЕПОЛЯРИЗУЮЩИЕСЯ ЭЛЕКТРОДЫ: хлорсеребряный электродБлагодаря стабильности потенциала и
- 17. Микроэлектроды введены в 1946 американскими учёными Р.
- 18. Слайд 18
- 19. Внутриклеточная регистрация трансмембранных потенциалов и электростимуляция клеточной
- 20. В лабораторных исследованиях используются металлические микроэлектроды с
- 21. РЕГИСТРАЦИЯ МП НЕРВНОЙ КЛЕТКИ А) путем введения микроэлектрода;Б) путем введения микроэлектрода внутрь аксона
- 22. Слайд 22
- 23. Метод пэтч-кламп введен в лабораторную практику Э. Неером и Б. Сакманом в 1976 г.
- 24. Клеточная мембрана формирует очень плотный контакт с
- 25. Слайд 25
- 26. ИЗМЕРЕНИЯ НА ПРИКРЕПЛЕННОЙ, НО НЕПОВРЕЖДЕННОЙ КЛЕТКЕИЗМЕРЕНИЯ НА ЦЕЛОЙ КЛЕТКЕ ПРИ РАЗРУШЕНИИ МЕМБРАНЫ В КОНЧИКЕ МИКРОПИПЕТКИ
- 27. Слайд 27
- 28. Мембранная теория возбуждения: при раздражении возбудимой клетки
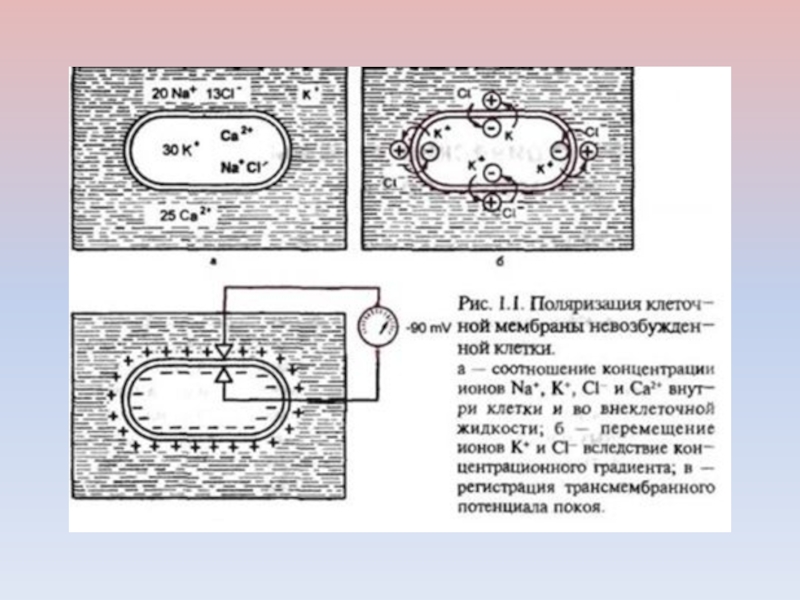
- 29. Основные положения мембранной теории возбуждения сформулированы немецким нейрофизиологом Ю. Бернштейном (1902) ПОЛЯРИЗАЦИЯ КЛЕТОЧНОЙ МЕМБРАНЫ В ПОКОЕ
- 30. Развитие мембранной теории возбуждения получило в трудах
- 31. Регистрация мембранного потенциала покоя А — микроэлектрод 1
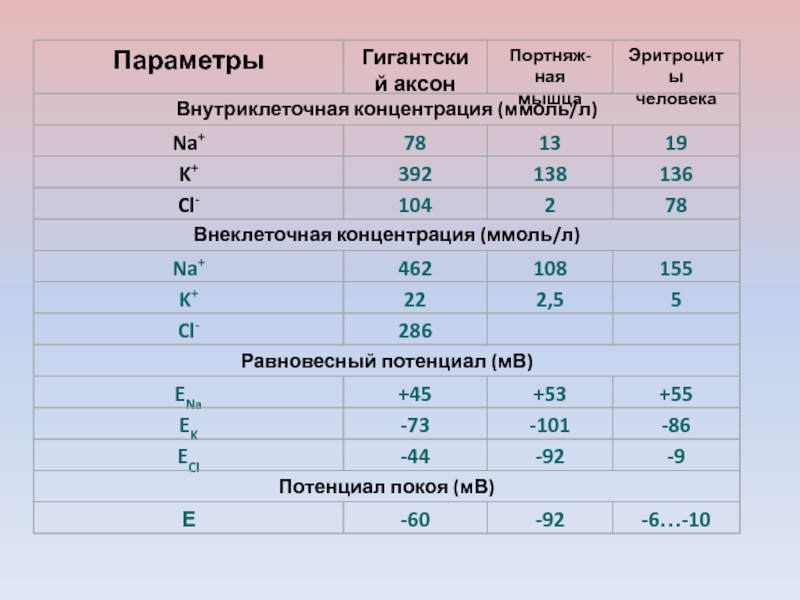
- 32. Потенциал покоя, механизм его формирования
- 33. Предположение Бернштейна:поверхностная мембрана возбудимой клетки в покое
- 34. ДИФФУЗИОННЫЙ ПОТЕНЦИАЛNa+Na+Na+Na+Cl-Cl-Cl-+-ПОДВИЖНОСТЬ ИОНОВ ХЛОРА (v) ВЫШЕ, ЧЕМ ИОНОВ НАТРИЯ (u)
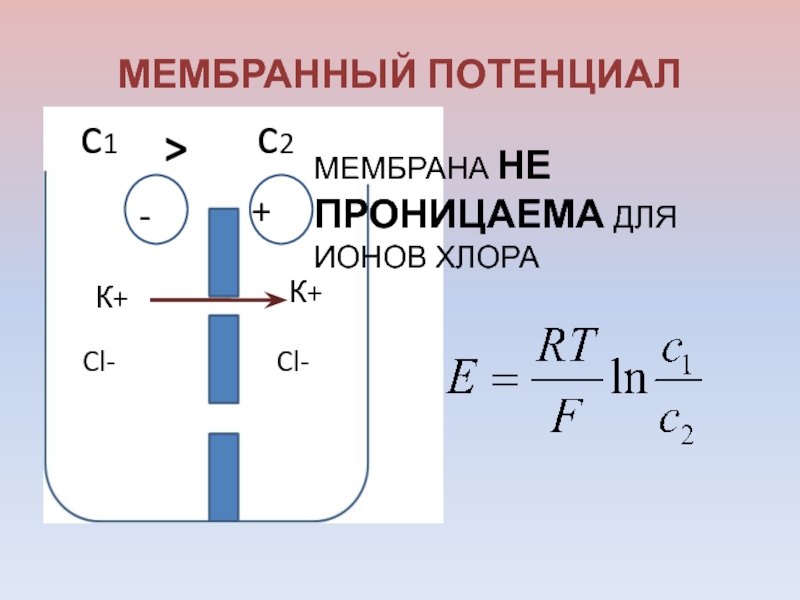
- 35. МЕМБРАННЫЙ ПОТЕНЦИАЛCl-Cl-К+К+МЕМБРАНА НЕ ПРОНИЦАЕМА ДЛЯ ИОНОВ ХЛОРА-+
- 36. ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛУСЛОВИЕ РАВНОВЕСИЯРАВНОВЕСНЫЕ ПОТЕНЦИАЛЫ:ENa=+35…+65 мВEK = -70…-100 мВ
- 37. Возникновение электрохимического равновесия на полупроницаемой мембране. Диффузионное
- 38. Слайд 38
- 39. Зависимость мембранного потенциала (МП) нервного волокна каракатицы
- 40. Зависимость величины ПП от [K+]е (расчетная и
- 41. Слайд 41
- 42. Слайд 42
- 43. состояние равновесия наступает в результате диффузии лишь
- 44. УРАВНЕНИЕ НЕРНСТАЗдесь и далее индекс «е» относится
- 45. Слайд 45
- 46. ПП гигантского аксона кальмара ( - 70
- 47. Итоговая величина ПП, обусловленного переносом многих ионов может быть достаточно точно рассчитана по формуле Гольдмана.
- 48. УРАВНЕНИЕ ГОЛЬДМАНАPK : PNa: PCl = 1
- 49. Вклад активного транспорта в формирование потенциала покоя
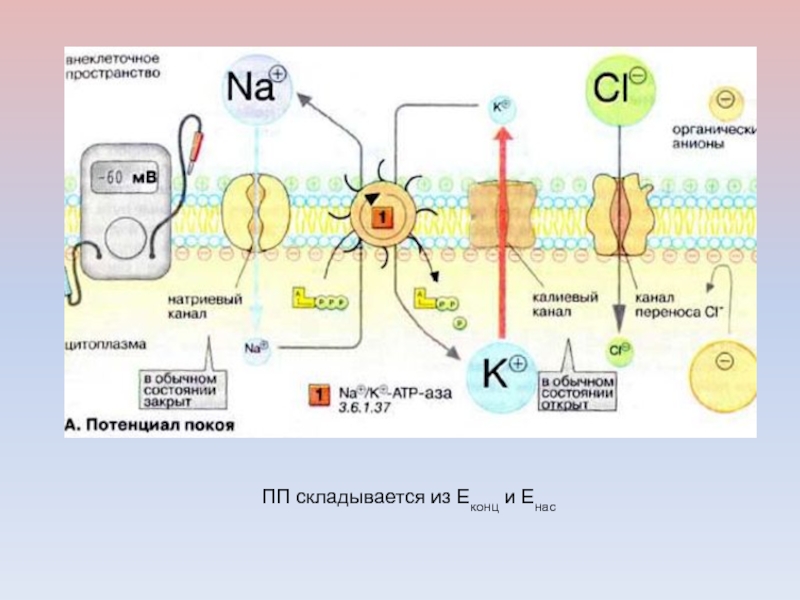
- 50. ПП складывается из Еконц и Енас
- 51. РОЛЬ Na/K НАСОСА В ГЕНЕРАЦИИ ПППоддержание высокой
- 52. Электротонический потенциал и локальный ответ, их сходство и различие
- 53. Схема регистрации мембранного потенциала клетки (А); мембранный
- 54. Изменение мембранного потенциала клетки (А) при действии электрического тока различной силы (Б):
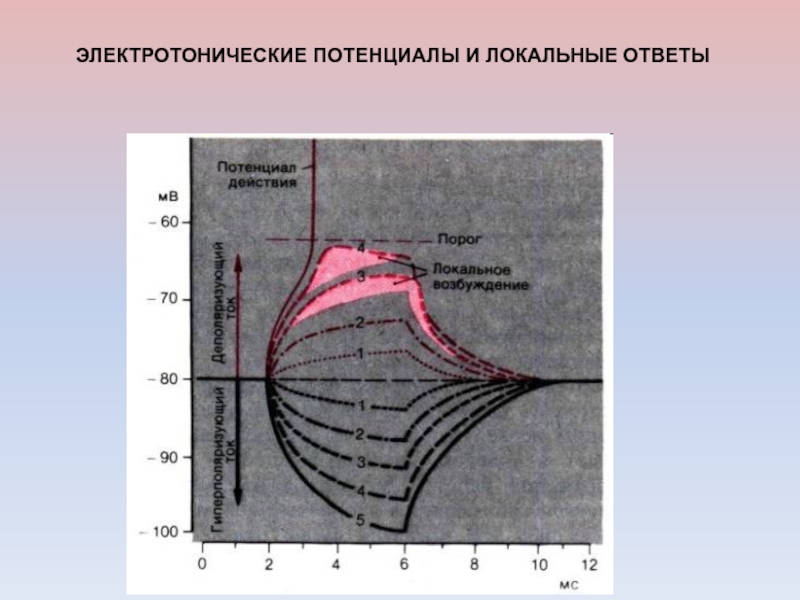
- 55. ЭЛЕКТРОТОНИЧЕСКИЕ ПОТЕНЦИАЛЫ И ЛОКАЛЬНЫЕ ОТВЕТЫ
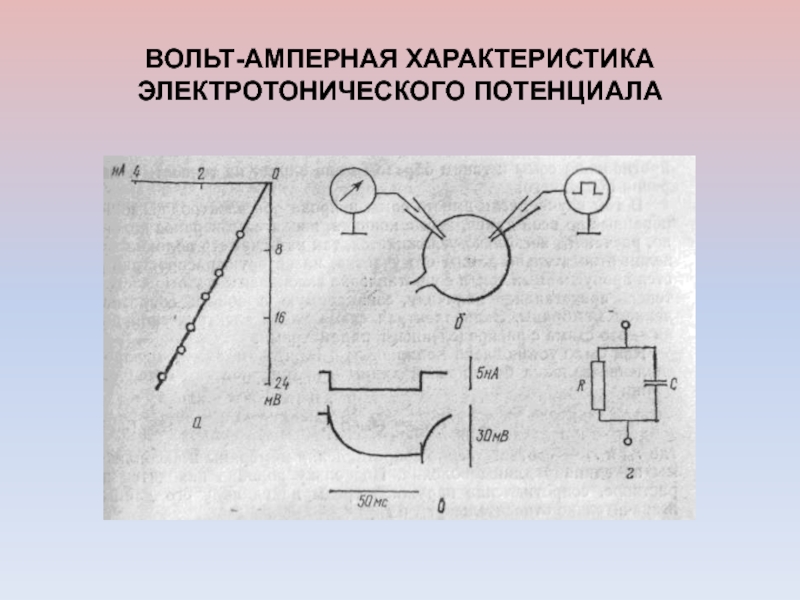
- 56. ВОЛЬТ-АМПЕРНАЯ ХАРАКТЕРИСТИКА ЭЛЕКТРОТОНИЧЕСКОГО ПОТЕНЦИАЛА
- 57. МП - мембранный потенциал покоя, ПД -
- 58. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Раздражимость и возбудимость клеток и тканей. Методы исследования электровозбудимых мембран. Потенциал покоя
и механизм его формирования
Слайд 4Мера возбудимости – порог раздражения, т.е. минимальная сила раздражителя, вызывающая
ответ.
ВОЗБУЖДЕНИЕ – сложный биологический процесс, который характеризуется специфическим изменением обмена
веществ, временной деполяризацией мембраны клеток и проявляющейся специализированной реакцией ткани.Слайд 6РАЗДРАЖИТЕЛИ
ФИЗИЧЕСКИЕ (механические, звуковые, световые, температурные, электрические)
ХИМИЧЕСКИЕ (щелочи, кислоты, гормоны, продукты
обмена веществ)
ФИЗИКО-ХИМИЧЕСКИЕ (изменения осмотического давления, рН и т.п.)
Слайд 12ПРОГРЕСС В ИССЛЕДОВАНИИ БИОПОТЕНЦИАЛОВ ОБЕСПЕЧЕН
РАЗРАБОТКОЙ МИКРОЭЛЕКТРОДНОГО МЕТОДА ВНУТРИКЛЕТОЧНОГО ОТВЕДЕНИЯ ПОТЕНЦИАЛОВ
СОЗДАНИЕ
СПЕЦИАЛЬНЫХ УСИЛИТЕЛЕЙ БИОПОТЕНЦИАЛОВ
ВЫБОР УДАЧНЫХ ОБЪЕКТОВ ИССЛЕДОВАНИЯ
Слайд 14ОСНОВНЫЕ ЭЛЕМЕНТЫ УСТАНОВКИ ДЛЯ ИЗУЧЕНИЯ ВОЗБУДИМЫХ КЛЕТОК И ТКАНЕЙ
1) электроды
для регистрации и стимуляции;
2) усилители биоэлектрических сигналов;
3) регистратор;
4) стимулятор;
5) система для обработки физиологической информации.
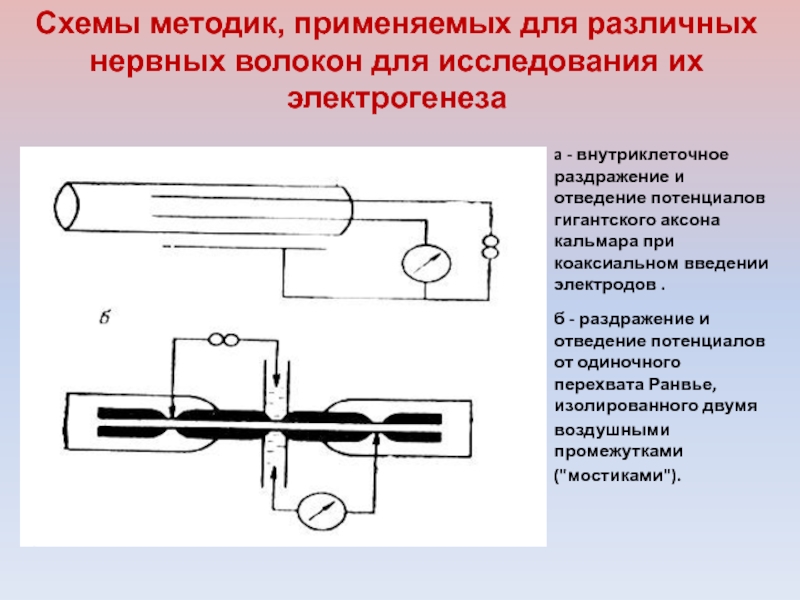
Слайд 15a - внутриклеточное раздражение и отведение потенциалов гигантского аксона кальмара
при коаксиальном введении электродов .
б - раздражение и отведение
потенциалов от одиночного перехвата Ранвье, изолированного двумя воздушными промежутками ("мостиками"). Схемы методик, применяемых для различных нервных волокон для исследования их электрогенеза
Слайд 16НЕПОЛЯРИЗУЮЩИЕСЯ ЭЛЕКТРОДЫ: хлорсеребряный электрод
Благодаря стабильности потенциала и простоте конструкции является
одним из наиболее часто употребляемых в лабораторной практике.
Представляет собой
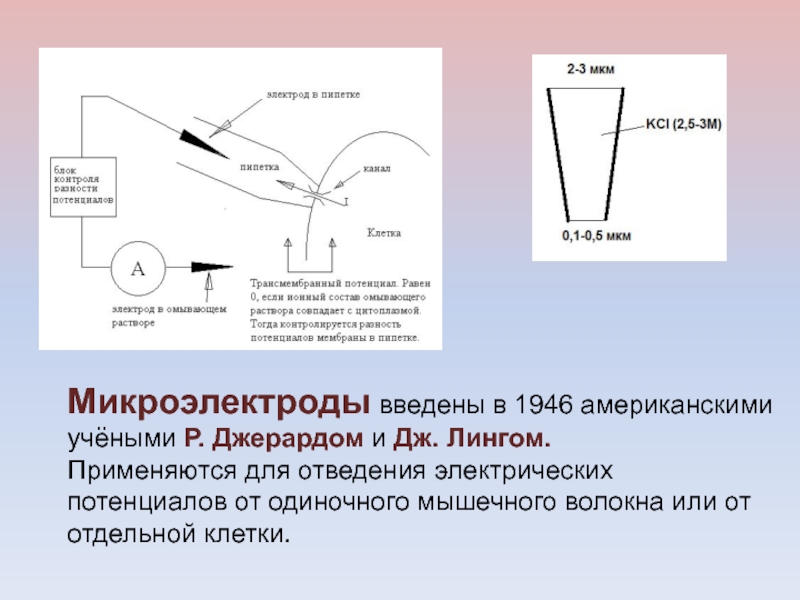
серебряную пластинку или проволочку, покрытую слоем малорастворимой солиПредставляет собой серебряную пластинку или проволочку, покрытую слоем малорастворимой соли серебраПредставляет собой серебряную пластинку или проволочку, покрытую слоем малорастворимой соли серебра (обычно - хлоридаПредставляет собой серебряную пластинку или проволочку, покрытую слоем малорастворимой соли серебра (обычно - хлорида) и опущенной в насыщенный растворПредставляет собой серебряную пластинку или проволочку, покрытую слоем малорастворимой соли серебра (обычно - хлорида) и опущенной в насыщенный раствор хлорида калия.Слайд 17Микроэлектроды введены в 1946 американскими учёными Р. Джерардом и Дж.
Лингом.
Применяются для отведения электрических потенциалов от одиночного мышечного волокна
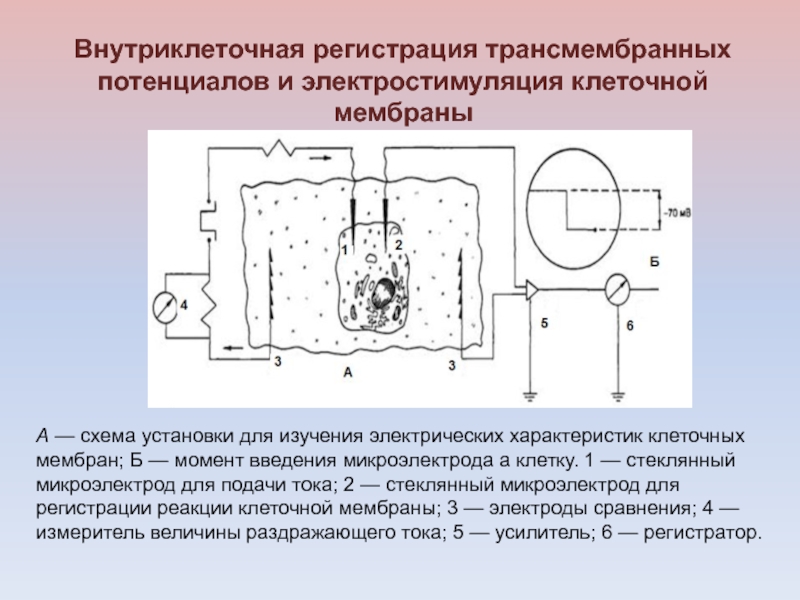
или от отдельной клетки. Слайд 19Внутриклеточная регистрация трансмембранных потенциалов и электростимуляция клеточной мембраны
А — схема
установки для изучения электрических характеристик клеточных мембран; Б — момент
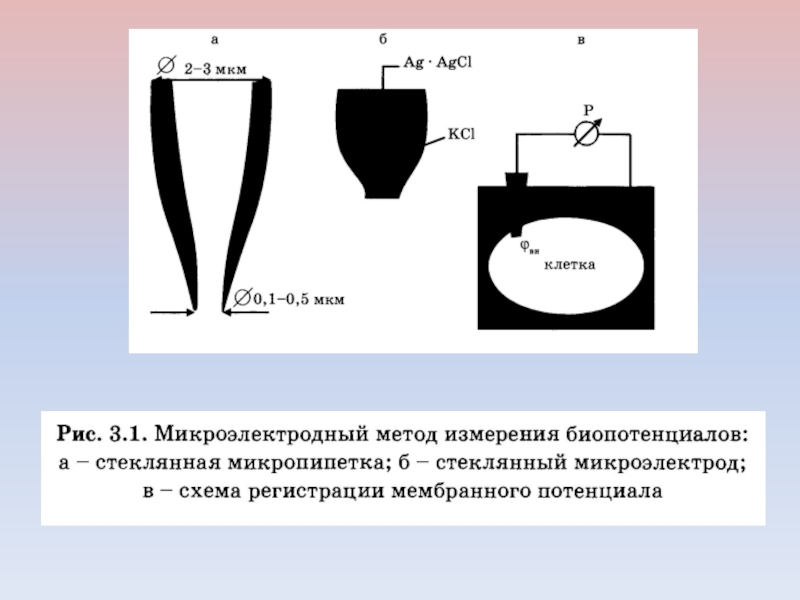
введения микроэлектрода а клетку. 1 — стеклянный микроэлектрод для подачи тока; 2 — стеклянный микроэлектрод для регистрации реакции клеточной мембраны; 3 — электроды сравнения; 4 — измеритель величины раздражающего тока; 5 — усилитель; 6 — регистратор.Слайд 20
В лабораторных исследованиях используются
металлические микроэлектроды с диаметром кончика порядка
1 мкм,
стеклянные микропипетки с диаметром кончика меньше 1 мкм,
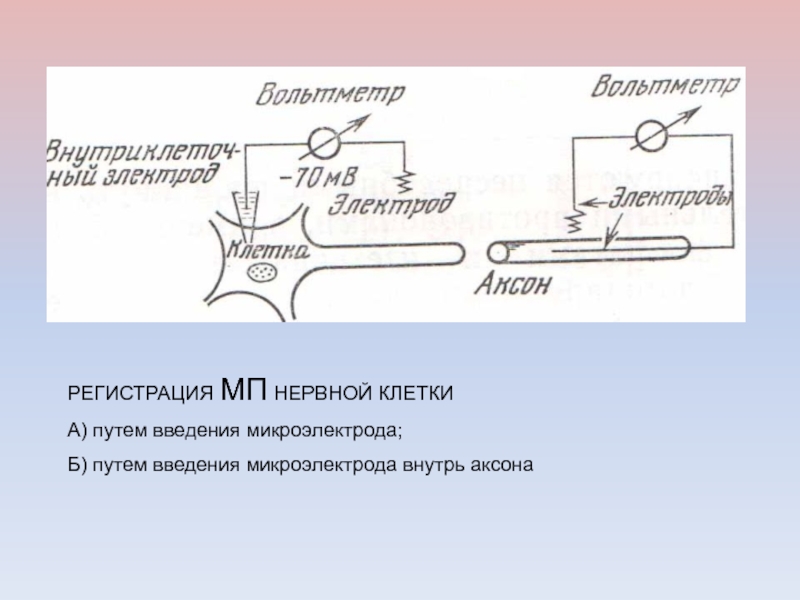
заполненные раствором электролитаСлайд 21РЕГИСТРАЦИЯ МП НЕРВНОЙ КЛЕТКИ
А) путем введения микроэлектрода;
Б) путем введения
микроэлектрода внутрь аксона
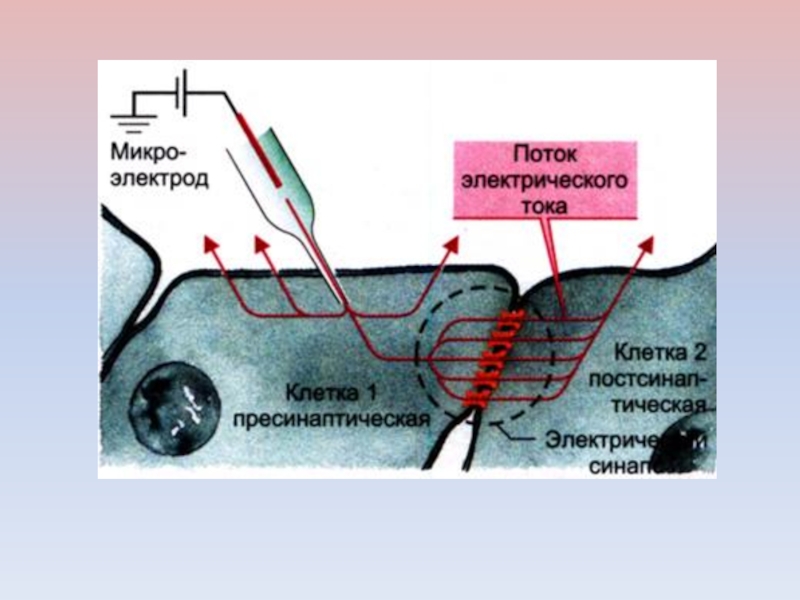
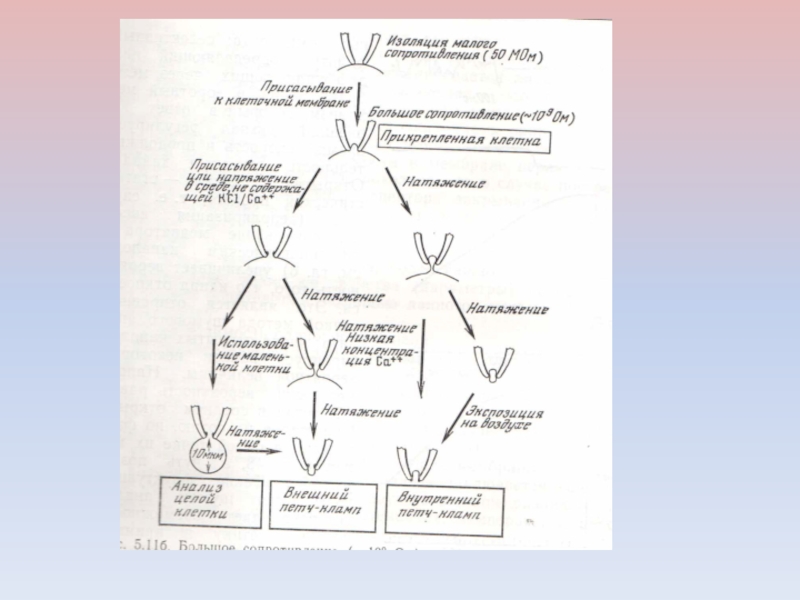
Слайд 24Клеточная мембрана формирует очень плотный контакт с поверхностью кончика микроэлектрода.
Между стеклом и мембранным фрагментом возникает контакт, имеющий гигаомное сопротивление.
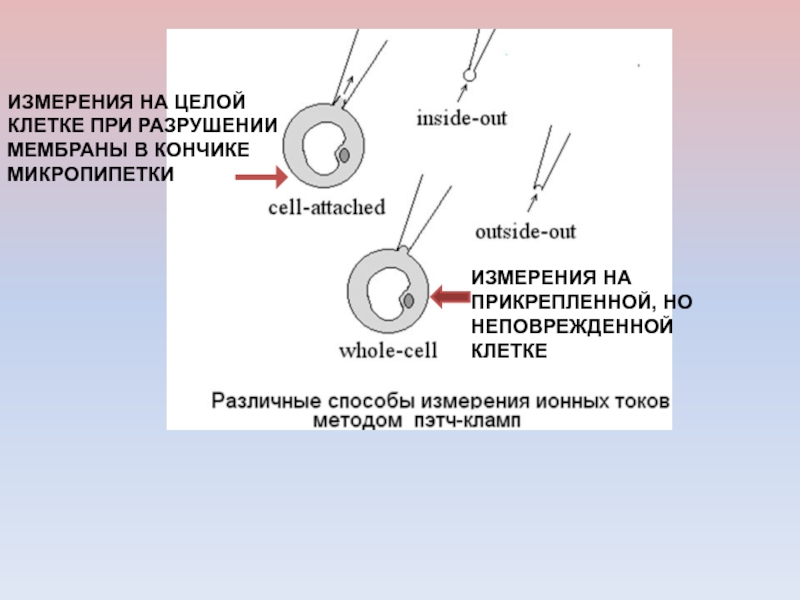
В результате образуется электрически изолированный участок мембраны, и шум регистрирующего сигнала уменьшается на несколько порядков. К участку прикладывается напряжение и меряется возникший ионный ток.Слайд 26ИЗМЕРЕНИЯ НА ПРИКРЕПЛЕННОЙ, НО НЕПОВРЕЖДЕННОЙ КЛЕТКЕ
ИЗМЕРЕНИЯ НА ЦЕЛОЙ КЛЕТКЕ ПРИ
РАЗРУШЕНИИ МЕМБРАНЫ В КОНЧИКЕ МИКРОПИПЕТКИ
Слайд 28Мембранная теория возбуждения:
при раздражении возбудимой клетки в её поверхностной
мембране происходит молекулярная перестройка, которая приводит к изменению проницаемости мембраны
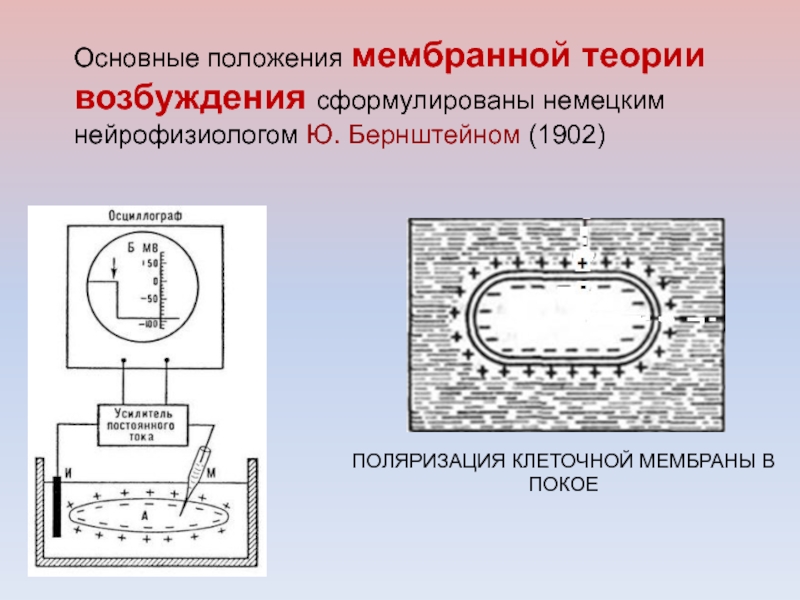
и появлению трансмембранных ионных токов.Слайд 29Основные положения мембранной теории возбуждения сформулированы немецким нейрофизиологом Ю. Бернштейном
(1902)
ПОЛЯРИЗАЦИЯ КЛЕТОЧНОЙ МЕМБРАНЫ В ПОКОЕ
Слайд 30Развитие мембранной теории возбуждения получило в трудах английских учёных: П.
Бойла и Э. Конуэя (1941), А. Ходжкина, Б. Каца, А.
Хаксли (1949).А. ХОДЖКИН
А. ХАКСЛИ
Нобелевская премия по физиологии и медицине, 1963 г
"За открытия, касающиеся ионных механизмов возбуждения и торможения в периферических и центральных участках мембраны нервных клеток"
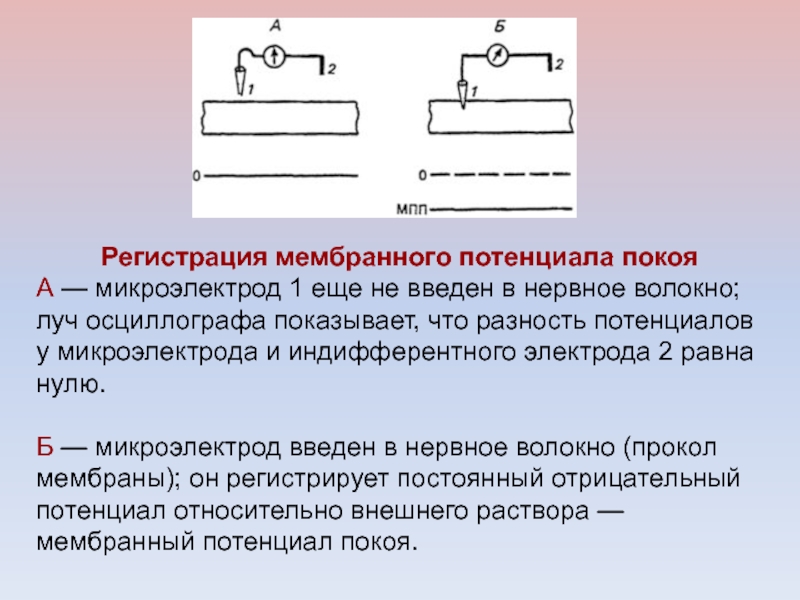
Слайд 31Регистрация мембранного потенциала покоя
А — микроэлектрод 1 еще не введен
в нервное волокно; луч осциллографа показывает, что разность потенциалов у
микроэлектрода и индифферентного электрода 2 равна нулю.Б — микроэлектрод введен в нервное волокно (прокол мембраны); он регистрирует постоянный отрицательный потенциал относительно внешнего раствора — мембранный потенциал покоя.
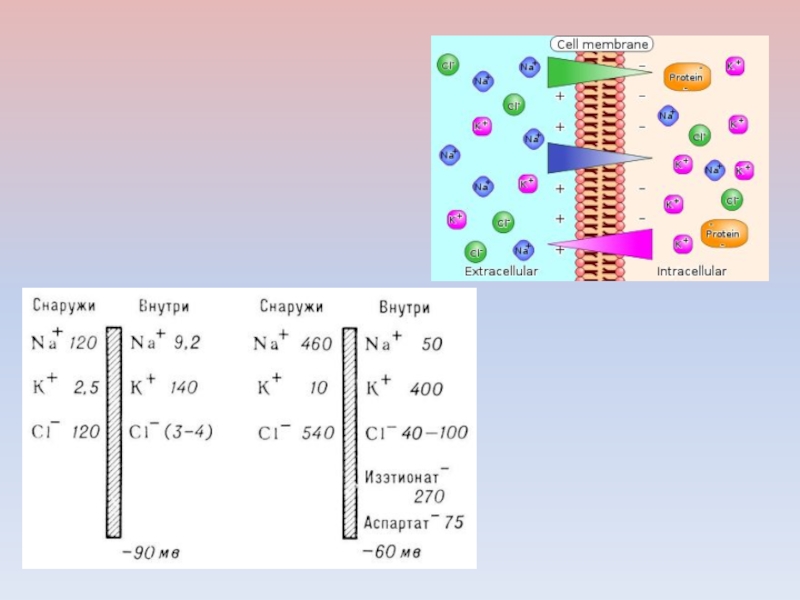
Слайд 33Предположение Бернштейна:
поверхностная мембрана возбудимой клетки в покое обладает избирательной проницаемостью:
ионы K+ проходят через неё гораздо легче, чем ионы Na+
и Cl-.Т. к. концентрация K+ в клетке выше, чем во внеклеточной среде, диффузия этих ионов через мембрану создаёт на ней разность потенциалов —потенциал покоя (ПП), причём внутренняя сторона мембраны оказывается заряженной отрицательно, а внешняя — положительно.
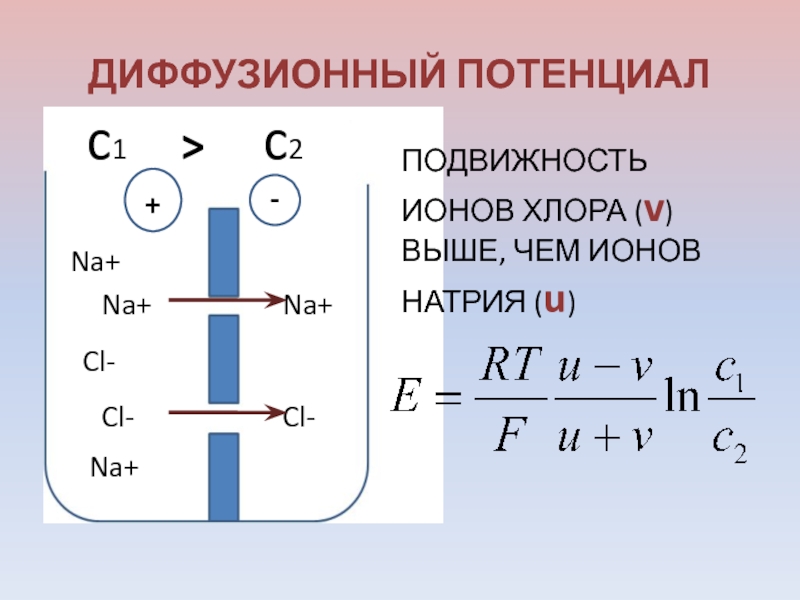
Слайд 34ДИФФУЗИОННЫЙ ПОТЕНЦИАЛ
Na+
Na+
Na+
Na+
Cl-
Cl-
Cl-
+
-
ПОДВИЖНОСТЬ ИОНОВ ХЛОРА (v) ВЫШЕ, ЧЕМ ИОНОВ НАТРИЯ (u)
Слайд 36
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ
УСЛОВИЕ РАВНОВЕСИЯ
РАВНОВЕСНЫЕ ПОТЕНЦИАЛЫ:
ENa=+35…+65 мВ
EK = -70…-100 мВ
Слайд 37
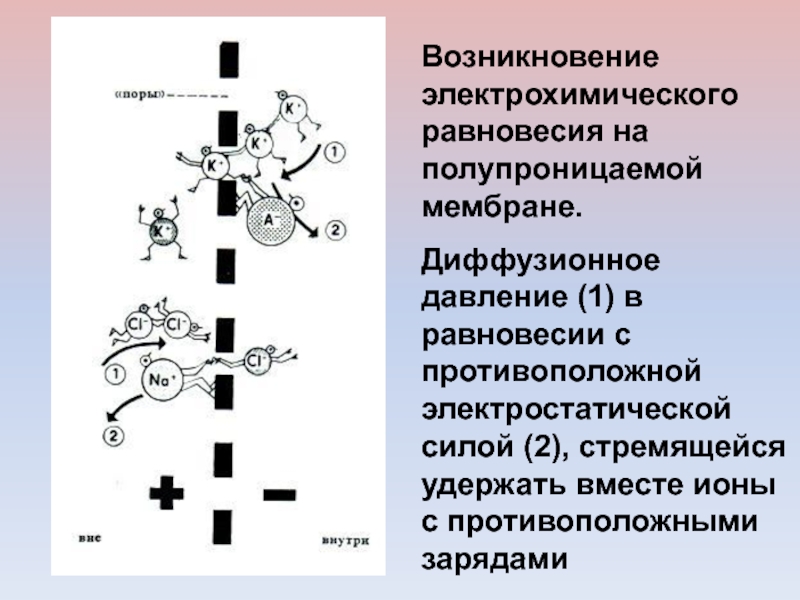
Возникновение электрохимического равновесия на полупроницаемой мембране.
Диффузионное давление (1) в
равновесии с противоположной электростатической силой (2), стремящейся удержать вместе ионы
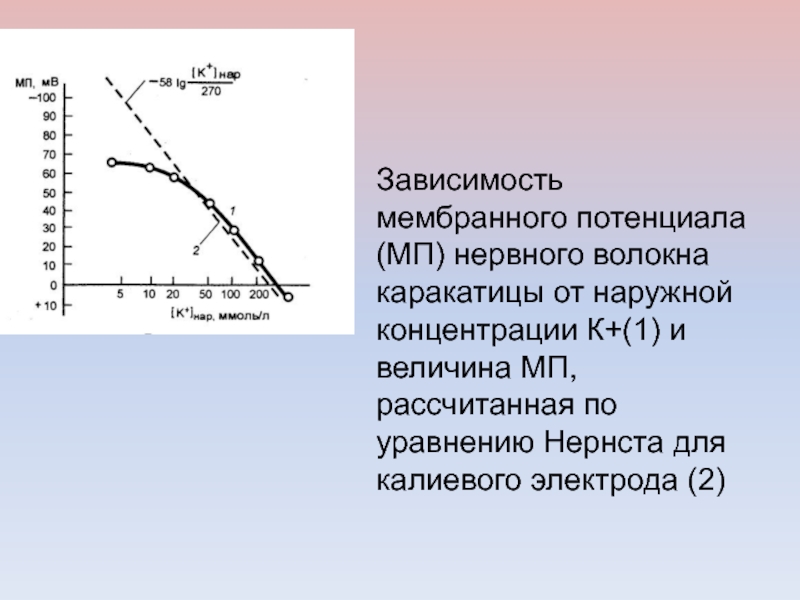
с противоположными зарядамиСлайд 39Зависимость мембранного потенциала (МП) нервного волокна каракатицы от наружной концентрации
К+(1) и величина МП, рассчитанная по уравнению Нернста для калиевого
электрода (2)Слайд 40Зависимость величины ПП от [K+]е (расчетная и экспериментальная кривые).
По
оси абсцисс – содержание калия во внешней среде в мМ,
по оси ординат – величина мембранного потенциала в мВ.Слайд 43состояние равновесия наступает в результате диффузии лишь очень небольшого количества
ионов (по сравнению с их общим содержанием);
калиевый равновесный потенциал всегда
больше (по абсолютному значению) реального потенциала покояСлайд 44УРАВНЕНИЕ НЕРНСТА
Здесь и далее индекс «е» относится к внешним концентрациям
ионов, а индекс «i» - ко внутренним.
Слайд 46ПП гигантского аксона кальмара ( - 70 мВ) близок к
его Ек ( - 75 мВ), но не равен ему.
ПРИЧИНА:ПП
формирует утечка и других ионов: Na+, Cl-. При этом поступление Сl- в аксон, (Еcl> - 70 мВ) повышает, a Na+ понижает ПП (ENa=+55MB).
Слайд 47Итоговая величина ПП, обусловленного переносом многих ионов может быть достаточно
точно рассчитана по формуле Гольдмана.
Слайд 48УРАВНЕНИЕ ГОЛЬДМАНА
PK : PNa: PCl = 1 : 0,04 :
0,45
Соотношение проницаемостей потенциалообразующих ионов в состоянии покоя
Слайд 51РОЛЬ Na/K НАСОСА В ГЕНЕРАЦИИ ПП
Поддержание высокой концентрации К+ внутри
клетки, что обеспечивает постоянство величины ПП. Электрогенность насоса: вклад в
ПП.Поддержание низкой концентрации Na+ внутри клетки, что, с одной стороны, обеспечивает генерацию потенциала действия, с другой — обеспечивает сохранение нормальных осмолярности и объема клетки.
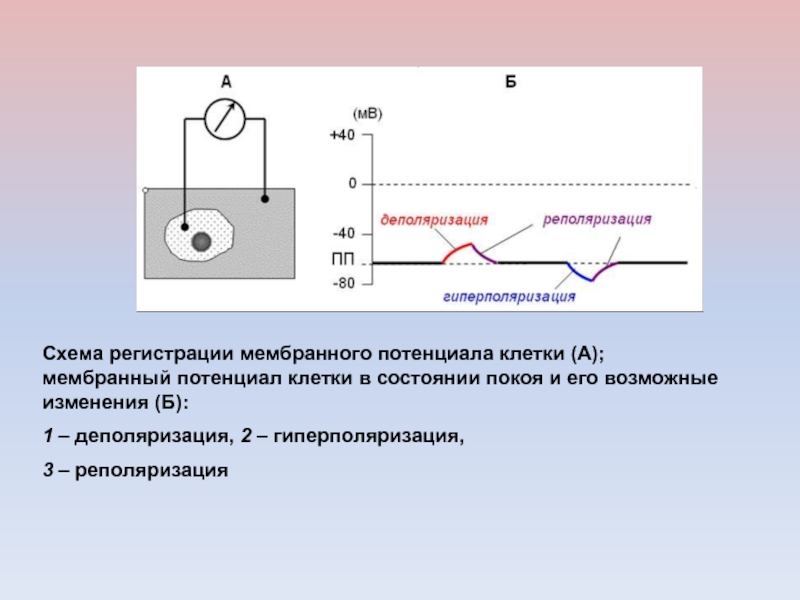
Слайд 53Схема регистрации мембранного потенциала клетки (А); мембранный потенциал клетки в
состоянии покоя и его возможные изменения (Б):
1 – деполяризация, 2
– гиперполяризация, 3 – реполяризация
Слайд 54Изменение мембранного потенциала клетки (А) при действии электрического тока различной
силы (Б):
Слайд 57
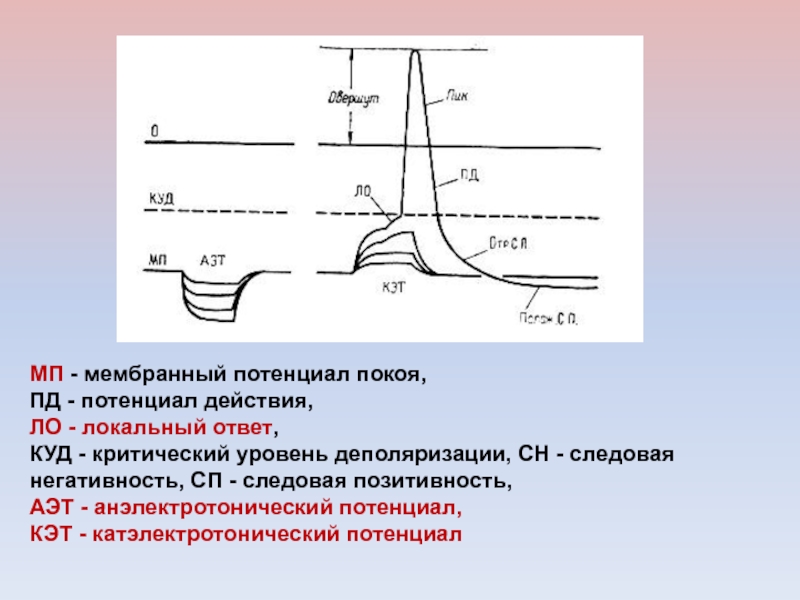
МП - мембранный потенциал покоя,
ПД - потенциал действия,
ЛО
- локальный ответ,
КУД - критический уровень деполяризации, СН -
следовая негативность, СП - следовая позитивность, АЭТ - анэлектротонический потенциал,
КЭТ - катэлектротонический потенциал




















![Раздражимость и возбудимость клеток и тканей. Методы исследования электровозбудимых мембран. Потенциал покоя и механизм его форм Зависимость величины ПП от [K+]е (расчетная и экспериментальная кривые). По оси Зависимость величины ПП от [K+]е (расчетная и экспериментальная кривые). По оси абсцисс – содержание калия во внешней](/img/thumbs/2fcc56e48b5b58a64ff08fe9e839d67c-800x.jpg)