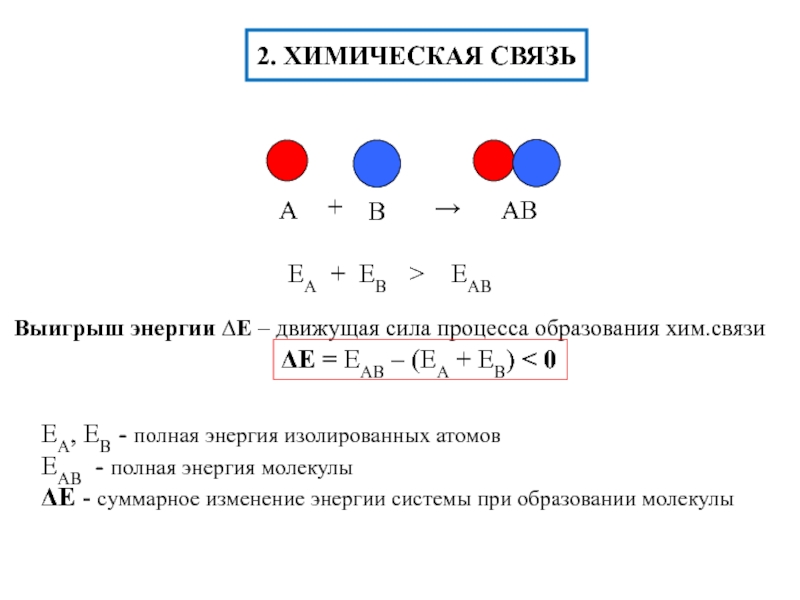
интеграл» - описывает изменение ∆Е энергии системы из-за электростатич.взаимодействия ядер
и эл-нов (в молекуле водорода Н2)
I – «обменный интеграл», «интеграл обменного взаимодействия» - ∆Е вследствие неразличимости эл-нов (электрон принадлежит обоим ядрам)
S –“интеграл перекрывания”-∆Е вследствие перекрывания АО - 0S<1
r: Q0, I 0, S 0 r0: Q 0, I 0, S 1
r rсв Q < 0, I < 0, причем Q<I, 0 < S < 1 → (1 ± S2) > 0 Всё зависит от знака обменного интеграла I в ∆E(r)s и ∆E(r)A [см. слайд 8]
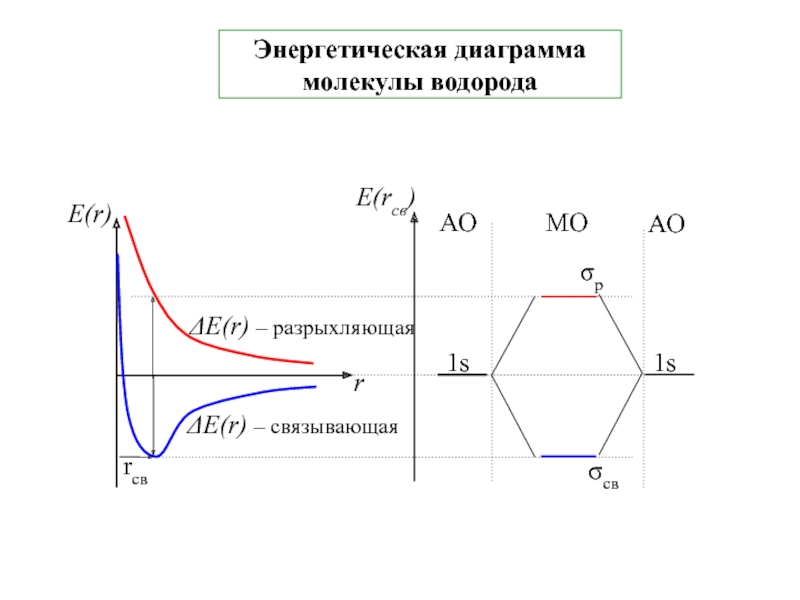
Получаем ∆E(r)s < 0, а ∆E(r)A > 0. Тогда
E < 2ЕО для ∆E(r)s [Е = 2Ео + ΔЕ(r)S, A,] - выигрыш энергии → образование связи между атомами и следовательно молекулы Н2.
E > 2ЕО для ∆E(r)A – связь между атомами водорода не образуется т.к. энергия Е связанной системы (молекулы Н2) больше энергии двух изолированных атомов 2ЕО
Вывод: при образовании хим.связи основное значение имеет обменное взаимодействие, удовлетворяющее условию антипараллельности (↑↓) спинов электронов
![2. ХИМИЧЕСКАЯ СВЯЗЬ 2.1 Кривая Морзе. Основные параметры химической связиrсв[Å] - длина химической связиEсв[эВ, 2.1 Кривая Морзе. Основные параметры химической связиrсв[Å] - длина химической связиEсв[эВ, кДжмоль] - энергия химической связиα А-В-С](/img/thumbs/8c93605a8d3a0c58e2d5265bd4373580-800x.jpg)

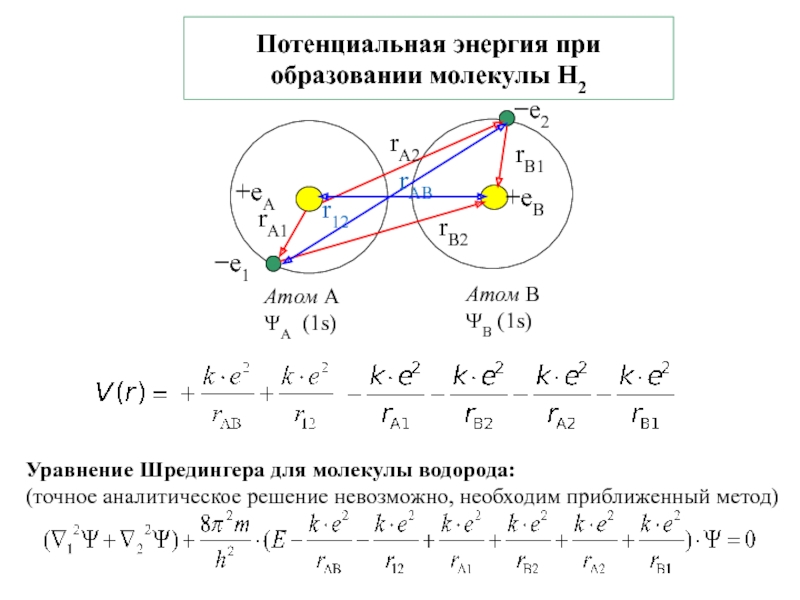

![2. ХИМИЧЕСКАЯ СВЯЗЬ Решение ур.Шредингера [подстановка S и А в ур.Шредингера и нахождение Решение ур.Шредингера [подстановка S и А в ур.Шредингера и нахождение ΔЕ(r)S и ΔЕ(r)A соответственно]](/img/thumbs/e545b2cfde1cdf9c8d87115c6f4cd6b0-800x.jpg)

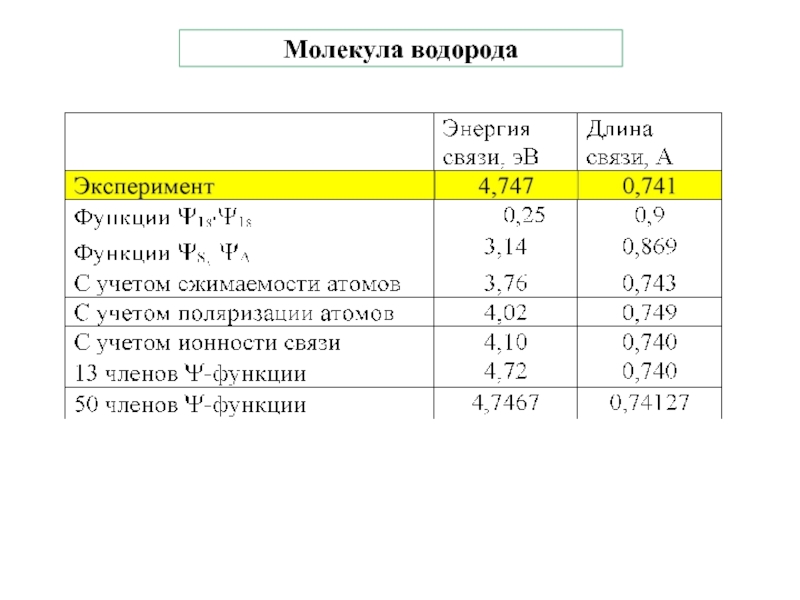

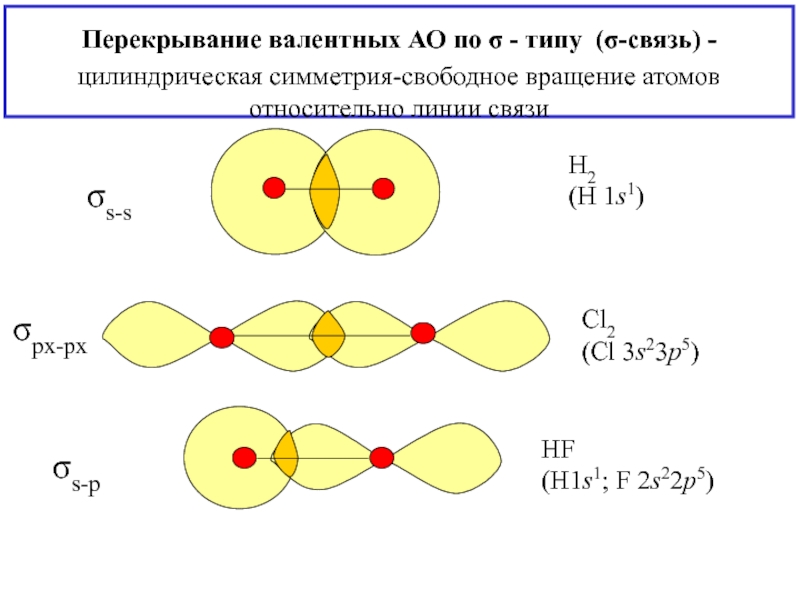
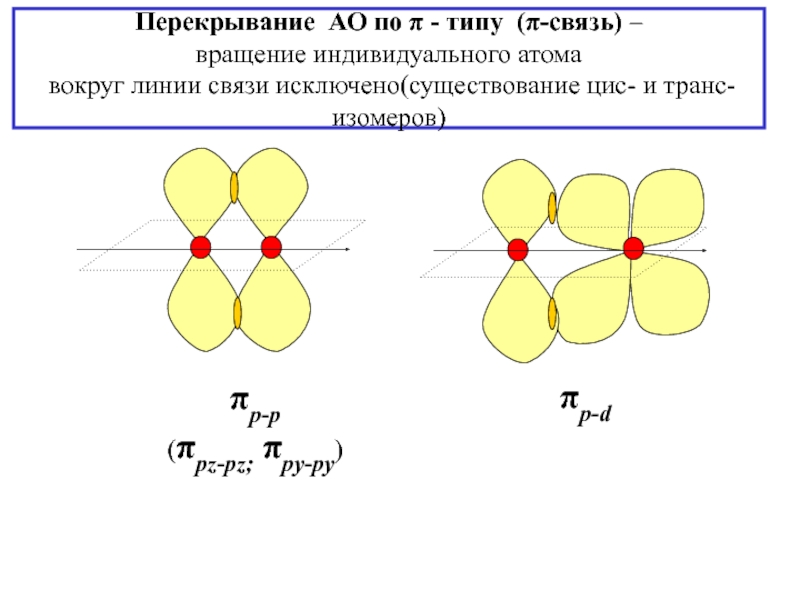


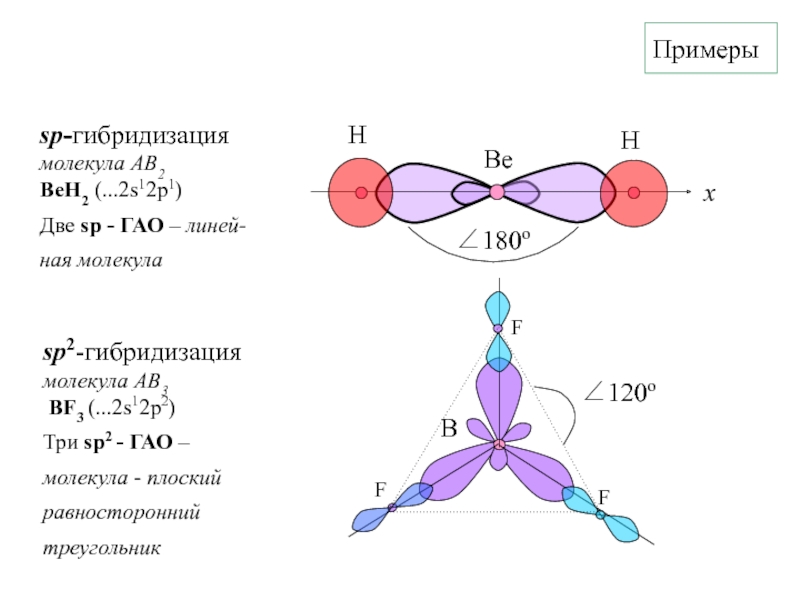
![2. ХИМИЧЕСКАЯ СВЯЗЬ Примерdsp2-гибридизация молекулярный ион [CuCl4]-2 плоский квадрат Cu Примерdsp2-гибридизация молекулярный ион [CuCl4]-2 плоский квадрат Cu](/img/thumbs/a46a5559a121f5cf68c725519e162a03-800x.jpg)
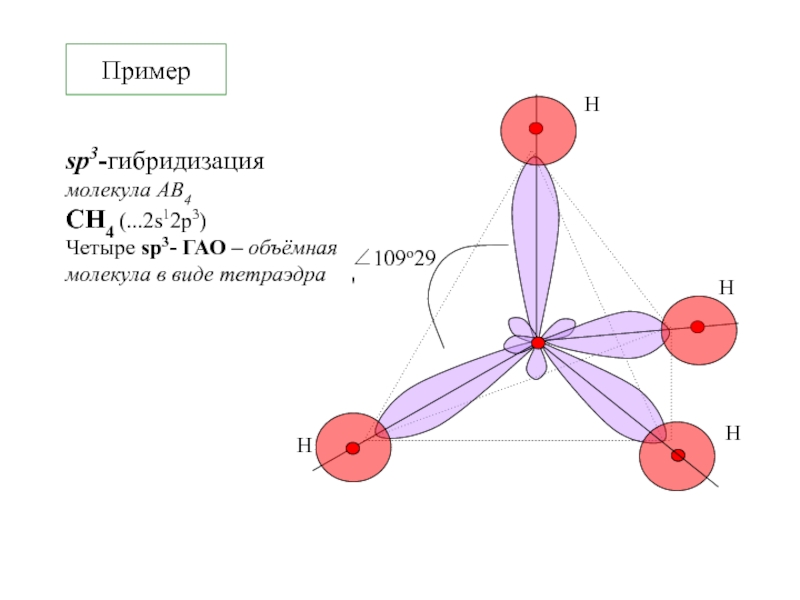
![2. ХИМИЧЕСКАЯ СВЯЗЬ Ион [NH4]+ NH3 + H+ [NH4]+Из эксперимента - четыре равноценных Ион [NH4]+ NH3 + H+ [NH4]+Из эксперимента - четыре равноценных атома водорода, тетраэдрическая конфигурация sp3-гибридизация](/img/thumbs/52d87459a16d9ee7454e1fce4f73f47d-800x.jpg)


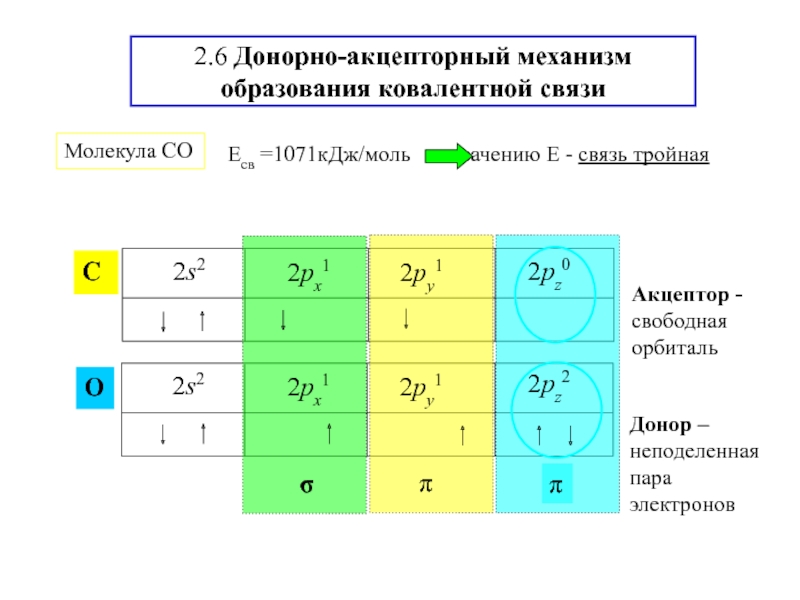
![2. ХИМИЧЕСКАЯ СВЯЗЬ Пример: энергетическая диаграмма молекулы NOПарамагнетик – наличие неспаренных электронов на МОДиамагнетик Пример: энергетическая диаграмма молекулы NOПарамагнетик – наличие неспаренных электронов на МОДиамагнетик – отсутствие неспаренных электроновNO [св(s)]2 [(s)](/img/thumbs/0de3b99a7ccf67014b3aadbca17ecb3c-800x.jpg)