Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Аммнок-ты углеводы1.ppt
Содержание
- 1. Аммнок-ты углеводы1.ppt
- 2. Содержание лекции № 1Классификация, номенклатураХимические св-ваβ-лактамные антибиотики:
- 3. Классификация, номенклатура2HN-(CH2)n-CH-COOH
- 4. Алифатические аминокислотыГлицин, аланин, валин, лейцин и изолейцин
- 5. ГидроксиаминокислотыСерин, треонин, тирозин
- 6. Дикарбоновые аминокислоты и их амидыАспарагиновая, глутаминовая, аспарагин, глутамин
- 7. Аминокислоты с катионообразующими группамиГистидин, лизин, аргинин
- 8. Серосодержащие аминокислотыЦистеин, цистин, метионин
- 9. Ароматические аминокислотыФенилаланин, тирозин, триптофан
- 10. Иминокислота Пролин Аминокислоты делятся на полярные и
- 11. Незаменимые аминокислоты (8)Лизин
- 12. Оптическая изомерия α-аминокислот
- 13. Кислотно-основные свойстваR-CH-COOH R-CH-COO- R-CH-COO-
- 14. Химические свойства Дезаминирование а/кR-CH-COOH + HNO2
- 15. Химические свойстваДекарбоксилированиеR-CH-COOH R-CH2-NH2
- 16. Декарбоксилирование а/кHOOC-CH-CH2-CH2-COOH NH2-CH2-CH2-CH2-COOH
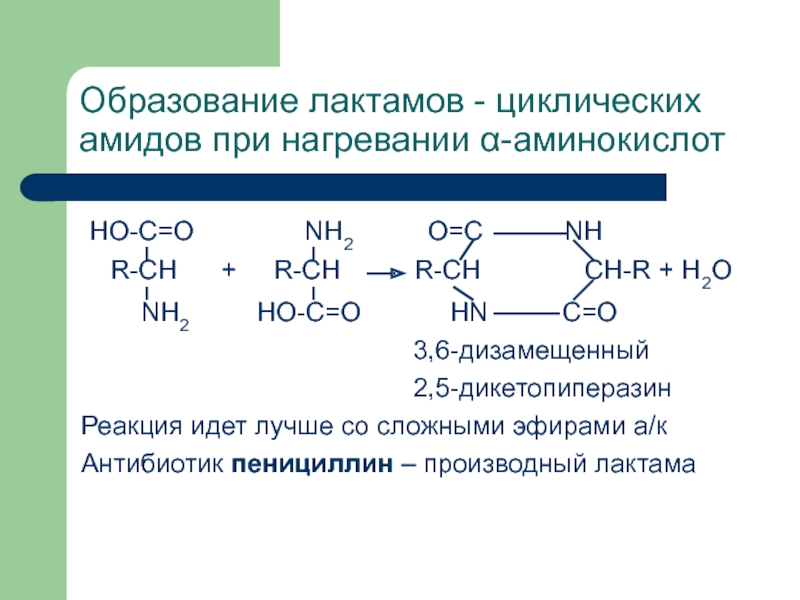
- 17. Образование лактамов - циклических амидов при нагревании
- 18. Количественный и качественный анализ а/кФормольное титрованиеR-CH-COOH
- 19. Пептиды и белкиПептиды содержат от 2 до
- 20. Структура белковБелки – биополимеры со сложной пространственной
- 21. Частичный и полный гидролиз полипептидов
- 22. п-аминобензойная кислота и ее производныеновокаин новокаинамид
- 23. Содержание лекции № 2Моносахариды. Классификация: альдозы и
- 24. Оптическая изомерия углеводов
- 25. Скачать презентанцию
Содержание лекции № 1Классификация, номенклатураХимические св-ваβ-лактамные антибиотики: пенициллинα-аминокислоты. Классификация, биполярная структура, стереоизомерия, качественные реакцииПептиды, белки. Пептидная связь, структура, гидролизп-аминобензойная кислота и ее производные (новокаин, новокаинамид)
Слайды и текст этой презентации
Слайд 2Содержание лекции № 1
Классификация, номенклатура
Химические св-ва
β-лактамные антибиотики: пенициллин
α-аминокислоты. Классификация, биполярная
структура, стереоизомерия, качественные реакции
и ее производные (новокаин, новокаинамид)Слайд 3Классификация, номенклатура
2HN-(CH2)n-CH-COOH
R
n=0, α-аминокислоты
n=1, β-аминокислоты
Аминокислоты – поли-функциональные соединения, которые содержат
карбоксильную группу, аминогруппу и могут содержать другие функциональные группы в боковом радикале R
Слайд 10Иминокислота
Пролин
Аминокислоты делятся на полярные и неполярные. Полярные, например,
аспарагиновая кислота, гидроксиаминокислоты.
Неполярные: алифатические, пролин и др.
Слайд 11Незаменимые аминокислоты (8)
Лизин
Метионин
Фенилаланин
ЛейцинВалин Изолейцин
Треонин Триптофан
Заменимые синтезируются в организме из α-кетокислот
Слайд 13Кислотно-основные свойства
R-CH-COOH R-CH-COO- R-CH-COO-
+NH3
+NH3 NH2
катион диполярный анион
ион
цвиттер-ион
рН<7 рН=7 рН>7
Соли с Cu2+ - хелаты синего цвета
Слайд 14Химические свойства Дезаминирование а/к
R-CH-COOH + HNO2 R-CH-COOH
+ N2 + H2O
NH2
OH гидроксикислота
В организме дезаминирование происходит под действием ферментов - дезаминаз
Слайд 15Химические свойства
Декарбоксилирование
R-CH-COOH R-CH2-NH2 + CO2
NH2
OH-CH2-CH-COOH ферм. OH-CH2-CH2-NH2
NH2 этаноламин (коламин)серин биогенный амин
входит в состав фосфолипидов
Слайд 16Декарбоксилирование а/к
HOOC-CH-CH2-CH2-COOH NH2-CH2-CH2-CH2-COOH
NH2
γ-аминомасляная к-таглутаминовая а/к ГАМК
нейромедиатор головного
мозга
гистидин гистамин
выбрасывается в кровь
при повреждении тканей,
образуется под действием Ig
Слайд 17Образование лактамов - циклических амидов при нагревании α-аминокислот
HO-C=O
NH2
O=C NHR-CH + R-CH R-CH CH-R + H2O
NH2 HO-C=O HN C=O
3,6-дизамещенный
2,5-дикетопиперазин
Реакция идет лучше со сложными эфирами а/к
Антибиотик пенициллин – производный лактама
Слайд 18Количественный и качественный анализ а/к
Формольное титрование
R-CH-COOH + CH2=O
R-CH-COOH
NH2
NHCH2OHметилольное производное
ОснОвные свойства метилольного производного снижены, его можно титровать щелочью для определения кислоты.
Нингидриновая реакция с а/к и белками – качественная (сине-фиолетовое окрашивание). Обнаруживают менее 1 мкг альфа и бета-а/к; мешают амины, аммиак, мочевина.
Слайд 19
Пептиды и белки
Пептиды содержат от 2 до 50 остатков а/к,
между которыми – пептидная связь. Синтез трипептидов:
NH2-CH-COOH + NH2-CH-COOH
+ NH2-CH-COOH R1 R2 R3 -2H2O
O O
NH2-CH-C-NH-CH-C-NH-CH-COOH
R1 R2 R3
Например, R1=Ala, R2=Met, R3=Phe: Ala-Met-Phe
Слайд 20Структура белков
Белки – биополимеры со сложной пространственной структурой, состоящие из
остатков а/к, соединенных пептидной связью.
Первичная структура – последовательность а/к.
Вторичная структура:
спираль, складчатый лист, статистический клубок. Первые две образованы водородными связями, последняя – хаотична.Третичная структура – сложная пространственная; формируется как правило, ковалентными сшивками (S-S-мостики) и др. взаимодействиями.
Четвертичная - агрегат 2-х и более полипептидных цепей, удерживаемых межмолекулярными водородными связями, электростатическими и т.д.
Слайд 21Частичный и полный гидролиз полипептидов
O
O ферментNH2-CH-C-NH-CH-C-NH-CH-COOH + H2O
R1 R2 R3
NH2-CH-COOH + NH2-CH-COOH + NH2-CH-COOH
R1 R2 R3
Частичный гидролиз белка происходит, если не все пептидные связи разрываются
Слайд 23Содержание лекции № 2
Моносахариды. Классификация: альдозы и кетозы, пентозы и
гексозы. Стереоизомерия: D-, L-ряды. Открытые и циклические формы: пиранозы, фуранозы.
Таутомерия, мутаротация, α, β-аномеры. Конформация D-глюкозы.Химические свойства. Образование простых и сложных эфиров. Реакции полуацетальной группы: восст. св-ва, образование О-гликозидов. N-гликозиды, гидролиз.
Окисление моносахаридов. Глюконовая, глюкаровая, глюкуроновая кислоты. Восстановление моносахаридов до полиолов (сорбит).
Пентозы: D-рибоза, 2-дезокси-D-рибоза. Гексозы: глюкоза, галактоза, фруктоза. Аминосахара (D-глюкозамин, N-ацетил-D-глюкозамин). Аскорбиновая кислота.
Олигосахариды. Строение. Восстановительные св-ва. Гидролиз.
Мальтоза, лактоза, сахароза.
Полисахариды. Строение. Гомо- и гетерополисахариды. Гидролиз.
Крахмал (амилоза и амилопектин), гликоген, целлюлоза.
Гиалуроновая кислота, хондроитинсульфат, гепарин.