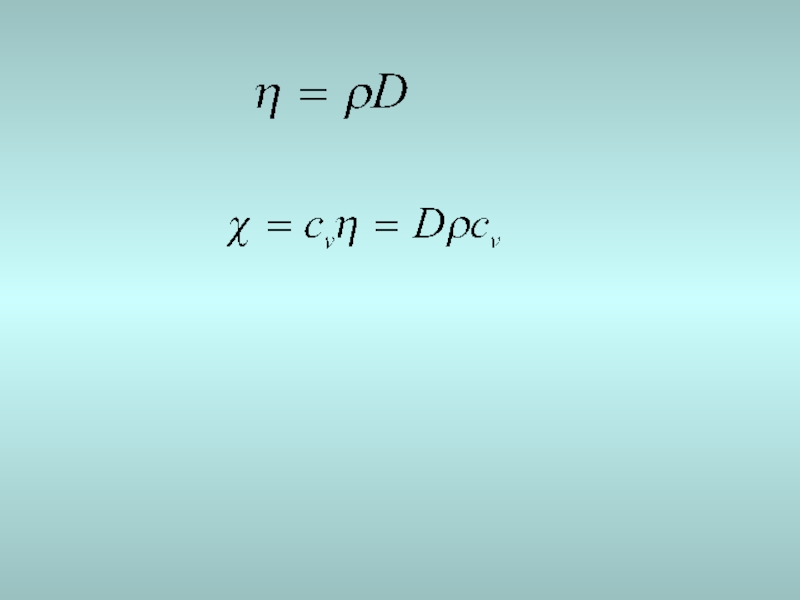Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Қарағанды мемлекеттік техникалық университеті Физика кафедрасы ФИЗИКА
Содержание
- 1. Қарағанды мемлекеттік техникалық университеті Физика кафедрасы ФИЗИКА
- 2. Эффективтік диаметрТасымалдау құбылысыМолекуллрдың өзара әсерлесуіВан-дер-Ваальс теңдеуіВан-дер-Ваальс изотермасыФазалық ауысу Күй диаграммасыДәріс жоспары
- 3. МОЛЕКУЛАНЫҢ ЭФФЕКТИВТІК ДИАМЕТРІdМолекуланың эффективтік диаметрі – молекулалардың
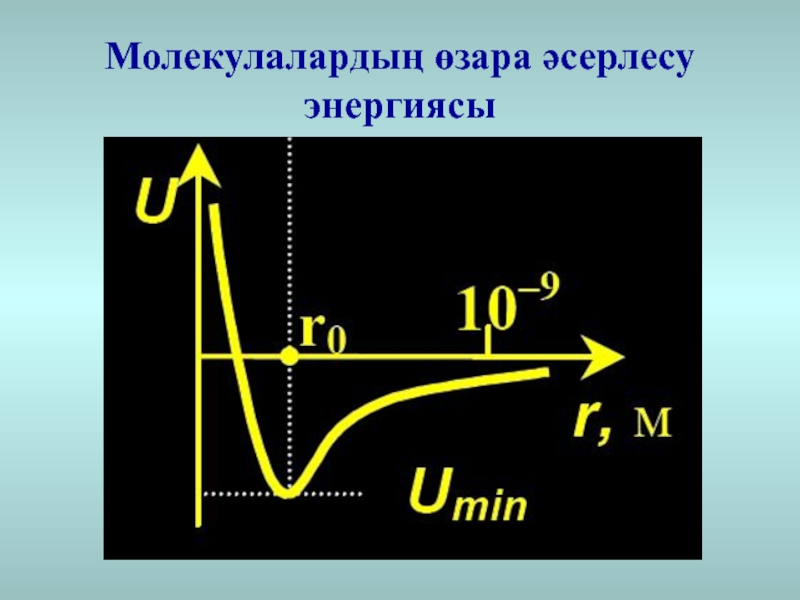
- 4. Молекулалардың өзара әсерлесу энергиясы
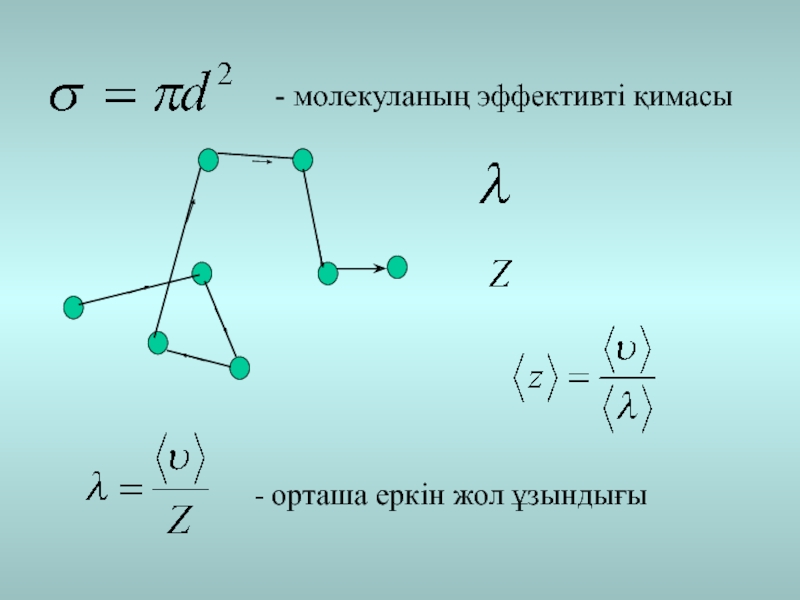
- 5. - молекуланың эффективті қимасы- орташа еркін жол ұзындығы
- 6. Слайд 6
- 7. Слайд 7
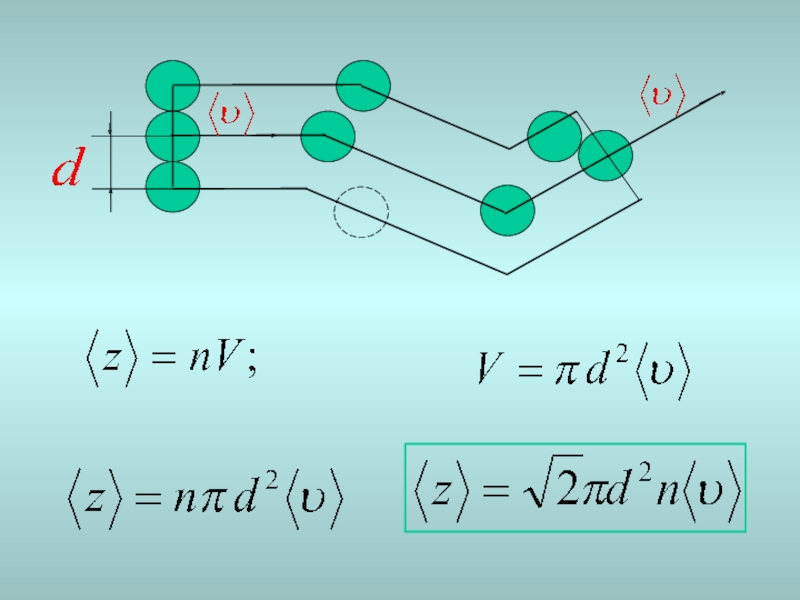
- 8. Орташа еркін жол ұзындығы
- 9. ДиффузияТасымалдау құбылысыФик заңы
- 10. -диффузия коэффициенті
- 11. Тұтқырлық
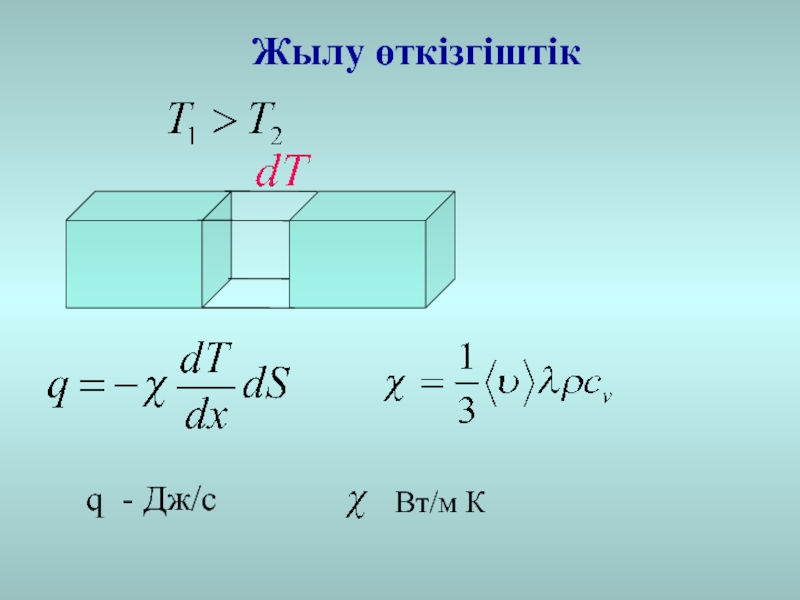
- 12. Жылу өткізгіштікq - Дж/c Вт/м К
- 13. Слайд 13
- 14. Нақты газдарДәлдіктің жеткілікті дәрежесіндегі сиретілген нақты газдар
- 15. Идеал газ моделіндегі молекулалар – арасында әсерлесу
- 16. Қысым ұлғайғанда сығылғын газ көлемі молекулалардың өздері алатын көлемге теңеседі
- 17. Идеал газ күйінің теңдеуі төмен қысымда және
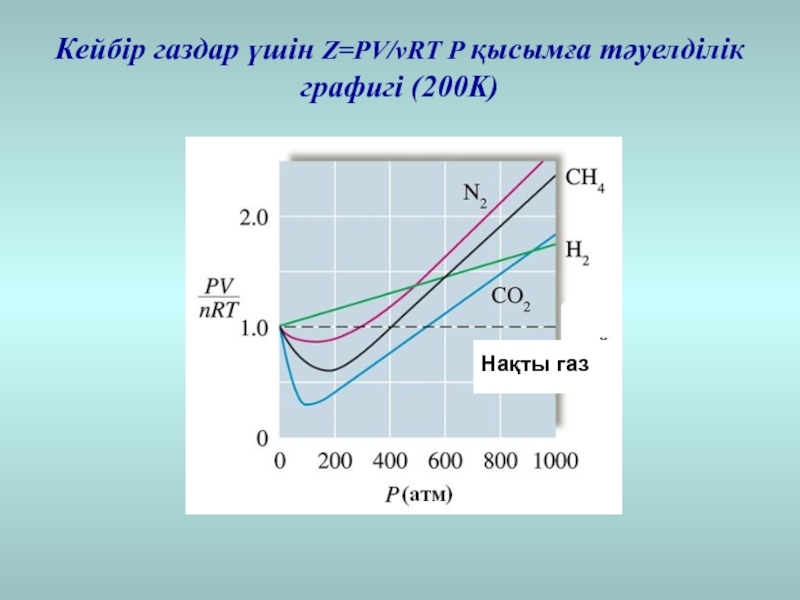
- 18. Кейбір газдар үшін Z=PV/νRT P қысымға тәуелділік графигі (200K)
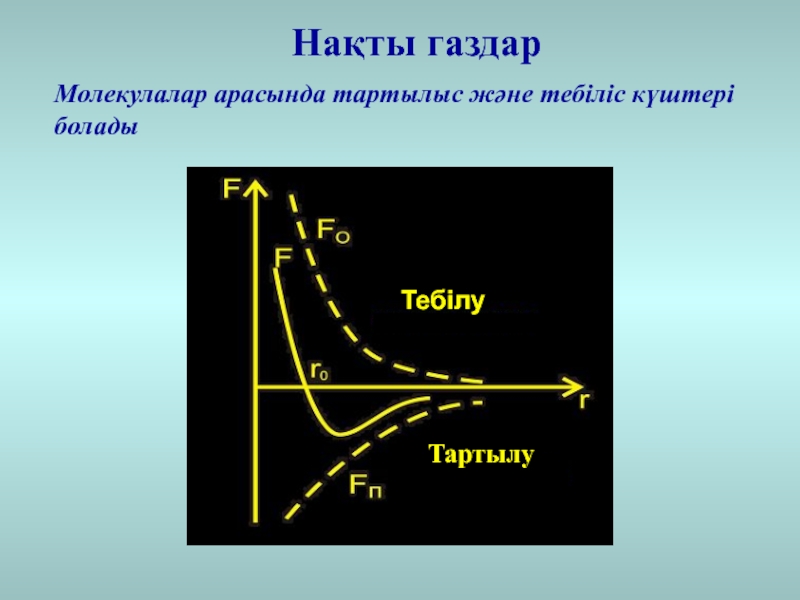
- 19. Нақты газдарМолекулалар арасында тартылыс және тебіліс күштері болады
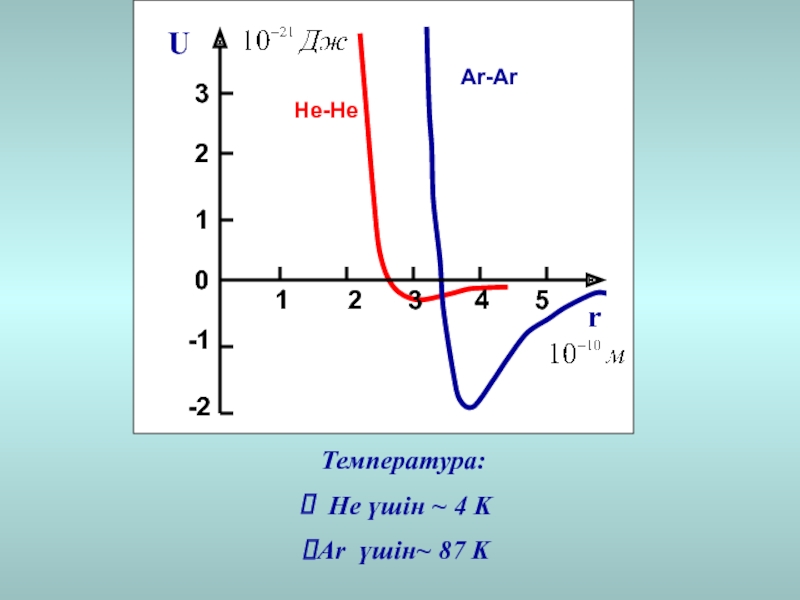
- 20. Температура: He үшін ~ 4 KAr үшін~ 87 KНе-НеAr-ArUr
- 21. Молекулалардың потенциялдық және кинетикалық энергиялары арасындағы арақатынас агрегаттық күйлерге бөлу үшін сындық болып табылады
- 22. Нақты газ күйінің теңдеуі –Ван-дер-Ваальс теңдеуіНақты газдарда
- 23. ВАН-ДЕР-ВААЛЬС ТЕҢДЕУІМолекулалардың өзара әсерлесуін ескеруМолекуланың өз көлеміне түзетілімГаздың туынды массасы үшінГаздың 1 молі үшін
- 24. Bтұрақтысы молекула өлшеміне байланысты: үлкен молекула үшін
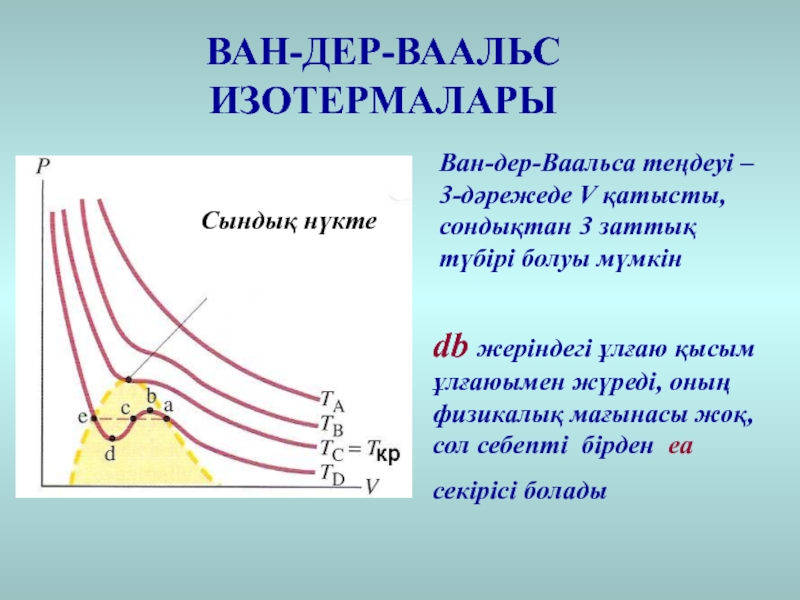
- 25. Сындық нүктеВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫdb жеріндегі ұлғаю қысым ұлғаюымен
- 26. ВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫЖоғары температураларда идеал газ изотермаларынан ауытқу кішірек көрсетілген
- 27. Нақты газдың ішкі энергиясыНақты газдың ішкі энергиясы
- 28. Фазалық ауысуларФаза – химиялық құрамы бірдей және
- 29. температураМолекулярлық қозғалысМолекулалардың өзара әсерлесуіҚатты күйсұйықтықгазБіртекті қоспа үшін фаза ұғымы агрегаттық күймен сәйкес келеді
- 30. Егер жүйе біртекті болса, онда фаза ұғымы
- 31. Күй диаграммасыСу үшін
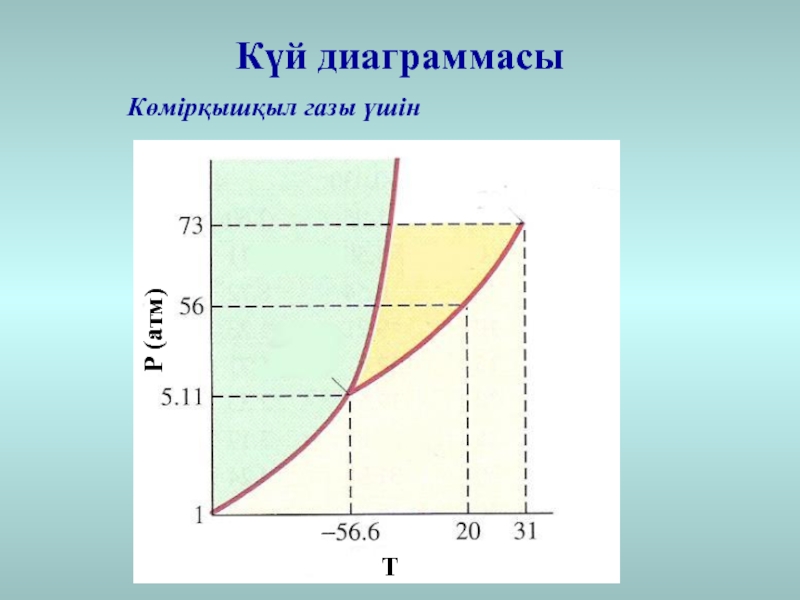
- 32. Күй диаграммасыКөмірқышқыл газы үшінТР (атм)
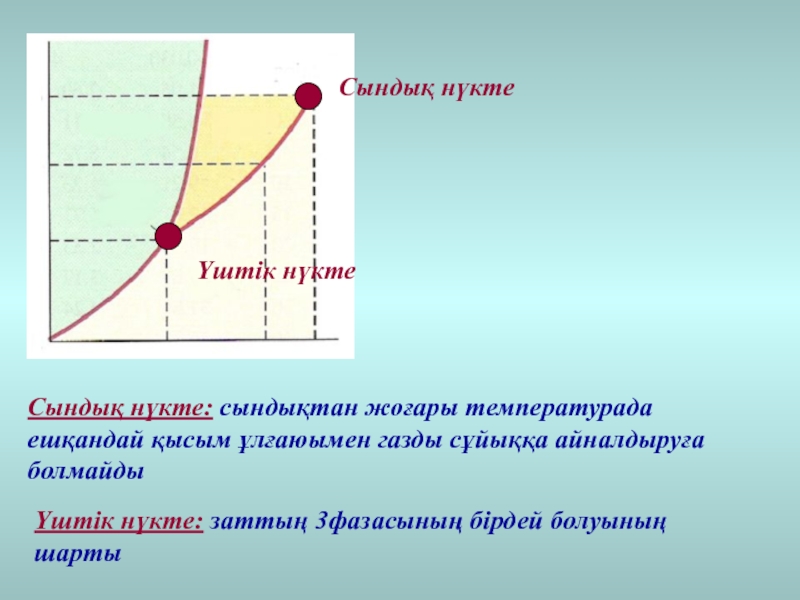
- 33. Үштік нүктеСындық нүктеСындық нүкте: сындықтан жоғары температурада
- 34. Ван-дер-Ваальс теңдеуіне бағынатын газ үшінкүйлердің сындық шамаларының мәндері
- 35. Назар аударғандарыңызға рахмет!
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Қарағанды мемлекеттік техникалық университеті
Физика кафедрасы
ФИЗИКА 1
ТАСЫМАЛДАУ ҚҰБЫЛЫСЫ. НАҚТЫ ГАЗДАР
Слайд 2Эффективтік диаметр
Тасымалдау құбылысы
Молекуллрдың өзара әсерлесуі
Ван-дер-Ваальс теңдеуі
Ван-дер-Ваальс изотермасы
Фазалық ауысу
Күй диаграммасы
Дәріс
жоспары
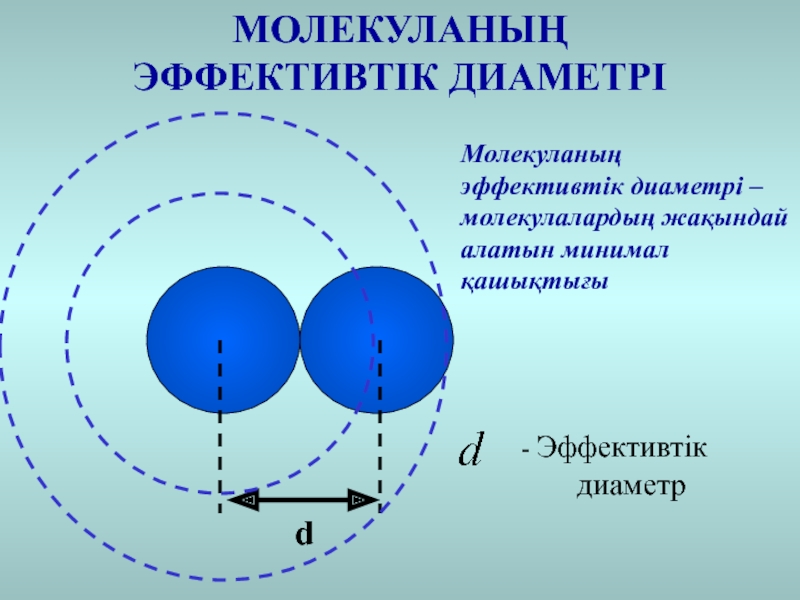
Слайд 3МОЛЕКУЛАНЫҢ ЭФФЕКТИВТІК ДИАМЕТРІ
d
Молекуланың эффективтік диаметрі – молекулалардың жақындай алатын минимал
қашықтығы
- Эффективтік
диаметр
Слайд 14Нақты газдар
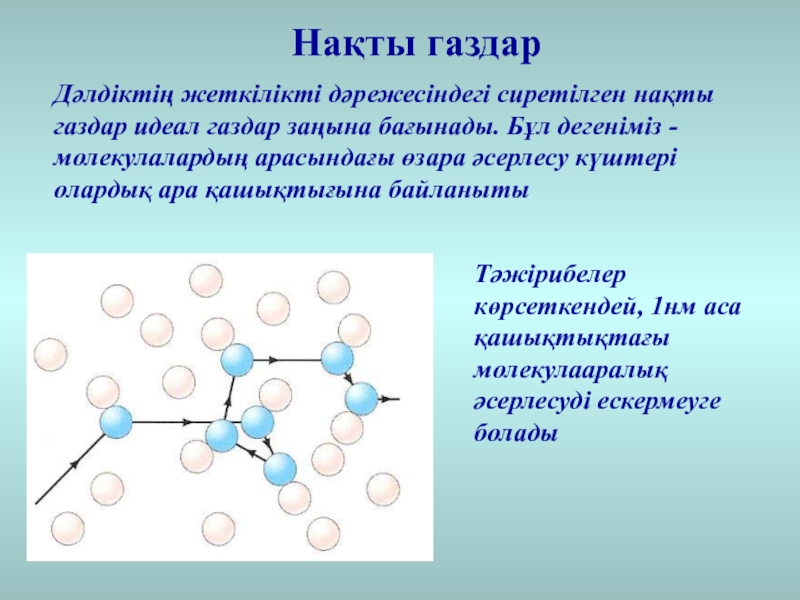
Дәлдіктің жеткілікті дәрежесіндегі сиретілген нақты газдар идеал газдар заңына
бағынады. Бұл дегеніміз - молекулалардың арасындағы өзара әсерлесу күштері олардық
ара қашықтығына байланытыТәжірибелер көрсеткендей, 1нм аса қашықтықтағы молекулааралық әсерлесуді ескермеуге болады
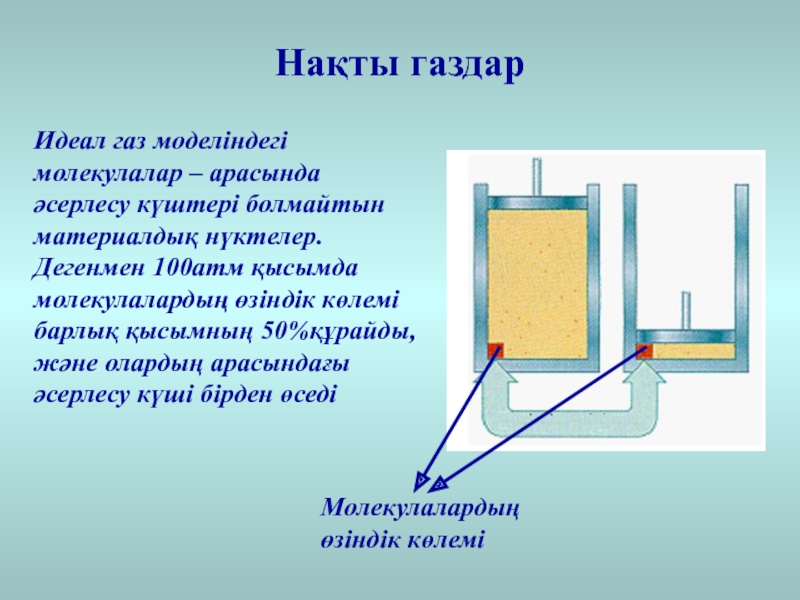
Слайд 15Идеал газ моделіндегі молекулалар – арасында әсерлесу күштері болмайтын материалдық
нүктелер. Дегенмен 100атм қысымда молекулалардың өзіндік көлемі барлық қысымның 50%құрайды,
және олардың арасындағы әсерлесу күші бірден өседіМолекулалардың өзіндік көлемі
Нақты газдар
Слайд 17Идеал газ күйінің теңдеуі төмен қысымда және жоғары температурадағы газдар
әрекетін сипаттауға пайдалы.
Идеал газадың берілген күйден ауытқуы сығылу коэффициентімен
Z сипатталадыЕгер Z = 1 болса, идеал газ қасиетіне жақын болады
Сығылу коэффициенті Z 1-ден өзгеше болса,солғұрлым идеал газадан ауытқуы күштірек болады
Слайд 21Молекулалардың потенциялдық және кинетикалық энергиялары арасындағы арақатынас агрегаттық күйлерге бөлу
үшін сындық болып табылады
Слайд 22Нақты газ күйінің теңдеуі –Ван-дер-Ваальс теңдеуі
Нақты газдарда келесі ескерілу керек:
Бөлшектерде
өз көлемі болады
Молекулалар арасында тартылыс және тебіліс күштері бар
Идеал газ
күйінің теңдеуі молекулалардың өз көлемі мен олардың әсерлесуі ескерілетіндей түрлендірілуі қажет
Слайд 23ВАН-ДЕР-ВААЛЬС ТЕҢДЕУІ
Молекулалардың өзара әсерлесуін ескеру
Молекуланың өз көлеміне түзетілім
Газдың туынды массасы
үшін
Газдың 1 молі үшін
Слайд 24Bтұрақтысы молекула өлшеміне байланысты: үлкен молекула үшін оның мәні де
үлкен
a молекулалар арасындағы тартылыс күшінің шамасы
Слайд 25Сындық нүкте
ВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫ
db жеріндегі ұлғаю қысым ұлғаюымен жүреді, оның физикалық
мағынасы жоқ, сол себепті бірден ea
секірісі болады
Ван-дер-Ваальса теңдеуі – 3-дәрежеде
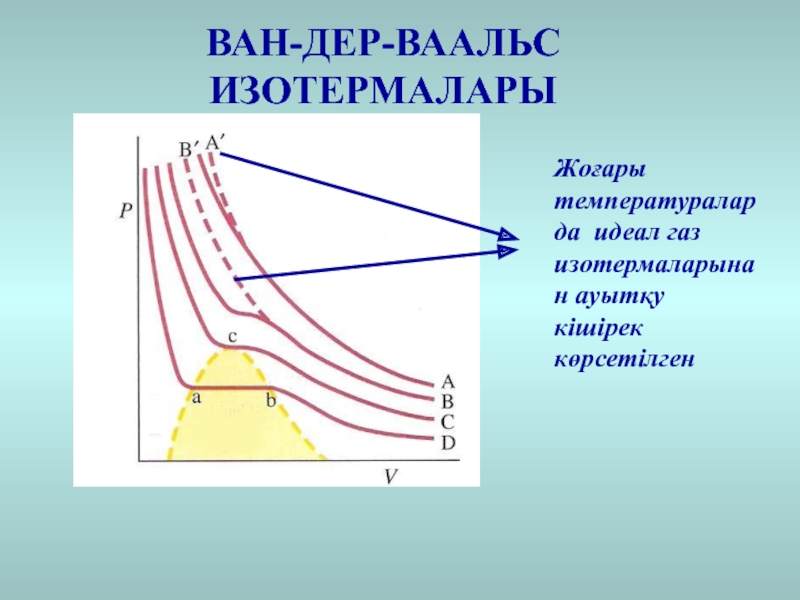
V қатысты, сондықтан 3 заттық түбірі болуы мүмкінСлайд 26ВАН-ДЕР-ВААЛЬС ИЗОТЕРМАЛАРЫ
Жоғары температураларда идеал газ изотермаларынан ауытқу кішірек көрсетілген
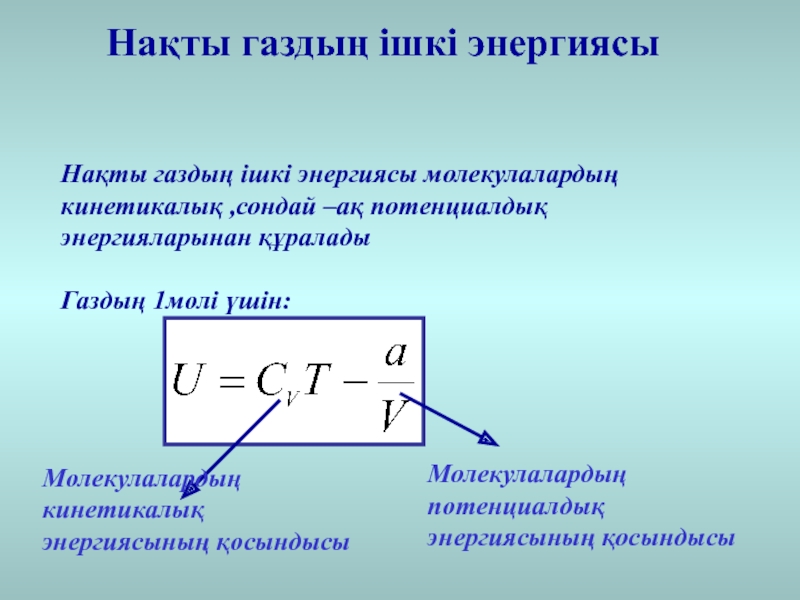
Слайд 27Нақты газдың ішкі энергиясы
Нақты газдың ішкі энергиясы молекулалардың кинетикалық ,сондай
–ақ потенциалдық энергияларынан құралады
Газдың 1молі үшін:
Молекулалардың кинетикалық энергиясының қосындысы
Молекулалардың потенциалдық
энергиясының қосындысыСлайд 28Фазалық ауысулар
Фаза – химиялық құрамы бірдей және 1 термодинамикалық күйдегі
жүйенің
барлық бөліктерінің байланысы
1 реттік фазалық ауысу мысалдары:
2 реттік фазалық
ауысу мысалдары:балқу – қату
булану – конденсация
Сублимация
ферромагнетиктің парамагнетикке ауысуы және керісінше. Металдың жоғары өтімді күйге ауысуы
Сұйық гелийдің аққыштығы жоғары күйге айналуы
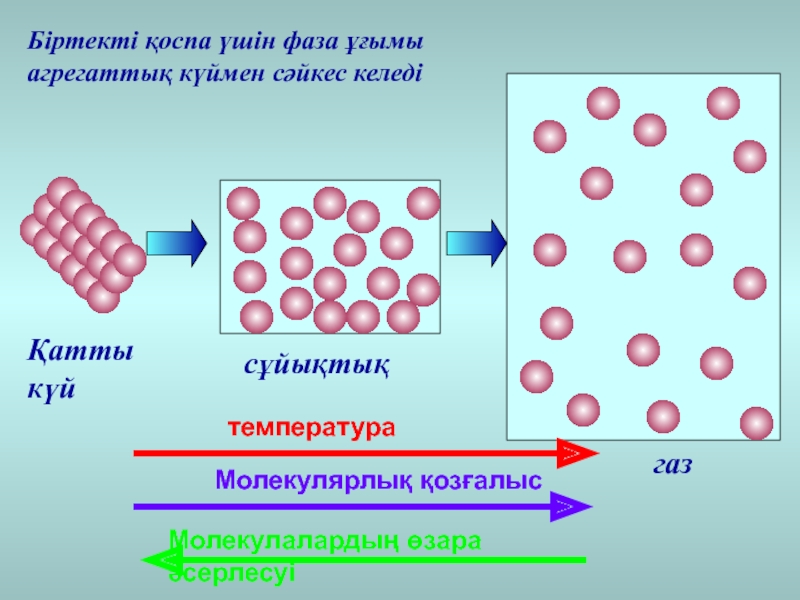
Слайд 29температура
Молекулярлық қозғалыс
Молекулалардың өзара әсерлесуі
Қатты күй
сұйықтық
газ
Біртекті қоспа үшін фаза ұғымы агрегаттық
күймен сәйкес келеді
Слайд 30Егер жүйе біртекті болса, онда фаза ұғымы агрегаттық күймен сәйкес
келеді
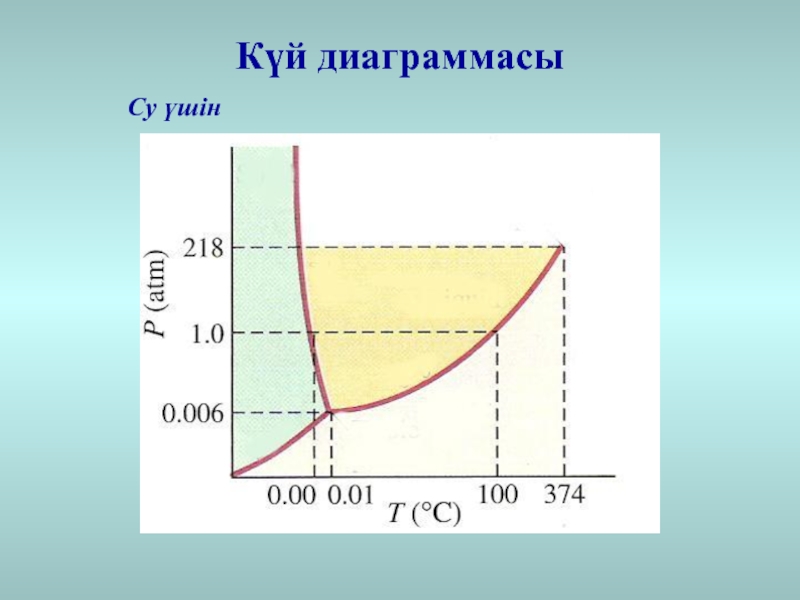
Күй диаграммасы – фазалық ауысудың температурасы мен қысымы арасындағы тәуелділік
диаграмманы 3ке бөлетін қатты ,сұйық,газ шарттарына сай булану,балқу,сублимация қисықтары түріндегі графикте бейнеленгенКүй диаграммасы
С