Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биоэлектрогенез в сердечной мышце
Содержание
- 1. Биоэлектрогенез в сердечной мышце
- 2. Проводящая система сердцаПСС состоит из особых субпопуляций
- 3. История1845 – Johannes E. von Purkinje описал
- 4. История1906 — Л. Ашофф (L. Ashoff, Германия)
- 5. Проводящая система сердца
- 6. Электрическая активность клеток сердца зависит от 1)
- 7. Строение проводящей системы сердцаСУ (синусно-предсердный) – узел
- 8. Проводящая система сердца
- 9. Синусовый узел Кейса-ФлэкаРасположен субэпикардиально в задней части
- 10. Тракт Бахмана (передний путь)Проходит по передне-верхней стенке
- 11. Тракт Венкебаха (средний путь)Проходит по задней части МПП к верхней части предсердно-желудочкового соединения
- 12. Тракт Тореля (задний тракт)Проходит по нижней части
- 13. Другие предсердные путиОписаны только электрофизиологическиПуть Шерлага (1967)
- 14. Предсердно-желудочковый узел Ашоффа-ТаварыРасположен в нижней части ПП
- 15. Функционально-анатомическая структура связей AV-узлаТрёхслойное строение, сравниваемое с
- 16. Собственно структура AV-узлаВерхняя часть, в которую проникают
- 17. Структура предсердно-желудочкового узла
- 18. Предсердно-желудочковый пучок - Пучок ГисаСостоит из 2-х
- 19. Ножки пучка ГисаПучок разделяется на две ножки
- 20. Волокна ПуркиньеПронизывают весь миокард желудочковСкорость проведения составляет 4-5 м/сЦентр автоматизма третьего порядка (15-30 имп/мин)Проведение через коннексоны
- 21. Аномальные дополнительные пути проведенияВызывают более раннее возбуждение
- 22. Добавочные путиПучок КентаТракт МахаймаТракт ДжеймсаПучок Брешенмаше
- 23. Пучок КентаПредсердно-желудочковое соединениеМышечный мостик 1-8 мм, внедряющийся
- 24. Тракты МахаймаПравосторонние дополнительные трактыАтриофасцикулярный тракт, внедряющийся в
- 25. Тракт ДжеймсаПредсердно-желудочковый узловой шунт – задний межузловой
- 26. Аномальные дополнительные пути проведения
- 27. Проводящая система сердца
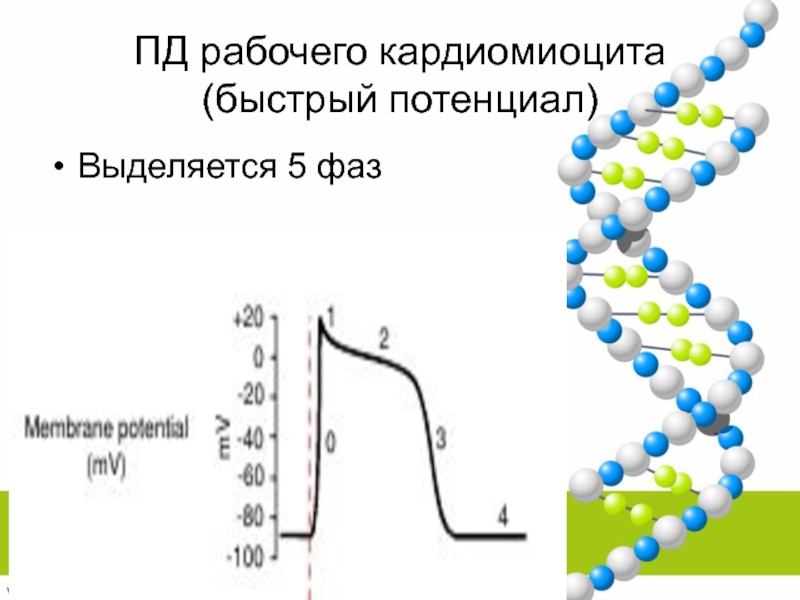
- 28. ПД рабочего кардиомиоцита (быстрый потенциал)Выделяется 5 фаз
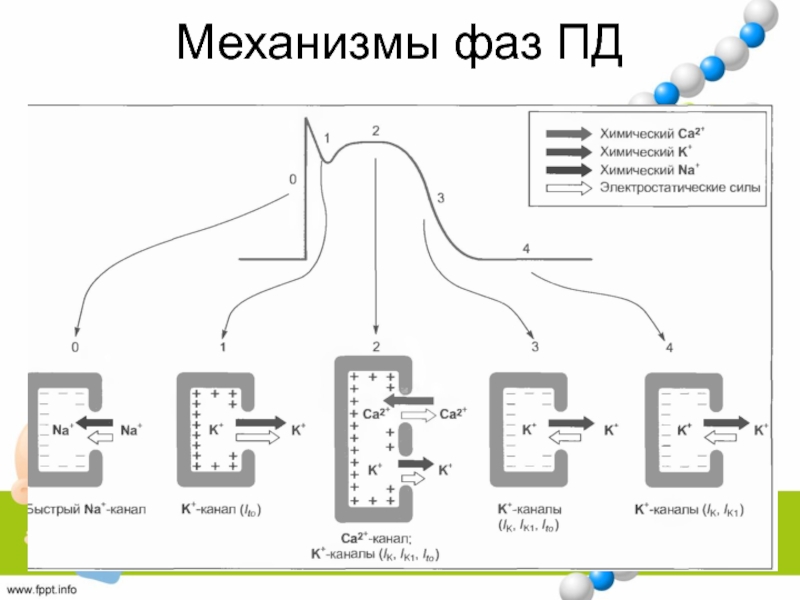
- 29. Механизмы фаз ПД
- 30. Фаза 0 - Нарастание ПДМПП сократительного кардиомиоцита
- 31. Фаза 4 (начало фазы 0)M – активационные ворота;H – инактивационные ворота;Участвуют химическая и электростатическая силы.
- 32. Фаза 0
- 33. Фаза 0
- 34. Фаза 0
- 35. Фаза 0
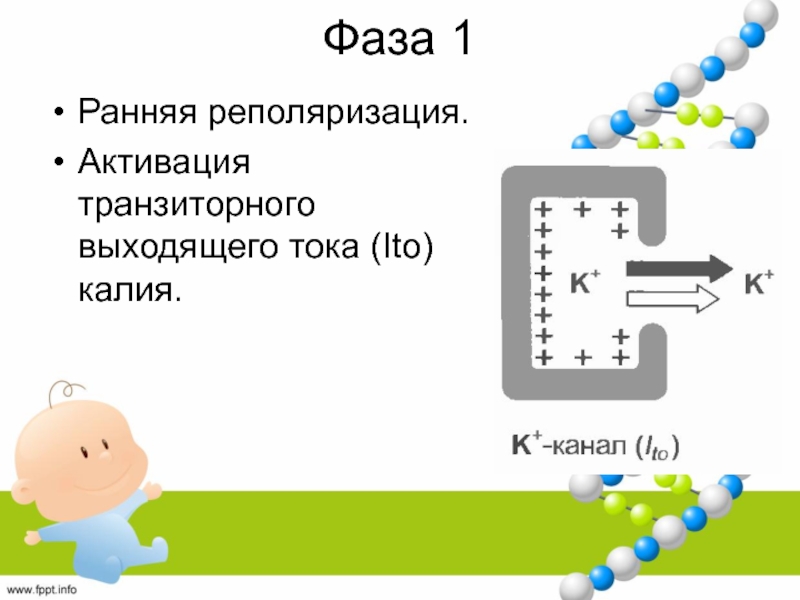
- 36. Фаза 1Ранняя реполяризация.Активация транзиторного выходящего тока (Ito) калия.
- 37. Фаза 2Плато.1) Вход Са через L-каналы. Ток
- 38. Фаза 3Окончательная реполяризация.1) Выход К (Ito, Ik,
- 39. Фаза 4Восстановление ионных концентраций.Работа Na/K, Na/Ca-АТФаз, Са-АТФазы.Утечка К (Ik) обеспечивает МПП.
- 40. Основные каналы 1) Потенциал-зависимые Na-каналы (быстрый ток,
- 41. Основные каналы 3) Потенциал-управляемые К-каналы аномального выпрямления
- 42. Основные каналы 4) Потенциал-управляемые К-каналы транзиторного тока
- 43. Основные каналы 4) Потенциал-управляемые К-каналы транзиторного тока
- 44. Основные каналы 5) Потенциал-зависимые K-каналы задержанного выпрямления (Ik, Ikr, Iks) – выход К при деполяризации мембраны.
- 45. Основные каналы 6) Лиганд-управляемый К-канал (открывается АХ
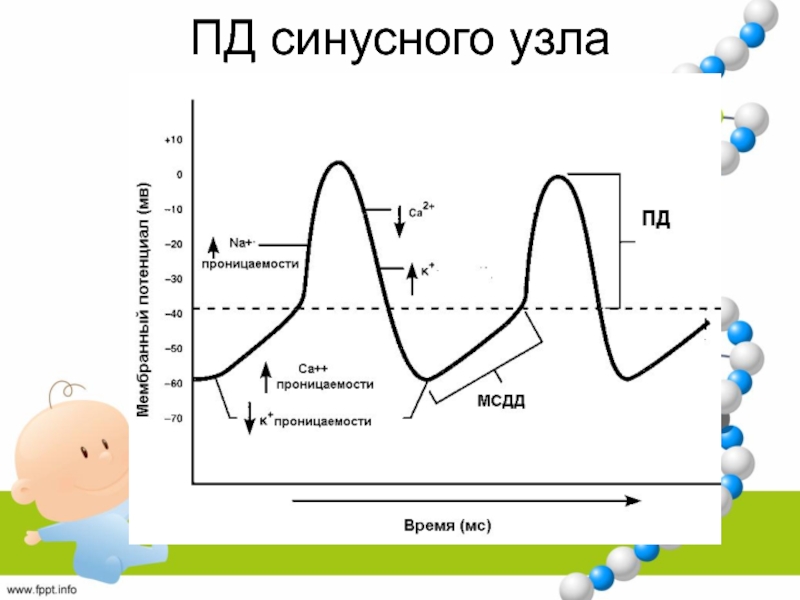
- 46. ПД синусного узла
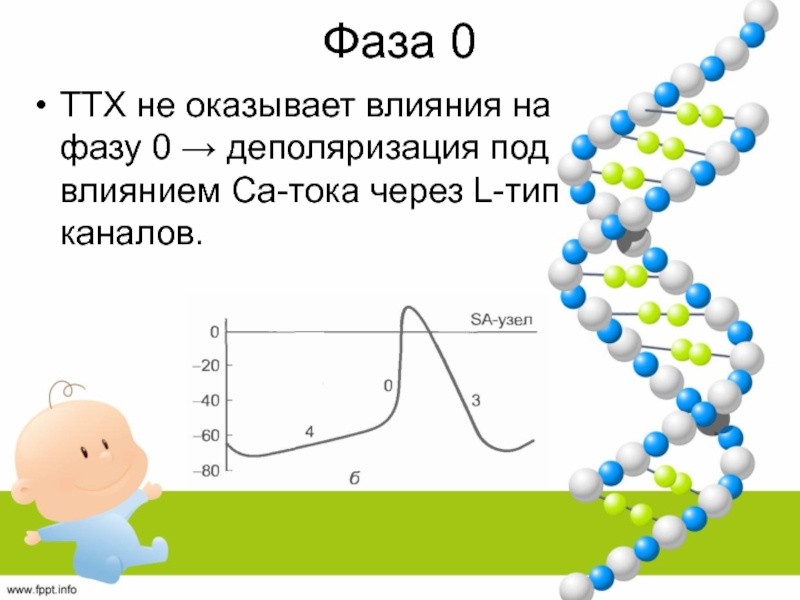
- 47. Фаза 0ТТХ не оказывает влияния на фазу 0 → деполяризация под влиянием Са-тока через L-тип каналов.
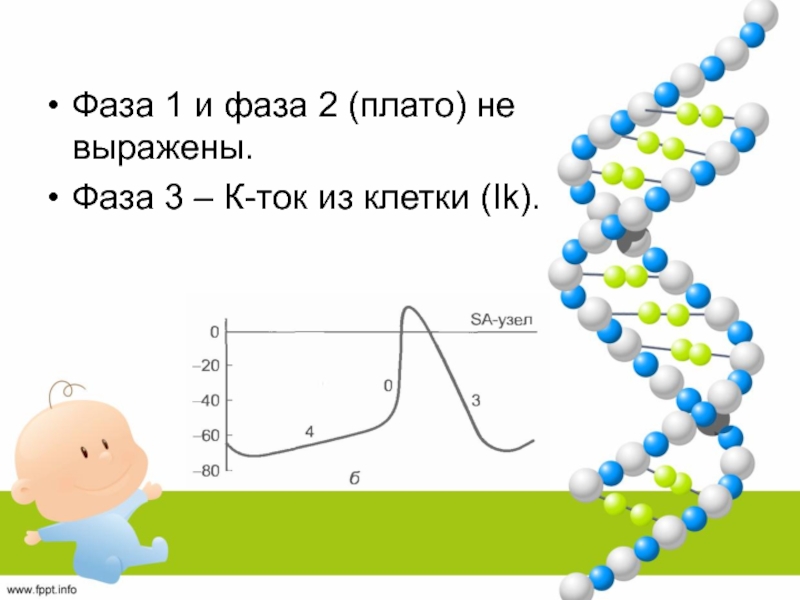
- 48. Фаза 1 и фаза 2 (плато) не выражены.Фаза 3 – К-ток из клетки (Ik).
- 49. Фаза 4Медленная спонтанная диастолическая деполяризация.1) Ток Са
- 50. Фаза 43) Ток K (Ik) через каналы
- 51. HCN-каналыКаналы, связанные с циклическими нуклеотидами, активируемые гиперполяризацией (funny-каналы). Ток ДиФранческо, пейсмейкерный ток (If, Ih).
- 52. HCN-каналыСемейство из 4х каналов (HCN1-4). 6 сегментов.
- 53. HCN-каналы1) Больше всего в СУ.HCN4 – 80%,
- 54. Физиологическая роль If1) Формирование импульса в ПСС
- 55. Модуляция IfМодулируется посредством вегетативных влияний через действие
- 56. Нарушение If1) Синдром слабости синусового узла.Характеризуется такой
- 57. Потенциал-зависимые Ca-каналыСа-каналы классифицируются на типы T, L,
- 58. Слайд 58
- 59. Блокаторы Са-каналовТри группы:1) Фенилалкиламины (верапамил);2) Бензотиазипины (дилтиазем);3)
- 60. Са-каналыТ-тип Са-каналов, или каналы, активирующиеся при низком
- 61. Са-каналыВысоко-пороговые Са-каналы могут быть разделены, посредством их
- 62. Са-каналыТ-каналы – от слова tiny и transient,
- 63. Строение Са-каналаL-тип Са-каналов – комплекс из 5
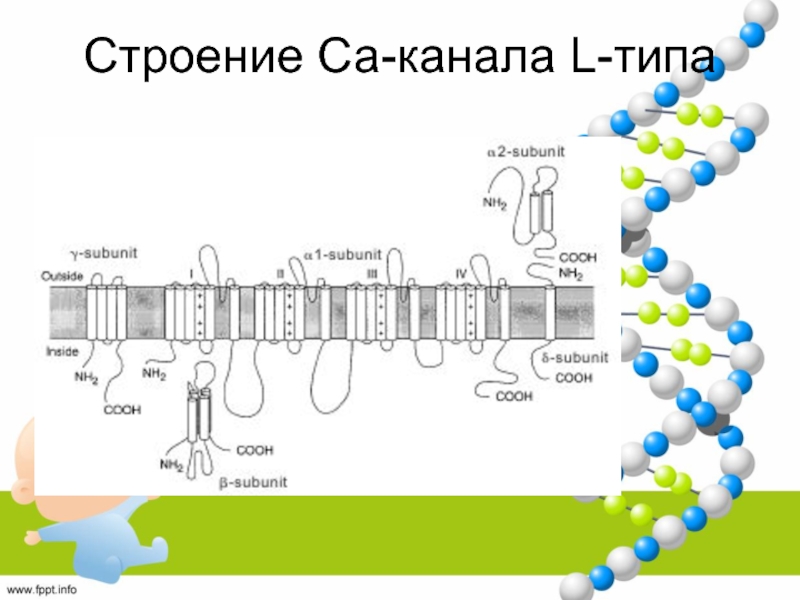
- 64. Строение Са-канала L-типа
- 65. Сердечные каналопатии
- 66. Синдром длинного QTα-CЕ IKs-калиевого канала (задержанного выпрямления
- 67. Синдром Бругадаα-CЕ ПЗНК (5-я, сердечная изоформа) –
- 68. Синдром внезапной необъяснимой смерти взрослыхα-CЕ IKs-калиевого канала
- 69. Синдром внезапной сердечной смерти детейα-CЕ ПЗНК (5-я, сердечная изоформа) – фаза 0 - 3%–5%
- 70. Скачать презентанцию
Проводящая система сердцаПСС состоит из особых субпопуляций клеток, которые спонтанно генерируют электрическую активность и проводят её по сердцу.
Слайды и текст этой презентации
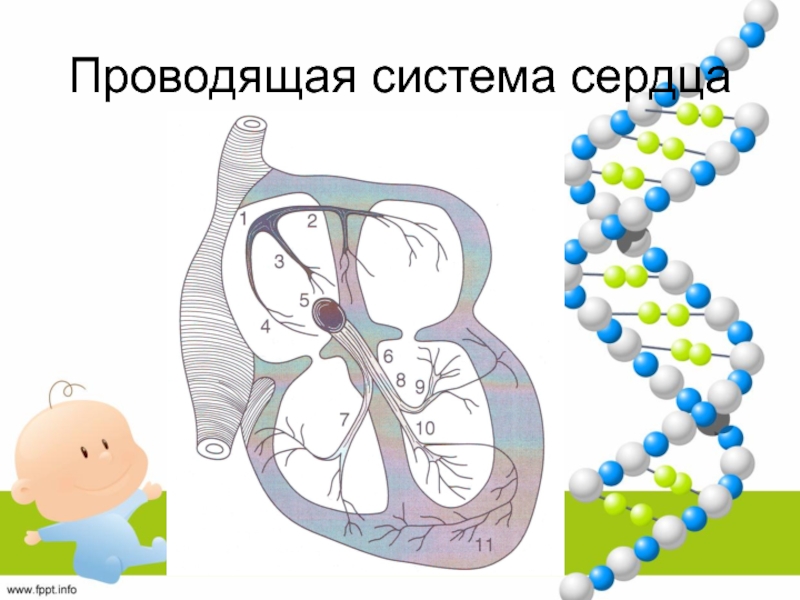
Слайд 2Проводящая система сердца
ПСС состоит из особых субпопуляций клеток, которые спонтанно
генерируют электрическую активность и проводят её по сердцу.
Слайд 3История
1845 – Johannes E. von Purkinje описал проводящую систему желудочков.
1882
– Gaskell использовал выражение «сердечный блок».
1893 — В. Гис (Wilhelm
His Jr., Германия) обнаружил предсердно—желудочковый пучок (пучок Гиса).Слайд 4История
1906 — Л. Ашофф (L. Ashoff, Германия) и С. Тавара
(S. Tawara, Япония) описали предсердно—желудочковый узел (узел Ашоффа—Тавары).
1907 — А.
Кейс и М. Флэк (A. Keith, M. Flack, Великобритания) обнаружили синусно—предсердный узел.Слайд 6Электрическая активность клеток сердца зависит от
1) Градиента ионов;
2) Изменения
проницаемости мембраны для различных ионов при участии ионных каналов.
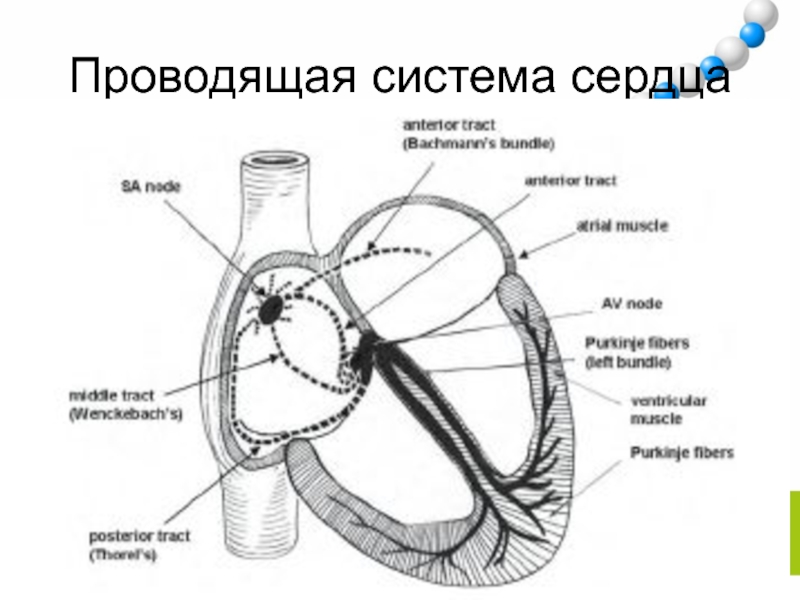
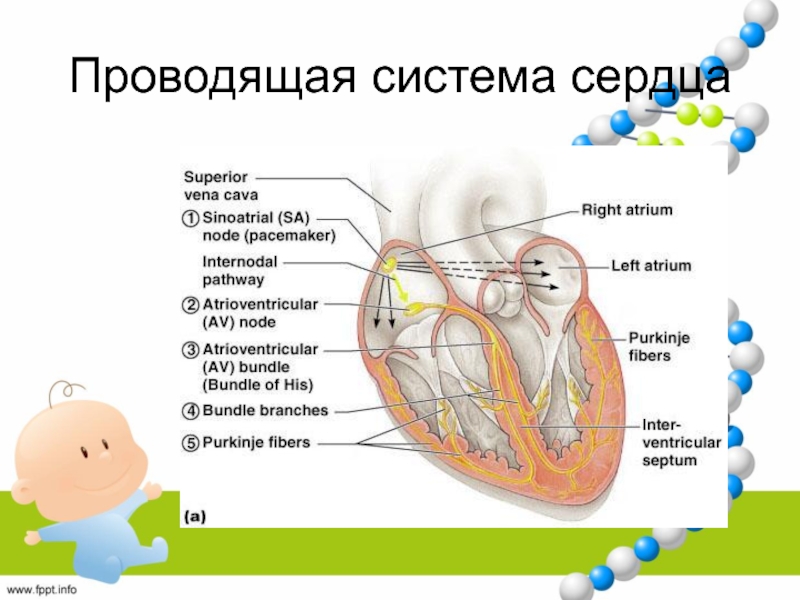
Слайд 7Строение проводящей системы сердца
СУ (синусно-предсердный) – узел Кейса-Флэка (1906)
Предсердные межузловые
пути
Передний тракт Бахмана (1916)
Средний тракт Венкебаха (1907)
Задний тракт Тореля (1909)
Предсердно-желудочковый
узел Ашоффа-Тавары (1901, 1906)Система пучка Гиса (1883), состоящая из общего ствола и ножек пучка Гиса (левая делится на две ветви – переднюю и заднюю)
Сеть волокон Пуркинье (1845) , направляются в толщу миокарда (от эндокарда к эпикарду), где контактируют с рабочими кардиомиоцитами
Слайд 9Синусовый узел Кейса-Флэка
Расположен субэпикардиально в задней части ПП, медиальнее устья
верхней полой вены у основании ушка ПП
Центральная часть узла представлена
Р-клетками, окружённые мембраной и напоминающие гроздья виноградаОбладают пейсмейкерной активностью
Периферическая часть узла представлена Т-клетками (transition – перемещение)
Слайд 10Тракт Бахмана (передний путь)
Проходит по передне-верхней стенке ПП и у
межпредсердной перегородки (МПП) разделяется на две ветви, одна из которых
ведёт к предсердно-желудочковому соединению, вторая – к левому предсердию с задержкой импульсов на 20 мс.Слайд 11Тракт Венкебаха (средний путь)
Проходит по задней части МПП к верхней
части предсердно-желудочкового соединения
Слайд 12Тракт Тореля (задний тракт)
Проходит по нижней части МПП к нижней
части предсердно-желудочкового соединения с распространением волокон к стенке ПП
Слайд 13Другие предсердные пути
Описаны только электрофизиологически
Путь Шерлага (1967) – соединяет нижнюю
часть предсердий
Путь Сузуки – проходит в нижней части межпредсердной перегородки,
проникая в мышечную часть левого предсердия (ЛП)Слайд 14Предсердно-желудочковый узел Ашоффа-Тавары
Расположен в нижней части ПП справа от МПП,
рядом с устьем коронарного синуса, вдаваясь в перегородку между предсердиями
и желудочкамиОсновные функции AV-узла:
Проведение импульсов с задержкой от предсердий к желудочкам
Фильтрация (сортировка) предсердных волн возбуждения (не более 200 имп/мин)
Проведение возбуждение длится около 80 мс
Скорость проведения импульса – 0,05 м/с
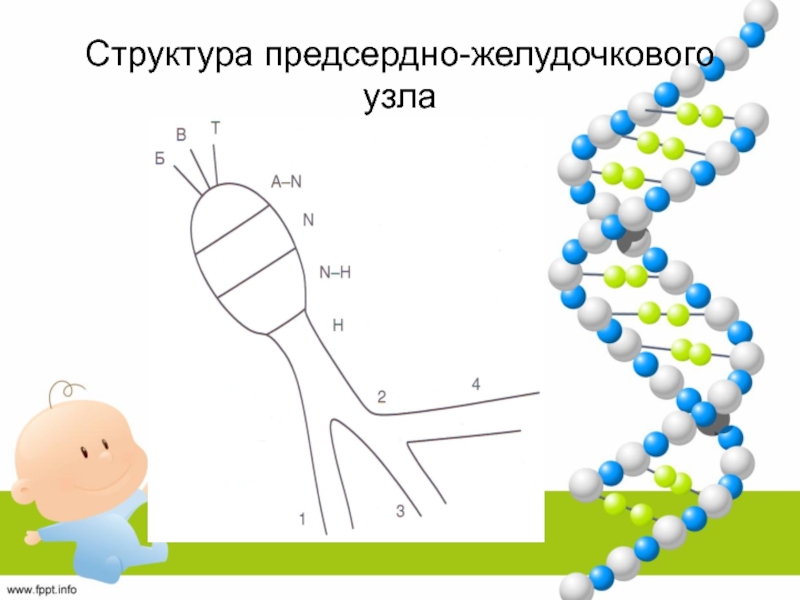
Слайд 15Функционально-анатомическая структура связей AV-узла
Трёхслойное строение, сравниваемое с лабиринтом:
Пограничная зона между
предсердиями и AV-узлом
Собственно AV-узел
Общий ствол пучка Гиса
Слайд 16Собственно структура AV-узла
Верхняя часть, в которую проникают предсердно-желудочковые тракты (A-N-часть,
atrium-nodus – предсердно-узловая)
Выполняет функцию задержки и синхронизации – декрементная область
Средняя
часть – собственно узел (N-часть - nodus)Выполняет функцию задержки – декрементная область
Нижняя часть, переходящая в ствол Гиса (N-H часть – nodus-His нодально-гисальная)
Выполняет функцию ускорения проведения – инкрементная область
Является центром автоматизма II порядка
Слайд 18Предсердно-желудочковый пучок - Пучок Гиса
Состоит из 2-х частей:
Проксимального отдела (пенетрирующая
часть пучка Гиса), не имеющая контакта с сократительными кардиомиоцитами
Дистальная часть
(мебранозная или ветвящаяся часть пучка Гиса)Разделяется на «кабельные структуры» коллагеновыми прослойками, обеспечивая изолированное разделение фронта возбуждения на отдельно движущиеся волны возбуждения
Слайд 19Ножки пучка Гиса
Пучок разделяется на две ножки правую и левую
Левая
ножка разделяется на переднюю (передневерхнюю) и заднюю (задневерхнюю)
Скорость проведения возбуждения
составляет 3-4 м/сЦентр автоматизма третьего порядка (15-40 имп/мин)
Слайд 20Волокна Пуркинье
Пронизывают весь миокард желудочков
Скорость проведения составляет 4-5 м/с
Центр автоматизма
третьего порядка (15-30 имп/мин)
Проведение через коннексоны
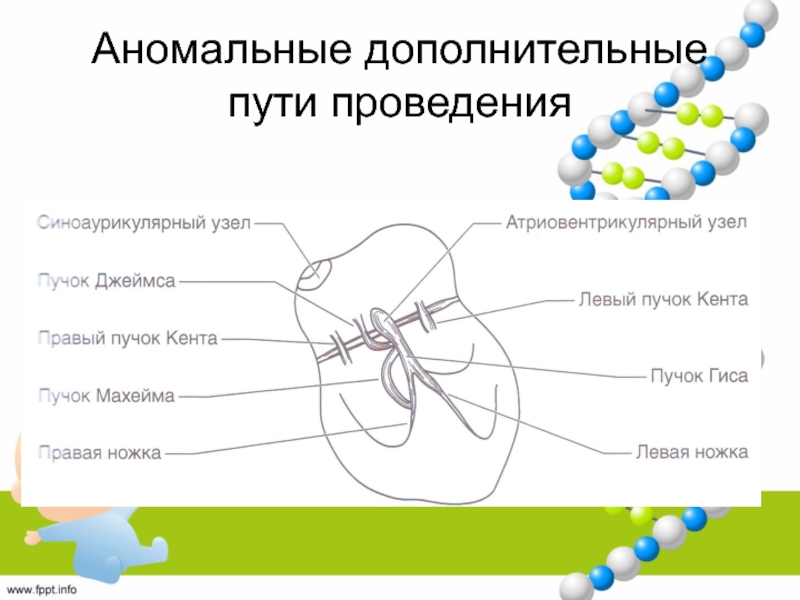
Слайд 21Аномальные дополнительные пути проведения
Вызывают более раннее возбуждение участков желудочка –
синдром преждевременного возбуждения
Изменение фенотипа (конфигурация) ЭКГ
Включаются в круговое движение волны
возбуждения (re-entry)Слайд 23Пучок Кента
Предсердно-желудочковое соединение
Мышечный мостик 1-8 мм, внедряющийся в миокард желудочков.
Выделяют
около 10 возможных локализаций пучков Кента
Анатомический субстрат синдрома Вольфа-Паркинсона-Уайта (WPW-Синдром)
Слайд 24Тракты Махайма
Правосторонние дополнительные тракты
Атриофасцикулярный тракт, внедряющийся в дистальную часть правой
ножки пучка Гиса
Длинный и короткий предсердно-желудочковые тракты, оканчивающиеся в сократительном
миокардеВызывают наджелудочковую тахикардию с морфологией комплекса QRS по типу блокады левой ножки пучка Гиса и смещение ЭОС влево
Слайд 25Тракт Джеймса
Предсердно-желудочковый узловой шунт – задний межузловой (атрио-нодальный) тракт, соединяющий
СУ с нижней частью предсердно-желудочкового узла
Синдром укороченного интервала PQ (PR)
Есть
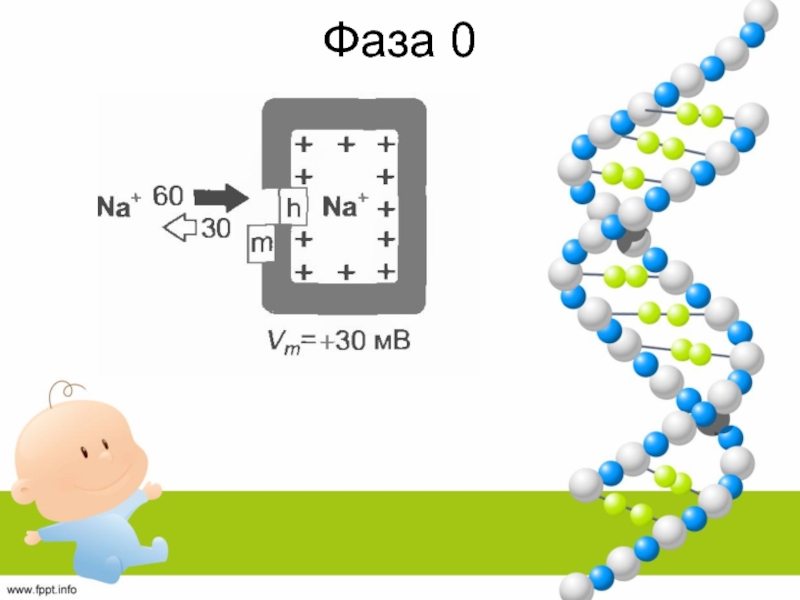
у всех людей, но не функционируетСлайд 30Фаза 0 - Нарастание ПД
МПП сократительного кардиомиоцита =
- 90
мВ.
Вход Na в кардиомиоцит за счёт ↑ проводимости для Na.
При
достижении порогового значения- 65 мВ, Na входит через быстрые Na-каналы (блокируются ТТХ).
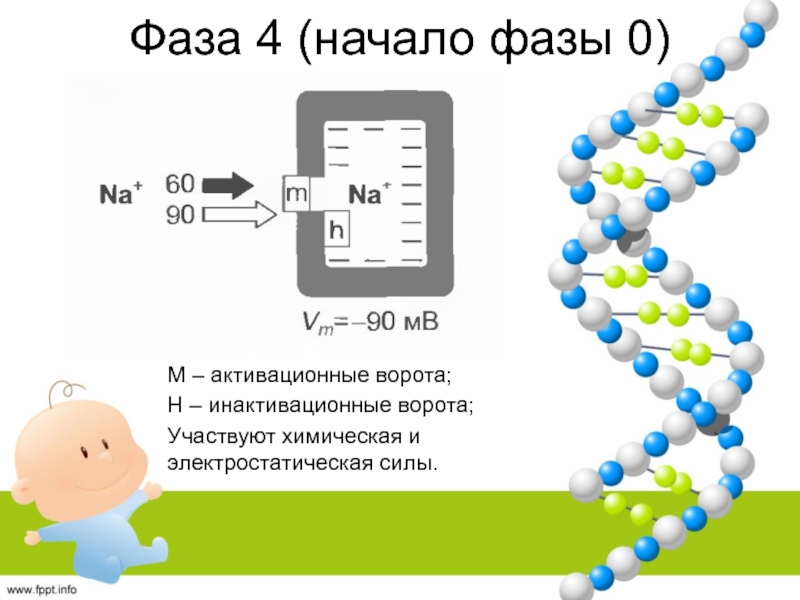
Слайд 31Фаза 4 (начало фазы 0)
M – активационные ворота;
H – инактивационные
ворота;
Участвуют химическая и электростатическая силы.
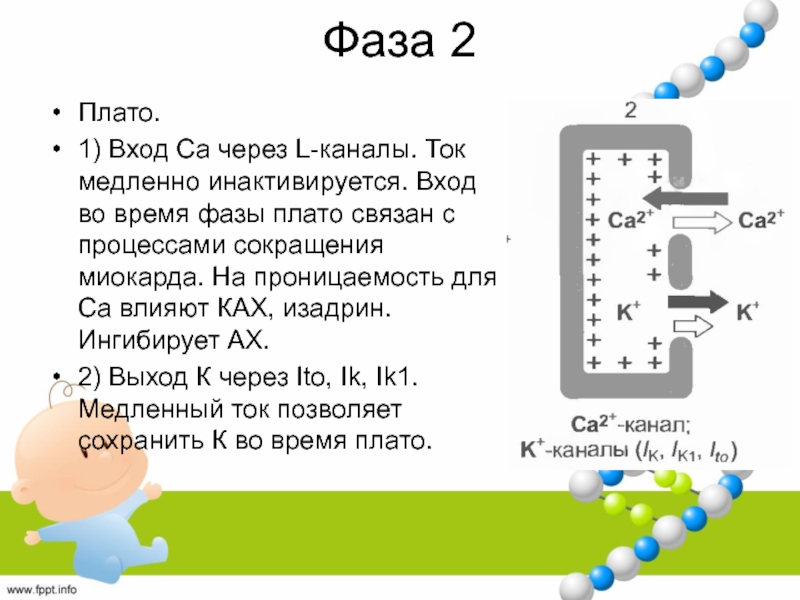
Слайд 37Фаза 2
Плато.
1) Вход Са через L-каналы. Ток медленно инактивируется. Вход
во время фазы плато связан с процессами сокращения миокарда. На
проницаемость для Са влияют КАХ, изадрин. Ингибирует АХ.2) Выход К через Ito, Ik, Ik1. Медленный ток позволяет сохранить К во время плато.
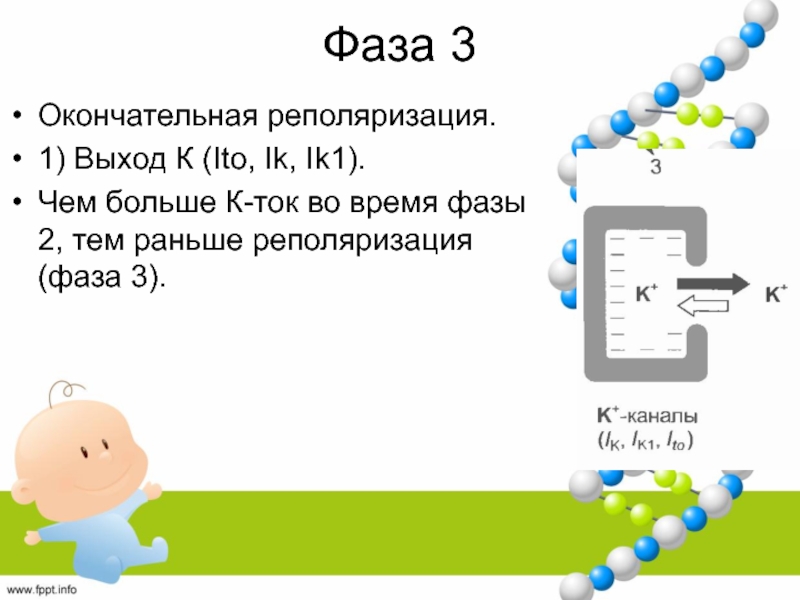
Слайд 38Фаза 3
Окончательная реполяризация.
1) Выход К (Ito, Ik, Ik1).
Чем больше К-ток
во время фазы 2, тем раньше реполяризация (фаза 3).
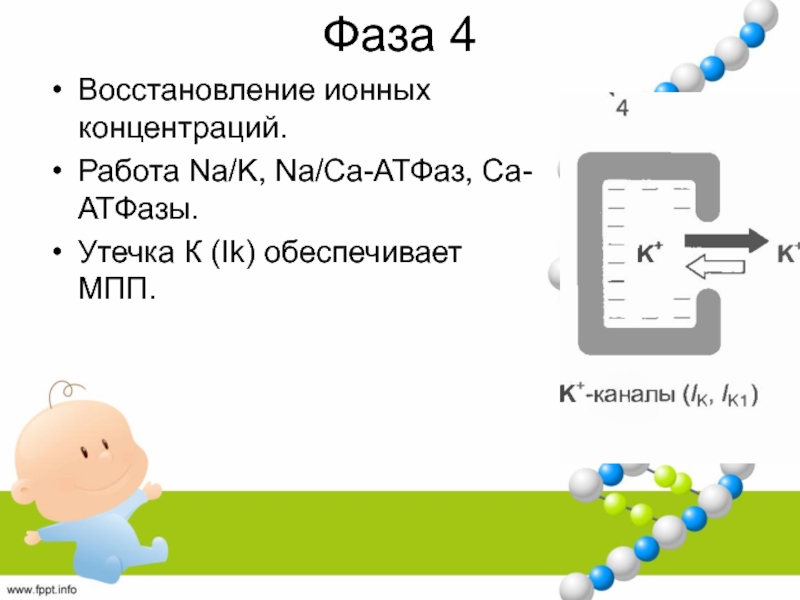
Слайд 39Фаза 4
Восстановление ионных концентраций.
Работа Na/K, Na/Ca-АТФаз, Са-АТФазы.
Утечка К (Ik) обеспечивает
МПП.
Слайд 40Основные каналы
1) Потенциал-зависимые Na-каналы (быстрый ток, Ina) – Фаза
0 ПД.
2) Потенциал-зависимые Ca-каналы (Ical – медленный ток) – Фаза
2 ПД, когда мембрана деполяризована.Слайд 41Основные каналы
3) Потенциал-управляемые К-каналы аномального выпрямления (Ik1) – поддерживают
МПП (фаза 4), обеспечивая выход K при высокоотрицательных значениях МП.
Слайд 42Основные каналы
4) Потенциал-управляемые К-каналы транзиторного тока (Ito) – обеспечивают
выход К в фазу 1, при положительном уровне мембранного потенциала
Слайд 43Основные каналы
4) Потенциал-управляемые К-каналы транзиторного тока (Ito) – обеспечивают
выход К в фазу 1, при положительном уровне мембранного потенциала
Слайд 44Основные каналы
5) Потенциал-зависимые K-каналы задержанного выпрямления (Ik, Ikr, Iks)
– выход К при деполяризации мембраны.
Слайд 45Основные каналы
6) Лиганд-управляемый К-канал (открывается АХ и аденозином). Гиперполяризует
мембрану в фазу 4 и укорачивает фазу 2.
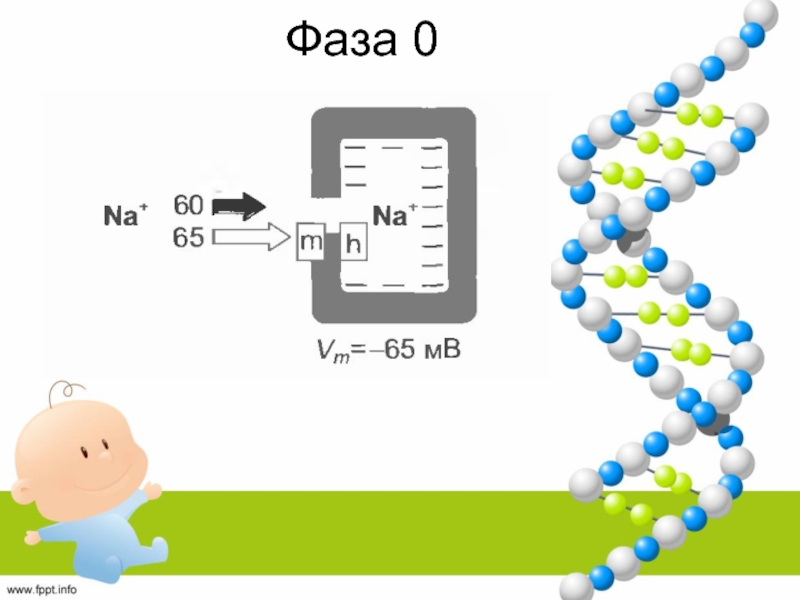
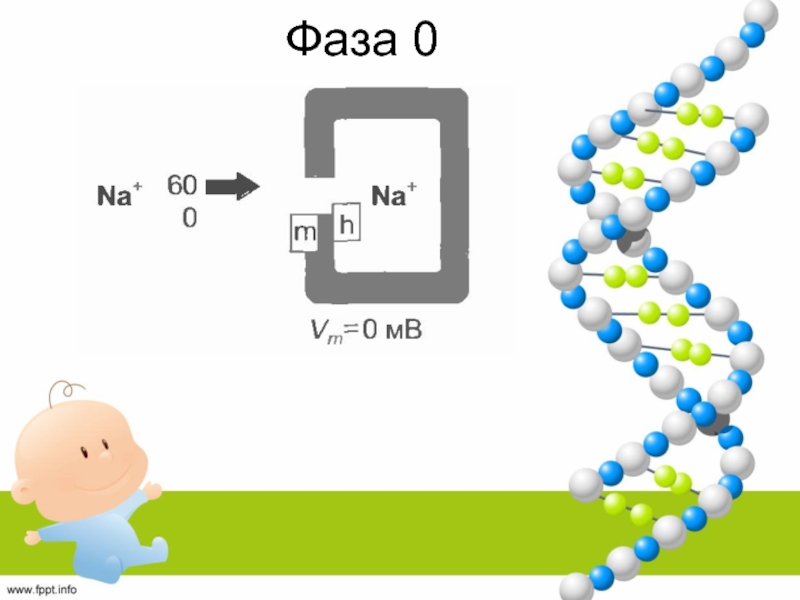
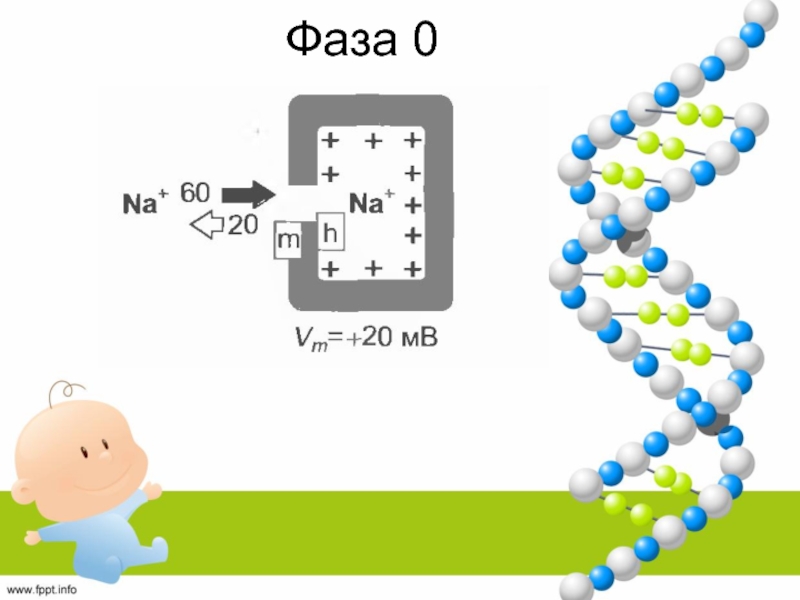
Слайд 47Фаза 0
ТТХ не оказывает влияния на фазу 0 → деполяризация
под влиянием Са-тока через L-тип каналов.
Слайд 49Фаза 4
Медленная спонтанная диастолическая деполяризация.
1) Ток Са через Т-тип каналов
(активируется при -55 мВ).
2) Funny-ток (If) (Вход Na и выход
К). Активируется гиперполяризацией (от -50 мВ и ниже, чем выраженнее гиперполяризация, тем выше активация).Слайд 50Фаза 4
3) Ток K (Ik) через каналы задержанного выпрямления, противодействуя
Ica и If, постепенно уменьшается в фазу 4.
4) Ток К
(IkG), управляемый G-белком, открывается при действии АХ и аденозина, гиперполяризует мембрану в фазу 4.Слайд 51HCN-каналы
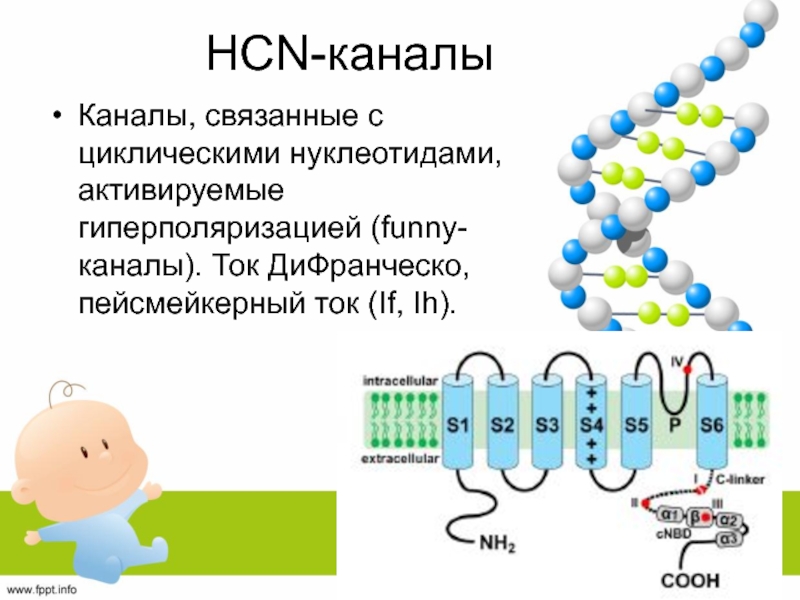
Каналы, связанные с циклическими нуклеотидами, активируемые гиперполяризацией (funny-каналы). Ток ДиФранческо,
пейсмейкерный ток (If, Ih).
Слайд 52HCN-каналы
Семейство из 4х каналов (HCN1-4). 6 сегментов.
S1-S4 – сенсор
напряжения.
P-домен между S5 и S6 – пора и селективный фильтр.
Есть
домен, связывающий циклические нуклеотиды (цНСД).Слайд 54Физиологическая роль If
1) Формирование импульса в ПСС (МСДД).
2) Защита клеток
СУ от гиперполяризующего влияния окружающих его волокон предсердия.
Слайд 55Модуляция If
Модулируется посредством вегетативных влияний через действие АХ и НА
на уровень цАМФ.
НА ↑ уровень цАМФ, активируя АДЦ при связывании
с β-рецепторами (β2 – в большей степени).АХ ↓ уровень цАМФ, ингибируя АДЦ при связывании с М2-рецепторами.
HCN модулируются непосредственно циклическими нуклеотидами (цАМФ и цГМФ), без фосфорилизации.
Слайд 56Нарушение If
1) Синдром слабости синусового узла.
Характеризуется такой ЧСС, которая неадекватна
физиологическим требованиям, и проявляется головокружением, усталостью и обморочными состояниями.
Первичная дегенерация
СУ, хроническая ишемия, действие фармакологических агентов. Мутация генов HCN, чаще всего HCN4.Слайд 57Потенциал-зависимые Ca-каналы
Са-каналы классифицируются на типы T, L, N, P, Q
и R и отличаются по их чувствительности к фармакологическим блокаторам,
проводимости, кинетике и зависимости от вольтажа.Слайд 59Блокаторы Са-каналов
Три группы:
1) Фенилалкиламины (верапамил);
2) Бензотиазипины (дилтиазем);
3) Дигидропиридины (нифедипин).
Связываясь с
а1-СЕ, ↓ длительность плато и силу сокращения миокарда при сердечной
недостаточности. Уменьшают постнагрузку, вызывая вазодилатацию.Слайд 60Са-каналы
Т-тип Са-каналов, или каналы, активирующиеся при низком пороге, открываются небольшой
деполяризацией от МПП.
L, N, P, Q и R-каналы, требуют
более сильной деполяризации для их открытия.Слайд 61Са-каналы
Высоко-пороговые Са-каналы могут быть разделены, посредством их фармакологических свойств.
L-каналы
блокируются дигидропиридинами, а N-каналы – двумя токсинами - ω-конотоксин GVIA
и ω-конотоксин MVIIA, полученными из моллюска Conus geographus.Токсин, полученный из яда паука Agelenopsis aperta, ω-агатоксин IVa, блокирует P-тип каналов и, с низким сродством, Q-тип каналов.
Слайд 62Са-каналы
Т-каналы – от слова tiny и transient,
L-каналы – large
и long-lasting.
N-каналы – neither и neuron-specific.
Слайд 63Строение Са-канала
L-тип Са-каналов – комплекс из 5 СЕ, α1, α2,
β, γ, δ.
За исключением цитоплазматической β-СЕ, все остальные пронизывают
мембрану. α1-СЕ функционально наиболее значима, так как действует как пора канала, сенсор напряжения и рецептор для многих лекарств.
Слайд 66Синдром длинного QT
α-CЕ IKs-калиевого канала (задержанного выпрямления – фаза 3)
- 30%–35%.
α-CЕ IKr-калиевого канала (задержанного выпрямления – фаза 3) -
25%–40%α-CЕ ПЗНК (5-я, сердечная изоформа) – фаза 0 - 5%–10%
Потери сознания и внезапная смерть, вызванная пароксизмами желудочковой тахикардии.
Слайд 67Синдром Бругада
α-CЕ ПЗНК (5-я, сердечная изоформа) – фаза 0 -
20% – 30%.
50% внезапных, некоронарогенных смертей в молодом возрасте.
Открыт в
1992 году братьями Бругада.Характеризуется частым возникновением обмороков на фоне приступов желудочковой тахикардии и внезапной смертью, преимущественно во сне, а также отсутствием признаков органического поражения миокарда при аутопсии.