Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
C игналинг в овулярной фазе
Содержание
- 1. C игналинг в овулярной фазе
- 2. Сигнальные механизмы в пестикеПреовулярные механизмы направляют рост
- 3. ROP ГТФазы и рецепторные киназыВ клетках растений
- 4. Начальные стадии прорастанияАктивация пыльцы как in vitro,
- 5. ROP1В растущей пыльцевой трубке специфичная для пыльцы
- 6. Регуляция по принципу обратной связиРецепторная киназуа RLK
- 7. Эффекторные белкиПуть, идущий через RIC4, приводит к
- 8. А что же АФК?Как мы помним, АФК
- 9. Ещё немного о Са2+ и АФКФосфорилирование НАДФН-оксидазы
- 10. Убегание от NO? YESОксид азота содержится в
- 11. NO как сигнал от семяпочкиНацеливание трубки на
- 12. NO и кальцийПри «убегании» трубок лилии от
- 13. NО, актин и пектины
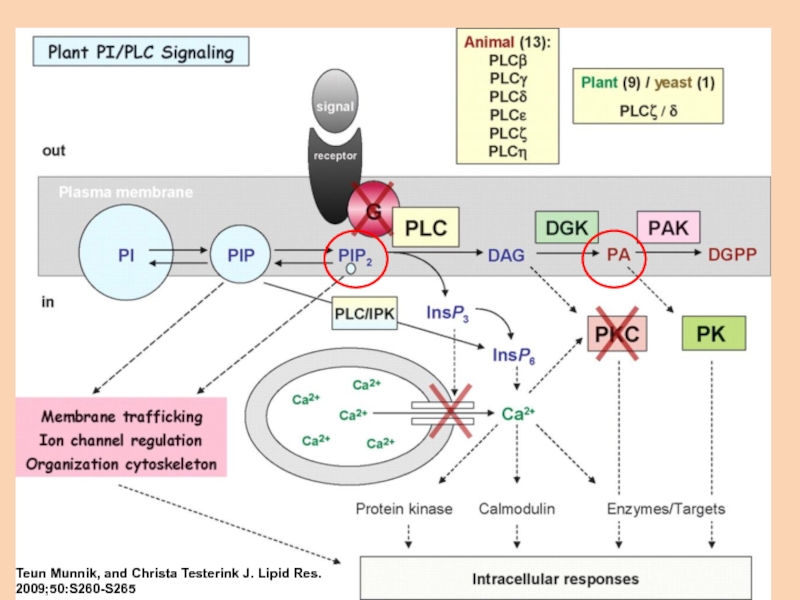
- 14. Teun Munnik, and Christa Testerink J. Lipid Res. 2009;50:S260-S265
- 15. Распределение фосфолипидовФосфатидная кислота сосредоточена в субапикальной плазмалемме,
- 16. Фосфолипиды и актинPI(4,5)P2 может различными способами влиять
- 17. Фосфолипиды и везикулярный транспортЭкзогенная PA и ингибитор
- 18. Итак, приближаемся к семяпочкеОвулярный этап разделяют на
- 19. Фуникулярные сигналыПрирода фуникулярных сигналов, исходящих из семяпочки,
- 20. GABAИнгибирование глутаматдекарбоксилазы – фермента, лимитирующего скорость биосинтеза
- 21. Как действует GABA? Активирует вход кальцияРегулирует экспрессию
- 22. GABA в пестикеВ пестике табака обнаружен градиент
- 23. Микропилярные сигналыЭти сигналы имеют короткий радиус действия
- 24. Механика врастанияВ конце своего пути пыльцевая трубка
- 25. Зона взаимодействия гаметЦитоплазмы ВК и С смешиваютсяПлазмалемма
- 26. ОплодотворениеПосле разрыва трубки, скорость движения спермиев возрастает
- 27. Экспрессировали в спермиях флуоресцентный белок, способный к
- 28. Одинаковые ли синергиды?Две синергиды в зрелом зародышевом
- 29. Нитчатый аппаратНитчатый аппарат представляет собой систему извилистых
- 30. Сигнальные пептиды 2ДВ числе первых аттрактантов, синтезируемых
- 31. А у однодольных?У кукурузы Z. Mays EGG
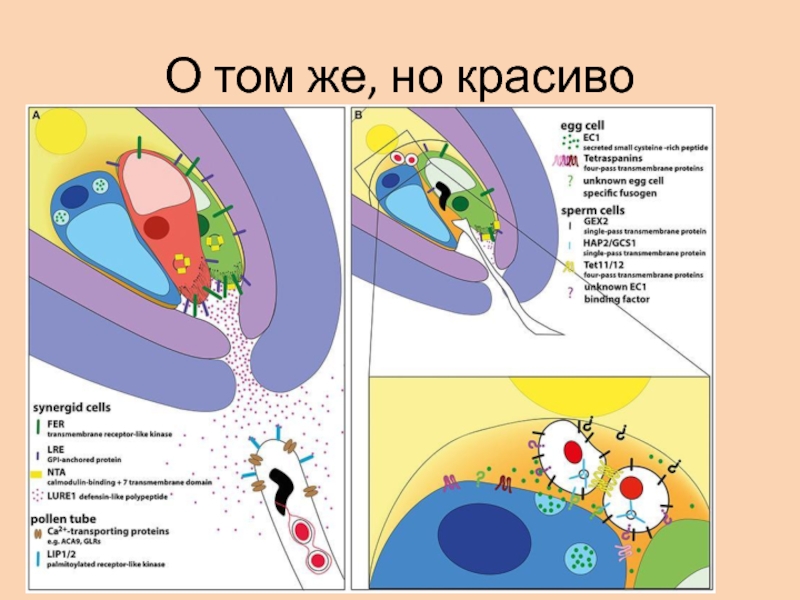
- 32. О том же, но красиво
- 33. Богиня плодородияКлючевую роль в разрыве трубки играют
- 34. Причем тут АФК?Итак, FERONIA должна вызвать разрыв
- 35. Другие участникиДва других белка синергиды, контролирующих поведение
- 36. Красивые имена NORTIA и LORELEIДля NTA, как
- 37. LRE, как и FER, индуцирует образование АФК
- 38. Взаимодействие гамет. ОплодотворениеДвойное оплодотворение у покрытосеменных растений
- 39. Гаметы и Са2+ (in vitro)При слиянии спермия
- 40. Кальциевая подпись in vivo
- 41. In vivo 2 пикаБолее сложная картина: 2
- 42. А что в синергидах?В синергиде при непосредственном
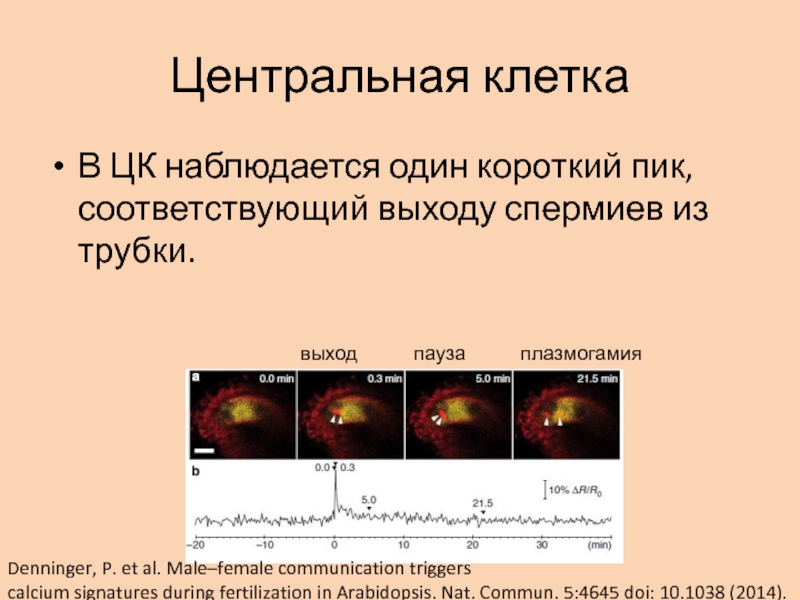
- 43. Центральная клеткаВ ЦК наблюдается один короткий пик,
- 44. Диалог гамет во время «паузы»GENERATIVE CELL SPECIFIC
- 45. Адгезия и слияниеОказалось, что адгезия мембран и
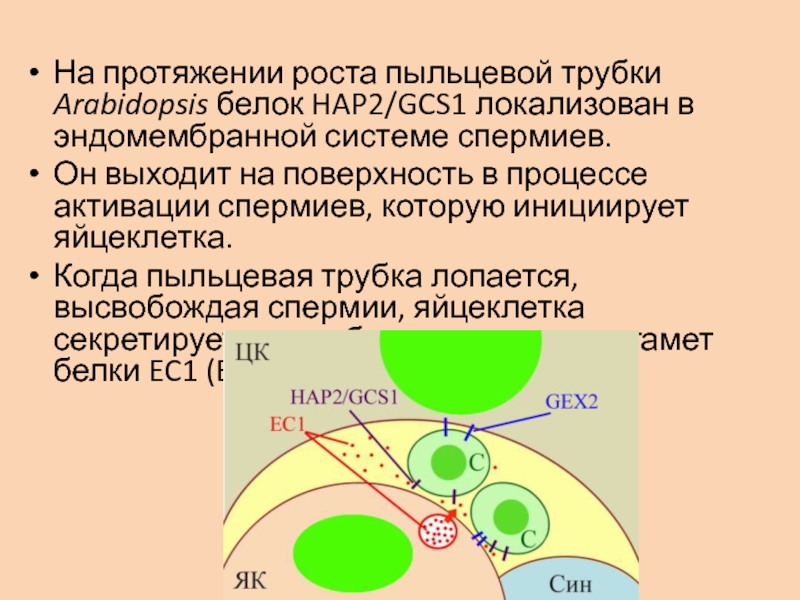
- 46. На протяжении роста пыльцевой трубки Arabidopsis белок
- 47. Активация гаметПри этом из эндомембранной системы на
- 48. Яйцеклетка: скромная или активная?В целом, слияние гамет
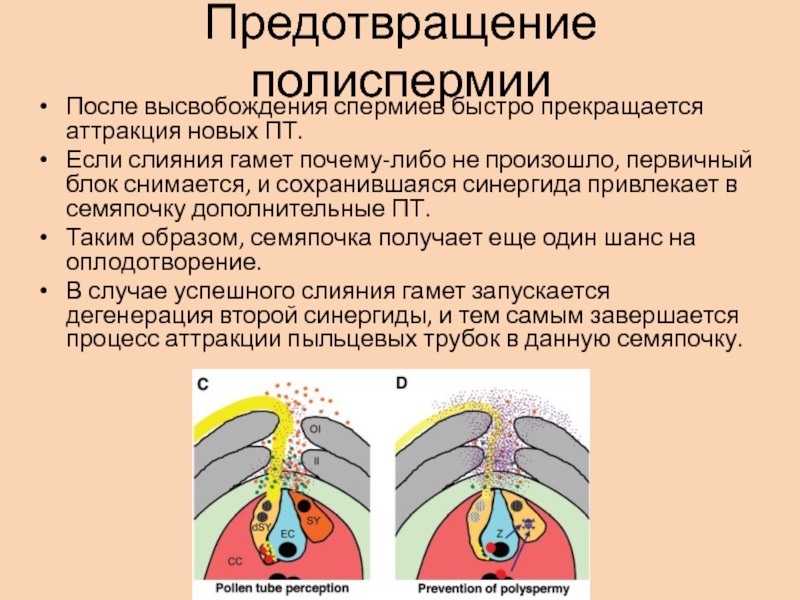
- 49. Предотвращение полиспермииПосле высвобождения спермиев быстро прекращается аттракция
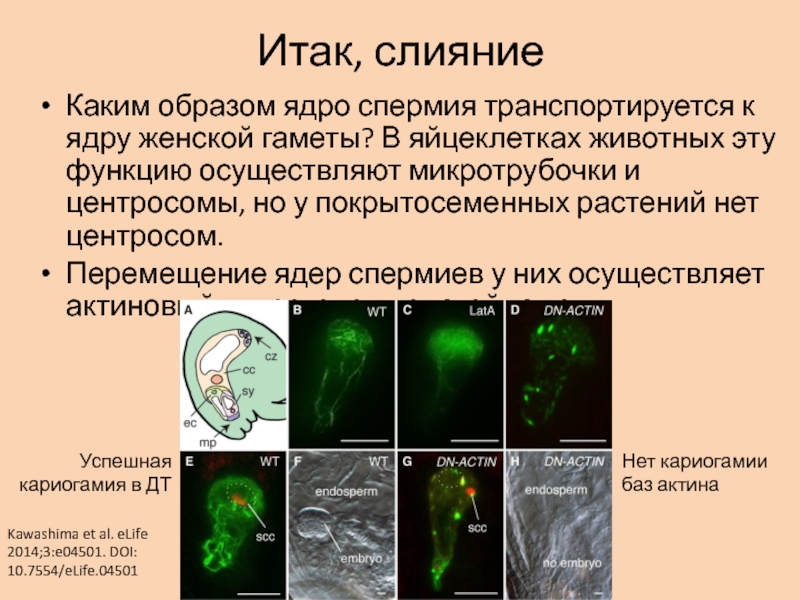
- 50. Итак, слияниеКаким образом ядро спермия транспортируется к
- 51. Актин в ЦКАктин – основной участник движения
- 52. ДеталиЯдро спермия, войдя в цитоплазму ЦК, окружалось
- 53. Кариогамия1) наружные ядерные мембраны гамет соприкасаются и
- 54. В системе in vitro у риса путь
- 55. СамонесовместимостьКогда «родной» вовсе значит «желанный»
- 56. Два типа СНГаметофитная СН: фенотип пыльцы определяется
- 57. Гаметофитная СН. S-RNAseРост пыльцы подавляется только тогда,
- 58. S-РНКазаЭтот фермент деградирует рРНК в самонесовместимой пыльцеПри
- 59. Две моделиДумали, что транспорт S-РНКаз в трубку
- 60. Чужие SРНКазы «не узнаются» и отправляются на
- 61. Спорофитная СН у капустыМеняемся ролями: мужской пепитид
- 62. Мужская детерминанта – SCR/SPP (S-locus cystein-rich protein,
- 63. Слайд 63
- 64. ARC1 взаимодействует с киназным доменом SRK и
- 65. Скачать презентанцию
Слайды и текст этой презентации
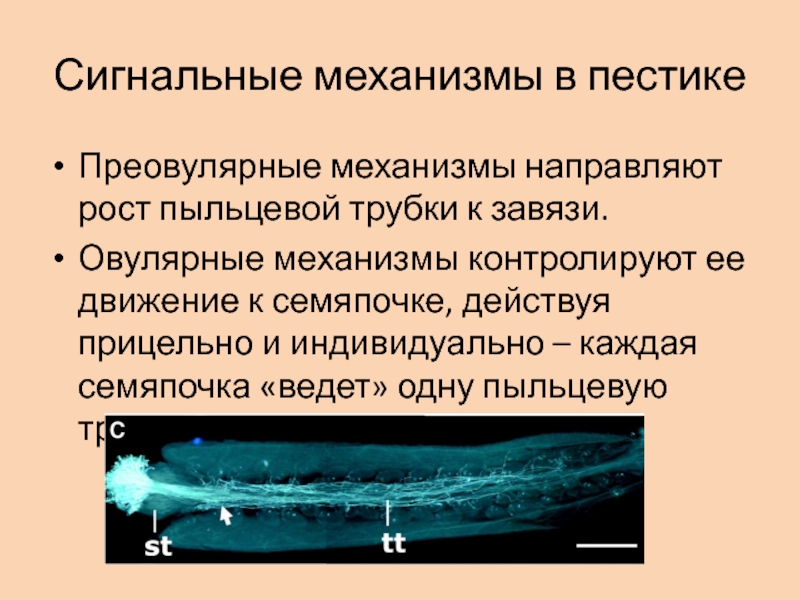
Слайд 2Сигнальные механизмы в пестике
Преовулярные механизмы направляют рост пыльцевой трубки к
завязи.
и индивидуально – каждая семяпочка «ведет» одну пыльцевую трубку.Слайд 3ROP ГТФазы и рецепторные киназы
В клетках растений основную роль играют
мономерные (малые) G белки (20-30 кДа).
Эти ГТФазы цилически переходят
из неактивной цитозольной формы (G-ГДФ) в активную форму (G-ГТФ), связанную с мембранойМалые ГТФазы, обозначаемые как Rac/Rop или ROP (Rho of plants) выполняют функции клеточных хабов – центральных переключателей и интеграторов сигналов.
В качестве мишеней для активированных ГТФаз могут, в частности, служить белки, связанные с функционированием цитоскелета и везикулярным транспортом.
Слайд 4Начальные стадии прорастания
Активация пыльцы как in vitro, так и in
vivo сопровождается активацией ROP ГТФаз (NtRAC).
В чистой воде этого
не происходит!В условиях in vitro высокий уровень активированных ГТФаз поддерживается на протяжении 30 мин, после чего снижается примерно к 60 мин.
Одной из мишеней этих белков в данном случае является актиндеполимеризующий фактор ADF.
Molecular Plant 2013 6, 1358-1361DOI: (10.1093/mp/sst074)
Слайд 5ROP1
В растущей пыльцевой трубке специфичная для пыльцы ГТФаза ROP1 локализована
преимущественно в апикальной плазмалемме.
Экспериментальный сдвиг баланса активации ROP1 в
ту или другую сторону приводит к полной остановке роста (снижение) или вызывает расширение кончика (повышение)Слайд 6Регуляция по принципу обратной связи
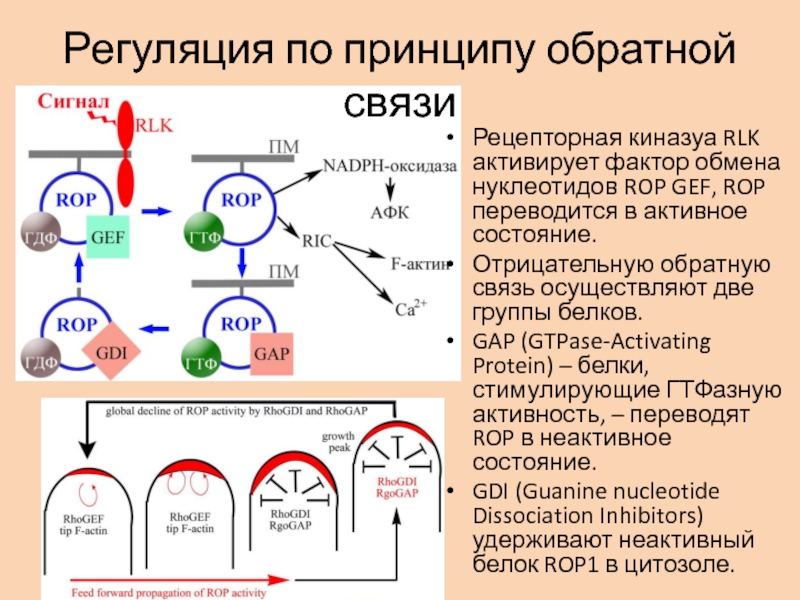
Рецепторная киназуа RLK активирует фактор обмена
нуклеотидов ROP GEF, ROP переводится в активное состояние.
Отрицательную обратную
связь осуществляют две группы белков.GAP (GTPase-Activating Protein) – белки, стимулирующие ГТФазную активность, – переводят ROP в неактивное состояние.
GDI (Guanine nucleotide Dissociation Inhibitors) удерживают неактивный белок ROP1 в цитозоле.
Слайд 7Эффекторные белки
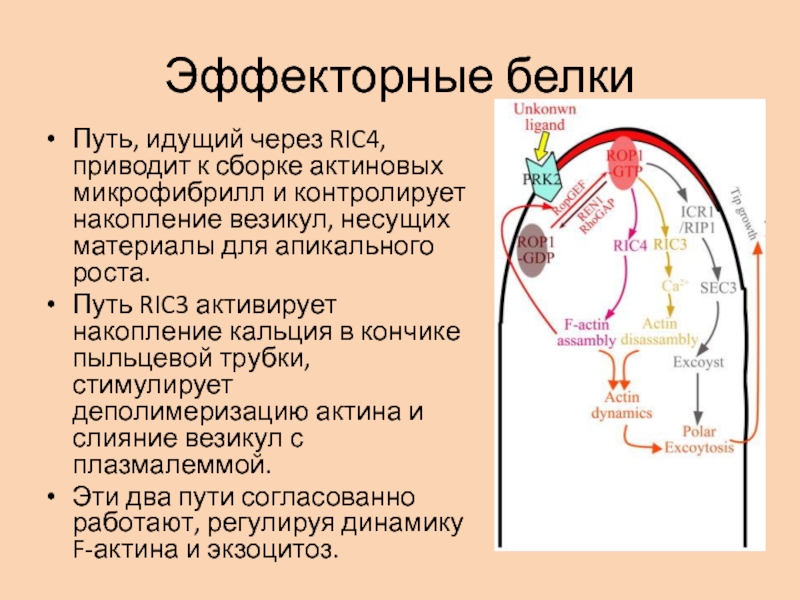
Путь, идущий через RIC4, приводит к сборке актиновых микрофибрилл
и контролирует накопление везикул, несущих материалы для апикального роста.
Путь
RIC3 активирует накопление кальция в кончике пыльцевой трубки, стимулирует деполимеризацию актина и слияние везикул с плазмалеммой. Эти два пути согласованно работают, регулируя динамику F-актина и экзоцитоз.
Слайд 8А что же АФК?
Как мы помним, АФК контролируют 3 этапа
прогамной фазы: собственно прорастание, рост трубки и… разрыв трубки
Основными источниками
АФК являются НАДФН-оксидаза плазмалеммы и ДЦ в митохондриях, но первая больше работает «на сигнал»Самая классическая схема «АФК-кальций» в репродукции была утверждена буквально «на днях»
Слайд 9Ещё немного о Са2+ и АФК
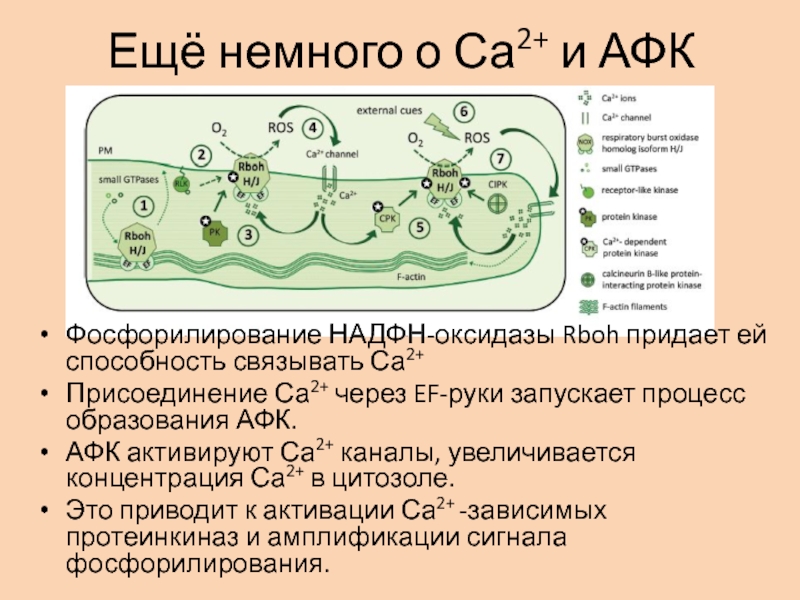
Фосфорилирование НАДФН-оксидазы Rboh придает ей
способность связывать Са2+
Присоединение Са2+ через EF-руки запускает процесс образования АФК.
АФК
активируют Са2+ каналы, увеличивается концентрация Са2+ в цитозоле. Это приводит к активации Са2+ -зависимых протеинкиназ и амплификации сигнала фосфорилирования.
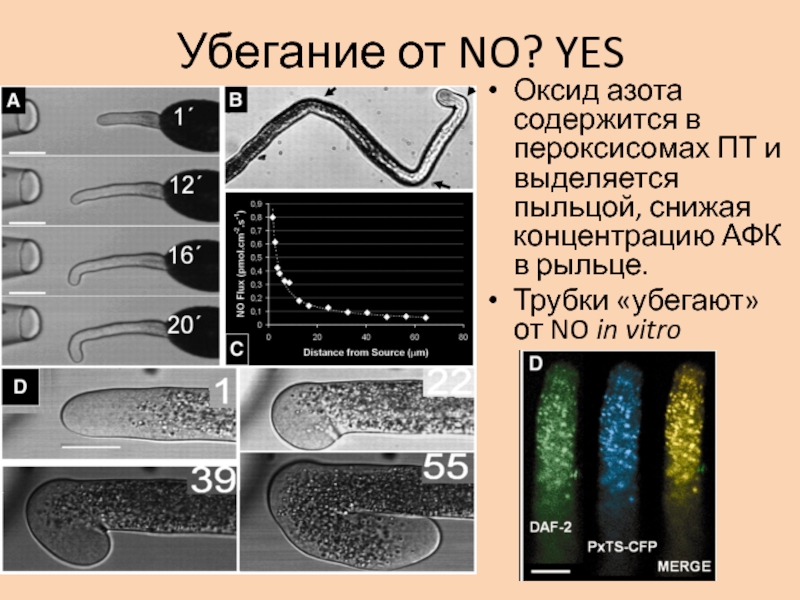
Слайд 10Убегание от NO? YES
Оксид азота содержится в пероксисомах ПТ и
выделяется пыльцой, снижая концентрацию АФК в рыльце.
Трубки «убегают» от
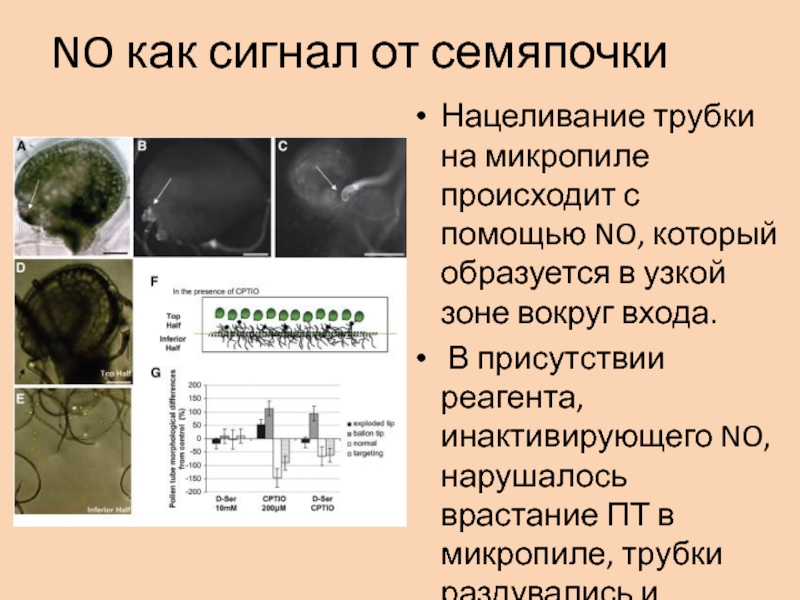
NO in vitroСлайд 11NO как сигнал от семяпочки
Нацеливание трубки на микропиле происходит с
помощью NO, который образуется в узкой зоне вокруг входа.
В
присутствии реагента, инактивирующего NO, нарушалось врастание ПТ в микропиле, трубки раздувались и лопались.Слайд 12NO и кальций
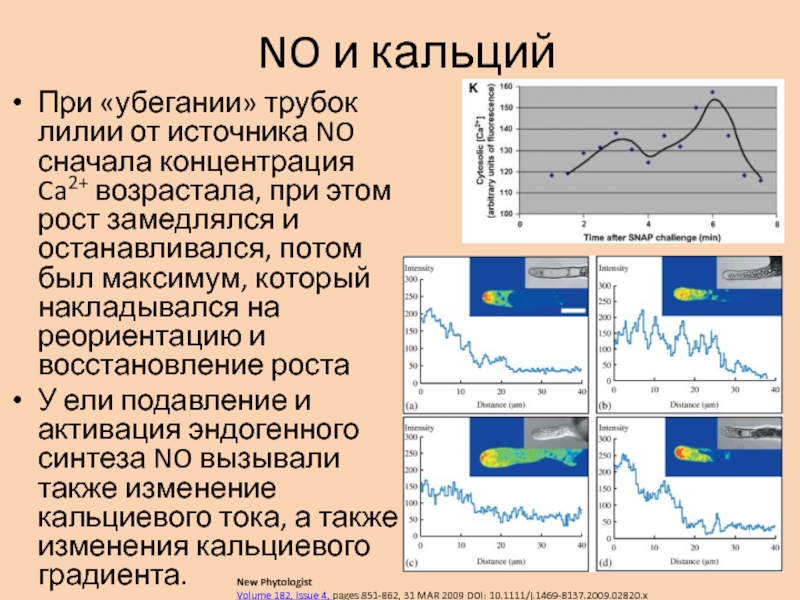
При «убегании» трубок лилии от источника NO сначала
концентрация Ca2+ возрастала, при этом рост замедлялся и останавливался, потом
был максимум, который накладывался на реориентацию и восстановление ростаУ ели подавление и активация эндогенного синтеза NO вызывали также изменение кальциевого тока, а также изменения кальциевого градиента.
New Phytologist
Volume 182, Issue 4, pages 851-862, 31 MAR 2009 DOI: 10.1111/j.1469-8137.2009.02820.x
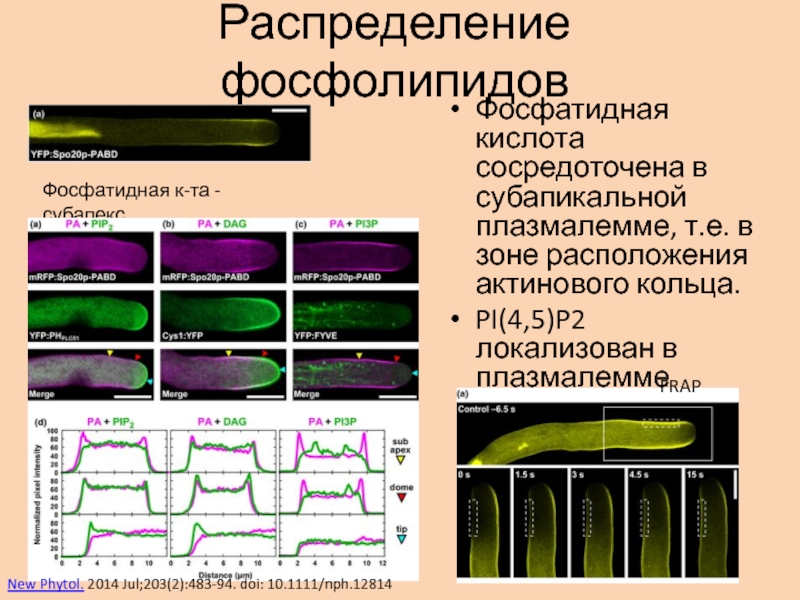
Слайд 15Распределение фосфолипидов
Фосфатидная кислота сосредоточена в субапикальной плазмалемме, т.е. в зоне
расположения актинового кольца.
PI(4,5)P2 локализован в плазмалемме апекса трубки.
Фосфатидная к-та
- субапексFRAP
New Phytol. 2014 Jul;203(2):483-94. doi: 10.1111/nph.12814
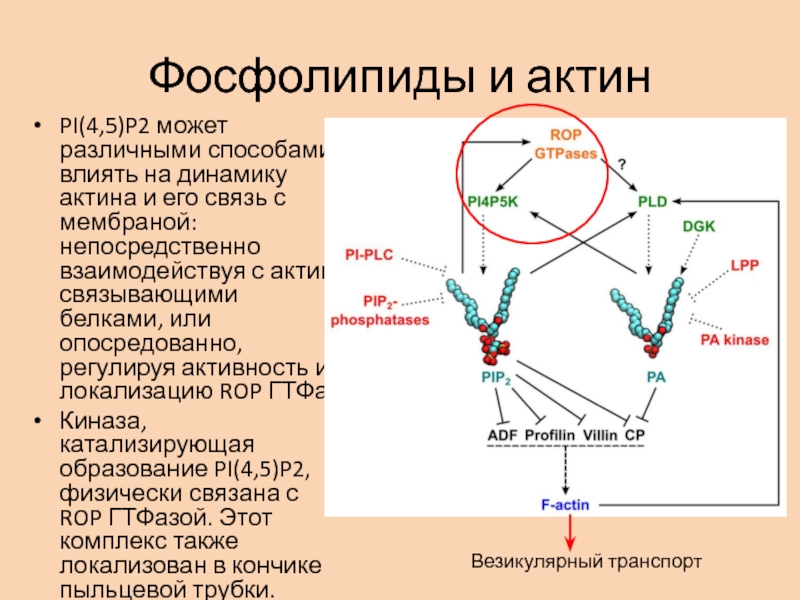
Слайд 16Фосфолипиды и актин
PI(4,5)P2 может различными способами влиять на динамику актина
и его связь с мембраной: непосредственно взаимодействуя с актин-связывающими белками,
или опосредованно, регулируя активность и локализацию ROP ГТФазКиназа, катализирующая образование PI(4,5)P2, физически связана с ROP ГТФазой. Этот комплекс также локализован в кончике пыльцевой трубки.
Везикулярный транспорт
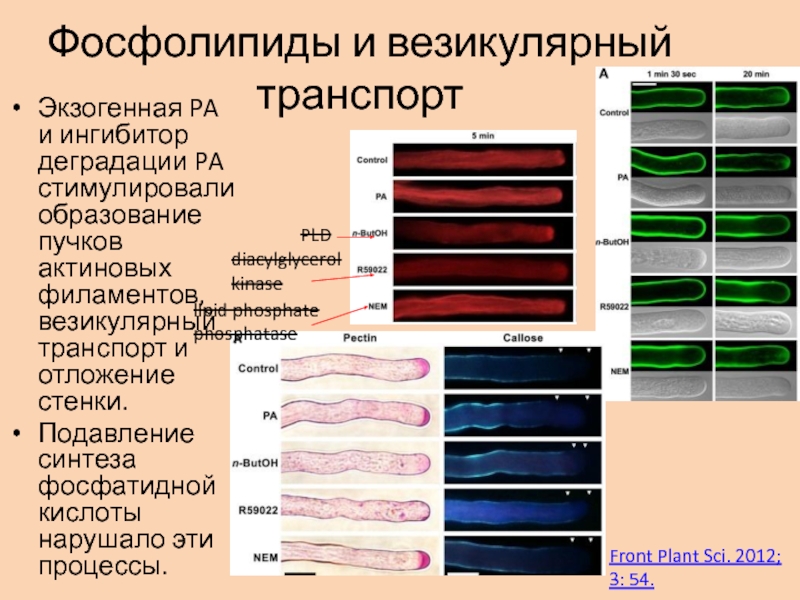
Слайд 17Фосфолипиды и везикулярный транспорт
Экзогенная PA и ингибитор деградации PA стимулировали
образование пучков актиновых филаментов, везикулярный транспорт и отложение стенки.
Подавление
синтеза фосфатидной кислоты нарушало эти процессы.PLD
diacylglycerol kinase
lipid phosphate phosphatase
Front Plant Sci. 2012; 3: 54.
Слайд 18Итак, приближаемся к семяпочке
Овулярный этап разделяют на две фазы регуляции
роста пыльцевой трубки:
фуникулярная и
микропилярная.
Фуникулярная регуляция включает сигналы,
исходящие из семяпочки, которые заставляют трубку выйти из проводникового тракта и расти к семяпочке по поверхности фуникулуса. Микропилярная регуляция направляет трубку к микропиле и яйцевому аппарату.
Фуникулярная регуляция у Arabidopsis, как полагают, осуществляется совместными усилями спорофита и женского гаметофита.
Микропилярную регуляцию осуществляет женский гаметофит.
Слайд 19Фуникулярные сигналы
Природа фуникулярных сигналов, исходящих из семяпочки, неясна. В числе
кандидатов рассматривают NO и D-серин, о которых мы говорили ранее,
а также γ-аминомасляную кислоту (GABA)Слайд 20GABA
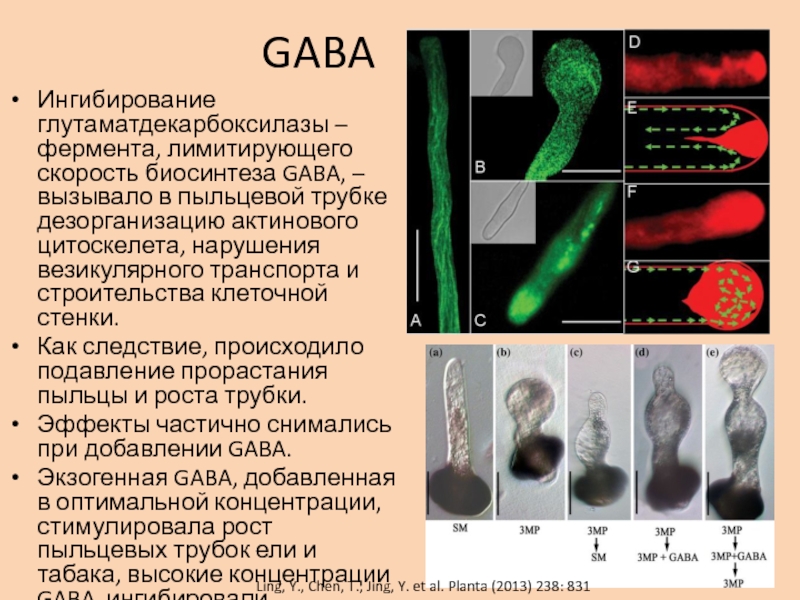
Ингибирование глутаматдекарбоксилазы – фермента, лимитирующего скорость биосинтеза GABA, – вызывало
в пыльцевой трубке дезорганизацию актинового цитоскелета, нарушения везикулярного транспорта и
строительства клеточной стенки.Как следствие, происходило подавление прорастания пыльцы и роста трубки.
Эффекты частично снимались при добавлении GABA.
Экзогенная GABA, добавленная в оптимальной концентрации, стимулировала рост пыльцевых трубок ели и табака, высокие концентрации GABA ингибировали.
Ling, Y., Chen, T., Jing, Y. et al. Planta (2013) 238: 831
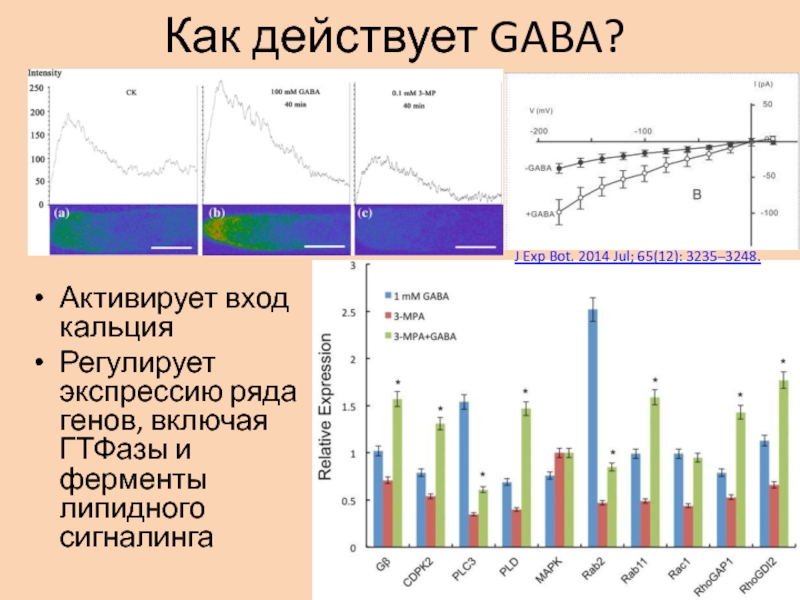
Слайд 21Как действует GABA?
Активирует вход кальция
Регулирует экспрессию ряда генов, включая
ГТФазы и ферменты липидного сигналинга
J Exp Bot. 2014 Jul; 65(12):
3235–3248.Слайд 22GABA в пестике
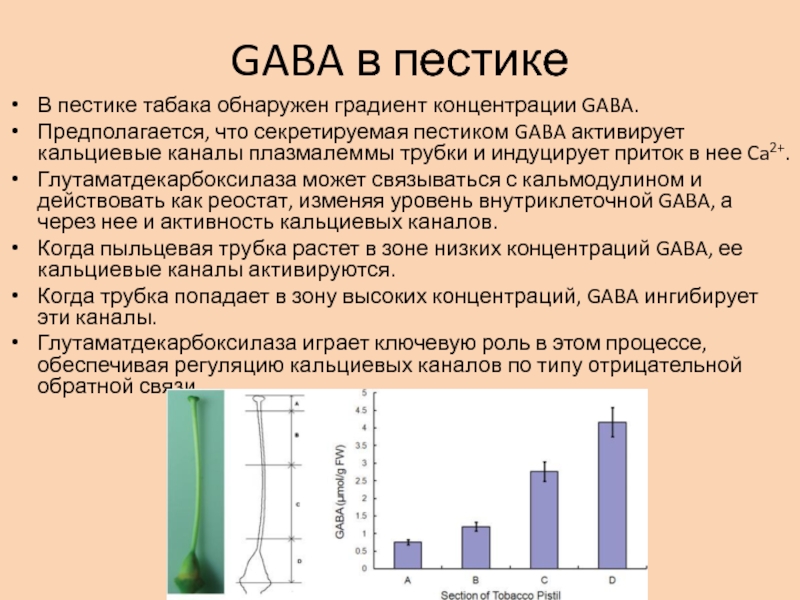
В пестике табака обнаружен градиент концентрации GABA.
Предполагается,
что секретируемая пестиком GABA активирует кальциевые каналы плазмалеммы трубки и
индуцирует приток в нее Ca2+.Глутаматдекарбоксилаза может связываться с кальмодулином и действовать как реостат, изменяя уровень внутриклеточной GABA, а через нее и активность кальциевых каналов.
Когда пыльцевая трубка растет в зоне низких концентраций GABA, ее кальциевые каналы активируются.
Когда трубка попадает в зону высоких концентраций, GABA ингибирует эти каналы.
Глутаматдекарбоксилаза играет ключевую роль в этом процессе, обеспечивая регуляцию кальциевых каналов по типу отрицательной обратной связи.
Слайд 23Микропилярные сигналы
Эти сигналы имеют короткий радиус действия (100-200 мкм от
микропиле), значит, здесь могут работать достаточно крупные молекулы, например, небольшие
белки.Любимый объект - Torenia fournieri, у которой «полуголый» зародышевый мешок выступает из семяпочки, так что синергиды, яйцеклетка и часть центральной клетки находятся в гнезде завязи
Эксперименты с последовательной лазерной абляцией (удалением) клеток ЗМ показали, что для привлечения пыльцевой трубки к женскому гаметофиту необходимо и достаточно, чтобы сохранялась хотя бы одна синергида.
Судя по всему, синергида - главный источник хемоаттракции пыльцевых трубок
Слайд 24Механика врастания
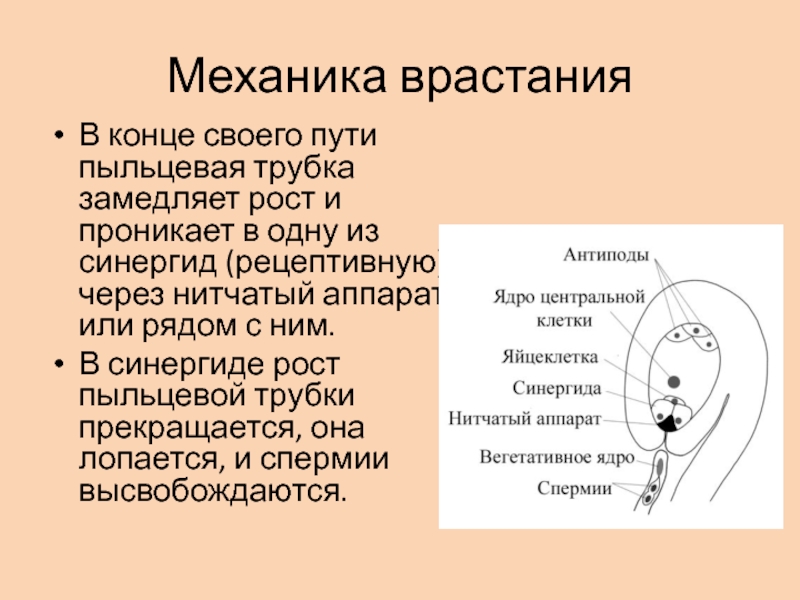
В конце своего пути пыльцевая трубка замедляет рост и
проникает в одну из синергид (рецептивную) через нитчатый аппарат или
рядом с ним.В синергиде рост пыльцевой трубки прекращается, она лопается, и спермии высвобождаются.
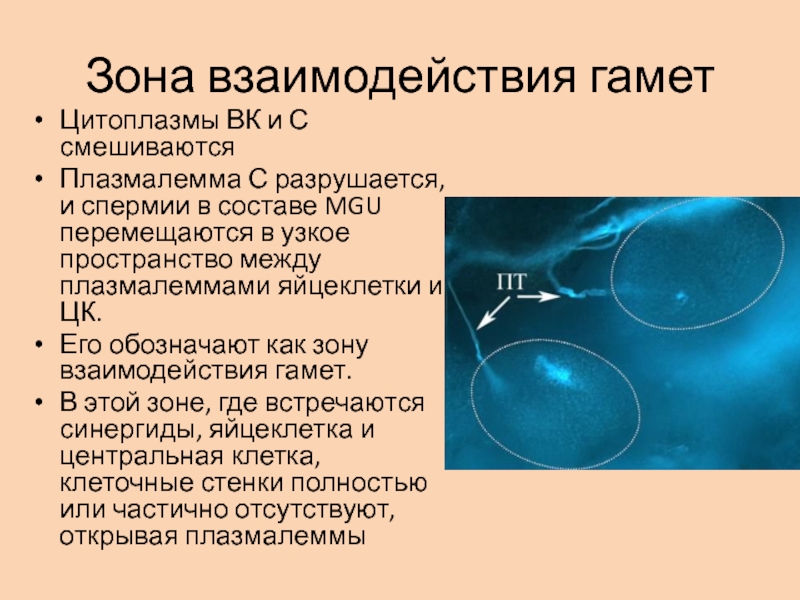
Слайд 25Зона взаимодействия гамет
Цитоплазмы ВК и С смешиваются
Плазмалемма С разрушается, и
спермии в составе MGU перемещаются в узкое пространство между плазмалеммами
яйцеклетки и ЦК.Его обозначают как зону взаимодействия гамет.
В этой зоне, где встречаются синергиды, яйцеклетка и центральная клетка, клеточные стенки полностью или частично отсутствуют, открывая плазмалеммы
Слайд 26Оплодотворение
После разрыва трубки, скорость движения спермиев возрастает примерно в 100
раз.
Неизвестно, используется ли на этом этапе активный транспорт, или спермии
перемещаются с потоком цитоплазмы, выходящей из лопнувшей пыльцевой трубки.После такого быстрого движения спермии останавливаются в зоне взаимодействия гамет. У Arabidopsis эта «остановка» длится около 7 мин.
В этот период дегенерирует ядро вегетативной клетки, происходит активация спермиев, адгезия плазматических мембран и объединение цитоплазмы в обеих парах гамет (плазмогамия).
После чего ядра спермиев перемещаются к ядрам женских гамет и сливаются с ними (кариогамия).
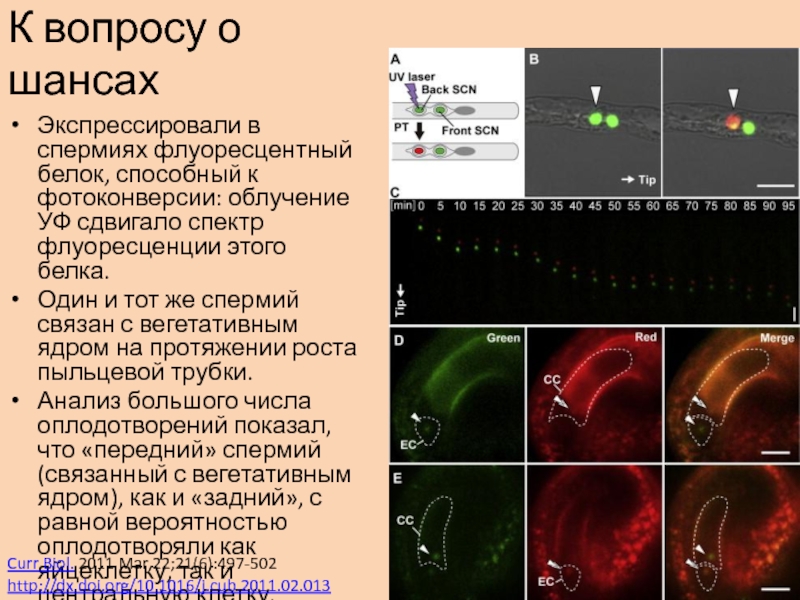
Слайд 27Экспрессировали в спермиях флуоресцентный белок, способный к фотоконверсии: облучение УФ
сдвигало спектр флуоресценции этого белка.
Один и тот же спермий
связан с вегетативным ядром на протяжении роста пыльцевой трубки. Анализ большого числа оплодотворений показал, что «передний» спермий (связанный с вегетативным ядром), как и «задний», с равной вероятностью оплодотворяли как яйцеклетку, так и центральную клетку.
К вопросу о шансах
Curr Biol. 2011 Mar 22;21(6):497-502
http://dx.doi.org/10.1016/j.cub.2011.02.013
Слайд 28Одинаковые ли синергиды?
Две синергиды в зрелом зародышевом мешке многих растений
неразличимы, и выбор трубкой рецептивной синергиды, по-видимому, происходит случайным образом.
Гибель
рецептивной синергиды у Arabidopsis, например, запускается после непосредственного контакта с пыльцевой трубкой. А гибель второй синергиды происходит после оплодотворения.
У других видов растений, таких как табак, рецептивная синергида определена до прибытия трубки и отличается по ультраструктуре; кроме того, в ней накапливаются значительные количества мембраносвязанного кальция
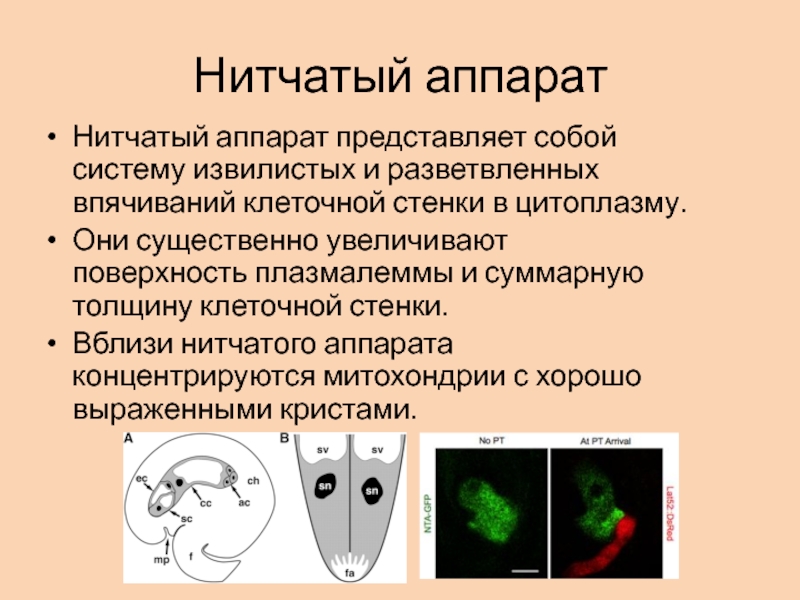
Слайд 29Нитчатый аппарат
Нитчатый аппарат представляет собой систему извилистых и разветвленных впячиваний
клеточной стенки в цитоплазму.
Они существенно увеличивают поверхность плазмалеммы и
суммарную толщину клеточной стенки.Вблизи нитчатого аппарата концентрируются митохондрии с хорошо выраженными кристами.
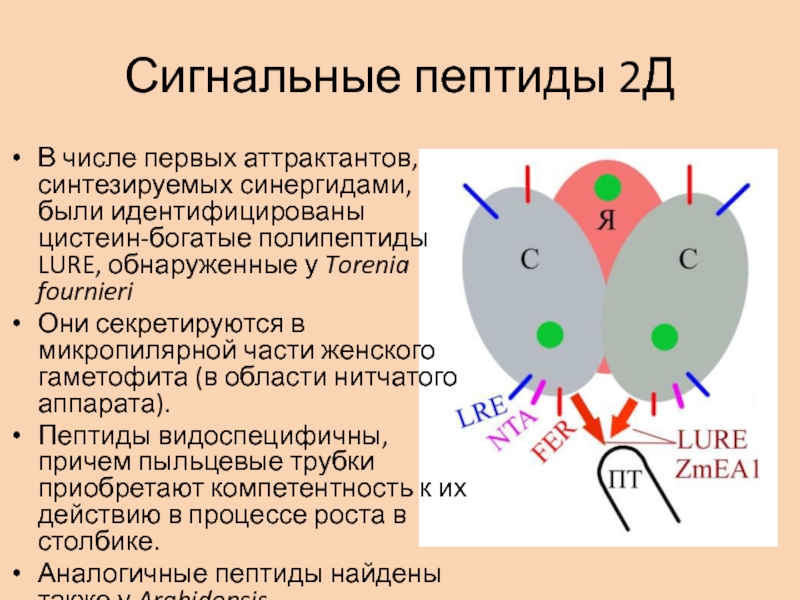
Слайд 30Сигнальные пептиды 2Д
В числе первых аттрактантов, синтезируемых синергидами, были идентифицированы
цистеин-богатые полипептиды LURE, обнаруженные у Torenia fournieri
Они секретируются в микропилярной
части женского гаметофита (в области нитчатого аппарата). Пептиды видоспецифичны, причем пыльцевые трубки приобретают компетентность к их действию в процессе роста в столбике.
Аналогичные пептиды найдены также у Arabidopsis.
Слайд 31А у однодольных?
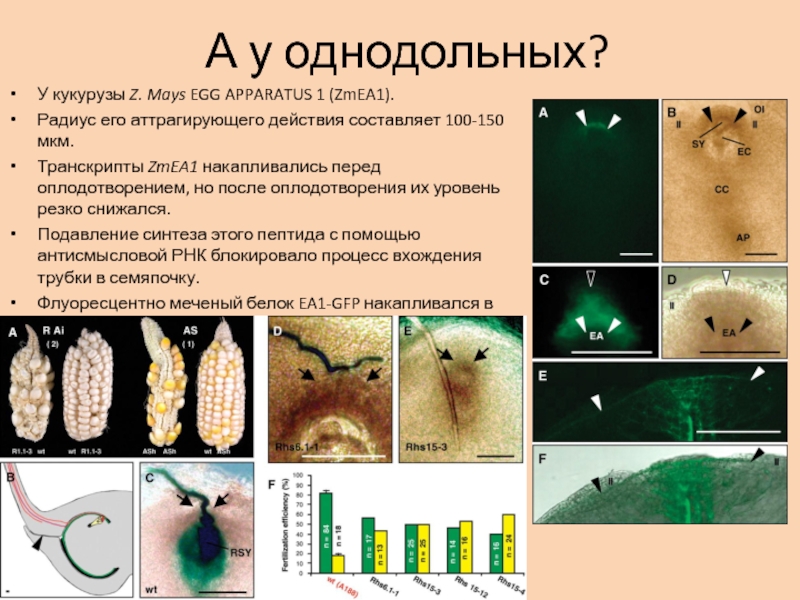
У кукурузы Z. Mays EGG APPARATUS 1 (ZmEA1).
Радиус его аттрагирующего действия составляет 100-150 мкм.
Транскрипты ZmEA1 накапливались
перед оплодотворением, но после оплодотворения их уровень резко снижался. Подавление синтеза этого пептида с помощью антисмысловой РНК блокировало процесс вхождения трубки в семяпочку.
Флуоресцентно меченый белок EA1-GFP накапливался в стенках клеток нуцеллуса, расположенных вокруг микропилярного конца женского гаметофита.
Слайд 33Богиня плодородия
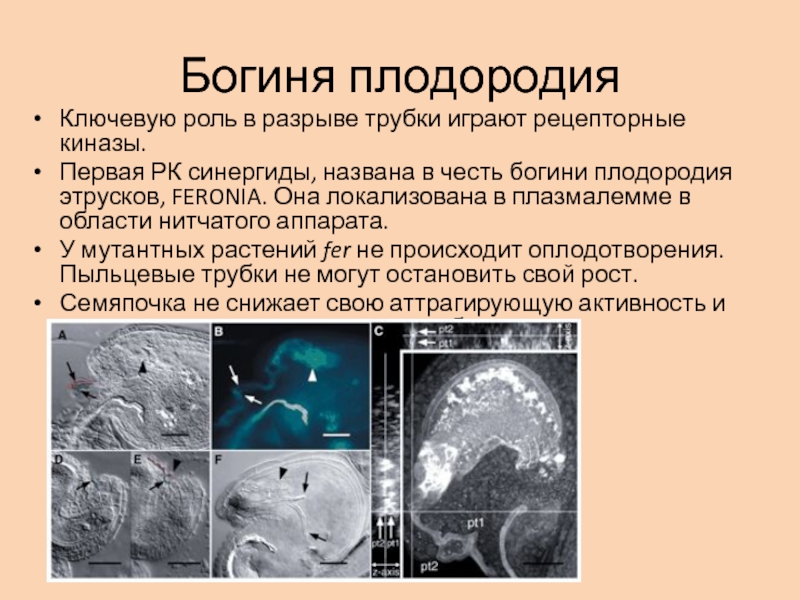
Ключевую роль в разрыве трубки играют рецепторные киназы.
Первая
РК синергиды, названа в честь богини плодородия этрусков, FERONIA. Она
локализована в плазмалемме в области нитчатого аппарата.У мутантных растений fer не происходит оплодотворения. Пыльцевые трубки не могут остановить свой рост.
Семяпочка не снижает свою аттрагирующую активность и привлекает новые пыльцевые трубки.
Слайд 34Причем тут АФК?
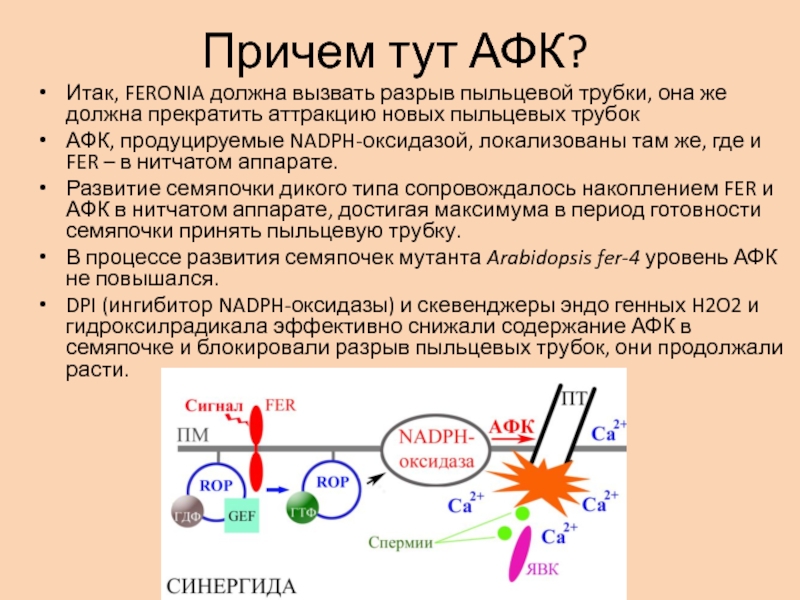
Итак, FERONIA должна вызвать разрыв пыльцевой трубки, она
же должна прекратить аттракцию новых пыльцевых трубок
АФК, продуцируемые NADPH-оксидазой, локализованы
там же, где и FER – в нитчатом аппарате.Развитие семяпочки дикого типа сопровождалось накоплением FER и АФК в нитчатом аппарате, достигая максимума в период готовности семяпочки принять пыльцевую трубку.
В процессе развития семяпочек мутанта Arabidopsis fer-4 уровень АФК не повышался.
DPI (ингибитор NADPH-оксидазы) и скевенджеры эндо генных H2O2 и гидроксилрадикала эффективно снижали содержание АФК в семяпочке и блокировали разрыв пыльцевых трубок, они продолжали расти.
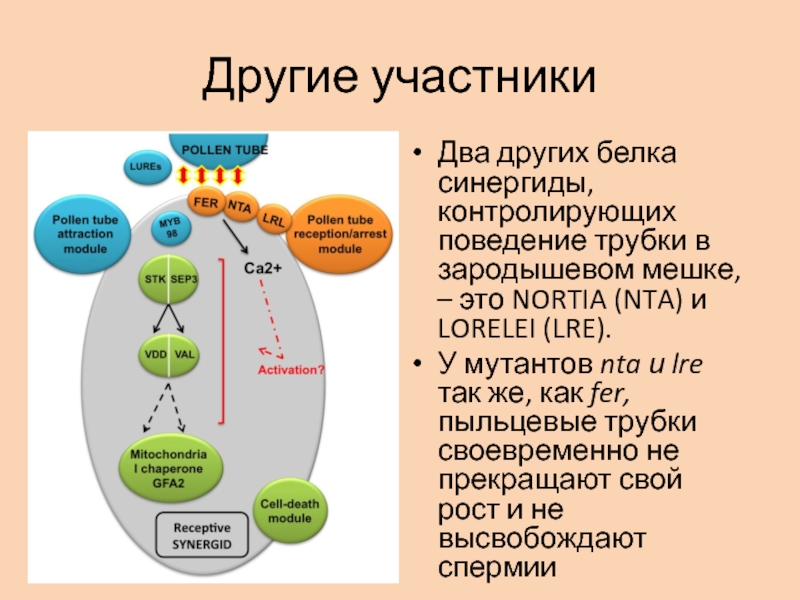
Слайд 35Другие участники
Два других белка синергиды, контролирующих поведение трубки в зародышевом
мешке, – это NORTIA (NTA) и LORELEI (LRE).
У мутантов
nta и lre так же, как fer, пыльцевые трубки своевременно не прекращают свой рост и не высвобождают спермииСлайд 36Красивые имена NORTIA и LORELEI
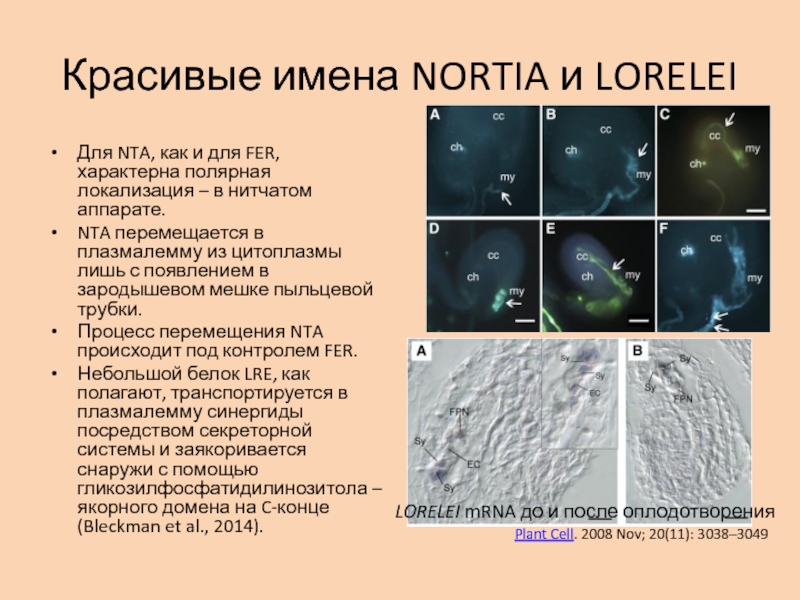
Для NTA, как и для FER,
характерна полярная локализация – в нитчатом аппарате.
NTA перемещается в
плазмалемму из цитоплазмы лишь с появлением в зародышевом мешке пыльцевой трубки. Процесс перемещения NTA происходит под контролем FER.
Небольшой белок LRE, как полагают, транспортируется в плазмалемму синергиды посредством секреторной системы и заякоривается снаружи с помощью гликозилфосфатидилинозитола – якорного домена на C-конце (Bleckman et al., 2014).
LORELEI mRNA до и после оплодотворения
Plant Cell. 2008 Nov; 20(11): 3038–3049
Слайд 37LRE, как и FER, индуцирует образование АФК в нитчатом аппарате
Популярная
версия: LRE, наряду с FER, входит в сигнальный модуль, который
включает ROP ГТФазу и обеспечивает высокий уровень АФК на входе в женский гаметофитСлайд 38Взаимодействие гамет. Оплодотворение
Двойное оплодотворение у покрытосеменных растений было открыто С.Г.
Навашиным в конце XIX в.
Первые успешные эксперименты по оплодотворению in
vitro были поставлены в начале 1990х. Kranz с коллегами индуцировали слияние спермия и яйцеклетки кукурузы с помощью электрических импульсов. Далее научились использовать для слияния Ca2+ или ПЭГ.
Слайд 39Гаметы и Са2+ (in vitro)
При слиянии спермия и яйцеклетки кукурузы
in vitro наблюдали временное увеличение цитозольной концентрации кальция.
Кальций поступал
в яйцеклетку извне. Этот процесс начинался сразу после слияния гамет в месте входа спермия. Затем он распространялся в виде волны по поверхности яйцеклетки со скоростью около 1 мкм/с, и в итоге охватывал всю клетку
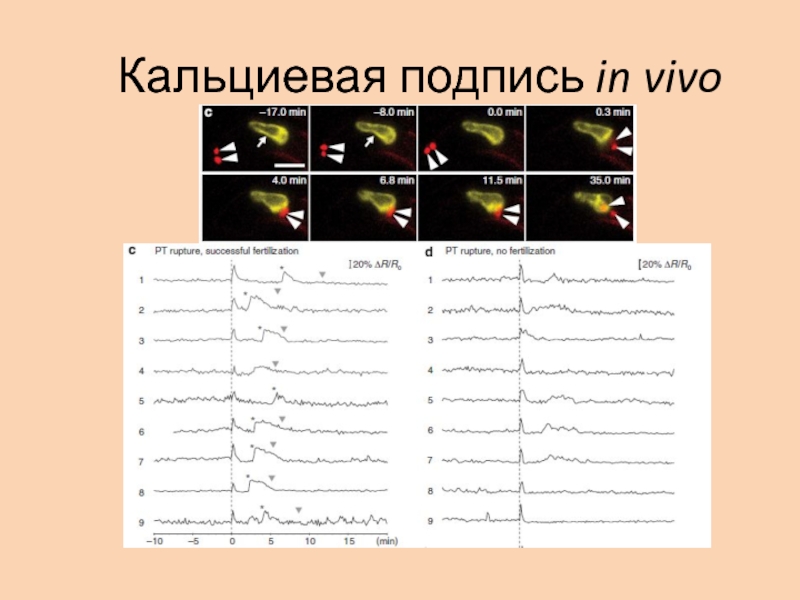
Слайд 41In vivo 2 пика
Более сложная картина: 2 пика!
Первый пик
соответствует высвобождению спермиев.
Значение этого спайка не выяснено. Он предшествует
секреции белка EC1, активирующего спермии. Возможно, этот спайк связан с активацией яйцеклетки.Второе транзиторное увеличение кальция в яйцеклетке соответствует плазмогамии.
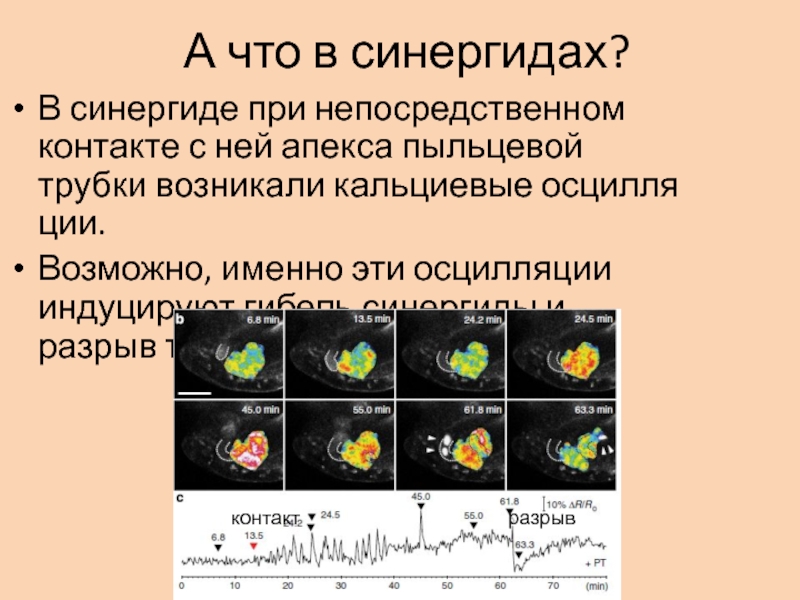
Слайд 42А что в синергидах?
В синергиде при непосредственном контакте с ней
апекса пыльцевой трубки возникали кальциевые осцилля ции.
Возможно, именно эти
осцилляции индуцируют гибель синергиды и разрыв трубки.контакт
разрыв
Слайд 43Центральная клетка
В ЦК наблюдается один короткий пик, соответствующий выходу спермиев
из трубки.
выход
пауза
плазмогамия
Denninger, P. et al. Male–female communication triggers
calcium signatures during
fertilization in Arabidopsis. Nat. Commun. 5:4645 doi: 10.1038 (2014).Слайд 44Диалог гамет во время «паузы»
GENERATIVE CELL SPECIFIC 1 (GCS1) у
Lilium longiflorum и его ортолог у Arabidopsis HAPLESS2 (HAP2) экспрессируется
только в генеративной клетке и спермиях.GCS1 – это трансмембранный белок, локализованный в плазмалемме.
GCS1 играет ключевую роль в слиянии спермиев с женскими гаметами
Mori T., Kawai-Toyooka H., Igawa T., and Nozaki H. (2015). Gamete Dialogs in Green Lineages. Mol. Plant. 8, 1442–1454.
Слайд 45Адгезия и слияние
Оказалось, что адгезия мембран и их слияние –
разные процессы.
Гаметы мутантных растений hap2/gcs1 успешно проходили стадию адгезии мембран,
но они были не способны к слияниюGAMETE EXPRESSED 2 (GEX2) зато экспрессировался только в спермиях.
У мутантов gex2 было нарушено прикрепление спермиев к одной из женских гамет или к обеим, что не характерно для мутантов gcs1.
По-видимому, GEX2 контролирует этап адгезии гамет, а не их слияния.
Остается открытым вопрос о белках-партнерах на поверхности яйцеклетки и центральной клетки, с которыми взаимодействует GEX2.
Слайд 46На протяжении роста пыльцевой трубки Arabidopsis белок HAP2/GCS1 локализован в
эндомембранной системе спермиев.
Он выходит на поверхность в процессе активации
спермиев, которую инициирует яйцеклетка. Когда пыльцевая трубка лопается, высвобождая спермии, яйцеклетка секретирует в зону будущего слияния гамет белки EC1 (Egg Cell 1).
Слайд 47Активация гамет
При этом из эндомембранной системы на поверхность спермия выходят
белки HAP2/GCS1.
Это происходит одновременно с распадом MGU и разделением
спермиев и предшествует плазмогамии.Таким образом, гаметы растений, как и других эукариот, приобретают компетентность и способность к слиянию, лишь пройдя этап предварительной активации
Слайд 48Яйцеклетка: скромная или активная?
В целом, слияние гамет у растений происходит
почти так же, как у животных, однако при другом распределении
ролей.У животных яйцеклетка остается в состоянии покоя до тех пор, пока не сливается со спермием.
У Arabidopsis перед слиянием активируются обе гаметы, причем ведущую роль играет яйцеклетка
Слайд 49Предотвращение полиспермии
После высвобождения спермиев быстро прекращается аттракция новых ПТ.
Если
слияния гамет почему-либо не произошло, первичный блок снимается, и сохранившаяся
синергида привлекает в семяпочку дополнительные ПТ.Таким образом, семяпочка получает еще один шанс на оплодотворение.
В случае успешного слияния гамет запускается дегенерация второй синергиды, и тем самым завершается процесс аттракции пыльцевых трубок в данную семяпочку.
Слайд 50Итак, слияние
Каким образом ядро спермия транспортируется к ядру женской гаметы?
В яйцеклетках животных эту функцию осуществляют микротрубочки и центросомы, но
у покрытосеменных растений нет центросом.Перемещение ядер спермиев у них осуществляет актиновый цитоскелет женской гаметы.
Kawashima et al. eLife 2014;3:e04501. DOI: 10.7554/eLife.04501
Успешная кариогамия в ДТ
Нет кариогамии баз актина
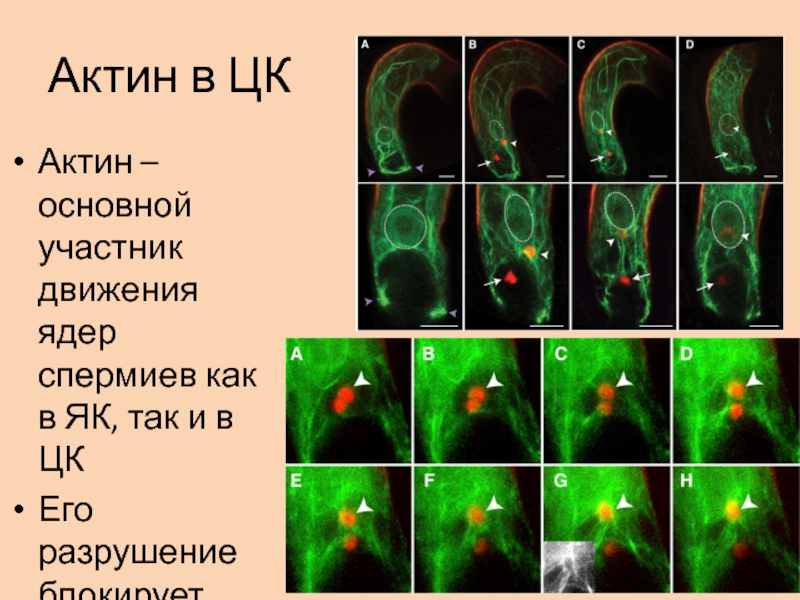
Слайд 51Актин в ЦК
Актин – основной участник движения ядер спермиев как
в ЯК, так и в ЦК
Его разрушение блокирует кариогамию
Слайд 52Детали
Ядро спермия, войдя в цитоплазму ЦК, окружалось волокнами F-актина с
образованием звездообразной структуры.
Вся эта структура вместе с ядром спермия
мигрировала по направлению к ядру ЦК. Актиновая сеть в центральной клетке постоянно движется внутрь – от периферии клетки к ее ядру.
Этот процесс, по-видимому, играет важную роль в перемещении ядра спермия.
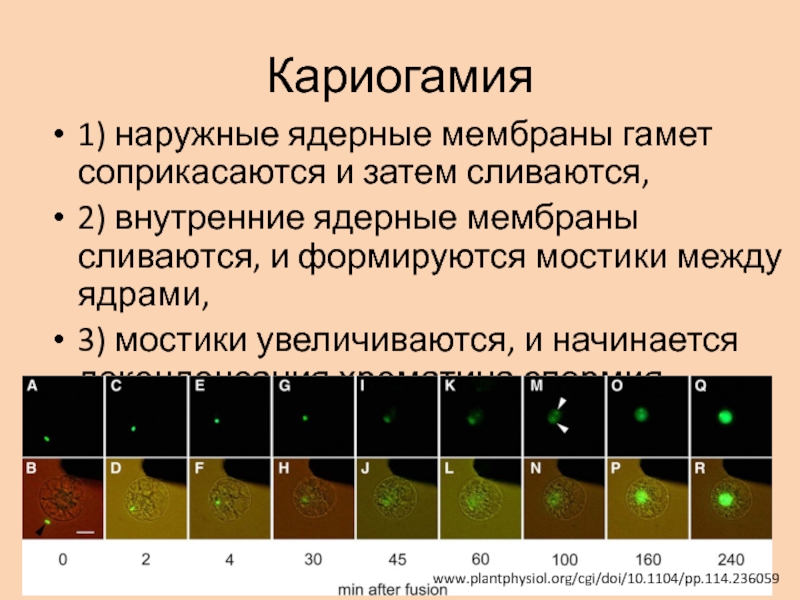
Слайд 53Кариогамия
1) наружные ядерные мембраны гамет соприкасаются и затем сливаются,
2)
внутренние ядерные мембраны сливаются, и формируются мостики между ядрами,
3)
мостики увеличиваются, и начинается деконденсация хроматина спермия.www.plantphysiol.org/cgi/doi/10.1104/pp.114.236059
Слайд 54В системе in vitro у риса путь ядра спермия до
ядра яйцеклетки занимал 5-10 мин, причем, как и у Arabidopsis,
транспортировку ядра спермия осуществлял актиновый цитоскелет.Затем начинался процесс кариогамии, и хроматин яйцеклетки переходил в ядро спермия, увеличиваяего объем.
В интервале 30-70 мин после плазмогамии хроматин спермия деконденсировался, и кариогамия завершалась.
Слайд 56Два типа СН
Гаметофитная СН: фенотип пыльцы определяется гаплоидным геномом (гаметофитным)
Спорофитная
СН: фенотип пыльцы определяется геномом родителя (спорофита)
Гаметофитная СН шире распространена
(60-90 семейств)Слайд 57Гаметофитная СН. S-RNAse
Рост пыльцы подавляется только тогда, когда она вошла
в проводниковый тракт столбика.
Что же такое S-ген пестика?
Он кодирует
рибонуклеазуА на рыльце казалось, что всё у нас получится…
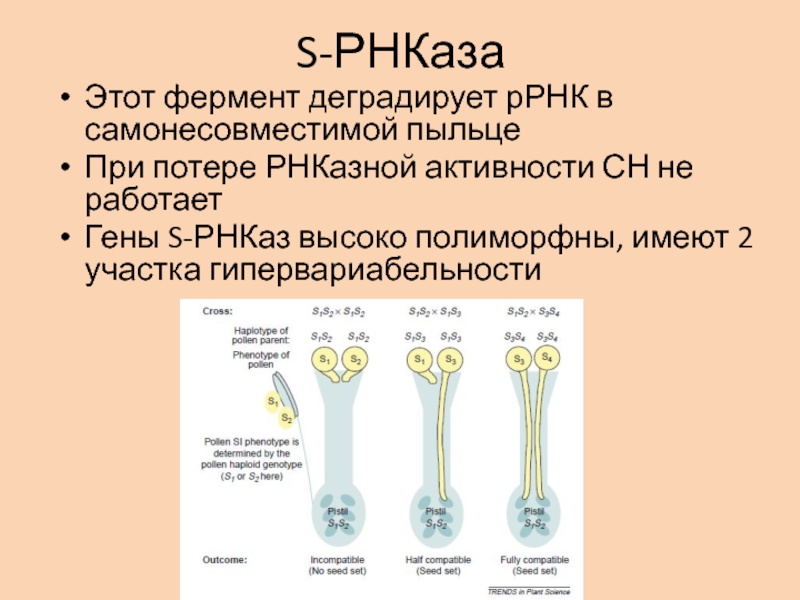
Слайд 58S-РНКаза
Этот фермент деградирует рРНК в самонесовместимой пыльце
При потере РНКазной активности
СН не работает
Гены S-РНКаз высоко полиморфны, имеют 2 участка гипервариабельности
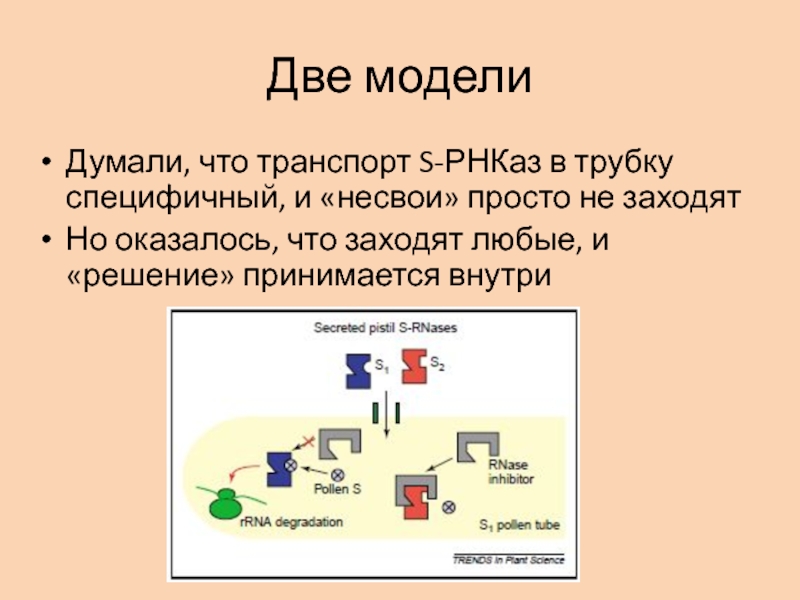
Слайд 59Две модели
Думали, что транспорт S-РНКаз в трубку специфичный, и «несвои»
просто не заходят
Но оказалось, что заходят любые, и «решение» принимается
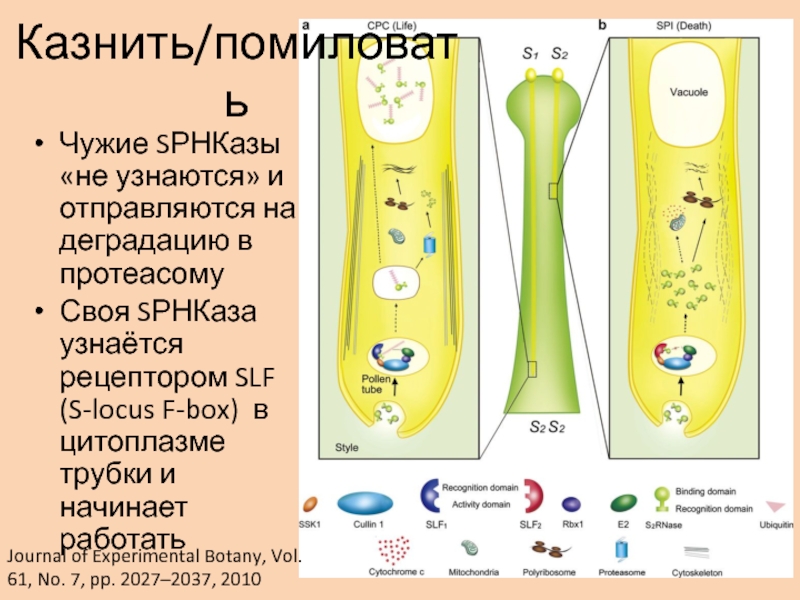
внутриСлайд 60Чужие SРНКазы «не узнаются» и отправляются на деградацию в протеасому
Своя
SРНКаза узнаётся рецептором SLF (S-locus F-box) в цитоплазме трубки и
начинает работатьКазнить/помиловать
Journal of Experimental Botany, Vol. 61, No. 7, pp. 2027–2037, 2010
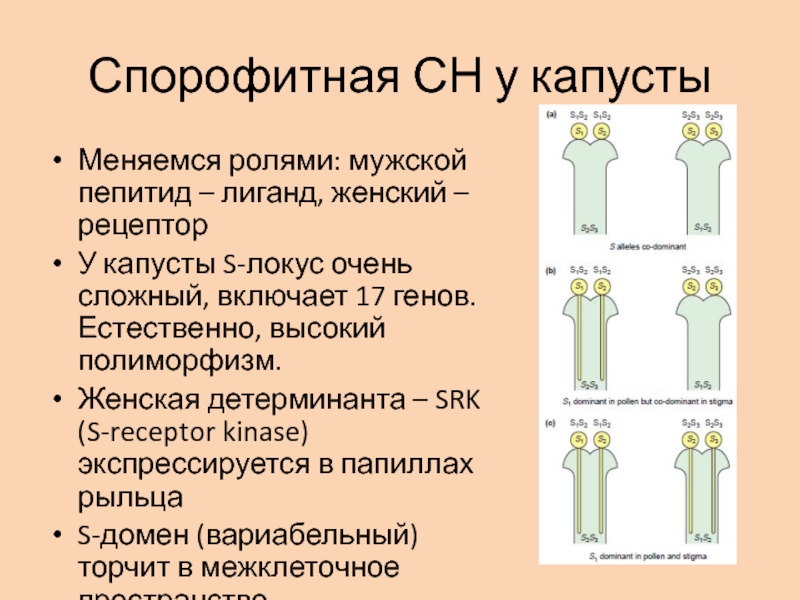
Слайд 61Спорофитная СН у капусты
Меняемся ролями: мужской пепитид – лиганд, женский
– рецептор
У капусты S-локус очень сложный, включает 17 генов. Естественно,
высокий полиморфизм.Женская детерминанта – SRK (S-receptor kinase) экспрессируется в папиллах рыльца
S-домен (вариабельный) торчит в межклеточное пространство
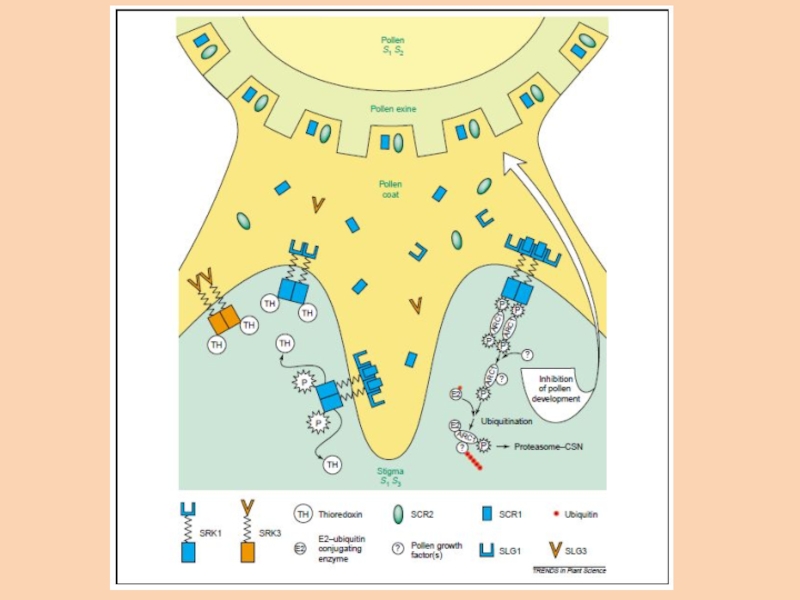
Слайд 62Мужская детерминанта – SCR/SPP (S-locus cystein-rich protein, S-locus pollen protein)
Полиморфизм
мужской детерминанты выше
Она экспрессируется в тапетуме и встраивается в трифину
(pollen coat)Также в S-локусе присутствует SLG (S-locus glycoprotein) – секретируемый гликопротеин рыльца.
Он помогает, но не является обязательным.
Возможно, стабилизирует/активирует накопление киназы
Слайд 64ARC1 взаимодействует с киназным доменом SRK и может провоцировать убиквитинирование
белков рыльца
Очевидно, при СН ответе уничтожаются белки рыльца, которые должны
провоцировать/поддерживать рост трубкиСН и совместимые зерна могут лежать совсем рядом
Разница между ними будет заметна уже через 10-20 минут