Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Чем определяется способность полимеров к химическим превращениям ?
Содержание
- 1. Чем определяется способность полимеров к химическим превращениям ?
- 2. Практическая важность химических реакций полимероввозможностью синтеза одного
- 3. Основные типы реакций в химических превращениях полимеровреакции
- 4. Слайд 4
- 5. Слайд 5
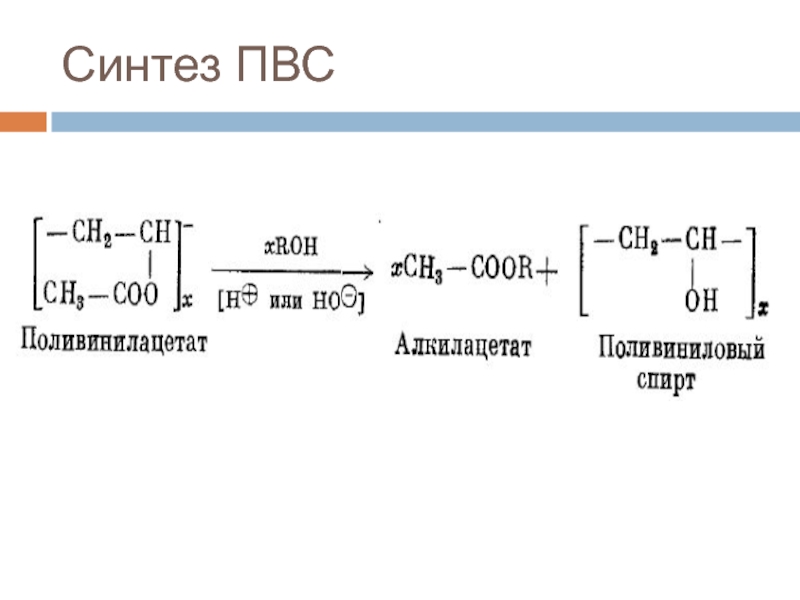
- 6. Синтез ПВС
- 7. ПоливинилбутиральПоливинилбутираль - продукт ацеталирования поливинилового спирта масляным
- 8. Получение пористого поливинилформаляАцеталирование ПВС протекает в одну
- 9. Слайд 9
- 10. Чем обусловлено неполное превращение в макромолекулярных реакциях?может
- 11. Слайд 11
- 12. - меньшая доступность функциональных групп в высокомолекулярных
- 13. Термоокислительная (антиоксиданты)Озонная (антиозонанты)Механическая (противоутомители) Фотохомическая (светостабилизаторы)Радиационная (антирады)Химическая деструкция (гидролиз, ацидолиз, алкоголиз, аминолиз)БиодеструкцияВиды деструкции
- 14. Эти нежелательные явления могут быть устранены путем:
- 15. Реакции ингибированного окисленияInH – молекула ингибитора
- 16. Ароматические амины и пространственно-затрудненные фенолы – важнейшие стабилизаторы I типаЛовушки пероксидных радикаловЛовушки алкильных радикалов
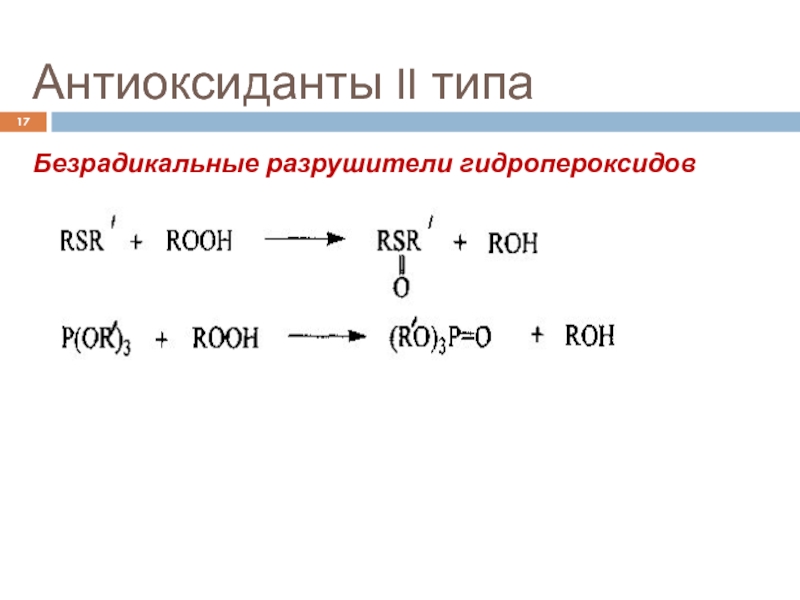
- 17. Антиоксиданты II типаБезрадикальные разрушители гидропероксидов
- 18. Полифункциональные стабилизаторы пространственно-затрудненные амины (HALS)сульфиды пространственно-затрудненных фенолов
- 19. Ухудшение механических свойствРис. 1. Зависимость разрывной прочности
- 20. Термоокислительной деструкцией называют разрушение макромолекул при одновременном
- 21. Кинетика окисленияРис. 2. Кинетические кривые поглощения кислорода в процессе окисления нестабилизированного (1) и стабилизированного (2) полимеров
- 22. Стадии процесса окисления1) Инициирование кинетических цепей2) Продолжение
- 23. Инициирование кинетических цепей Процесс зарождения кинетических
- 24. Продолжение цепи Эта стадия включает в
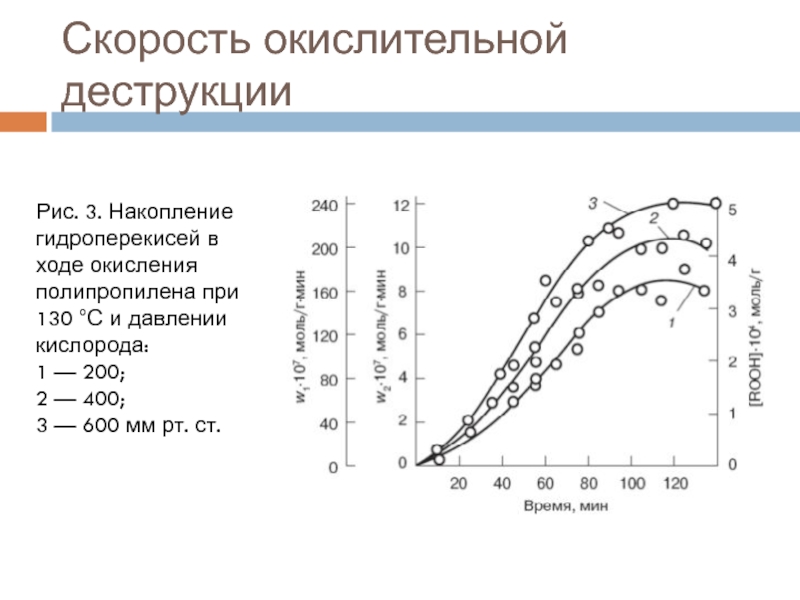
- 25. Скорость окислительной деструкцииРис. 3. Накопление гидроперекисей в
- 26. Разветвление кинетической цепиROOH → RO∙ + ∙OH
- 27. Обрыв кинетической цепиУравнения скорости поглощения кислорода полимеров:- для квадратичного обрыва цепи- для линейного обрыва цепи
- 28. Принципы стабилизации полимеровВ процессе переработки в готовые
- 29. Термостабилизаторы1) Акцепотры низкомолекулярных продуктов деструкции (HCl, H2O,
- 30. АнтиоксидантыСхема 1. Основные реакции окисления полимера, показанные
- 31. Ароматические ингибиторыВ качестве ингибиторов можно использовать:Фенолы, нафтолы,
- 32. Примеры ароматических ингибиторовИрганокс-1010 - эфир 3,5-ди-третбутил-4-гидроксифенилпропионовой кислоты и пентаэритритаИрганокс-1076 - 2,6-ди-трет-бутил-4-октадецилпропионил-фенол
- 33. Стабилизаторы, разрушающие инициаторы
- 34. Примеры стабилизаторов, разрушающих инициаторыБис-(2-окси-5-метил-3-третбутилфенил)-сульфид Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид
- 35. Эффективность стабилизаторов в полимерах зависит от ряда
- 36. Формулы расхода антиоксиданта и концентрации активных центров
- 37. Критическая концентрация антиоксидантаЕсли фактор автокатализа больше kx,
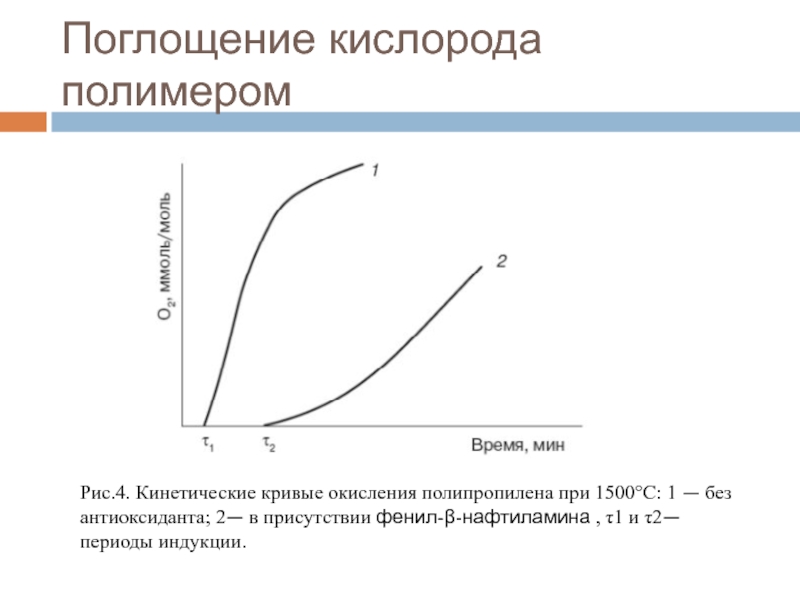
- 38. Поглощение кислорода полимеромРис.4. Кинетические кривые окисления полипропилена
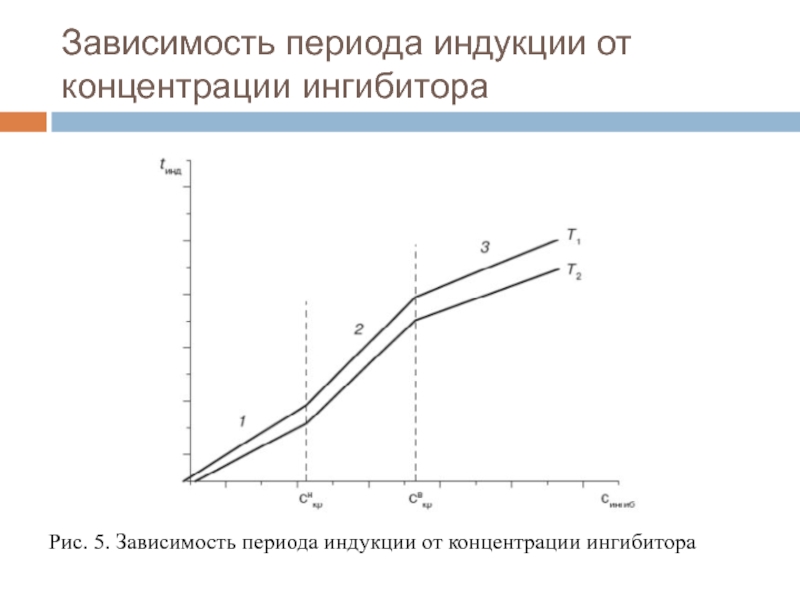
- 39. Зависимость периода индукции от концентрации ингибитораРис. 5. Зависимость периода индукции от концентрации ингибитора
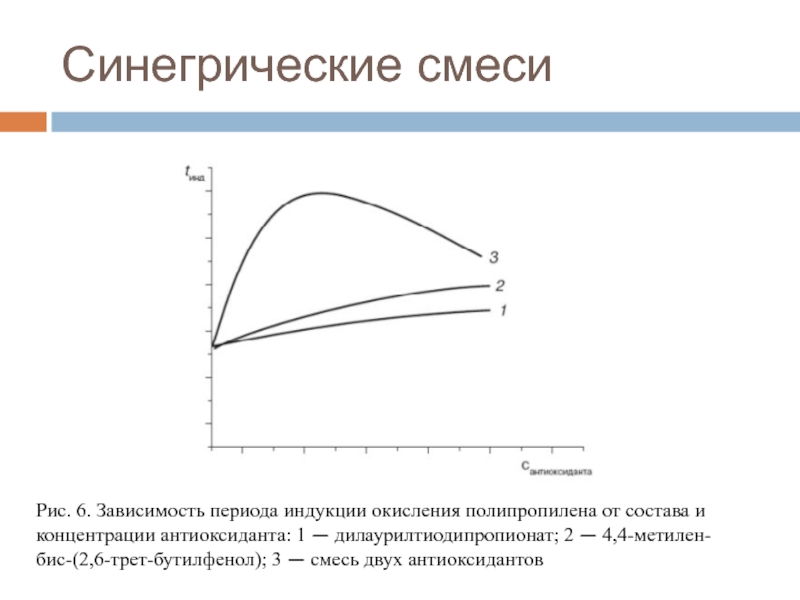
- 40. Синегрические смесиРис. 6. Зависимость периода индукции окисления
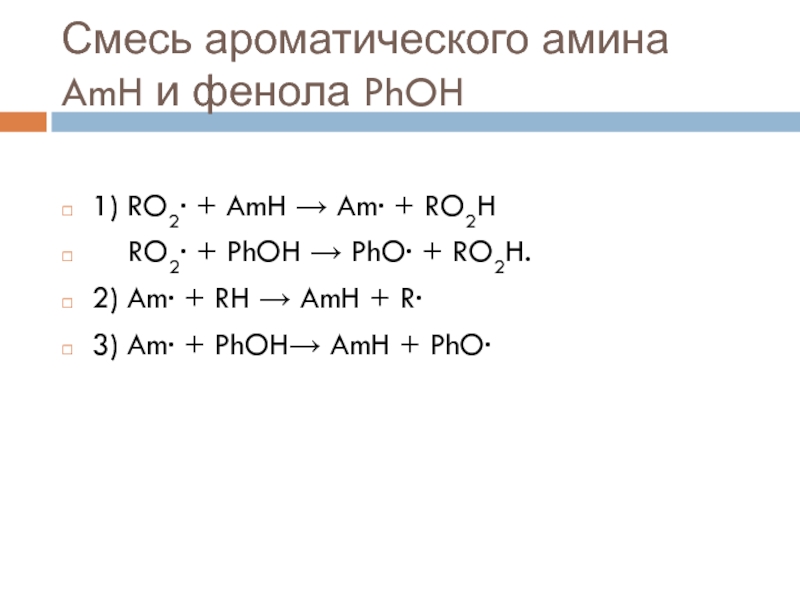
- 41. Смесь ароматического амина AmH и фенола PhOH1)
- 42. Скачать презентанцию
Практическая важность химических реакций полимероввозможностью синтеза одного полимера из другого, возможностью химической модификации полимеров введением в их состав различных атомов или групп возможностью осуществления химических превращений в процессе переработки полимеров в
Слайды и текст этой презентации
Слайд 1Чем определяется способность полимеров к химическим превращениям?
Природой связей, образующих основную
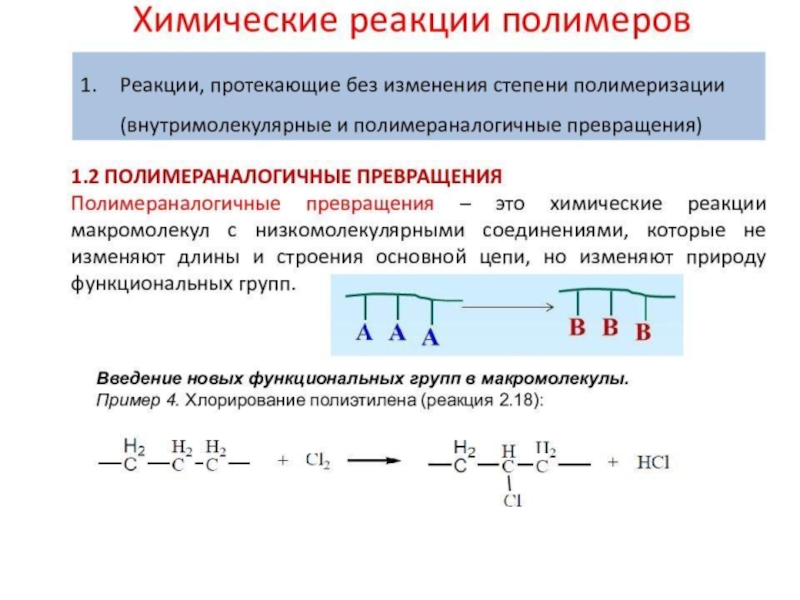
Слайд 2Практическая важность химических реакций полимеров
возможностью синтеза одного полимера из другого,
возможностью химической модификации полимеров введением в их состав различных атомов
или групп возможностью осуществления химических превращений в процессе переработки полимеров в изделия;возможностью выявления возможных условий использования полимеров и материалов на их основе,
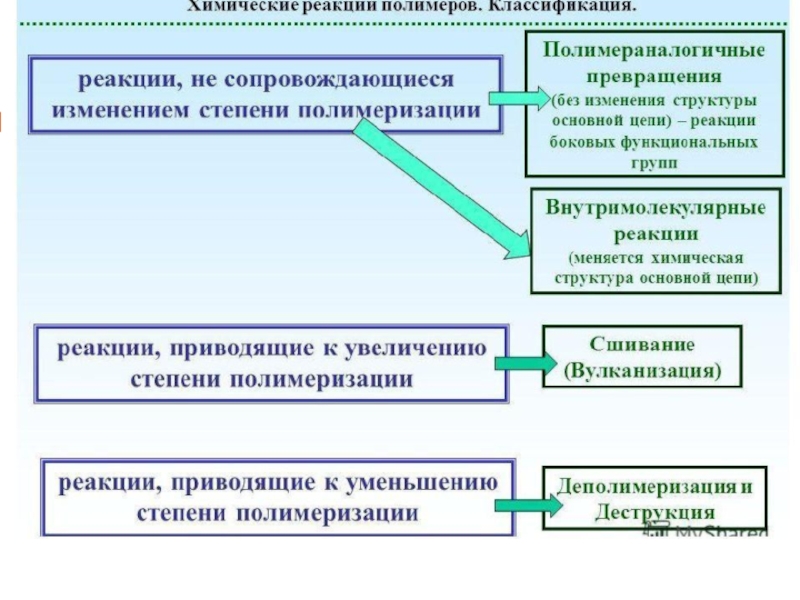
Слайд 3Основные типы реакций в химических превращениях полимеров
реакции в боковых или
основных цепях макромолекул, не приводящие к изменению их длины (это
полимераналогичные превращения),реакции деструкции, сопровождающиеся разрывом макромолекул под действием различных факторов
реакции с образованием разветвлённых или пространственных структур трехмерных полимеров)
Слайд 7Поливинилбутираль
Поливинилбутираль - продукт ацеталирования поливинилового спирта масляным альдегидом:
Характеризуется высокой адгезией
к различным поверхностям, отличными оптическими и пленкообразующими свойствами, хорошими физико-механическими
свойствами (эластичность, ударная прочность и износостойкость), морозо- и светостойкостью, устойчив к воздействию O2 и О3. Не растворим в воде, но хорошо растворяется в органических растворителях (эфиры, спирты, кетоны, бензол и др.).Поливинилбутираль широко применяется в производстве лаков, грунтовок, эмалей, мастик.
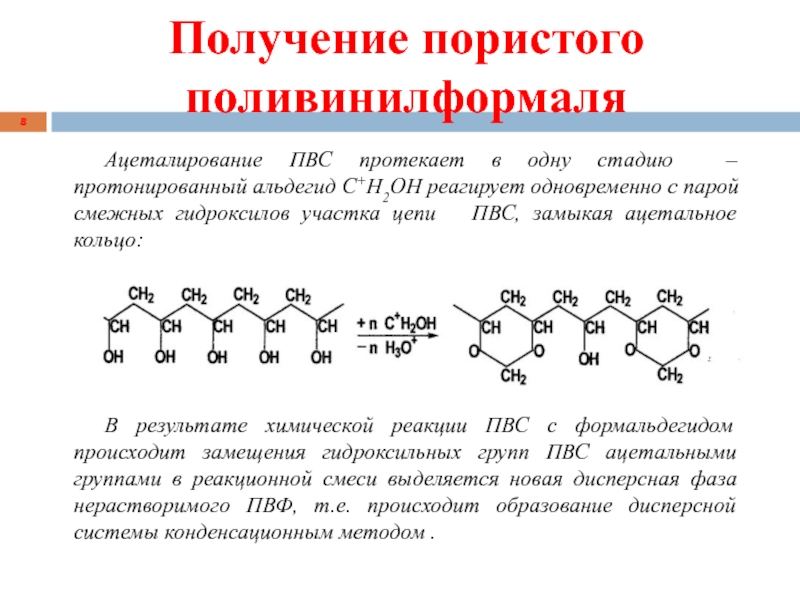
Слайд 8Получение пористого поливинилформаля
Ацеталирование ПВС протекает в одну стадию – протонированный
альдегид C+H2OH реагирует одновременно с парой смежных гидроксилов участка цепи
ПВС, замыкая ацетальное кольцо:В результате химической реакции ПВС с формальдегидом происходит замещения гидроксильных групп ПВС ацетальными группами в реакционной смеси выделяется новая дисперсная фаза нерастворимого ПВФ, т.е. происходит образование дисперсной системы конденсационным методом .
Слайд 10Чем обусловлено неполное превращение в макромолекулярных реакциях?
может быть следствием стерических
затруднений, а в некоторых случаях (когда в реакции участвуют две
соседние группы) обусловливается и статистическими причинами: образованием изолированных функциональных группСлайд 11
Почему скорость процесса и степень превращения ниже для реакций высокомолекулярных
соединений по сравнению со своими низкомолекулярными аналогами?
Слайд 12- меньшая доступность функциональных групп в высокомолекулярных соединениях,
- влияние
соседних групп,
- конфигурационный и конформационный эффекты,
- электростатический эффект,
-
надмолекулярный или морфологический эффект, - эффект негомогенной активности,
- влияние длины цепей и концентрации.
Слайд 13Термоокислительная (антиоксиданты)
Озонная (антиозонанты)
Механическая (противоутомители)
Фотохомическая (светостабилизаторы)
Радиационная (антирады)
Химическая деструкция (гидролиз, ацидолиз,
алкоголиз, аминолиз)
Биодеструкция
Виды деструкции
Слайд 14Эти нежелательные явления могут быть устранены путем:
наиболее рационального выбора
состава пластмассы,
удаления вредных примесей,
регулирования свойств полимеров на стадии
изготовления изделий в результате отжига или ориентации, пластификации или с помощью модифицирующих добавок, введения стабилизаторов.
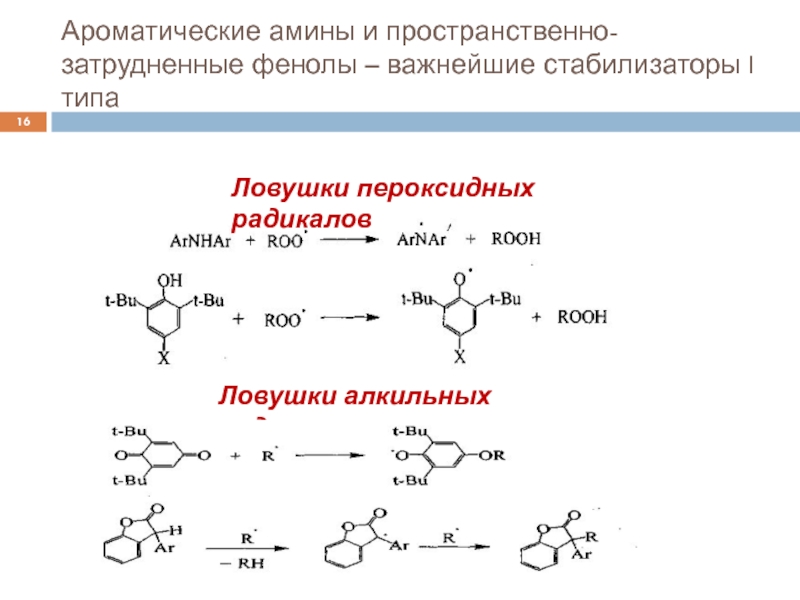
Слайд 16Ароматические амины и пространственно-затрудненные фенолы – важнейшие стабилизаторы I типа
Ловушки
пероксидных радикалов
Ловушки алкильных радикалов
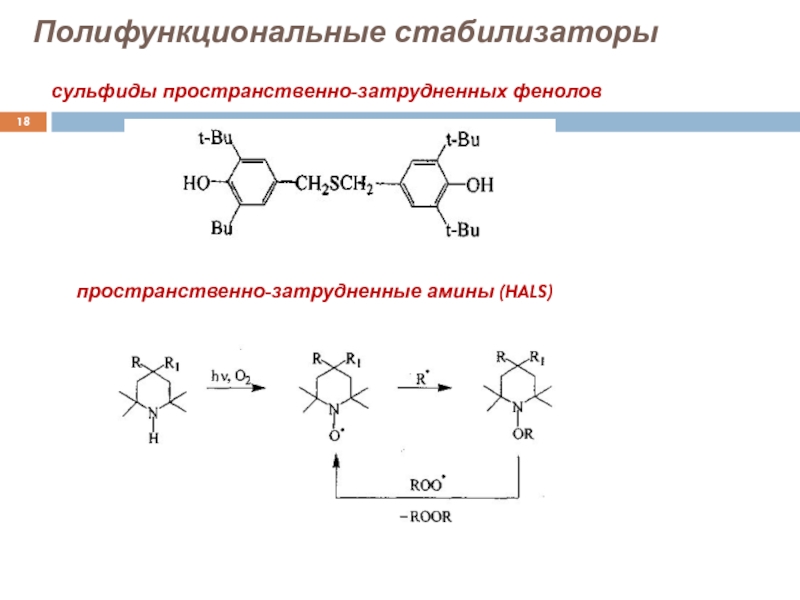
Слайд 18Полифункциональные стабилизаторы
пространственно-затрудненные амины (HALS)
сульфиды пространственно-затрудненных фенолов
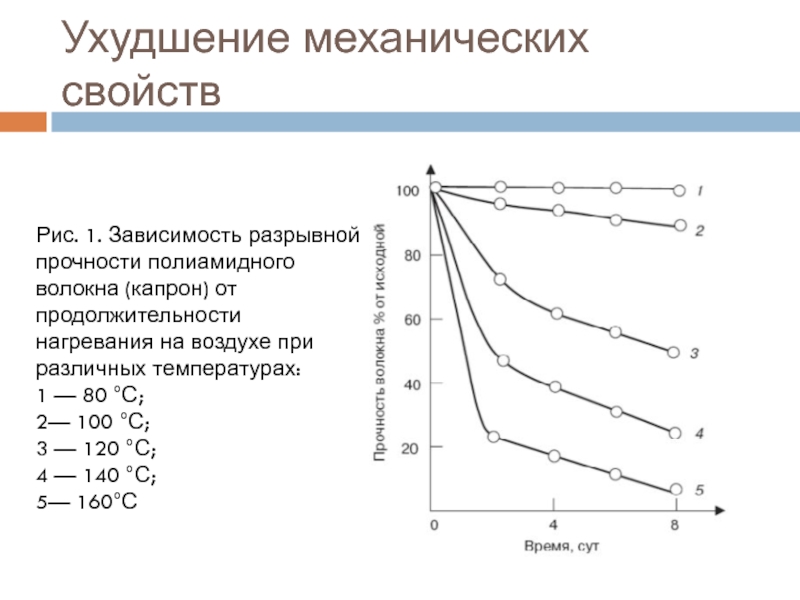
Слайд 19Ухудшение механических свойств
Рис. 1. Зависимость разрывной прочности полиамидного волокна (капрон)
от продолжительности нагревания на воздухе при различных температурах:
1 —
80 °С; 2— 100 °С;
3 — 120 °С;
4 — 140 °С;
5— 160°С
Слайд 20
Термоокислительной деструкцией называют разрушение макромолекул при одновременном воздействии тепла и
кислорода.
Условия, при которых возможно окисление:
1) Во время
переработки (расплав полимера)2) Во время эксплуатации (готовое изделие)
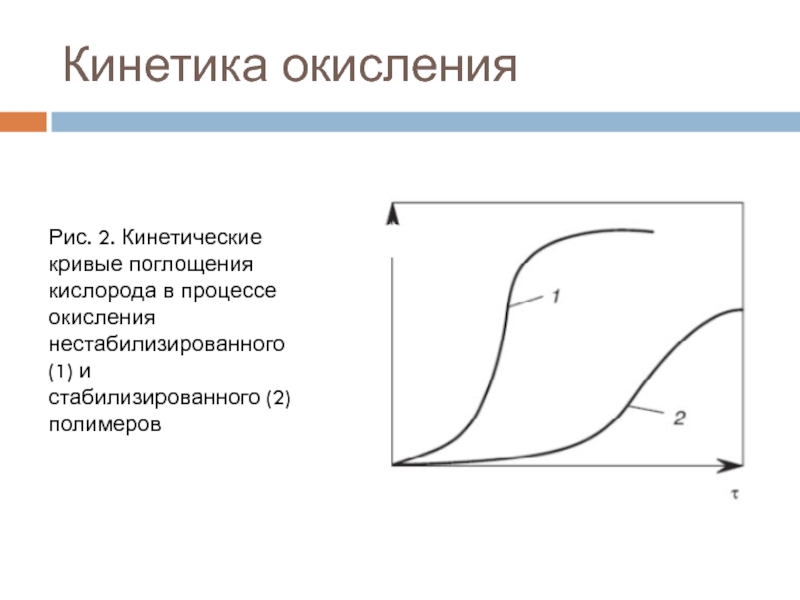
Слайд 21Кинетика окисления
Рис. 2. Кинетические кривые поглощения кислорода в процессе окисления
нестабилизированного (1) и стабилизированного (2) полимеров
Слайд 22Стадии процесса окисления
1) Инициирование кинетических цепей
2) Продолжение кинетической цепи
3)
Разветвление кинетической цепи
4) Обрыв кинетической цепи
Слайд 23Инициирование кинетических цепей
Процесс зарождения кинетических цепей происходит но
следующей схеме:
RH + O2 → R∙ + НO2∙
Радикал
НO2∙ может реагировать с другой макромолекулой, образуя алкильный радикал:НO2∙ + RH → R∙ + Н2O2
или рекомбинировать с R∙ -радикалом по реакции:
R∙ + НО2∙ → неактивные продукты
Слайд 24Продолжение цепи
Эта стадия включает в себя чередующиеся реакции:
1) R∙ + O2 → RO2∙
2) RO2∙ + RH →
ROOH + R∙ (возможна внутримолекулярная или межмолекулярная передача цепи)Слайд 25Скорость окислительной деструкции
Рис. 3. Накопление гидроперекисей в ходе окисления полипропилена
при 130 °С и давлении кислорода:
1 — 200;
2
— 400; 3 — 600 мм рт. ст.
Слайд 26Разветвление кинетической цепи
ROOH → RO∙ + ∙OH (I)
ROOH + RH
→ RO∙ + H2O + R∙ (II)
ROOH + ROOH →
RO∙ + H2O + RO2∙ (III)Слайд 27Обрыв кинетической цепи
Уравнения скорости поглощения кислорода полимеров:
- для квадратичного обрыва
цепи
- для линейного обрыва цепи
Слайд 28Принципы стабилизации полимеров
В процессе переработки в готовые изделия полимеры подвергаются
воздействию высоких температур и значительных сдвиговых усилий. Удалить кислород на
стадии переработки полностью практически невозможно или слишком дорого, поэтому на стадии переработки почти всегда протекает термоокислительная деструкция, оказывающая большое влияние на свойства полимера.При старении полимеров протекают одновременно два процесса: структурирование и деструкция. При переработке, сопровождающейся деструкцией, показатель текучести расплава полипропилена возрастает, а полиэтилена — уменьшается, что обусловлено образованием сшивок. Увеличение концентрации кислорода приводит к тому, что во всех полимерах основной становится реакция разрыва цепи. Концентрация гидропероксида возрастает с увеличением времени переработки.
Слайд 29Термостабилизаторы
1) Акцепотры низкомолекулярных продуктов деструкции (HCl, H2O, CH2O и др.)
2)
Акцепторы свободных радикалов
а) Увеличение скорости обрыва кинетических цепей
б) Уменьшение скоростей
зарождения и разветвления цепей3) Антиоксиданты
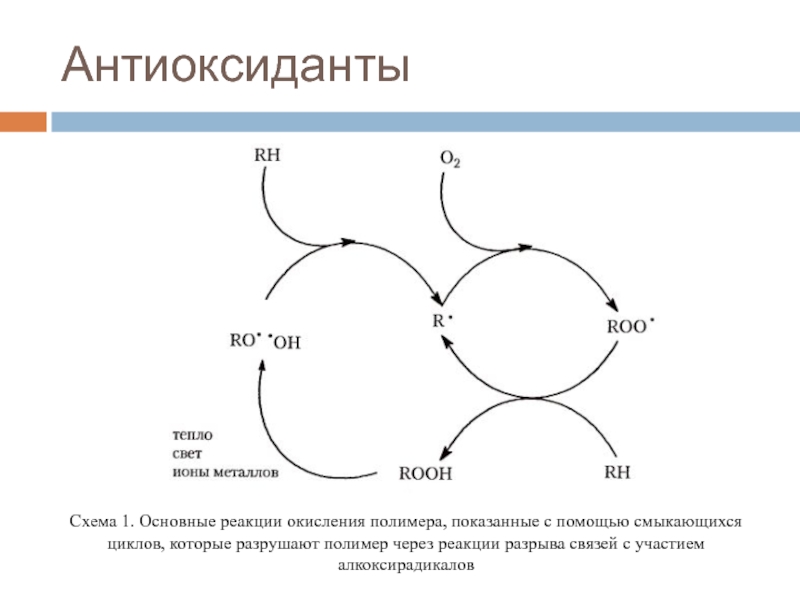
Слайд 30Антиоксиданты
Схема 1. Основные реакции окисления полимера, показанные с помощью смыкающихся
циклов, которые разрушают полимер через реакции разрыва связей с участием
алкоксирадикаловСлайд 31Ароматические ингибиторы
В качестве ингибиторов можно использовать:
Фенолы, нафтолы, ароматические амины, аминофенолы,
диамины
ROO∙ + InH → ROOH + In∙
Принцип действия:
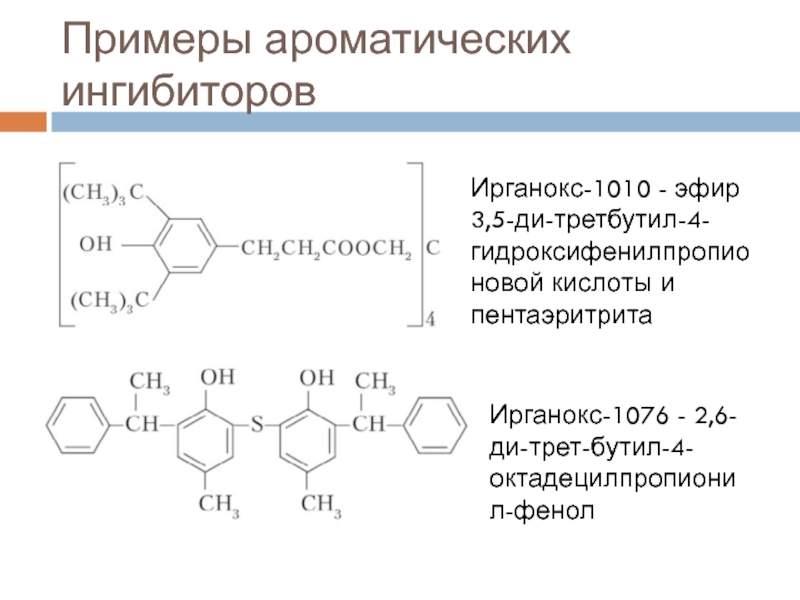
Слайд 32Примеры ароматических ингибиторов
Ирганокс-1010 - эфир 3,5-ди-третбутил-4-гидроксифенилпропионовой кислоты и пентаэритрита
Ирганокс-1076 -
2,6-ди-трет-бутил-4-октадецилпропионил-фенол
Слайд 34Примеры стабилизаторов, разрушающих инициаторы
Бис-(2-окси-5-метил-3-третбутилфенил)-сульфид
Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид
Слайд 35Эффективность стабилизаторов в полимерах зависит от ряда факторов, таких, как
влияние полимера на реакционную способность стабилизатора, совместимость стабилизатора с полимером,
химическая и физическая стойкость стабилизатора при воздействии высокой температуры в процессе переработки полимера, диффузия стабилизатора и т. п.Слайд 36Формулы расхода антиоксиданта и концентрации активных центров n
- концентрация активных
центров n
- расход антиоксиданта
где υu — скорость инициирования; φ —
фактор автокатализа; x — концентрация антиоксиданта; k — константа скорости реакции антиоксиданта с активными центрами в процессе окисления.Слайд 37Критическая концентрация антиоксиданта
Если фактор автокатализа больше kx, окисление ускоряется; если
меньше окисление протекает с постоянной малой скоростью. Значение концентрации антиоксиданта,
при которомφ-kx = 0, называют критической концентрацией (x'кр), т.е. x = φ/k.
Слайд 38Поглощение кислорода полимером
Рис.4. Кинетические кривые окисления полипропилена при 1500°С: 1
— без антиоксиданта; 2— в присутствии фенил-β-нафтиламина , τ1 и
τ2— периоды индукции.Слайд 39Зависимость периода индукции от концентрации ингибитора
Рис. 5. Зависимость периода индукции
от концентрации ингибитора
Слайд 40Синегрические смеси
Рис. 6. Зависимость периода индукции окисления полипропилена от состава
и концентрации антиоксиданта: 1 — дилаурилтиодипропионат; 2 — 4,4-метилен-бис-(2,6-трет-бутилфенол); 3
— смесь двух антиоксидантовСлайд 41Смесь ароматического амина AmH и фенола PhOH
1) RO2∙ + AmH
→ Am∙ + RO2H
RO2∙ + PhOH → PhO∙
+ RO2H.2) Am∙ + RH → AmH + R∙
3) Am∙ + PhOH→ AmH + PhO∙




















![Чем определяется способность полимеров к химическим превращениям ? Примеры стабилизаторов, разрушающих инициаторыБис-(2-окси-5-метил-3-третбутилфенил)-сульфид Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид Примеры стабилизаторов, разрушающих инициаторыБис-(2-окси-5-метил-3-третбутилфенил)-сульфид Бис-[2-окси-5-метил-3-α-метнлбензил)-фенил]-сульфид](/img/thumbs/6f079493a128790ad4989bc4dd1697bd-800x.jpg)