Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Энергообмен 2
Содержание
- 1. Энергообмен 2
- 2. Энергетический обменПЛАН ЛЕКЦИИ1. Тканевое дыхание. Регуляция, дыхательный контроль.2. Окислительное фосфорилирование3. Хемиоосмотическая теория сопряжения
- 3. 4-й ЭТАП КАТАБОЛИЗМА – ТКАНЕВОЕ ДЫХАНИЕЦепь переноса
- 4. ТКАНЕВОЕ ДЫХАНИЕ
- 5. МИТОХОНДРИЯ
- 6. Тканевое дыханиеТолько первый переносчик протонов и электронов
- 7. Тканевое дыхание Направленность потока электронов определяется величиной
- 8. ОВПВещества с положительным ОВП окисляют водород (отнимают
- 9. Дыхательная цепь (ЦПЭ) СИСТЕМА
- 10. Дыхательная цепь (ЦПЭ)Совокупность последовательных окислительно-восстановительных реакций называется цепью переноса (транспорта) электронов, или дыхательной цепью
- 11. Промежуточные переносчики коферменты: NAD+, FAD и FMN,
- 12. КОМПЛЕКСЫ ДЫХАТЕЛЬНОЙ ЦЕПИI комплекс – НАДН2: КоQ-оксидоредуктазаперенос
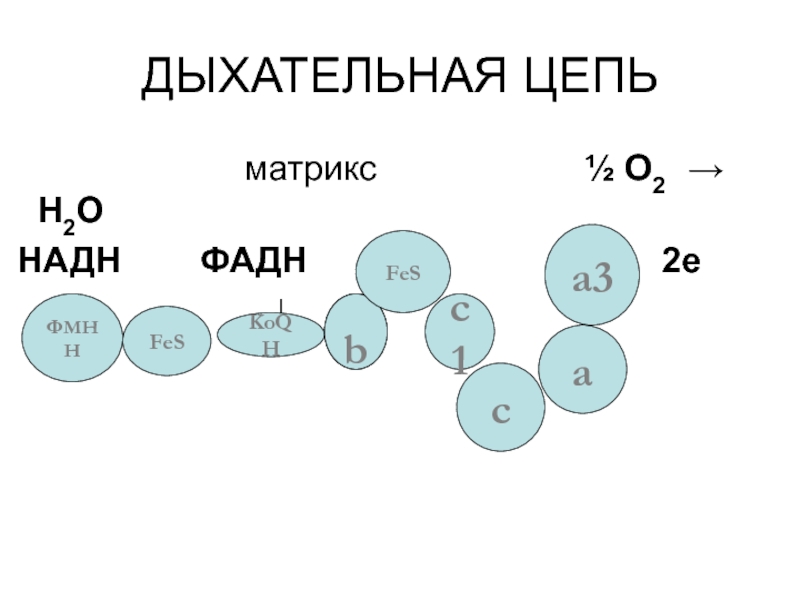
- 13. ДЫХАТЕЛЬНАЯ ЦЕПЬ
- 14. КОМПЛЕКС IКомплекс содержит 26 белков и небелковые
- 15. Комплекс IМитохондриальная протонтранслоцирующая NADH: КоQ-оксидоредуктазакатализируют окисление NADH
- 16. КОМПЛЕКС II Сукцинат: КоQ-оксидоредуктазаВ составе комплекса
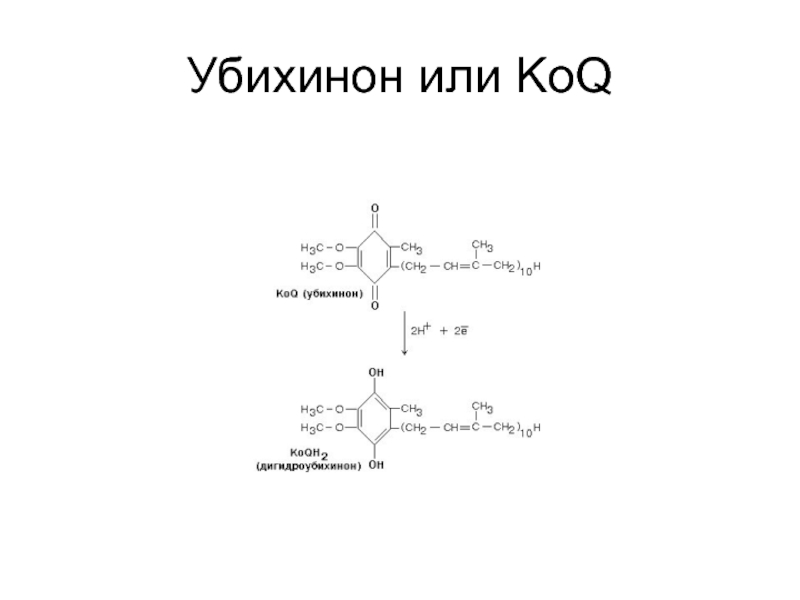
- 17. Убихинон или KoQ
- 18. КОМПЛЕКС III КоQН2: цитохром с-оксидоредуктаза1) Цитохромы b:
- 19. Комплекс III является протонным генератором, целью его работы является создание ΔμΗ+ Вторая точка сопряжения
- 20. КОМПЛЕКС IVКомплекс IV - ЦИТОХРОМОКСИДАЗА (цитохромы а
- 21. Межмембранное пространствоМатрикс
- 22. КОЭФФИЦИЕНТ P/OДля оценки эффективности работы ЦПЭ вычисляют
- 23. Дыхательный контроль Скорость дыхания митохондрий может контролироваться
- 24. ХЕМИОСМОТИЧЕСКАЯ ТЕОРИЯРазработана Митчеллом (1961-1966гг)Дыхание и фосфорилирование связаны
- 25. ХЕМИОСМОТИЧЕСКАЯ ТЕОРИЯВнутренняя мембрана митохондрий заряжается: снаружи +,
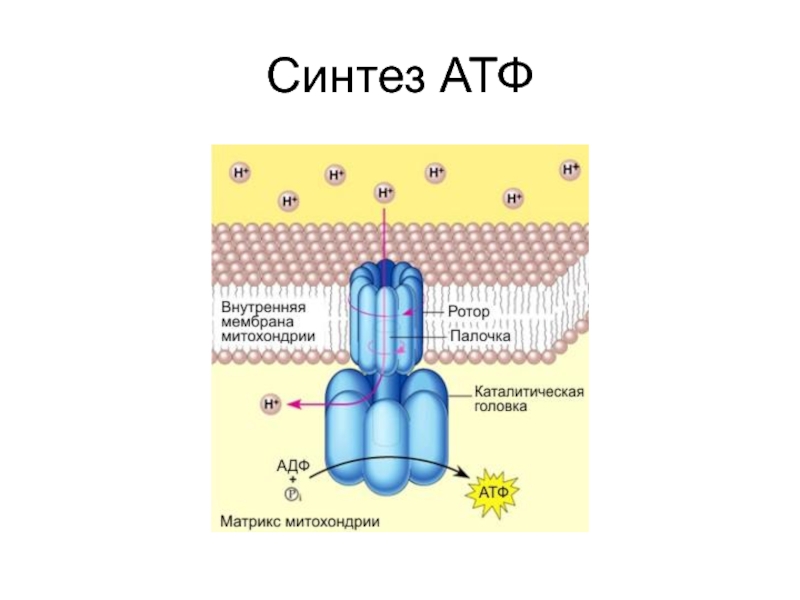
- 26. Синтез АТФ
- 27. АДФ + Ф + ЭНЕРГИЯ -------> АТФ
- 28. ЭНЕРГИЯ АТФ ИСПОЛЬЗУЕТСЯ 1. Синтез различных веществ.2. Активный транспорт 3. Механическое движение (мышечная работа).
- 29. ТЕОРИЯ СОПРЯЖЕНИЯ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ1. Транспорт
- 30. ВЕЩЕСТВА-РАЗОБЩИТЕЛИ ПРОЦЕССОВ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯСостояние, когда происходит
- 31. СПЕЦИФИЧЕСКИЕ ИНГИБИТОРЫ ТКАНЕВОГО ДЫХАНИЯ К ним относятся вещества,
- 32. Скачать презентанцию
Энергетический обменПЛАН ЛЕКЦИИ1. Тканевое дыхание. Регуляция, дыхательный контроль.2. Окислительное фосфорилирование3. Хемиоосмотическая теория сопряжения
Слайды и текст этой презентации
Слайд 2Энергетический обмен
ПЛАН ЛЕКЦИИ
1. Тканевое дыхание. Регуляция, дыхательный контроль.
2. Окислительное фосфорилирование
3.
Хемиоосмотическая теория сопряжения
Слайд 34-й ЭТАП КАТАБОЛИЗМА – ТКАНЕВОЕ ДЫХАНИЕ
Цепь переноса (транспорта) электронов –
ДЫХАТЕЛЬНАЯ ЦЕПЬ
ТКАНЕВОЕ ДЫХАНИЕ – перенос электронов от донора (НАДН) к
терминальному акцептору – кислородуДыхательная цепь локализована во внутренней мембране митохондрий
Слайд 4ТКАНЕВОЕ ДЫХАНИЕ
ДЫХАТЕЛЬНАЯ ЦЕПЬ
- мультиферментная система, транспортирующая протоны и электроны на кислород с
образованием воды.Все ферменты митохондриального окисления встроены во внутреннюю мембрану митохондрий.
Слайд 6Тканевое дыхание
Только первый переносчик протонов и электронов – НАД -зависимая
дегидрогеназа расположена в матриксе митохондрии.
Этот фермент отнимает водород
от субстрата и передает его следующему переносчику. Слайд 7Тканевое дыхание
Направленность потока электронов определяется величиной
РЕДОКС-ПОТЕНЦИАЛА
(ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ПОТЕНЦИАЛА, сокращенно - ОВП) каждого звена дыхательной цепи
Слайд 8ОВП
Вещества с положительным ОВП окисляют водород (отнимают от него электроны),
вещества с отрицательным ОВП окисляются водородом.
Самый низкий ОВП имеет
начальное звено цепи, самый высокий - у кислорода, расположенного в конце цепочки переносчиковПеренос электронов и протонов осуществляется с участием промежуточных переносчиков
Слайд 9Дыхательная цепь (ЦПЭ)
СИСТЕМА ОВП
НАД/НАДН -0.32
в
ФМН/ФМН -0.12 в
ФАД/ФАДН -0.05 в
КоQ/KoQH 0.0 в
Цитохром
b +0.07 вЦитохром c1 +0.22 в
Цитохром с +0.26 в
Цитохром a +0.29 в
Цитохром a3 +0.55 в
½ О2/Н2О + 0.82 в
Слайд 10Дыхательная цепь (ЦПЭ)
Совокупность последовательных окислительно-восстановительных реакций называется цепью переноса (транспорта)
электронов, или дыхательной цепью
Слайд 11Промежуточные переносчики
коферменты: NAD+, FAD и FMN,
кофермент Q (КoQ),
цитохромы ( b, С1, С, А, А3)
белки, содержащие
негеминовое железо. Слайд 12КОМПЛЕКСЫ ДЫХАТЕЛЬНОЙ ЦЕПИ
I комплекс – НАДН2: КоQ-оксидоредуктаза
перенос электронов от НАДН2
к КоQ
II комплекс – Сукцинат: КоQ-оксидоредуктаза
перенос электронов от сукцината к
КоQIII комплекс – КоQН2: цитохром с-оксидоредуктаза
перенос электронов от КоQН2 к цитохрому с
IV комплекс - цитохромоксидаза
Перенос электоронов от цитохрома с к кислороду
Слайд 14КОМПЛЕКС I
Комплекс содержит 26 белков и небелковые компоненты: (ФМН), 5
железо-серных центров: FeS1a, FeS1b FeS2, FeS3, FeS4.
Слайд 15Комплекс I
Митохондриальная протонтранслоцирующая NADH: КоQ-оксидоредуктаза
катализируют окисление NADH убихиноном
Реакция сопровождается
трансмембранным переносом четырех протонов при окислении одной молекулы NADH (2
электрона) и генерацией на сопрягающей мембране митохондрий разности электрохимического потенциала ионов водорода (∆µH+)Первая точка сопряжения
Слайд 16КОМПЛЕКС II
Сукцинат: КоQ-оксидоредуктаза
В составе комплекса – простетическая группа ФАД
и FeSII
От ФАД.Н2 два атома водорода переносятся на KoQ.
Слайд 18КОМПЛЕКС III
КоQН2: цитохром с-оксидоредуктаза
1) Цитохромы b: b566 (низкий ОВП) и
b562 с высоким ОВП.
2)FeSIII – железо-серные белки.
3) Цитохром С1.
Имеет в своем составе особый гем типа «с».
Слайд 19Комплекс III
является протонным генератором, целью его работы является создание
ΔμΗ+
Вторая точка сопряжения
Слайд 20КОМПЛЕКС IV
Комплекс IV - ЦИТОХРОМОКСИДАЗА
(цитохромы а и а3)
Цитохромоксидаза содержит
гем и ионы меди, которые способны менять валентность и таким
способом участвовать в переносе электроновТретья точка сопряжения
Слайд 22КОЭФФИЦИЕНТ P/O
Для оценки эффективности работы ЦПЭ вычисляют коэффициент Р/О
Он
показывает, сколько молекул неорганического фосфата присоединилось к АДФ в расчете
на один атом кислорода.НАДН.Н - Р/О=3 - 3 АТФ
Коэффициент полезного действия - 65%,
ФАНД.Н - P/O=2 - 2 АТФ
Слайд 23Дыхательный контроль
Скорость дыхания митохондрий может контролироваться концентрацией AДФ.
Ускорение ОФ
при повышении концентрации АДФ – называется дыхательный контроль.
Слайд 24ХЕМИОСМОТИЧЕСКАЯ ТЕОРИЯ
Разработана Митчеллом (1961-1966гг)
Дыхание и фосфорилирование связаны связаны через электрохимический
потенциал ионов водорода на митохондриальной мембране (ΔμΗ+)
На каждую пару
электронов выбрасывается три пары протонов в межмемб. пространствоВнутренняя мембрана митохондрий заряжается
Слайд 25ХЕМИОСМОТИЧЕСКАЯ ТЕОРИЯ
Внутренняя мембрана митохондрий заряжается: снаружи +, внутри –
Протоны Н+
стремятся по градиенту в матрикс
Проходят через мембрану через «попы», связанные
с АТФ-синтетазойПереход сопровождается выделением свободной энергии – синтезируется АТФ
ΔμΗ+ - СИНТЕЗ АТФ, ТЕПЛО, ОСМОС
Слайд 27АДФ + Ф + ЭНЕРГИЯ -------> АТФ + Н2О
На каждую
пару атомов водорода, отнятых от субстрата, возможен синтез
3-х молекул
АТФ.Синтез АТФ за счет энергии, которая выделяется в ЦПЭ, называется ОКИСЛИТЕЛЬНЫМ ФОСФОРИЛИРОВАНИЕМ.
Слайд 28
ЭНЕРГИЯ АТФ ИСПОЛЬЗУЕТСЯ
1. Синтез различных веществ.
2. Активный транспорт
3.
Механическое движение (мышечная работа).
Слайд 29ТЕОРИЯ СОПРЯЖЕНИЯ
ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ
1. Транспорт электронов должен создавать определённый
градиент
2. Силы и энергия, направленные на сведение градиента к 0,
должны проходить через устройство, использующие эту энергию для синтеза АТФ3. Подобное устройство должно представлять замкнутую систему
Слайд 30ВЕЩЕСТВА-РАЗОБЩИТЕЛИ ПРОЦЕССОВ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ
Состояние, когда происходит окисление субстратов, а
фосфорилирование (образование АТФ из АДФ и Ф) не идет, называется
РАЗОБЩЕНИЕМ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ.Разобщители являются слабыми кислотами, растворимыми в жирах. В межмембранном пространстве они связывают протоны, и затем диффундируют в матрикс, тем самым снижая ΔμΗ+.
Подобным действием обладает и йодсодержащие гормоны щитовидной железы – тироксин и трийодтиронин.
Слайд 31СПЕЦИФИЧЕСКИЕ ИНГИБИТОРЫ ТКАНЕВОГО ДЫХАНИЯ
К ним относятся вещества, прекращающие работу того
или иного комплекса дыхательной цепи.
Ингибитором комплекса I является яд растительного
происхождения РОТЕНОН.Ингибиторами комплекса IV являются ЦИАНИДЫ, угарный газ СО, сероводород H2S