Слайд 1Общая геохимия
Лекция 25
Геохимия почвы
Геохимическая миграция
Слайд 4Почва состоит из продуктов выветривания
материнских пород, разделяется по горизонтам, которые
отражают перемещение коллоидных частиц.
О: Органическое
вещество;
А: Органика и минералы;
Е: Коллоиды
выщелочены
(главным образом,
остается кварц);
В: Зона накопления
коллоидов (глинистые
минералы и оксиды Fe);
С: Разрушенные исходные
породы;
R: Неразрушенные
исходные породы.
О: Органическое
вещество;
А: Органика и минералы;
Е: Коллоиды выщелочены
(главным образом,
остается кварц);
В: Зона накопления
коллоидов (глинистые
минералы и оксиды Fe);
С: Разрушенные исходные
породы;
R: Неразрушенные
исходные породы.
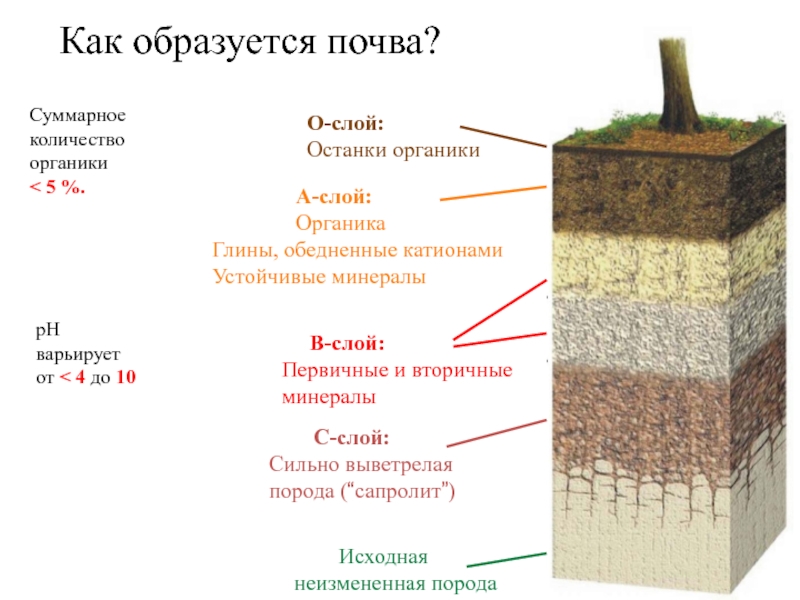
Слайд 5O-слой:
Останки органики
C-слой:
Сильно выветрелая
порода (“сапролит”)
B-слой:
Первичные и вторичные
минералы
A-слой:
Органика
Глины, обедненные катионами
Устойчивые минералы
Исходная неизмененная порода
Как образуется почва?
Суммарное
количество
органики
< 5 %.
pH
варьирует
от < 4 до 10
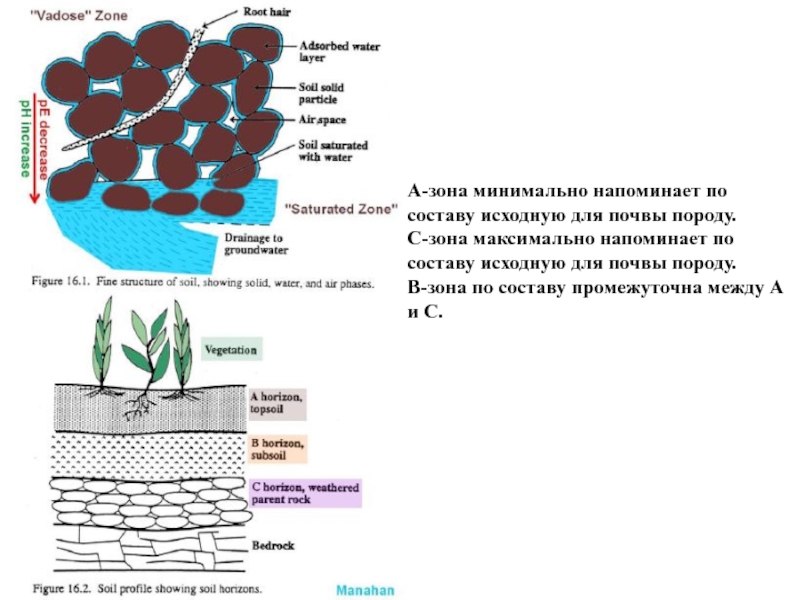
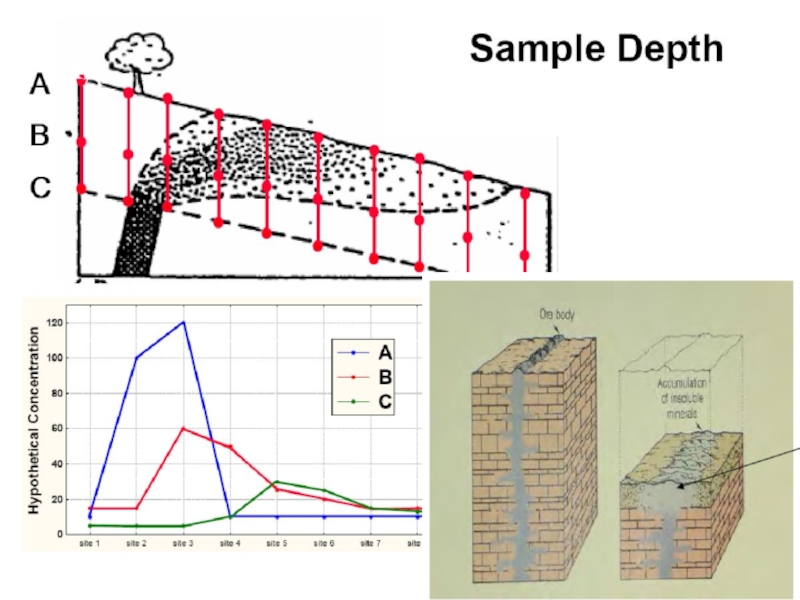
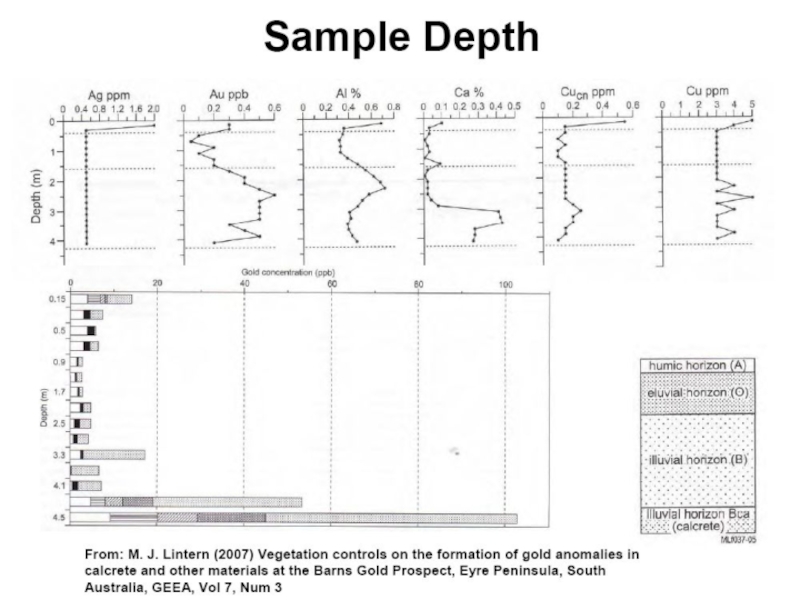
Слайд 6A-зона минимально напоминает по составу исходную для почвы породу.
C-зона максимально
напоминает по составу исходную для почвы породу.
B-зона по составу
промежуточна между А и С.
Слайд 7Устойчивые минералы (например, кварц) не растворяются.
Алюмосиликаты превращаются в глины.
Растворимые
элементы переходят в водный раствор.
Некоторые из них осаждаются ниже в
почве или в виде осадочной породы (оксиды Fe, карбонаты).
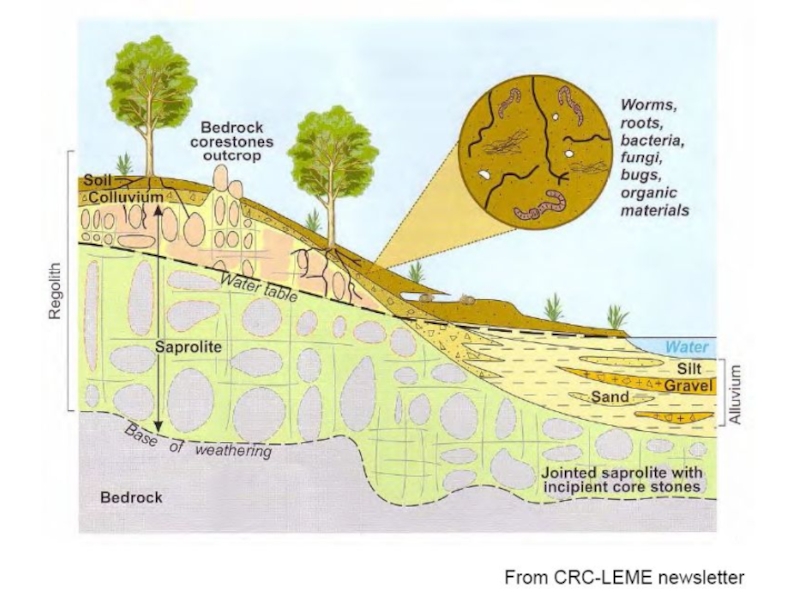
В результате получается реголит – «одеяло», состоящее из почвы (с органикой), осадков и продуктов выветривания горных пород.
Слайд 9
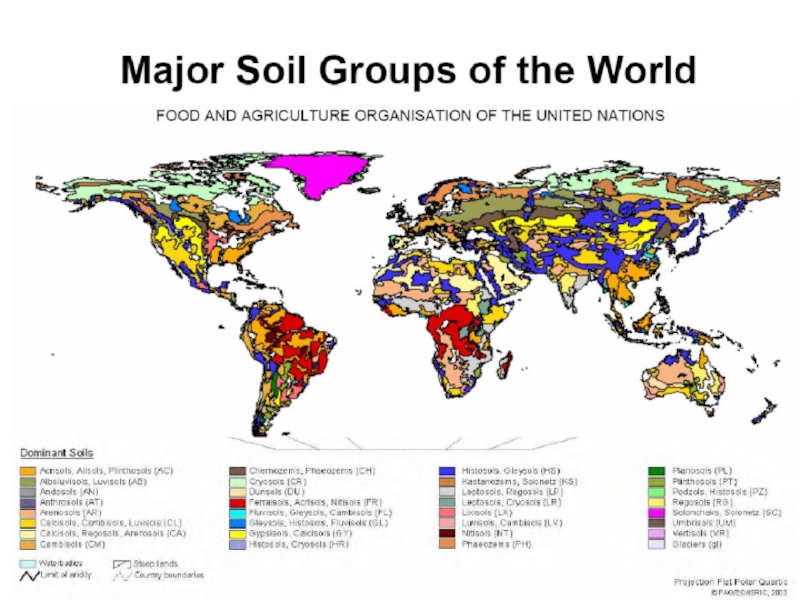
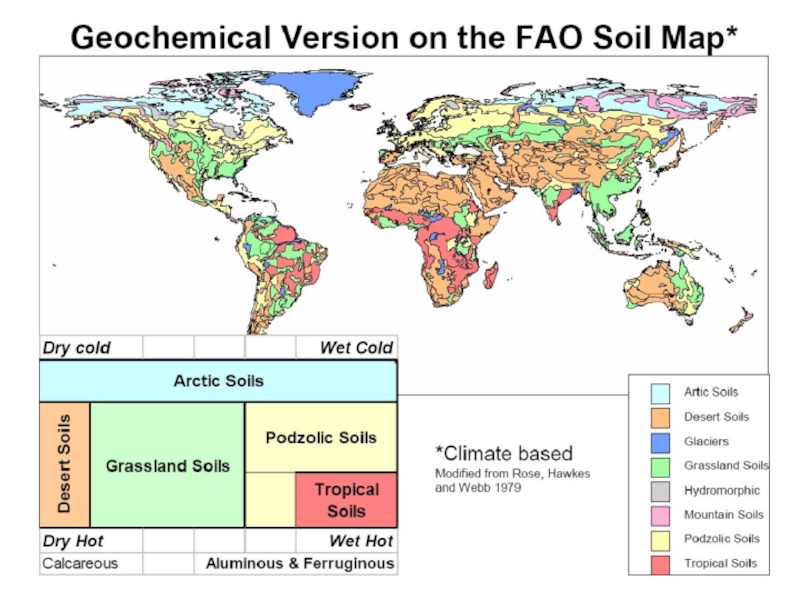
Тип почвы зависит от:
климата
состава (минералогии) пород
условий образования
Почвы служат источником информации:
Палеоклимат - недавний (почвы) и древний (палеопочвы)
Датирование тектонической
активности
Стратиграфия почв (активно используется в археологии)
“Латерит”
Существуют сотни классификаций и типов почв
Слайд 10разлагающаяся органика
гумусовый слой (перегной)
«подзол»
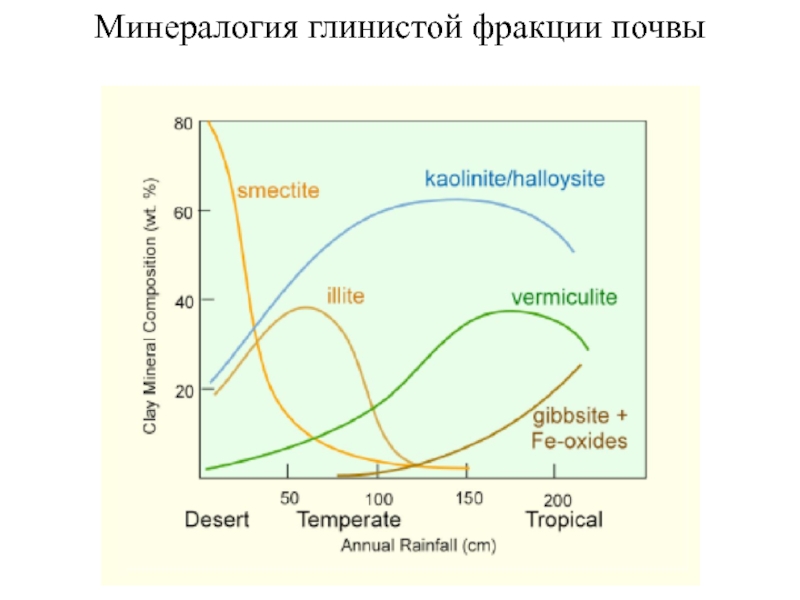
Слайд 11Почвы тропических и
субтропических регионов, как правило, продукт глубокого выветривания.
Они представляют
собой смесь
кварца, каолина, свободных оксидов, органического вещества.
Как правило, у них
нет четко определенных почвенных горизонтов.
Крайняя степень выветривания
может привести к образованию почв, которые
в значительной степени состоят только из просто Al- и Fe- гидроксидов и оксидов.
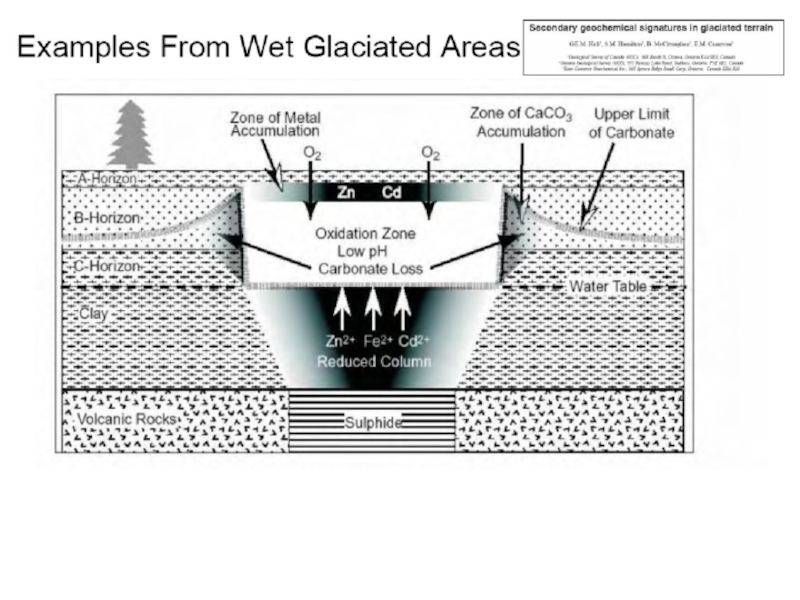
Слайд 13В гумидном (влажном) климате в почвах образуются зоны, богатые
глинами и
органикой.
Слайд 14Почвы районов с очень засушливым
климатом не способствуют
росту растений.
Характерно осаждение минералов
- простых солей: кальцит, гипс.
Эти почвы, как правило, с
низким содержанием
органических веществ.
Слайд 15Каличе, горизонт обызвесткования, образующийся вблизи поверхности в результате концентрации карбоната
кальция, поступающего с грунтовыми водами (путем капиллярного поднятия) и с
инфильтрующимися атмосферными водами.
Слайд 18silt – «ил» 20-50 мкм; алеврит – 10-100 (5-50) мкм.
Текстура
и минералогия почвы
Слайд 19Минералогия глинистой фракции почвы
Слайд 211. Первичные минералы горных пород нестабильны на дневной поверхности.
2. Минералы,
содержащие Al, инконгруэнтно (до конца) растворяются, образуя Al-содержащие глины и
растворенные катионы.
3. Реакции выветривания расходуют CO2 в атмосфере. Однако скорости реакции слишком малы, чтобы влиять на антропогенную составляющую.
Слайд 28Миграция химических элементов
Геохимические барьеры
Слайд 29Перельман Александр Ильич
(1916-1998)
Российский физико-географ, доктор геолого-минералогических наук (1954),
профессор МГУ (с 1966). Основные труды по геохимии ландшафтов и
геохимии гипергенных процессов. Автор учебника «Геохимия».
(2 изд. 1989). Гос. премия СССР (1986).
2003
1955
1999
Слайд 30Основные факторы миграции элементов в земной коре
Типы и виды миграции
химических элементов
Слайд 31
Выделяются 4 основных вида миграции:
1 – механический;
2 - физико-химический;
3 –
биогенный;
4 – техногенный, вызываемый антропогенной
деятельностью.
Основные типы миграции
выделяют при рассмотрении связи перемещения химических элементов с основными формами их нахождения в природе.
Слайд 32Первый тип миграции представляет собой изменение формы нахождения элементов без
их существенного перемещения,
например, переход элементов из минеральной
формы в раствор или из почв в растения.
Второй тип характеризует перемещение элементов без изменения форм их нахождения,
например, перемещение аэрозолей в атмосфере или обломков минералов в поверхностных водах.
Слайд 33Третий тип миграции объединяет два предыдущих и состоит в перемещении
элементов с изменением форм их нахождения.
Например, при
техногенном поступлении в поверхностные воды тяжелых металлов их значительная часть может находиться в форме растворов (первые км). Потом они продолжают миграцию на расстоянии до сотен км в минеральной и коллоидной форме.
Миграция элементов может прекращаться на время, а на отдельных участках при этом возможна существенная концентрация части элементов.
Слайд 34Внутренние факторы миграции
Электростатические свойства ионов
Свойства связи соединений
Химические свойства соединений
Гравитационные свойства
атомов
Радиоактивный распад
Слайд 35Электростатические свойства ионов
Ионный потенциал Картледжа
К=Z/Rj
где Z — разряд;
Rj
— радиус иона, в ангстремах
Слайд 36Энергетические коэффициенты Ферсмана
ЭК анионов = W2/2R
ЭК катионов =
(W2/2R )
[0.75(R+ 0.20)], где
W – валентность иона
R – радиус иона в
ангстремах
Слайд 37Внешние факторы миграции
Температура
Давление
Степень электролитической диссоциации
рН
Окислительно-востановительный потенциал (обстановка)
Поверхностные силы природных коллоидных
систем
Слайд 38рН
В щелочной среде:
Fe3+ + V4+
Fe2+ + V5+
В кислой среде:
2 Fe2+ + U6+
2 Fe3+ + U4+
Слайд 39Поверхностные силы природных коллоидных систем
Активно сорбирующиеся (+) заряженные частицы:
Аl, Fe
(III), Cr (III), Th (III), Тi (IV), Zr (IV), оксида
Мn (II)
Активно сорбирующиеся (-) заряженные
частицы:
кремнезем, большинство сульфидов, гидроксилов V (V), Мn (IV), Fe (II), гуминовые коллоиды.
Слайд 40Природные сорбенты
Коллоиды оксида Мn (IV) [Ni, Со, К, Ва, Сu,
Zn, Hg, Аu, W ]
Гидроксид Fe (III) [As, V, P,
Sb, Se ]
Кремнезем [радиоактивные элементы]
доломит [РЬ, Zn]
Слайд 412-е правило Пескова-Фаянса
на твердой поверхности адсорбируется тот ион, знак
которого противоположен по знаку поверхности и который может образовывать с
одним из ионов решетки мало растворимое соединение.
1.поливалентные ионы сорбируются лучше
2.Cs+>Rb+>K+>Na+>Li+;
I- >Вr->Сl-
Слайд 42В окислительной обстановке накапливаются:
катионогенные элементы переменной
валентности (Fe, Mn, Со)
В окислительной
обстановке растворяются:
Анионогенные элементы (V, Mo, Se, S, U, Re)
Слайд 43Все химические элементы, составляющие земную кору, атмосферу и гидросферу, находятся
в постоянном движении, которое и представляет их миграцию.
Интенсивность миграции
I = m/(tCk)
m – масса мигрирующего элемента
t – промежуток времени существования миграции
Ck – кларковое или фоновое содержание элемента в рассматриваемой геохимической системе.
Слайд 44Общие закономерности
физико-химической миграции
Слайд 45Химические элементы мигрируют в земной коре в виде:
Ионов
Недиссоциированных молекул
Коллоидных мицелл
отдельных частиц дисперсной фазы золя, т. е. высокодисперсной коллоидной
системы с жидкой дисперсионной средой
Свободных радикалов
Слайд 46Миграция в ионной форме характеризуется:
Потенциалом ионизации
Потенциалом возбуждения
Ионным радиусом
Электроотрицательностью
Энергетическим коэффициентом
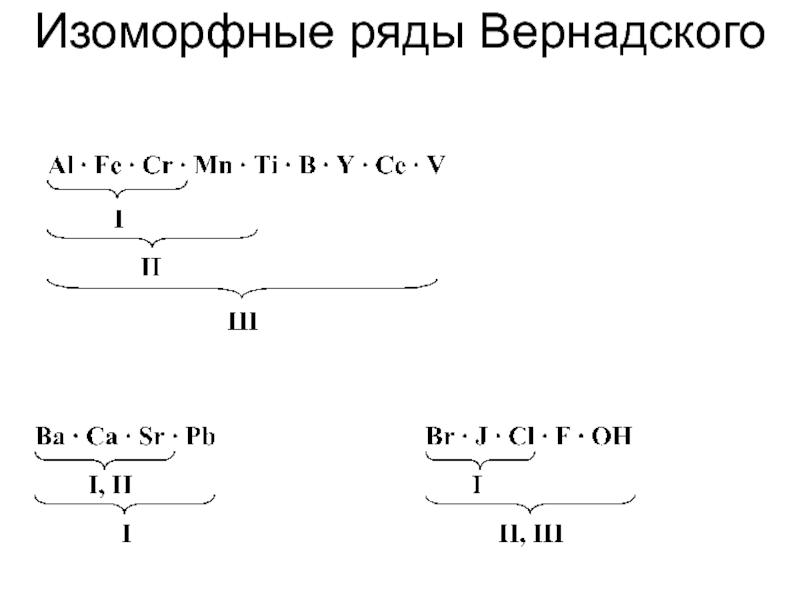
Слайд 47Изоморфизм возможен при:
Радиусы ионов и атомов различаются не более 15%
Химическая
индифферентность
Одинаковые поляризационные свойства атомов
Ионы одного знака
Сходная природа межатомной связи
Слайд 48Химическая индифферентность
Аu (0,144нм) и Аl (0,143нм) образуют
Аu Аl2 и
другие соединения.
Ga(0,062нм) и As(0,058нм) образуют
Ga As
Слайд 49Одинаковые поляризационные свойства атомов
Изоморфизма нет между:
- Na+1 (0,97А) Cu+1 (0,96А)
- Si и P
Слайд 50Валентная компенсация
Сa5(PO4)3(F, Cl, OH) – апатит
Сa2+ изоморфно замещается REE3+
Одновременно
F-1 изоморфно
замещается O-2
Сa5(PO4)3F
ТR5(PO4)3O
Слайд 51Сходная природа
межатомной связи
NaCl – галит и PbS – галенит
У
обоих кубические кристаллические решетки
Ионные радиусы близки у
Na (0,98 нм)и
Pb(1,3 нм)
Cl (1,81 нм) S (1,74 нм ), но
Связь NaCl ионная, а
PbS ковалентная
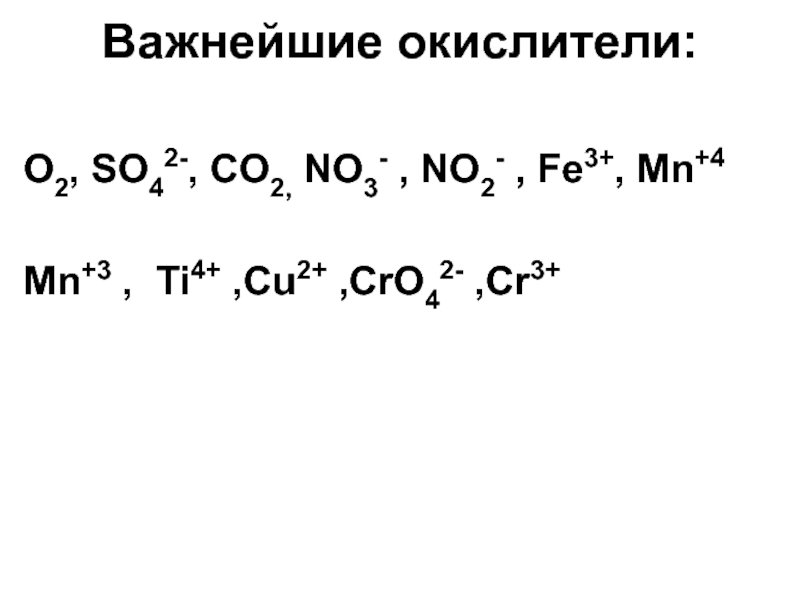
Слайд 53Важнейшие окислители:
О2, SO42-, CO2, NO3- , NO2- , Fe3+, Mn+4
Mn+3 , Ti4+ ,Cu2+ ,CrO42- ,Cr3+
Слайд 54Важнейшие восстановители
Гидратированный электрон – образующийся при радиолизе воды (поглощении излучения)
Cольватированный электрон – электрон, захваченный средой в результате поляризации
окружающих его молекул (гидратированный – в воде). Голубой цвет воды в солнечный день обусловлен именно наличием гидратированных электронов со временем жизни 10-5 с
Атомарный и молекулярный водород
Сероводород
СН4, СО, органические соединения, Fe2+, Mn+2
Слайд 55Ультраокислительная обстановка
Cr6+,V5+, Mn+4 ,Мо+6, Fe+3 N+5, U+6 (степи, пустыни,
содовые озера )
Окислительная обстановка
Fe+3 , Mn+4 , Cu+2
, U+6
(океаны, реки, озера)
Слайд 56Слабоокислительная обстановка
Fe+3 , Mn+2 , Cu+2 , U+6
(трещинные
воды скальных пород)
Слабовосстановительная обстановка
Fe+2 , Fe+3 ,Mn+2 (магма)
Слайд 57Восстановительная обстановка
Fe+2 (сероводородные гидротермы и илы морей, соляных озер,
болота тайги, тундры, влажных тропиков )
Ультравосстановительная обстановка
Fe0 (земное ядро,
нижняя мантия, железные и каменные метеориты)
Слайд 58Механизмы массопереноса:
Диффузия
Конвекция
Слайд 59Геохимические барьеры – те участки земной коры, где на коротком
расстоянии происходит резкое уменьшение интенсивности миграции химических элементов и, как
следствие, их концентрация. Играют важную роль в экзогенных процессах рудообразования.
В пределах большинства барьеров довольно резко изменяется форма нахождения элементов в мигрирующем потоке (изменение типа миграции), а затем происходят связанные с ней изменения интенсивности миграции и осаждение (концентрация определенных химических элементов или их соединений).
Слайд 60Концепция геохимических барьеров основывается на 3 эмпирических правилах:
1. Геохимические аномалии
формируются на геохимических барьерах (прежде всего, физико-химических).
2. Геохимические барьеры формируются
на границах сопряженных ландшафтов (природных географических комплексов) или подсистем ландшафтов – «эффект опушки».
3. На более контрастных геохимич. границах образуются самые емкие геохимические барьеры.
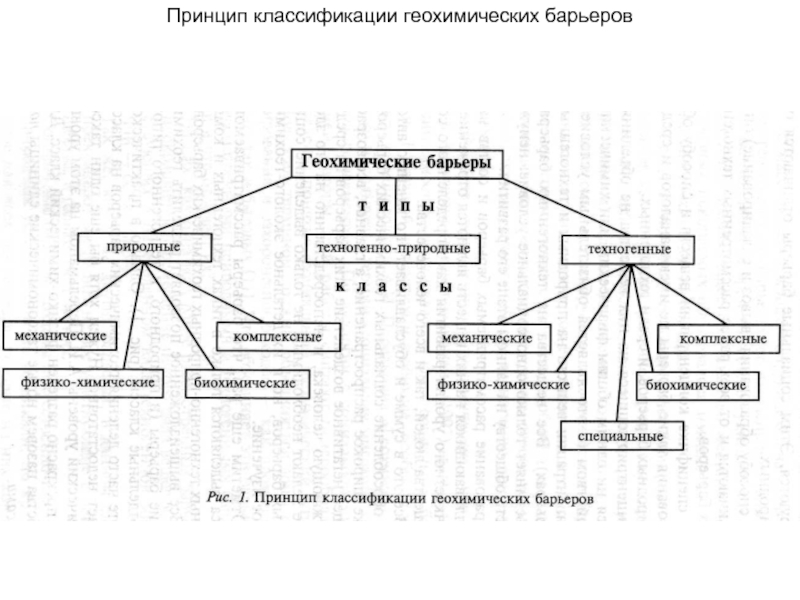
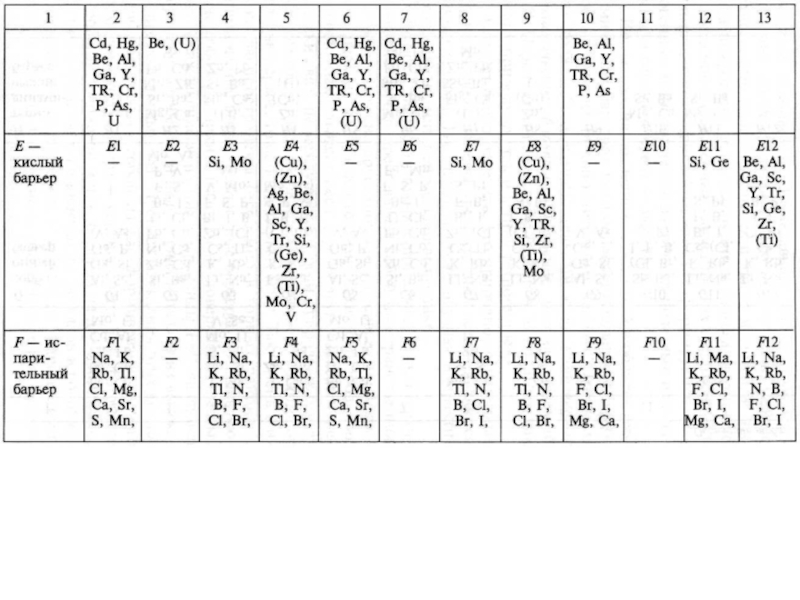
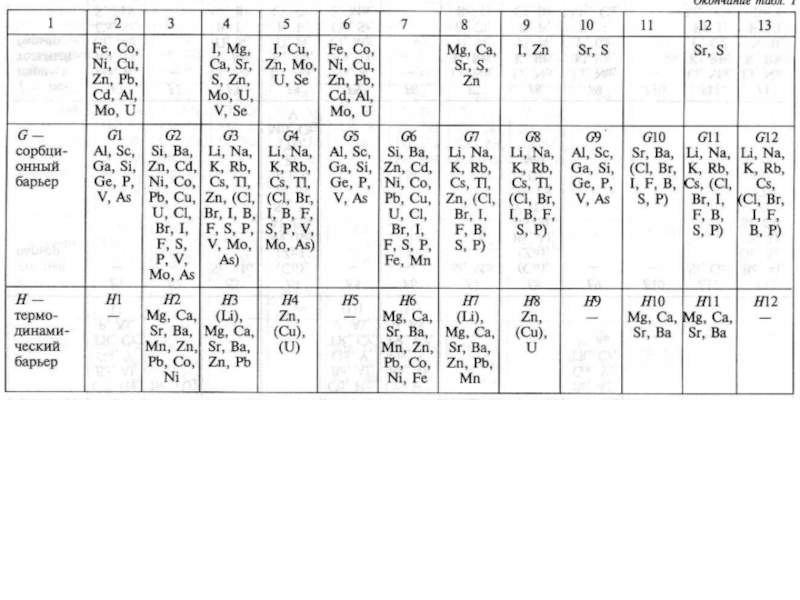
Слайд 61Принцип классификации геохимических барьеров
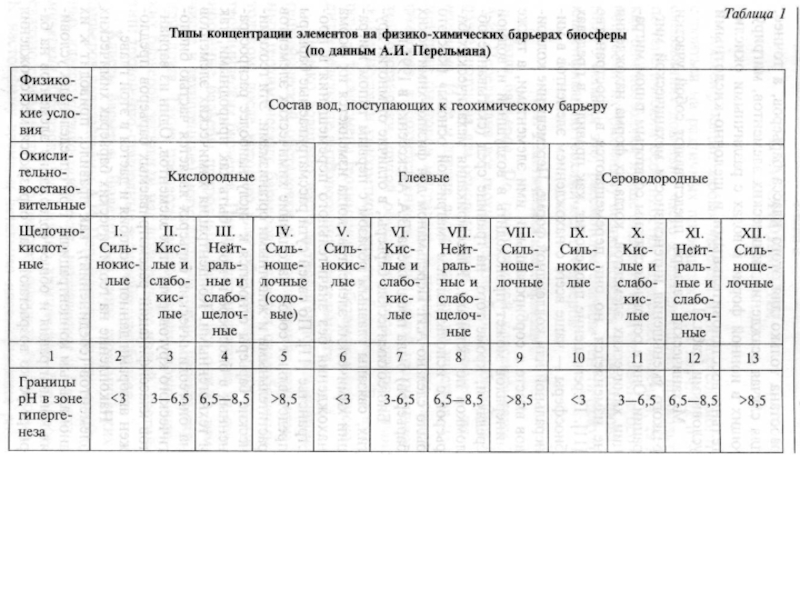
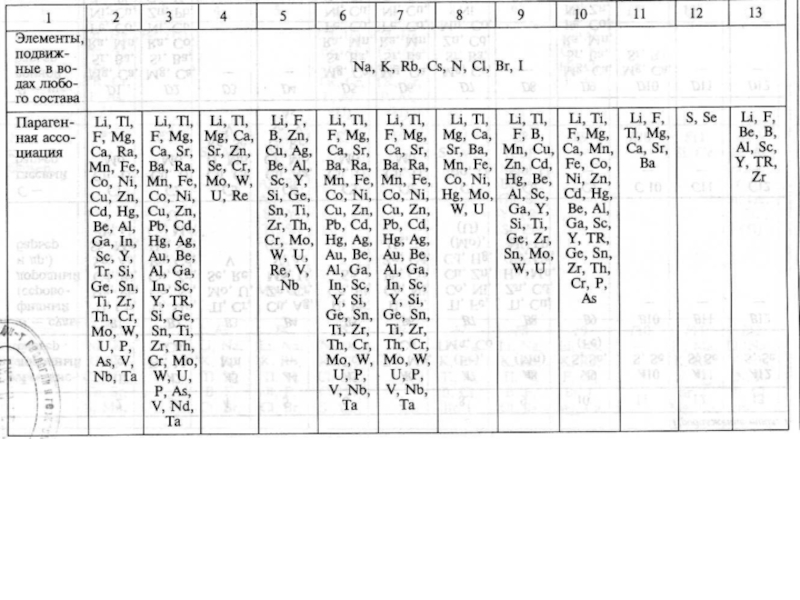
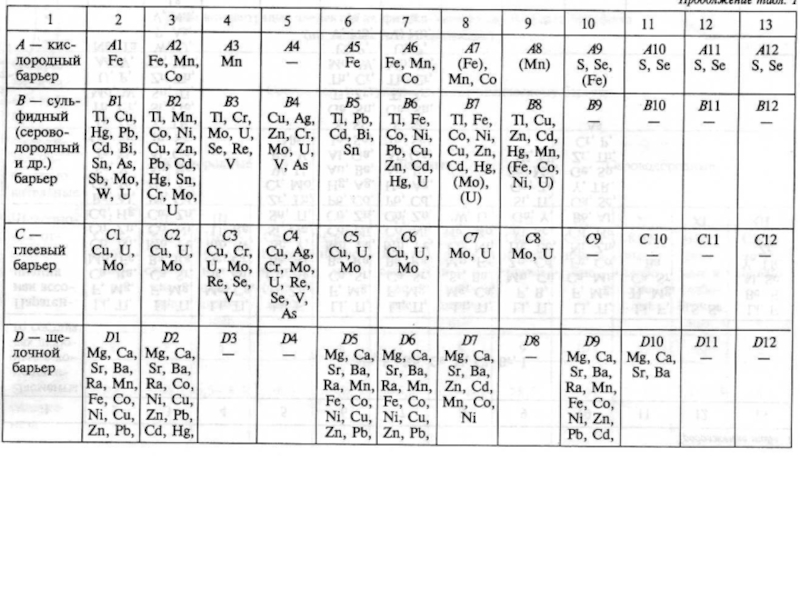
Слайд 62Физико-химические барьеры. Классификация разработана для случая осаждения х.э., мигрирующих в
ионной форме в водах с различными окислительно-восстановительными и щелочно-кислотными условиями.
Механические
барьеры. Форма нахождения элементов не меняется. Перемещение в пределах биосферы. Второй тип миграции.
Биогеохимические барьеры. Изменяется форма нахождения без значительного перемещения. Первый тип миграции. По сути накопление х.э. растительными и животными организмами.
Слайд 68S-контрастность
барьера
G-градиент барьера
G = (m1-m2)/l
Количественные характеристики
геохимических барьеров
S
= m1/m2
Слайд 69Окислительный барьер
При разгрузке минерализованных вод на поверхности окисление Fe2+ до
Fe3+
(железо выпадает в виде гидроксида).
Выпадение элементарной серы
в газовых фумаролах при окислении сероводорода.
Слайд 70Восстановительный барьер
Наличие в системе сульфидной серы снижает
подвижность халькофильных элементов («черные
курильщики»).
Барьеры,
где восстановитель органическое в-во
(без сероводорода) – глеевые. Например, болота.
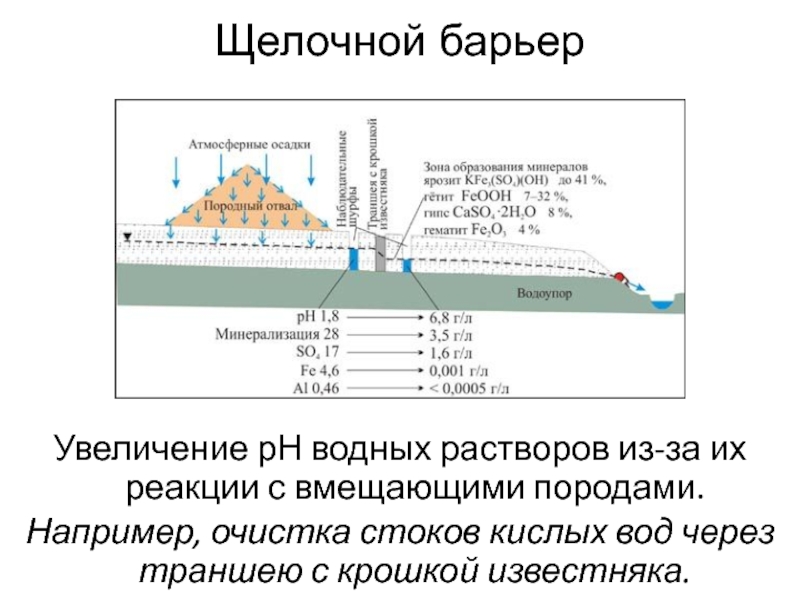
Слайд 71Щелочной барьер
Увеличение рН водных растворов из-за их реакции с вмещающими
породами.
Например, очистка стоков кислых вод через траншею с крошкой
известняка.
Слайд 72Кислотный барьер
(смешанный тип барьера)
В осадок выпадают элементы, подвижные в
щелочных растворах.
Например, смешение щелочных вод (природных) с кислыми (серная
кислота образуется при окислении руд).
Зона окисления сульфидного месторождения.
Слайд 73Сорбционный барьер
Где имеется активная и хорошо развитая минеральная поверхность.
Например,коры
выветривания, почвы, донные осадки.
Слайд 75В отвале с искусственно созданными геохимическими барьерами образуется металлическая медь,
покрытая слоем малахита Cu2[CO3](OH)2.
Техногенный барьер
























![Геохимия почвы. Миграция Энергетические коэффициенты ФерсманаЭК анионов = W2/2RЭК катионов = (W2/2R ) [0.75(R+ Энергетические коэффициенты ФерсманаЭК анионов = W2/2RЭК катионов = (W2/2R ) [0.75(R+ 0.20)], гдеW – валентность ионаR –](/img/thumbs/53201092bc0f5dd1f86022870713cbe6-800x.jpg)



![Геохимия почвы. Миграция Природные сорбенты Коллоиды оксида Мn (IV) [Ni, Со, К, Ва, Сu, Природные сорбенты Коллоиды оксида Мn (IV) [Ni, Со, К, Ва, Сu, Zn, Hg, Аu, W ]Гидроксид Fe](/img/thumbs/fafa8c01b83781f276007117413a39e4-800x.jpg)

























2.Техногенный барьер В отвале с искусственно созданными геохимическими барьерами образуется металлическая медь, покрытая слоем малахита Cu2[CO3](OH)2.Техногенный барьер](/img/thumbs/c6fce2e2a09e06be3c0afb7c1a710693-800x.jpg)