Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ХИМИЯ БЛАГОРОДНЫХ ГАЗОВ
Содержание
- 1. ХИМИЯ БЛАГОРОДНЫХ ГАЗОВ
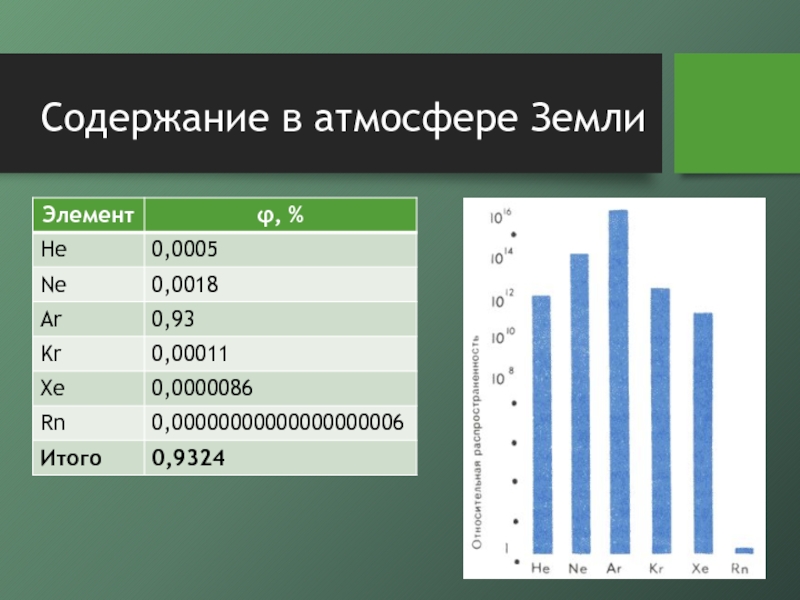
- 2. Содержание в атмосфере Земли
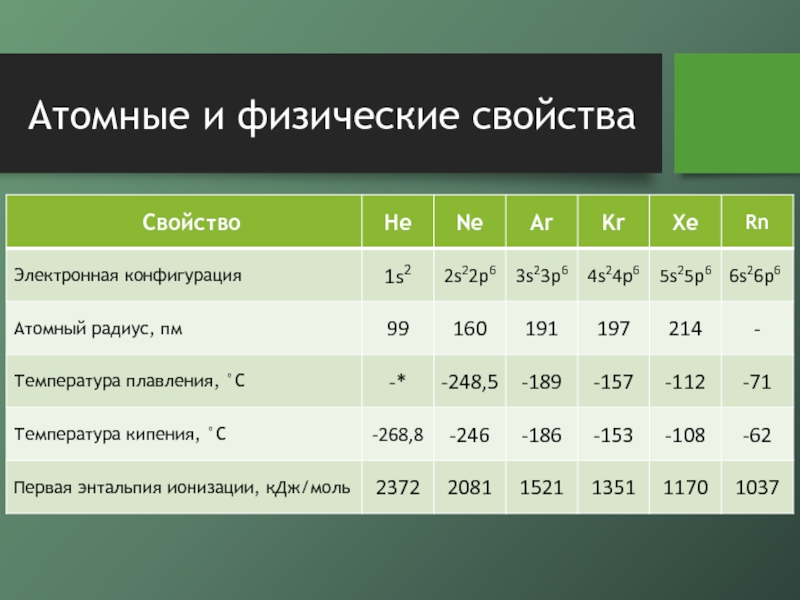
- 3. Атомные и физические свойства
- 4. КСЕНОН Первые химические соединения1962 г – синтез
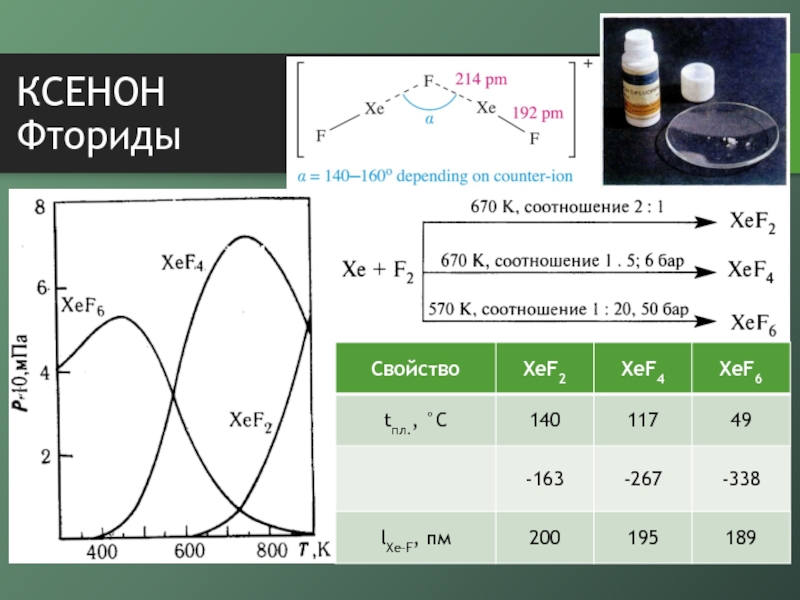
- 5. КСЕНОН Фториды
- 6. КСЕНОН ХлоридXeCl2 получен…при пропускании высокочастотного электроразряда через
- 7. КСЕНОН Оксидыизвестны только 2 оксида: XeO3, XeO4оксид
- 8. КСЕНОН Оксогалогенидыоксофториды известны для ксенона всех степеней
- 9. КСЕНОН ОксогалогенидыXe3OF3+ получается при реакции [XeF][AsF6] с
- 10. КСЕНОН Соединения со связями Xe-Me, Xe-Cпервое соединение Xe-Me – Fe(CO)4Xeс 2000-х Xe-Au, Xe-Hg
- 11. КРИПТОНдифторид получен Тёрнером и Пиментелем (1963) при
- 12. АРГОН, НЕОН И ГЕЛИЙпервое химическое соединение аргона
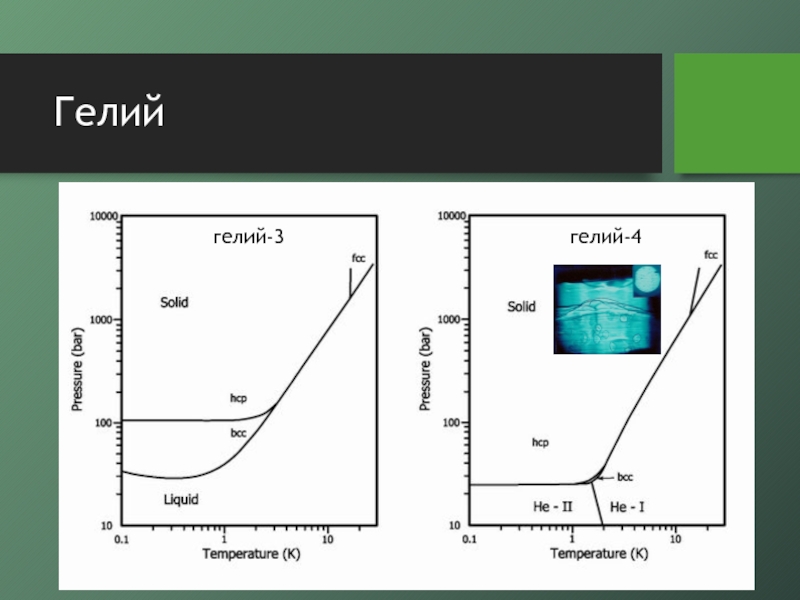
- 13. Гелий
- 14. Применение
- 15. Применение
- 16. Скачать презентанцию
Содержание в атмосфере Земли
Слайды и текст этой презентации
Слайд 4КСЕНОН
Первые химические соединения
1962 г – синтез Нила Бартлетта
[XeF][PtF6] термически устойчив
гидролизуется
с образованием ксенона
Слайд 6КСЕНОН
Хлорид
XeCl2 получен…
при пропускании высокочастотного электроразряда через смесь Xe, F2, CCl4
(1:1:1)
при микроволновом облучении смеси Xe и Cl2 в изолированной матрице
при
β-распаде производных иода-129в виде катиона XeCl+
Слайд 7КСЕНОН
Оксиды
известны только 2 оксида: XeO3, XeO4
оксид ксенона (VI) образуется при
гидролизе гексафторида при пониженной температуре с добавкой MgO
XeO3 – б/цв.
и гигроскопичные кристаллы, детонирует при ударе (ΔfH = 402 кДж/моль)оксид ксенона (VIII) получается при реакции серной кислоты с ксенатами
XeO4 – св.-ж. кристаллы, взрывоопасен (ΔfH = 642 кДж/моль)
Слайд 8КСЕНОН
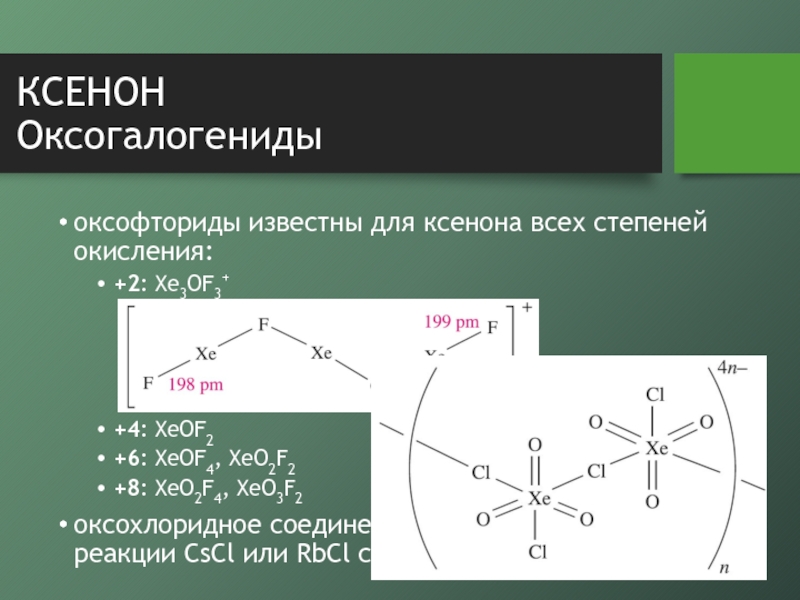
Оксогалогениды
оксофториды известны для ксенона всех степеней окисления:
+2: Xe3OF3+
+4: XeOF2
+6: XeOF4,
XeO2F2
+8: XeO2F4, XeO3F2
оксохлоридное соединение получается при реакции CsCl или RbCl
с XeO3Слайд 9КСЕНОН
Оксогалогениды
Xe3OF3+ получается при реакции [XeF][AsF6] с раствором воды в HF
XeOF2
получается при реакции XeF4 с раствором воды в HF (210
K)XeOF4 образуется при частичном гидролизе XeF6
XeO2F2 получается при реакции XeO3 с XeOF4
XeO2F4 получается при реакции XeF6 с XeO3F2 в XeOF4
XeO3F2 получается при реакции XeF6 с Na4XeO6 или XeF6 с XeO4
Слайд 10КСЕНОН
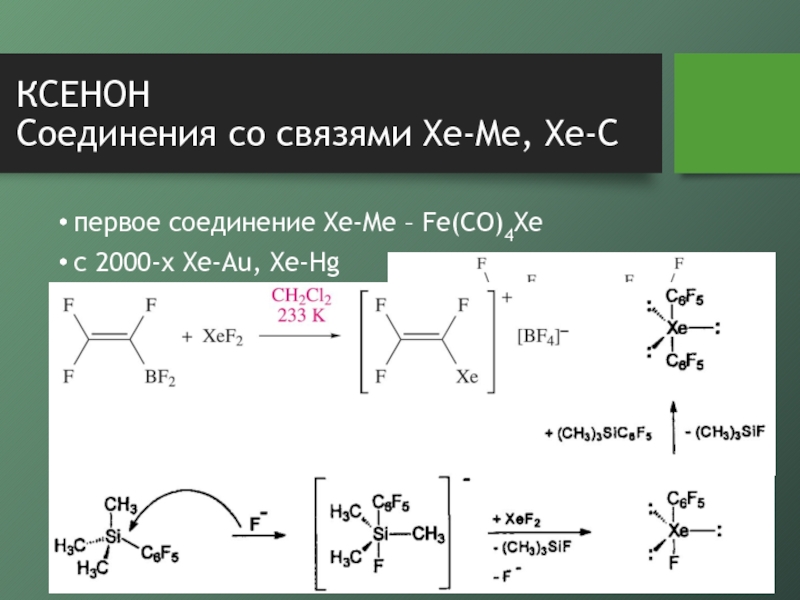
Соединения со связями Xe-Me, Xe-C
первое соединение Xe-Me – Fe(CO)4Xe
с 2000-х
Xe-Au, Xe-Hg
Слайд 11КРИПТОН
дифторид получен Тёрнером и Пиментелем (1963) при фотолизе смеси твердых
фтора, аргона и криптона при 20 К
разлагается при 250 К
легко
гидролизуется, особенно в кислой средеоксид криптона (KrO) не выделен в чистом виде
он получается при медленном гидролизе на влажном воздухе
очень взрывоопасен
Слайд 12АРГОН, НЕОН И ГЕЛИЙ
первое химическое соединение аргона получено в 2000
году Леонидом Хрящевым с сотрудниками
при фотолизе (127-160 нм) HF в
твердой аргоновой матрице ИК-спектрометрией было зафиксировано образование HArFнеон и гелий не образуют устойчивых химических соединений

![ХИМИЯ БЛАГОРОДНЫХ ГАЗОВ КСЕНОН Первые химические соединения1962 г – синтез Нила Бартлетта[XeF][PtF6] термически устойчивгидролизуется КСЕНОН Первые химические соединения1962 г – синтез Нила Бартлетта[XeF][PtF6] термически устойчивгидролизуется с образованием ксенонапиролиз приводит к образованию](/img/thumbs/f6e655da8c6f09050ed0f1dc1e73b928-800x.jpg)


![ХИМИЯ БЛАГОРОДНЫХ ГАЗОВ КСЕНОН ОксогалогенидыXe3OF3+ получается при реакции [XeF][AsF6] с раствором воды в HFXeOF2 КСЕНОН ОксогалогенидыXe3OF3+ получается при реакции [XeF][AsF6] с раствором воды в HFXeOF2 получается при реакции XeF4 с раствором](/img/thumbs/1d5d23c0975cbc8ef0ecd98f71750082-800x.jpg)