Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Хирургическое лечение рака яичника Выполнила: Коночкина Вероника
Содержание
- 1. Хирургическое лечение рака яичника Выполнила: Коночкина Вероника
- 2. Слайд 2
- 3. Слайд 3
- 4. 4) При отсутствии асцита выполняют цитологическое исследование
- 5. 6) Если проведенная ревизия не подтвердила наличие
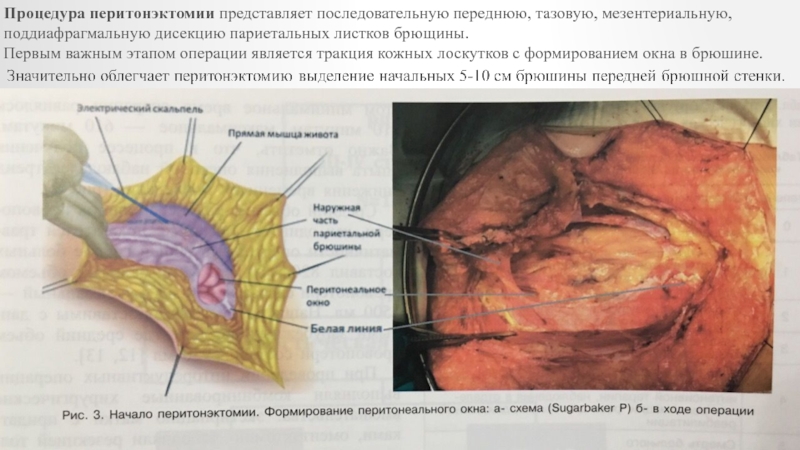
- 6. Процедура перитонэктомии представляет последовательную переднюю, тазовую, мезентериальную,
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Важным этапом операции является разделение перинеального туннеля
- 12. Слайд 12
- 13. Слайд 13
- 14. Слайд 14
- 15. Классификация хирургических осложнений клиники Memorial Sloan-Kettering Cancer Center.
- 16. Структура послеоперационных осложнений в соответствии с классификацией
- 17. Слайд 17
- 18. Органосохраняющее хирургическое вмешательство
- 19. Слайд 19
- 20. Лимфаденэктомия не улучшает выживаемость«Пациенты, успешно прошедшие хирургическое
- 21. Их исследование продемонстрировало, что показатели полной
- 22. Операция по сохранению фертильности (ФФС) основана на
- 23. Часто выполняемой висцеральной резекцией во время первичной
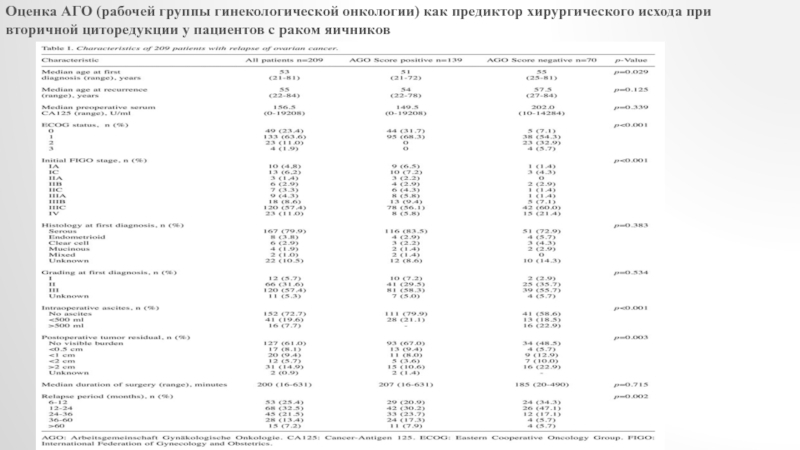
- 24. Оценка АГО (рабочей группы гинекологической онкологии) как
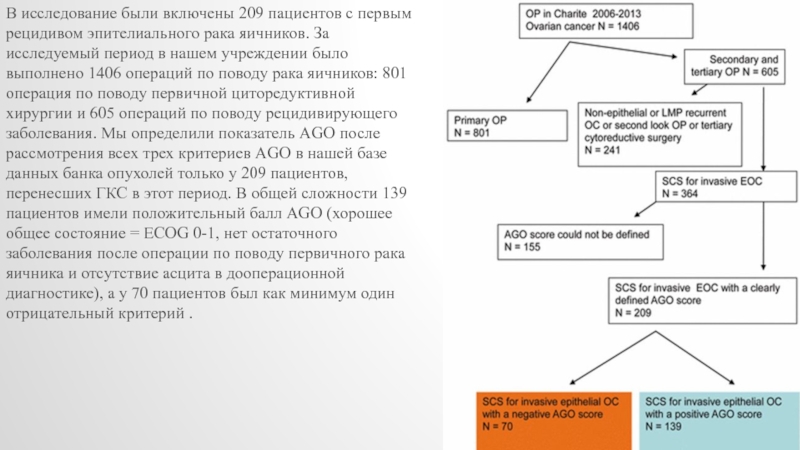
- 25. В исследование были включены 209 пациентов с
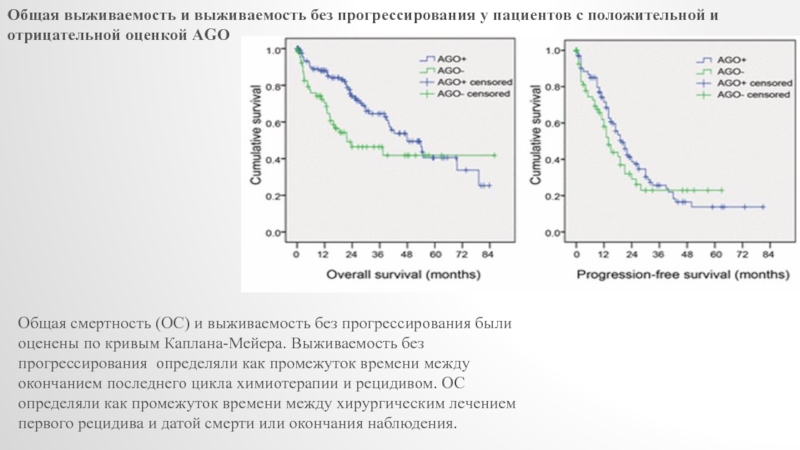
- 26. Общая выживаемость и выживаемость без прогрессирования у
- 27. Вывод:Оптимизируя хирургические навыки и инфраструктуру, мы можем
- 28. Спасибо за внимание!
- 29. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Хирургическое лечение рака яичника
Выполнила: Коночкина Вероника Игоревна,
студентка 5 курса
СПбГУ
Слайд 2
Термины и определения
Полная циторедуктивная операция – выполнение экстирпации матки с придатками, удаление большого сальника, а также всех видимых проявлений опухолевого процесса без макроскопически определяемых остаточных опухолевых масс.
Оптимальная циторедуктивная операция – выполнение экстирпации матки с придатками, удаление большого сальника, а также видимых проявлений опухолевого процесса с макроскопически определяемыми остаточными опухолевыми узлами, каждый из которых имеет диаметр не более 10 мм.
Неоптимальная циторедуктивная операция – экстирпации матки с придатками, удаление большого сальника, проявлений опухолевого процесса с макроскопически определяемыми остаточными узлами, из которых хотя бы один более 10 мм в диаметре.
Слайд 3
Хирургическое лечение I–II стадий рака яичников
•
При I–II стадиях заболевания при ревизии органов брюшной полости необходимо обязательно выполнить все процедуры хирургического стадирования.1) Срединная лапаротомия используется:
Для хорошего обзора с целью полноценной ревизии органов брюшной полости и малого таза
Для обеспечения адекватного доступа к большому сальнику
- Чтобы исключить распад опухоли при ее удалении (если произошел распад опухоли, то это свидетельствует о распространении опухолевого процесса по брюшной полости)
Малоинвазивные хирургические вмешательства могут быть использованы только для верификации диагноза, определения стадии или для прогнозирования объема циторедуктивной операции.
2) Если морфологической верификации диагноза нет, лапаротомию следует проводить со срочным интраоперационно-морфологическим исследованием.
3) Если обнаружен асцит, жидкость аспирируют для цитологического исследования.
Слайд 44) При отсутствии асцита выполняют цитологическое исследование смывов с брюшины
(в том числе с ее диафрагмальной поверхности, латеральных каналов и
малого таза).5) Тщательно осматриваются все отделы:
брюшной полости,
малого таза,
поддиафрагмальное пространство,
большой и малый сальник,
тонкую и толстую кишку и их брыжейки,
поверхность париетальной и висцеральной брюшины,
забрюшинное пространство,
Все участки брюшины и спайки, подозрительные в отношении метастазов, подвергают биопсии.
Вся поверхность брюшины должна быть осмотрена.
Спаечный процесс, препятствующий ревизии, должен быть отмечен.
Слайд 56) Если проведенная ревизия не подтвердила наличие метастазов, выполняют биопсию
случайно выбранных участков:
- брюшины
- стенок малого таза,
- прямокишечно-маточного углубления,
- мочевого пузыря, латеральных каналов,
- правого и левого куполов диафрагмы (может быть выполнен соскоб с поверхностей диафрагмы).
7) Удаление большого сальника является обязательным и выполняется на уровне большой кривизны желудка при распространенном раке яичников.
8) Тотальная тазовая и поясничная лимфаденэктомия до уровня почечных сосудов обязательна при I стадии рака яичников (кроме муцинозной аденокарциномы) для решения вопроса о необходимости адъювантной химиотерапии, во всех остальных случаях решается индивидуально.
9) Удаление аппендикса целесообразно в случае подозрения на его поражение.
10) При невыполнении процедур стадирования при подозрении на ранние стадии (I−II) заболевания во время первой операции рекомендуется выполнение повторного хирургического вмешательства с целью рестадирования.
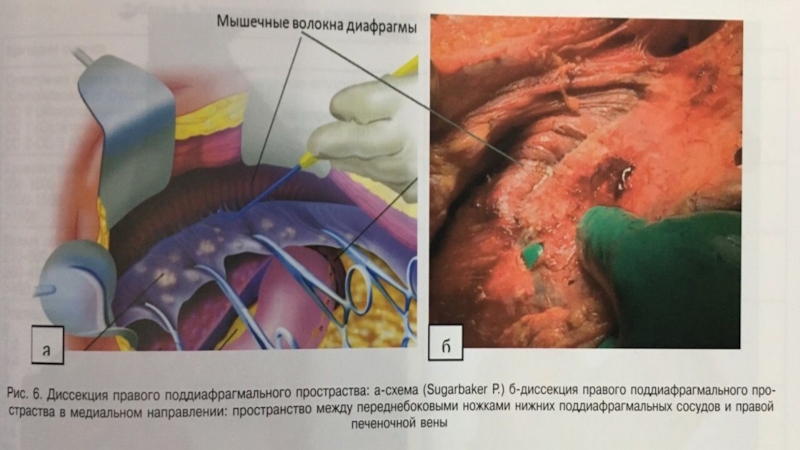
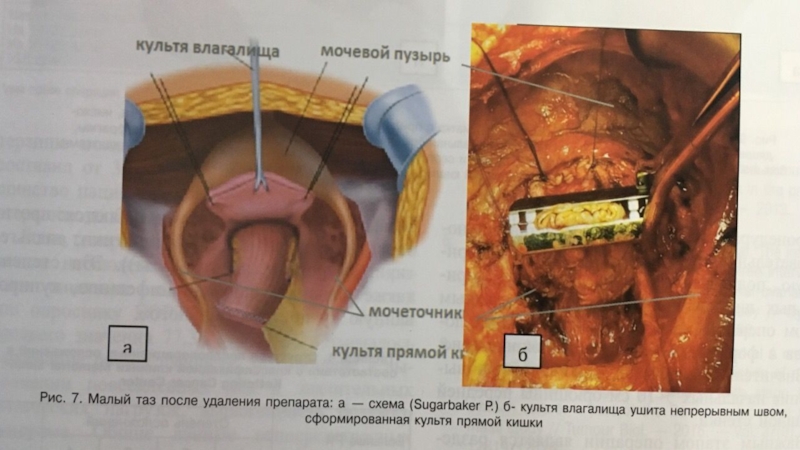
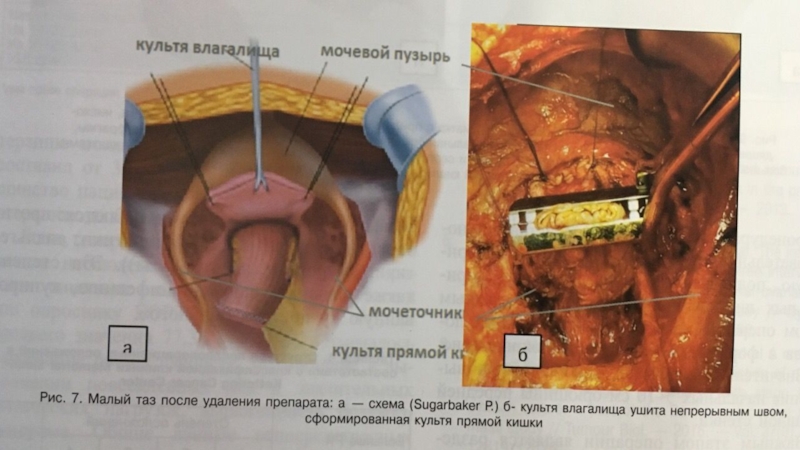
Слайд 6Процедура перитонэктомии представляет последовательную переднюю, тазовую, мезентериальную, поддиафрагмальную дисекцию париетальных
листков брющины.
Первым важным этапом операции является тракция кожных лоскутков
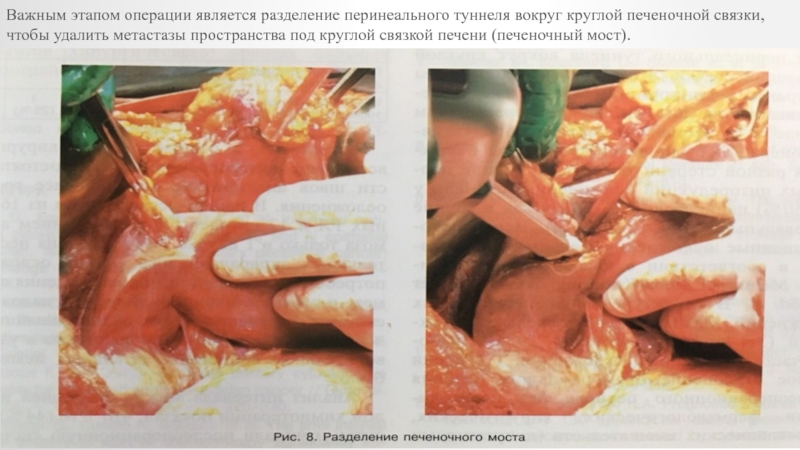
с формированием окна в брюшине. Слайд 11Важным этапом операции является разделение перинеального туннеля вокруг круглой печеночной
связки, чтобы удалить метастазы пространства под круглой связкой печени (печеночный
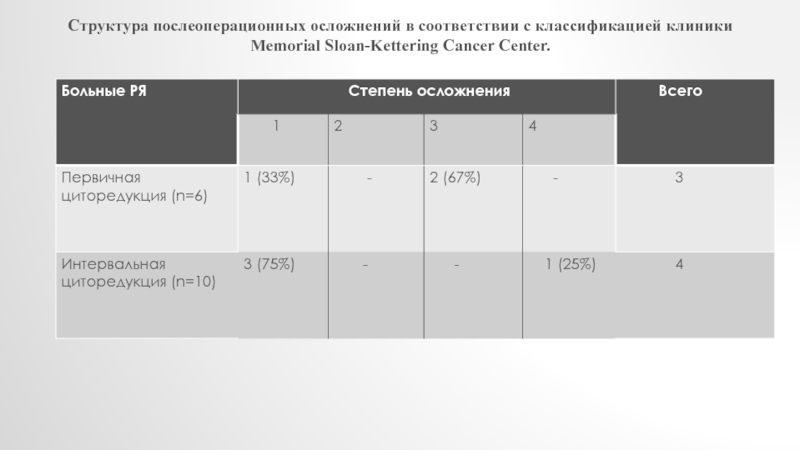
мост).Слайд 16Структура послеоперационных осложнений в соответствии с классификацией клиники
Memorial Sloan-Kettering Cancer Center.
Слайд 18
Органосохраняющее хирургическое вмешательство (односторонняя аднексэктомия с
резекцией второго яичника, оментэктомия, тазовая и поясничная лимфаденэктомия и выполнение
процедур стадирования) в виде исключения возможно у молодых больных, желающих сохранить фертильность,при серозной карциноме низкой степени злокачественности, эндометриоидной или муцинозной карциноме IA и IC1 стадий
при наличии возможности тщательного диспансерного наблюдения и доказанном отсутствии наследственного характера заболевания.
При эндометриоидном гистологическом варианте в этих случаях следует выполнить биопсию эндометрия для исключения синхронного рака эндометрия.
Слайд 19 Хирургическое лечение
III−IV стадий рака яичников
• При распространенности опухоли и состоянии пациентки,
позволяющих выполнить оптимальную циторедуктивную операцию на первом этапе, рекомендуется проведение хирургического вмешательства в объеме полной или оптимальной циторедукции, т.е. удаление всех видимых проявлений болезни.• При невозможности выполнения оптимальной циторедуктивной операции на первом этапе рекомендуется начинать лечение с химиотерапии.
К пациенткам, которым показана предоперационная химиотерапия, могут относиться больные с тяжелым соматическим статусом, а также пациентки с крайне выраженной распространенностью опухолевого процесса, делающей невозможным выполнение оптимальной циторедукции. Эти пациентки нуждаются в промежуточной циторедуктивной операции в максимально короткие сроки (после 2–3 курсов индукционной химиотерапии). После операции пациенткам проводится дополнительно 3–4 курса химиотерапии по той же схеме.
• Выполнение лимфаденэктомии при III–IV стадии целесообразно при полной циторедукции при увеличенных, подозрительных на метастатическое поражение лимфоузлах по данным предоперационного обследования или интраоперационной ревизии.
Удалению подлежат внутренние, наружные, общие подвздошные, запирательные, преаортальные, парааортальные, аортокавальные, прекавальные и паракавальные лимфоузлы до уровня почечных сосудов.
Клинические рекомендации. Рак яичников/рак маточной трубы/первичный рак брюшины. Кодирование по МКБ С48/C56/С57. Год 2019.
Слайд 20Лимфаденэктомия не улучшает выживаемость
«Пациенты, успешно прошедшие хирургическое лечение в специализированных
центрах, имеют относительно благоприятный прогноз»Общая выживаемость не различалась между двумя
группами.Женщины в группе без лимфаденэктомии жили в среднем 69,2 месяца после случайного назначения, а женщины в группе с лимфаденэктомией жили 65,5 месяцев.
Медиана выживаемости без прогрессирования , которая представляла собой промежуток времени от случайного назначения до возвращения болезни или смерти, составила 25,5 месяцев в обеих группах.
Когда патологи исследовали лимфатические узлы, удаленные от женщин в группе лимфаденэктомии, они обнаружили микроскопический метастатический рак почти у 56% этих пациентов.
Одинаковая общая выживаемость в обеих группах в этом исследовании свидетельствует о том, что именно неспособность контролировать заболевание в брюшной полости является наиболее частой причиной заболеваний и смерти, связанных с раком яичников, а не какой-либо остаточной болезнью в лимфатических узлах.
Больше осложнений
Женщины в группе лимфаденэктомии имели более частые осложнения во время и после операции, чем женщины в группе без лимфаденэктомии. Кроме того, приблизительно 3% пациентов в группе лимфаденэктомии умерли в течение 60 дней после операции, по сравнению с приблизительно 1% в группе без лимфаденэктомии.
Лимфаденэктомия обычно добавляет еще один час к уже длинной (4–5 часам) и сложной операции.
По ее словам, одним из важных выводов исследования является то, что «больше вреда в результате удаления большего количества лимфатических узлов и более длительной операции».
«Новое исследования разрешил критику многих предыдущих исследований», в которых пытались оценить ценность систематической лимфаденэктомии у женщин с распространенным раком яичников, у которых были удалены все видимые признаки опухолевой ткани, которые были удалены хирургическим путем.
27 марта 2019 г., сотрудники NCI
Слайд 21 Их исследование продемонстрировало, что показатели полной резекции, выживаемости без
прогрессирования заболевания (PFS) и общей выживаемости (OS) увеличились в течение
13-летнего периода оценки, несмотря на оперирование на более высокой стадии заболевания и пациентов с большей опухолевой нагрузкой. Предполагалось, что это во многом связано со сменой хирургической парадигмы, специально разработанной для достижения более полной хирургической циторедукции, даже для пациентов с менее благоприятным профилем заболевания.Published 2019 Jun 26
Maximal-Effort Cytoreductive Surgery for Ovarian Cancer Patients with a High Tumor Burden: Variations in Practice and Impact on Outcome
Слайд 22Операция по сохранению фертильности (ФФС) основана на одностороннейсальпингоофрэктомии и полном
хирургическом вмешательстве. Это управление кажется безопасным у пациентов с обычной
стадией IА низкой степени(серозный, эндометриоидный или муцинозный экспансионный подтип). Использование ФСС у пациентов со стадией болезни IC должно быть определенос использованием действующей в 2014 году системы организации FIGO. FSS приемлемо для опухолей стадии IC1, причем половина этих рецидивовизолированный на оставшемся яичнике и поэтому способный быть спасенным
путем последующей операции. Однако частота рецидивов выше
в стадии IC2, IC3 и 3 степени заболевания, хотя в основном в экстраовариальных участках и, следовательно, не четко коррелируют с
фертильность-щадящий подход. Адекватное консультирование, следовательно, необходимо в этой ситуации.В случаях заболевания стадии II или III применение ФСС является наблюдался высокий риск рецидивов. ФСС остается противопоказан этим пациентам, хотя неясно, такие рецидивы связаны с естественной историей болезни, а не с типом операции у этих пациентов с «высоким риском».
ФСС может быть безопасно предложена всем этапам IA и карциномы яичников низкой степени тяжести IC1.
Published online 2 May 2019
ESMO–ESGO consensus conference
recommendations on ovarian cancer: pathology and
molecular biology, early and advanced stages,
borderline tumours and recurrent disease
Слайд 23Часто выполняемой висцеральной резекцией во время первичной циторедукции была резекция
кишечника. В исследовании более 40% пациентов были подвергнуты резекции кишечника
для достижения полной резекции R0. Большие исследования уже продемонстрировали, что резекция кишечника является одной из наиболее часто выполняемых процедур для удаления больших опухолевых масс и оценили, что этот вид хирургии требуется почти в 50% оптимальных операций по удалению пятель. Многочисленные исследования показали, что резекция кишечника может значительно увеличить процент полной циторедукции и связана с аналогичными показателями выживаемости по сравнению с пациентами, перенесшими резекцию R0, но не нуждающимися в операции на кишечнике. Gillette-Cloven et al. продемонстрировали, что связь резекции кишечника с целью получения полной резекции была связана с медианной общей выживаемостью 35 месяцев по сравнению со средней выживаемостью 18 месяцев для случаев без резекции кишечника, но с остаточным заболеванием. В этом исследовании 48 случаев с диагнозом эпителиальный рак III-IV стадии ФИГО, подвергнутых резекции кишечника в рамках полной операции по циторедукции, Estes et al. продемонстрировали, что резекция кишечника может повысить эффективность выживания за счет увеличения скорости резекции R0; резекция кишечника была выполнена с приемлемой предперационной заболеваемостью; утечка анастомоза произошла в 2% случаев, а послеоперационная смертность составила 4%.2015 International Institute of Anticancer Research (Dr. John G. Delinassios), All rights reserved
Results of Primary Cytoreductive Surgery in Advanced-stage Epithelial Ovarian Cancer: A Single-center Experience