Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Хронические лейкозы ( II часть)
Содержание
- 1. Хронические лейкозы ( II часть)
- 2. Парапротеинемические гемобластозы- - опухолевые заболевание
- 3. КлассификацияМножественная миеломаМакроглобулинемия ВальденстремаБолезнь тяжелых цепей
- 4. Множественная миелома
- 5. Множественная миеломаМножественная миелома – плазмо-клеточная
- 6. История вопроса1845г. -первые описания (МсIntyre и Watson)1848г.-
- 7. Слайд 7
- 8. Эпидемиология- ММ составляет 1% всех онкологических заболеваний
- 9. ЭтиологияЭтиологическая роль вирусов и ионизирующего излучения не
- 10. Объектом опухолевой трансформации является клетка-предшественница В-лимфоцитов, прошедшая этапы актигензависимой дифференцировки, способная дифференцироваться до плазмоцита, секретирующего PIg;
- 11. Хромосомные поломки при ММПочти все пациенты с
- 12. Патогенез миеломыСтромальная клетка к/мМоноклональная гаммапатия неустан.генезаИнтрамедул.очагиЭкстрамедул.очагиММ
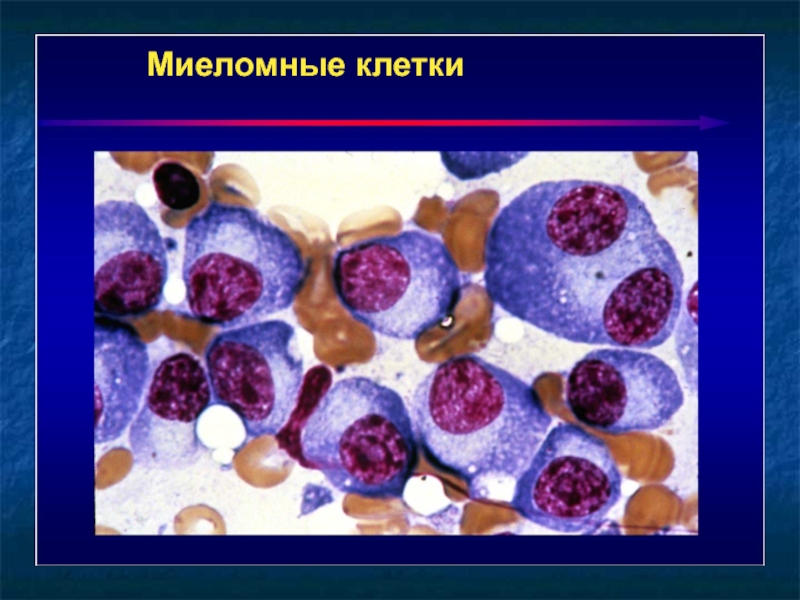
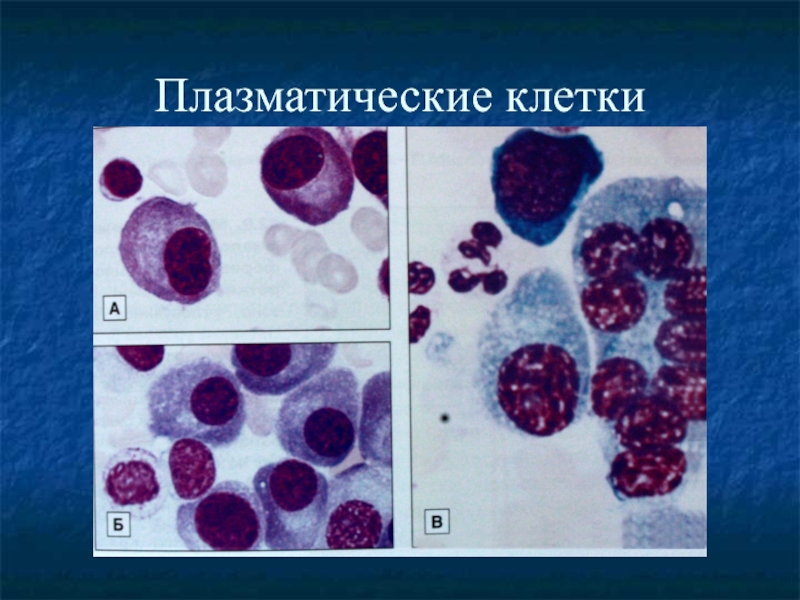
- 13. Миеломные клетки
- 14. Основные жалобыКостные боли: 58%Слабость: 32%Потеря веса: 24%Парестезии:
- 15. Клинические проявления миеломы
- 16. Слайд 16
- 17. Слайд 17
- 18. Показания к обследованию при подозрении на ММ
- 19. формирование монетных столбиков из эритроцитовСлабость, усталость, летаргия
- 20. Основные симптомы при диагностике МММоноклональный белок: 93%Костные
- 21. Слайд 21
- 22. Критерии диагноза.Гемограмма- анемия,
- 23. Лабораторная диагностика.Общий анализ крови с подсчетом тромбоцитов,
- 24. Лабораторная диагностика
- 25. Слайд 25
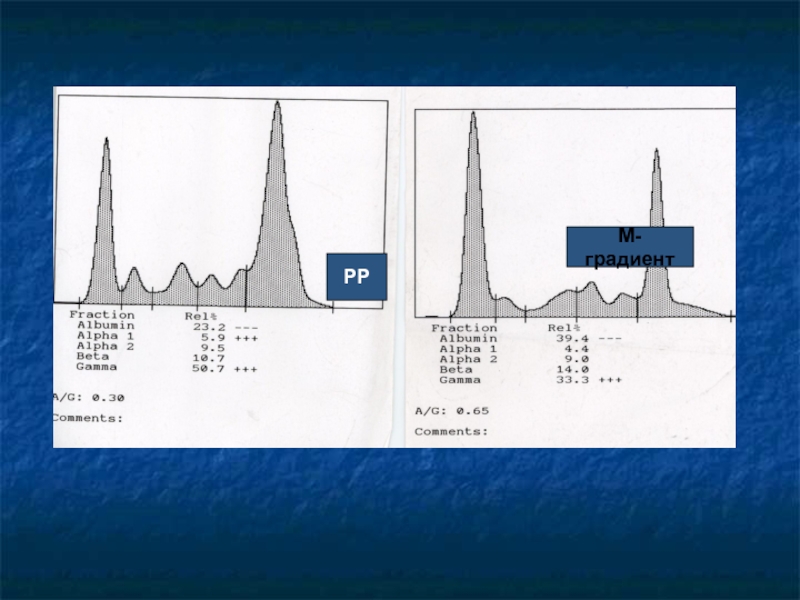
- 26. РРМ-градиент
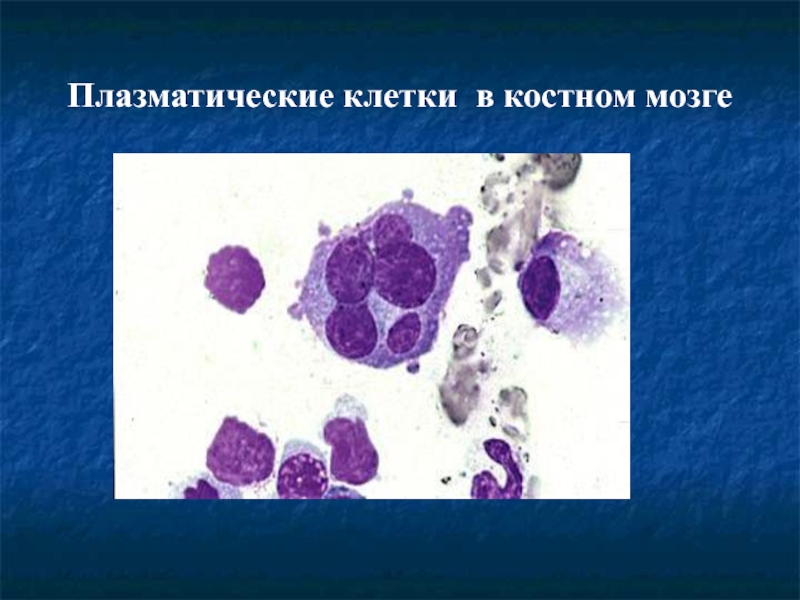
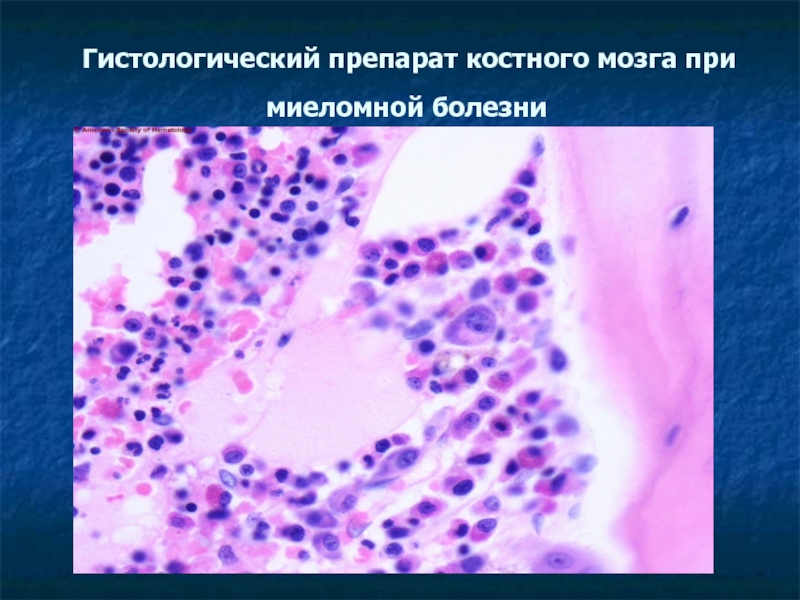
- 27. Плазматические клетки в костном мозге
- 28. Плазматические клетки
- 29. Гистологический препарат костного мозга при миеломной болезни
- 30. Флюоресцентная in situ гибридизация (FISH) показывает делецию
- 31. Косвенные признаки ММ.Ro-логический метод выявления остеодеструкций, но специфических изменений скелета не существует.Отсутствие остеодеструкций не исключает ММ.
- 32. Слайд 32
- 33. Слайд 33
- 34. Слайд 34
- 35. Слайд 35
- 36. Слайд 36
- 37. Слайд 37
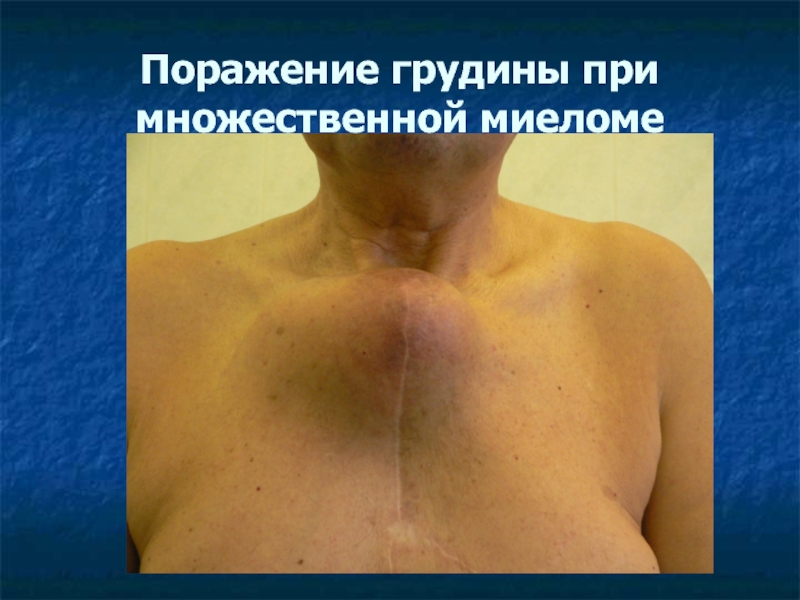
- 38. Поражение грудины при множественной миеломе
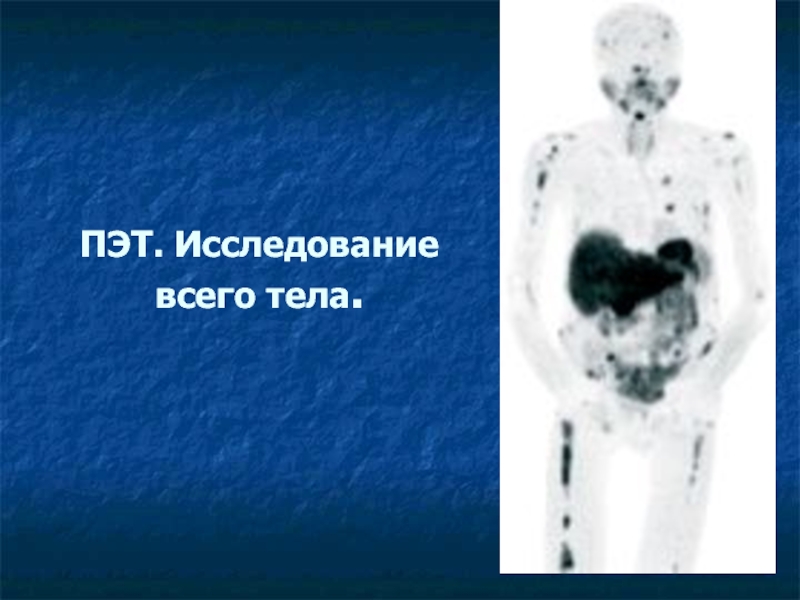
- 39. ПЭТ. Исследование всего тела.
- 40. Показания к лечению Критерием к
- 41. Принципы и цели терапииПринципы лечения-Подавление роста опухоли-Улучшение
- 42. Лечение ММХимиотерапия: используются протоколы: МР, СР, МСР, СVD, VAD;Сопроводительная терапия.Трансплантация костного мозга,
- 43. Иммуномодулирующая терапия ( талидомид, леналидомид).Механизмы действия
- 44. Критерии отбора пациентов на трансплантацию Возраст: менее
- 45. Трансплантация возможна? да
- 46. Лимфогранулематозгемобластоз с первичным поражением
- 47. Эпидемиология Заболеваемость в
- 48. ЭтиологияПричины возникновения болезни в настоящий момент окончательно
- 49. Морфология опухолевых клеток при ЛХ
- 50. Патогенез Клетки Березовского-Штернберга
- 51. Классификация.Лимфоцитарный с преобладанием лимфоидной ткани.Нодулярный (узловатый) склероз;Смешанно-клеточный;С подавлением лимфоидной ткани (лимфоцитарное истощение).
- 52. Стадии болезни. I
- 53. Стадии (продолжение) III стадия- поражение
- 54. Клиническая картина.Триада симптомов-профузные
- 55. Клиническая классификация (по
- 56. Стадия III -
- 57. Прогностические факторы.
- 58. Лабораторная диагностика:Гемограмма- нейтрофильный лейкоцитоз со сдвигом влево;Лимфоцитопения;Ускоренная
- 59. Диагностика Биопсия лимфатического узла
- 60. ЛечениеЛимфома Ходжкина – одна из немногих болезней,
- 61. Лечение:Химиотерапия.Лучевая терапия.Хирургический метод.
- 62. Наблюдение Физикальное обследование
- 63. БЛАГОДАРЮ ЗА ВНИМАНИЕ
- 64. Скачать презентанцию
Парапротеинемические гемобластозы- - опухолевые заболевание кроветворной ткани, представленные В-лимфоцитами и плазматическими клетками, которые синтезируют в избыточном количестве моноклональные (патологические) иммуноглобулины и их фрагменты (парапротеины).
Слайды и текст этой презентации
Слайд 2 Парапротеинемические гемобластозы-
- опухолевые заболевание кроветворной ткани, представленные
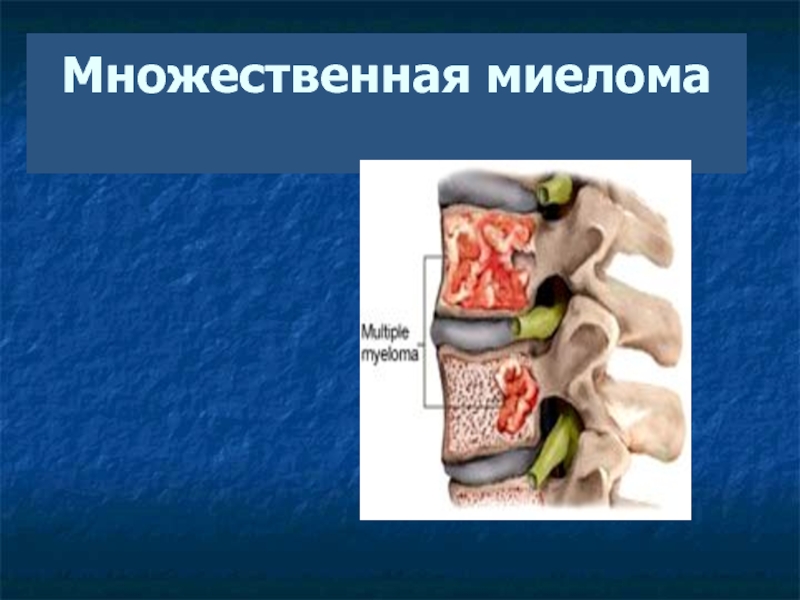
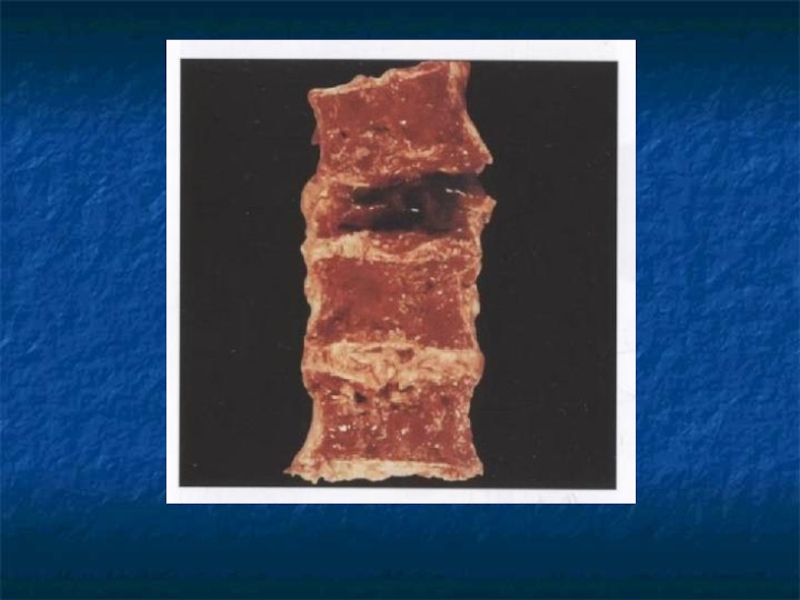
Слайд 5 Множественная миелома
Множественная миелома – плазмо-клеточная опухоль, характеризующаяся
деструктивным
поражением скелета,
развитием почечной недостаточности,
анемии и
гиперкальциемии ( CRAB)
Слайд 6История вопроса
1845г. -первые описания (МсIntyre и Watson)
1848г.- Bence-Jones описал некую
«живую материю» белкового происхождения, полученную из мочи пациента, выпадающую в
осадок при нагревании и вновь растворяющуюся при кипячении1873г- О.А.Рустицкий описал патологическую анатомию и гистологию заболевания, назвав его «множественной миеломой»
1889г- O.Kahler связал миелому Рустицкого с протеинурией Бенс-Джонса
1928г- М.И.Аринкин предложил методику прижизненного исследования костного мозга при помощи стернальной пункции
1931г- L.Lichtenstein, 1936г.- A.Ф. Коровников и Г.А.Алексеев – впервые выставлен диагноз ММ на основании данных стернальной пункции.
Слайд 8Эпидемиология
- ММ составляет 1% всех онкологических заболеваний и не многим
более 10% всех гемобластозов.
Частота ММ составляет 1- 4 случаев на
100 000 населения - Соотношение мужчин и женщин составляет 3:2
- Частота заболеваемости увеличивается с возрастом, средний возраст 69 лет
Слайд 9Этиология
Этиологическая роль вирусов и ионизирующего излучения не доказана
-Профессиональные вредности: пестициды,
инсектициды, продукты нефти, тяжелые металлы, асбест
- Радиация
-
Генетическая предрасположенность ( расовые различия, семейные случаи)- Хроническая антигенная стимуляция
( инфекции, воспаление, заболевания соединительной ткани, аутоиммунные процессы, аллергические заболевания, ревматоидный артрит)
Слайд 10Объектом опухолевой трансформации является клетка-предшественница В-лимфоцитов, прошедшая этапы актигензависимой дифференцировки,
способная дифференцироваться до плазмоцита, секретирующего PIg;
Слайд 11Хромосомные поломки при ММ
Почти все пациенты с ММ имеют хромосомные
аномалии
Нарушения кариотипа: 8-30% пациентов
– Плохой прогноз: моносомия 13 или гиподиплоидия
–
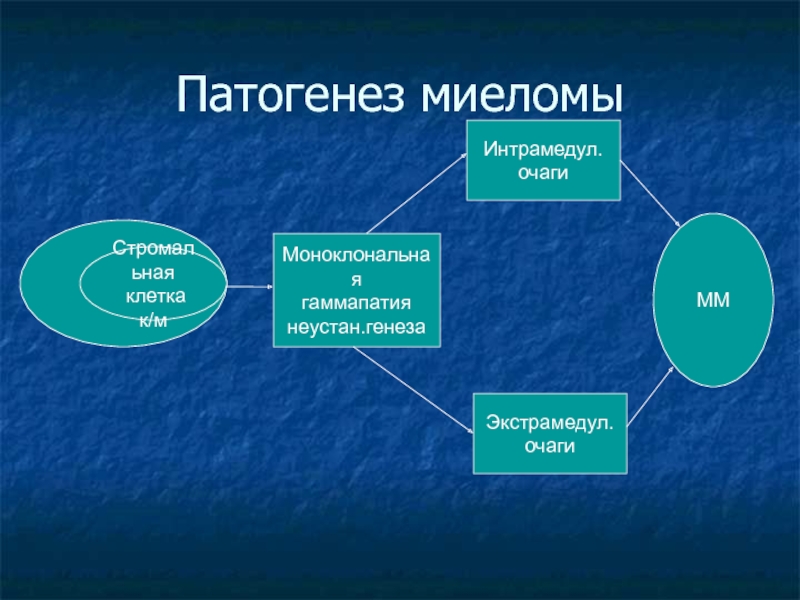
Хороший прогноз: нормальный кариотип, гипердиплоидияСлайд 12Патогенез миеломы
Стромальная
клетка к/м
Моноклональная
гаммапатия
неустан.генеза
Интрамедул.
очаги
Экстрамедул.
очаги
ММ
Слайд 14Основные жалобы
Костные боли: 58%
Слабость: 32%
Потеря веса: 24%
Парестезии: 5%
Около 20% пациентов
не имеют симптомов или они слабо выражены
Слайд 18Показания к обследованию при подозрении на ММ
Возраст старше 40 лет и любое из следующего:
Необъяснимая
боль в спине или костяхНеобъяснимые переломы
Остеолитические поражения или остеопения
Анемия
Почечная недостаточность
Необъяснимая протеинурия
Необъяснимые отеки или асцит
Нефротический синдром
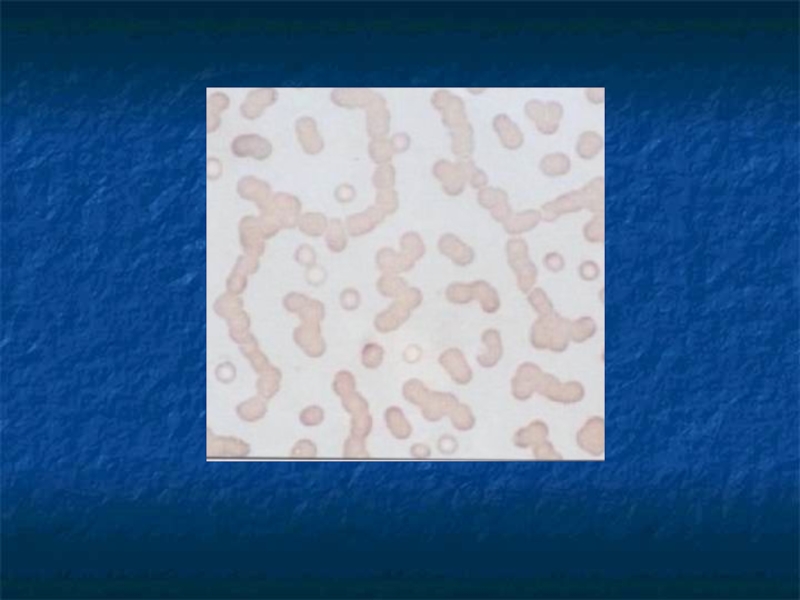
Слайд 19формирование монетных столбиков из эритроцитов
Слабость, усталость, летаргия
Рецидивирующие инфекции
Ускорение
СОЭ
Необъяснимая периферическая нейропатия
Гиперкальциемия
Гипервязкость
Приобретенные нарушения свертывания крови
Ортостатическая гипотензия
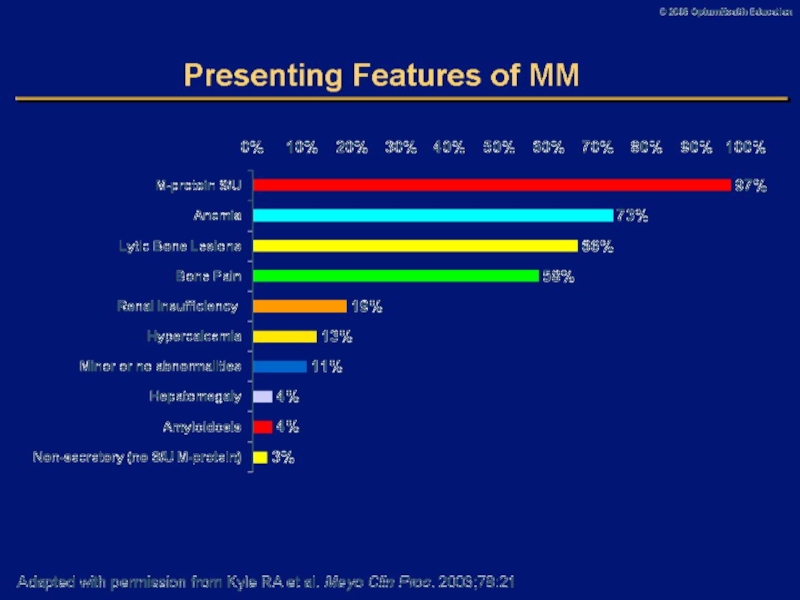
Слайд 20Основные симптомы при диагностике ММ
Моноклональный белок: 93%
Костные деструкции: 67%
Плазмацитоз в
костном мозге: 96%
Анемия (нормохромная нормоцитарная): 73%
Гиперкальциемия: 13%
Слайд 22 Критерии диагноза.
Гемограмма- анемия, ускоренная СОЭ, плазматические
клетки (более 5%);
Миелограмма- увеличение плазматических клеток (более 10%);
Парапротеинемия при БАК
(М-градиент в крови)Белок Бенс-Джонса в моче;
моноклоновый иммуноглобулин в сыворотке крови и в моче методом электрофореза.
Слайд 23Лабораторная диагностика.
Общий анализ крови с подсчетом тромбоцитов, ретикулоцитов;
ОАМ;
Определение общего белка
сыворотки крови;
Электрофорез сывороточных белков и определение М-компонента;
Определение суточной потери белка
с мочой- при наличии протеинурии;Слайд 24Лабораторная диагностика (продолжение).
БАК-
креатинин, мочевина, мочевая кислота, кальций, ЛДГ, щелочная фосфатаза, Bi, трансаминазы,
СРБ;Рентгенография всех костей скелета, кроме дистальных отделов конечностей, если нет клинических признаков поражения в этих областях);
Иммуннофенотипирование миеломных клеток (CD20+++, CD56(-));
Цитогенетическое исследование (транслокации, хромосомные аномалии, делеция или утрата 13 хромосомы и др.).
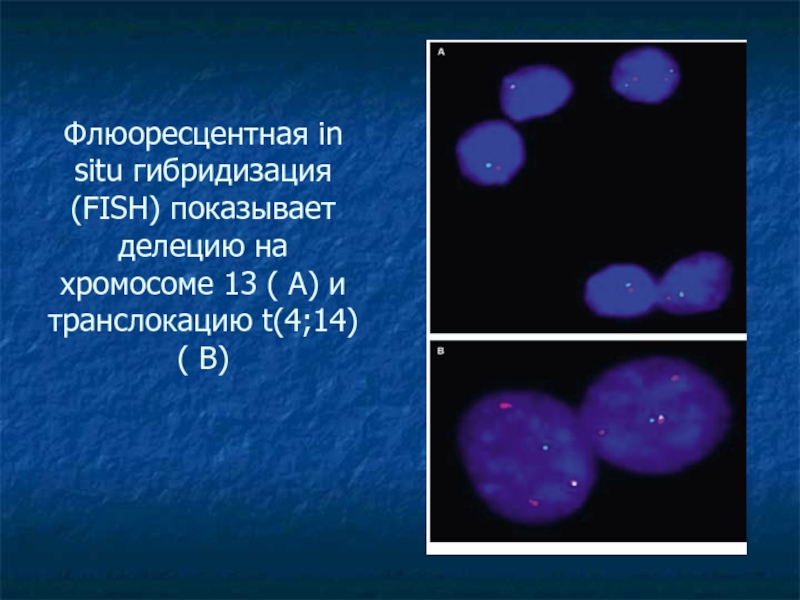
Слайд 30Флюоресцентная in situ гибридизация (FISH) показывает делецию на хромосоме 13
( А) и транслокацию t(4;14) ( В)
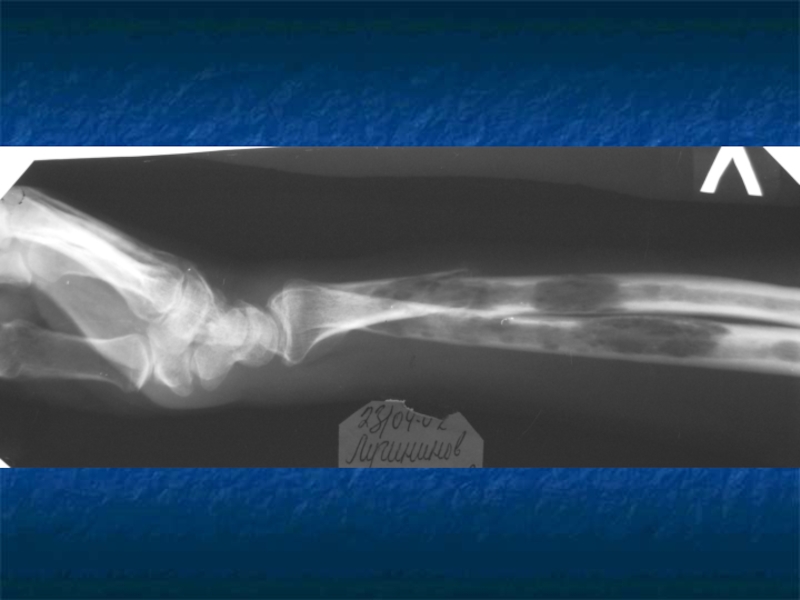
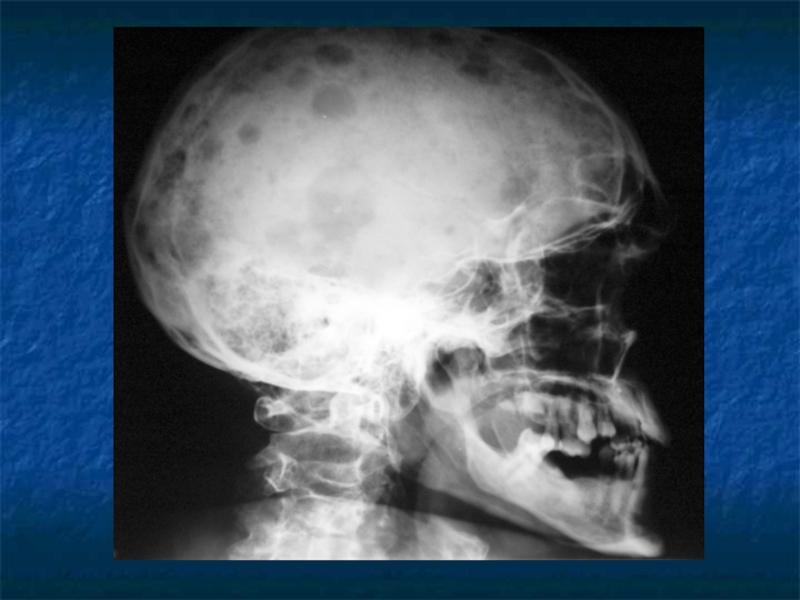
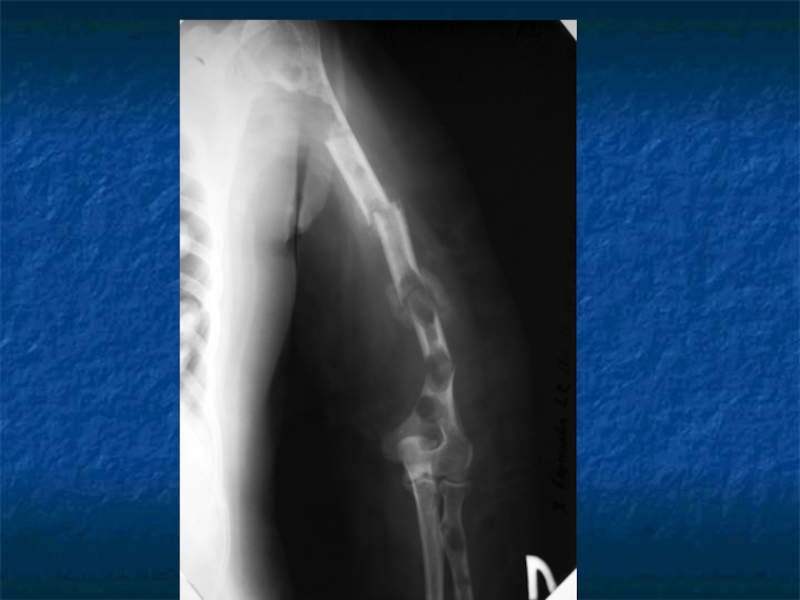
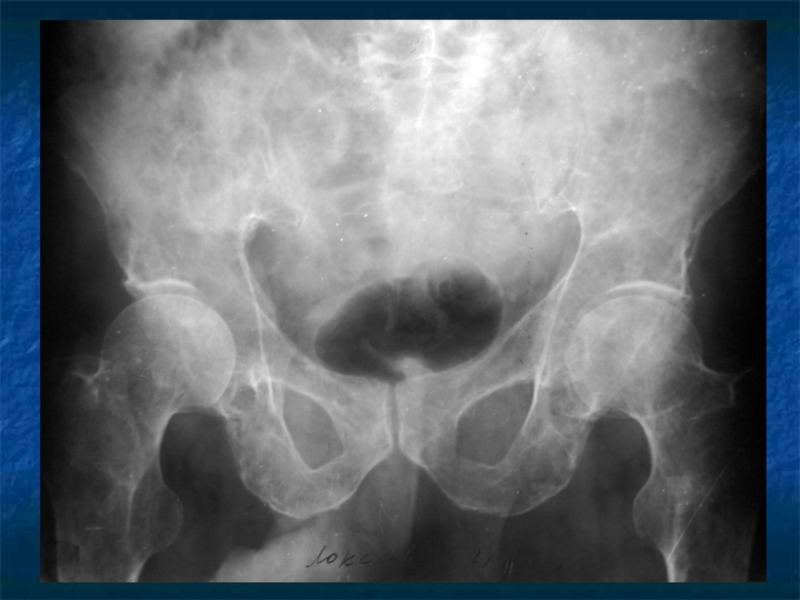
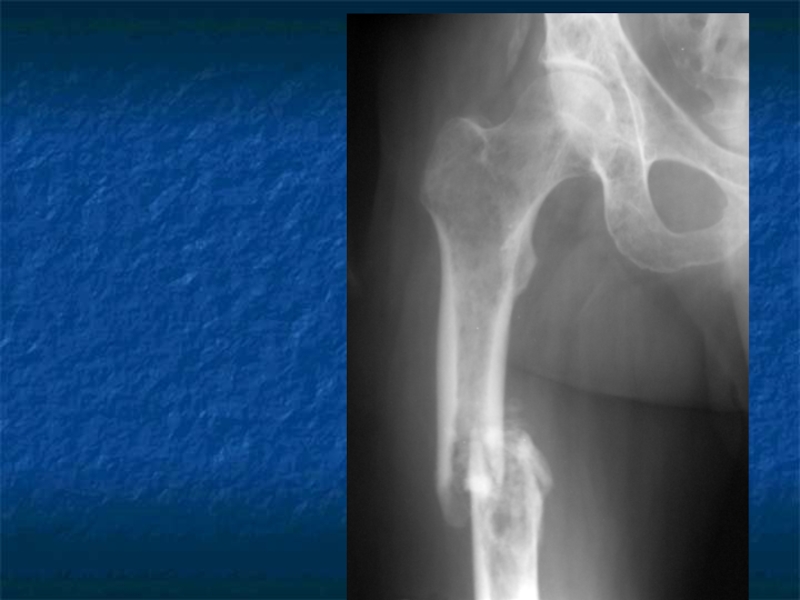
Слайд 31Косвенные признаки ММ.
Ro-логический метод выявления остеодеструкций, но специфических изменений скелета
не существует.
Отсутствие остеодеструкций не исключает ММ.
Слайд 40Показания к лечению
Критерием к началу проведения системной терапии
у пациентов с множественной миеломой является признаки прогрессирования заболевания с
появлением органных пораженийСлайд 41Принципы и цели терапии
Принципы лечения
-Подавление роста опухоли
-Улучшение качества жизни
-Увеличение общей
выживаемости
Цели терапии
Быстрый контроль заболевания и лечение осложнений, связанных с
заболеванием (анемия, гиперкальциемия, поражение почек)Хорошая переносимость с минимальной и контролируемой токсичностью
Снижение риска ранней смертности
Сохранение возможности для заготовки стволовых клеток крови, если планируется проведение аутологичной трансплантации.
Слайд 42Лечение ММ
Химиотерапия: используются протоколы: МР, СР, МСР, СVD, VAD;
Сопроводительная терапия.
Трансплантация
костного мозга,
Слайд 43Иммуномодулирующая терапия
( талидомид, леналидомид).
Механизмы действия
подавление адгезии, продукции цитокинов,
ангиогенеза
увеличение пролиферации Т-клеток, клеточную цитотоксичность,
Побочные эффекты
Тератогенный эффект (Т)
Периферическая нейропатия
(Т)Седация, слабость (Т)
Венозные тромбозы ( Т, Л)
Миелосупрессия (Т,Л ( нейтропения))
Слайд 44Критерии отбора пациентов на трансплантацию
Возраст: менее 70 лет для аутологичной
трансплантации
Соматический статус: статус по Карновскому более 70%, фракция выброса
левого желудочка более 40%, клиренс креатинина более 50мл/мин, ОВФ1 более 40%, удовлетворительная функция печени.Ответ на индукционную терапию: оптимальное время для проведения заготовки стволовых клеток после 4-6 курсов индукционной терапии. Отсутствие ответа на индукционную терапию не является противопоказанием для проведения аутологичной трансплантации костного мозга.
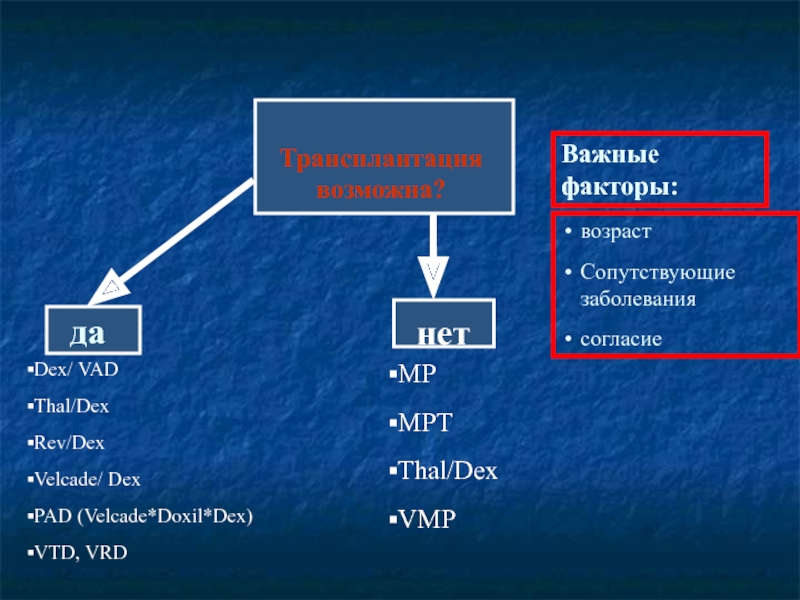
Слайд 45 Трансплантация возможна?
да
нет
Dex/ VAD
Thal/Dex
Rev/Dex
Velcade/ Dex
PAD (Velcade*Doxil*Dex)
VTD, VRD
возраст
Сопутствующие заболевания
согласие
MP
MPT
Thal/Dex
VMP
Важные факторы:
Слайд 46 Лимфогранулематоз
гемобластоз с первичным поражением лимфоидной ткани, в
основе которого лежит опухолевая пролиферация лимфоидных клеток с образованием специфической
гранулемы.Впервые описан как самостоятельное заболевание в 1832 г., английским врачом Ходжкиным, с 1965 г. заболевание называется болезнью Ходжкина.
Слайд 47Эпидемиология
Заболеваемость в России -
2,3 на 100000 населения.
Болеют лимфомой Ходжкина люди любого возраста.
Мужчины заболевают чаще, чем женщины.
Отмечается два пика заболеваемости в зависимости от возраста.
-большинство пациентов заболевают на третьем десятилетии жизни,
-другой небольшой подъем заболева-емости отмечается около 55 лет.
Слайд 48Этиология
Причины возникновения болезни в настоящий момент окончательно не установлены. Описаны
редкие случаи заболевания лимфомой в одной семье.
Больные, перенесшие инфекционный
мононуклеоз, заболевают ЛГМ в несколько раз чаще, чем бессимптомные носители.
Слайд 49Морфология опухолевых клеток при ЛХ
Опухолевым субстратом ЛХ являются клетки Березовского-Штернберга и их
варианты, расположенные среди реактивного клеточного компонента, составляющего до 99% клеточной популяции, включающей лимфоциты, гистиоциты, нейтрофильные и эозинофильные лейкоциты, плазмоциты, фибробласты.Слайд 50Патогенез
Клетки Березовского-Штернберга и клетки Ходжкина
происходят из генетически измененных В-лимфоцитов зародышевого центра, утративших способность к
апоптозу и синтезу Ig. Эти генетически измененные клеточные элементы являются мишенями иммунной атаки со стороны нормальных Т-лимфоцитов, которые составляют основную клеточную популяцию пораженных лимфоузлов и, возможно, сдерживают опухолевый рост. Истощение пула Т-лимфоцитов по мере развития лимфогранулематоза сопровождается ослаблением клеточного иммунного ответа и прогрессирующим ростом опухолиСлайд 51 Классификация.
Лимфоцитарный с преобладанием лимфоидной ткани.
Нодулярный (узловатый) склероз;
Смешанно-клеточный;
С подавлением лимфоидной
ткани (лимфоцитарное истощение).
Слайд 52 Стадии болезни.
I стадия- поражение одной
или двух смежных групп лимфоузлов, расположенных по одну сторону диафрагмы,
или поражение одного внелимфатического органа.II стадия- поражение двух или более несмежных групп лимфоузлов, расположенных по одну сторону диафрагмы ;
Слайд 53 Стадии (продолжение)
III стадия- поражение лимфоузлов любых областей
по обе стороны диафрагмы, сопровождаемое локализованным поражением одного внелимфатического органа.
IVстадия- диффузное поражение одного или более внелимфатических органов (печень, легкие, костный мозг) с поражением лимфоузлов или без такового.Слайд 54 Клиническая картина.
Триада симптомов-профузные ночные поты, лихорадка,
генерализованный кожный зуд.
Похудание на 10% и более за 6 мес.
Лимфаденопатия
(лимфоузлы плотно-эластической консистенции, спаянные между собой с образованием конгломератов – «мешок с картошкой»).Слайд 55 Клиническая классификация (по стадиям)
Стадия I - поражение
одной лимфатической зоны или одного лимфоидного органа (селезенка, тимус, Вальдейрово кольцо) или одного нелимфоидного органаСтадия II - поражение 2 и более лимфатических зон с одной стороны диафрагмы (поражение воротных лимфоузлов с обеих сторон диафрагмы относят ко II стадии);
Слайд 56
Стадия III - поражение лимфатических зон
с обеих сторон диафрагмы (III), которое может сопровождаться поражением селезенки
(IIIs) или локальным поражением по протяжению только одного нелимфоидного органа/ткани или и того и другого (IIISE);Стадия IV-диффузное или диссемини-рованное поражение нелимфоидного органа (или ткани), с поражением лимфоузлов или без него
Слайд 57 Прогностические факторы.
Неблагоприятные:
Наличие крупных более
5 см. лимфоузлов, образующих конгломераты;
Массивное поражение селезенки;
Ускоренная СОЭ- более 30
мм\ч;Повышение фибриногена более 5 г\л;
Повышение гаптоглобина более 1,5 мг\%;
Повышение церуплазмина более 0,4 ед.
Возраст старше 50 лет.
Слайд 58Лабораторная диагностика:
Гемограмма- нейтрофильный лейкоцитоз со сдвигом влево;
Лимфоцитопения;
Ускоренная СОЭ;
Миелограмма или трепанат
костного мозга- клетки Березовского- Штернберга.
БАК- увеличение фибриногена, гипогаммаглобулинемия.
Гистологическое исследование лимфоузла-
выявление клеток Березовского-Штернберга.Слайд 59Диагностика
Биопсия лимфатического узла
Рентгенограмма легких в
2 проекциях
Компьютерная томография органов шеи, ОГК, ОБП, ОМТ
Сканирование костей и при показаниях – рентгенография костей. ПЭТ
Слайд 60Лечение
Лимфома Ходжкина – одна из немногих болезней, смертность от которой
была существенно снижена в последние десятилетия.
Достижения:
1) Вылечивается 85
– 90% всех больных со всеми стадиями.
2) Не вылечивается 10 – 15%
3) Лечение приводит к развитию вторичных опухолей у 5 – 10% больных Слайд 62
Наблюдение
Физикальное обследование и лабораторные анализы выполняются :
-каждые 3 месяца в течение 1 года,
- раз в полгода до 3 лет наблюдения
-далее – ежегодно.
КТ необходима для подтверждения полной ремиссии, дополнительные КТ не рекомендуются, за исключением исследований, необходимых для оценки резидуальной болезни.
После радиотерапии с вовлечением ткани молочной железы, женщины старше 40 лет должны проходить стандартный скрининг (клинический + маммография) для исключения развития вторичного рака молочной железы