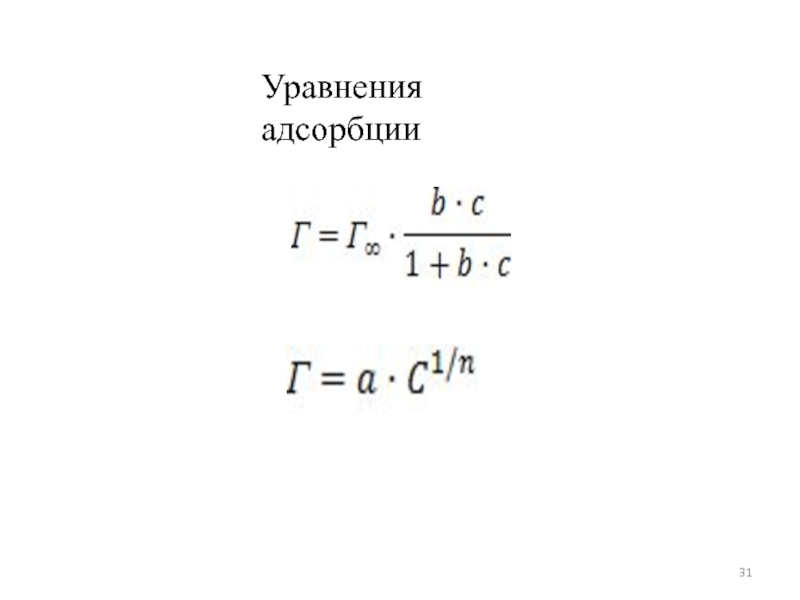Слайд 1Изучение процессов адсорбционно-десорбционных взаимодействий фосфатов кальция и аминокислот
Головченко К.
К.
2 курс, ХХМ-601-О
Научный руководитель:
Голованова О.А., проф., д.г.-м.н.
ОмГУ им. Ф.М. Достоевского
Кафедра неорганической химии
Омск 2018
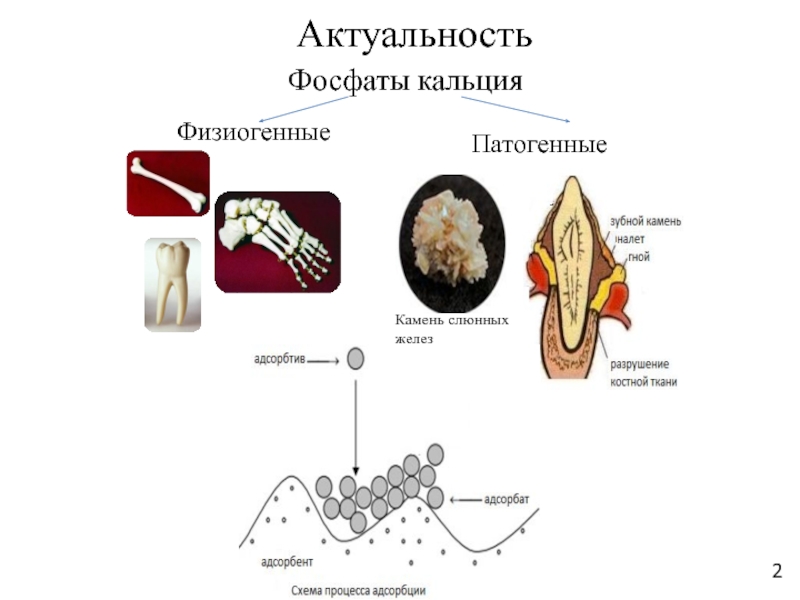
Слайд 2Актуальность
Фосфаты кальция
Патогенные
Физиогенные
Камень слюнных желез
Слайд 3Цель:
исследовать адсорбционно-десорбционные взаимодействия аминокислот с фосфатами кальция и их смесями
при варьировании рН раствора.
Задачи:
Синтез брушита и гидроксилапатита, изучение их
свойств;
Изучение адсорбционного взаимодействия аминокислот на поверхности брушита и гидроксилапатита;
Установление десорбционного взаимодействия аминокислот с поверхностями брушита и гидроксилапатита;
Определение адсорбционно-десорбционного взаимодействия аминокислот с поверхностями смесей на основе брушита и гидроксилапатита.
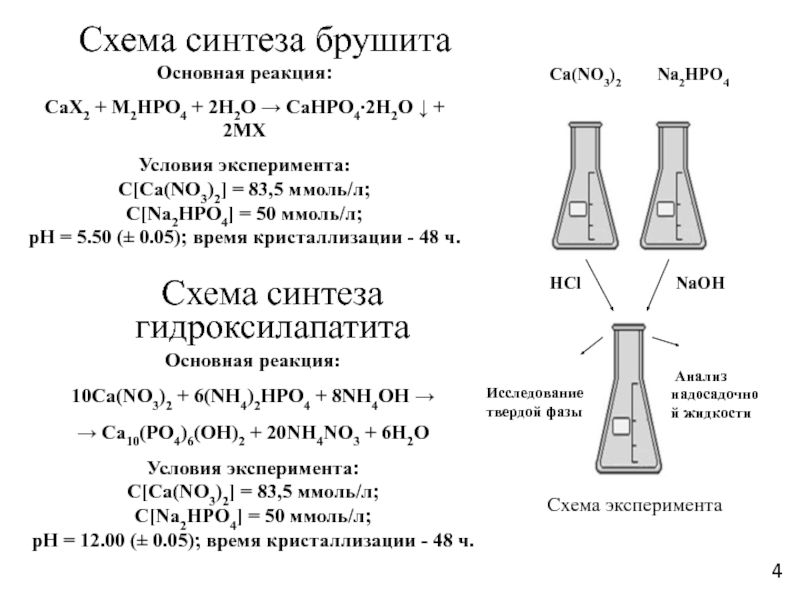
Слайд 4Схема синтеза гидроксилапатита
Основная реакция:
10Ca(NO3)2 + 6(NH4)2HPO4 + 8NH4OH →
→ Ca10(PO4)6(OH)2 + 20NH4NO3 + 6H2O
Условия эксперимента:
С[Са(NO3)2] = 83,5
ммоль/л;
C[Nа2НРО4] = 50 ммоль/л;
рН = 12.00 (± 0.05); время кристаллизации - 48 ч.
Схема синтеза брушита
Основная реакция:
CaX2 + M2HPO4 + 2Н2О → CaHPO4∙2Н2О ↓ + 2MX
Условия эксперимента:
С[Са(NO3)2] = 83,5 ммоль/л;
C[Nа2НРО4] = 50 ммоль/л;
рН = 5.50 (± 0.05); время кристаллизации - 48 ч.
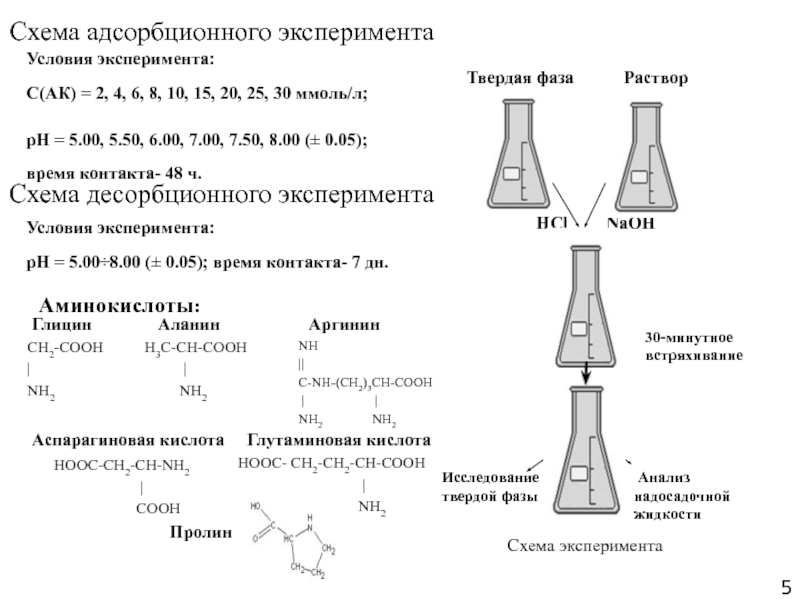
Слайд 5Условия эксперимента:
С(АК) = 2, 4, 6, 8, 10, 15,
20, 25, 30 ммоль/л;
рН = 5.00, 5.50, 6.00, 7.00, 7.50,
8.00 (± 0.05); время контакта- 48 ч.
Аминокислоты:
30-минутное встряхивание
Схема адсорбционного эксперимента
Условия эксперимента:
рН = 5.00÷8.00 (± 0.05); время контакта- 7 дн.
Схема десорбционного эксперимента
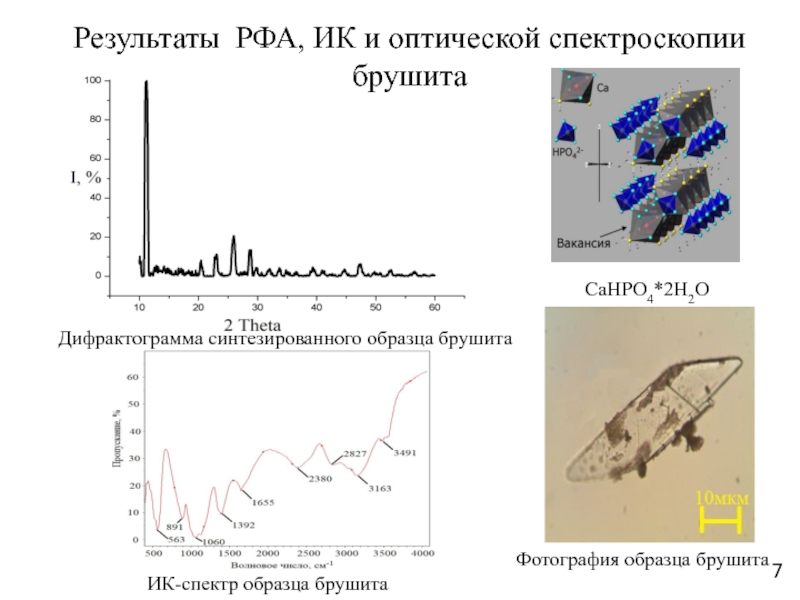
Слайд 7Дифрактограмма синтезированного образца брушита
ИК-спектр образца брушита
Фотография образца брушита
Результаты РФА, ИК
и оптической спектроскопии брушита
СaHPO4*2H2O
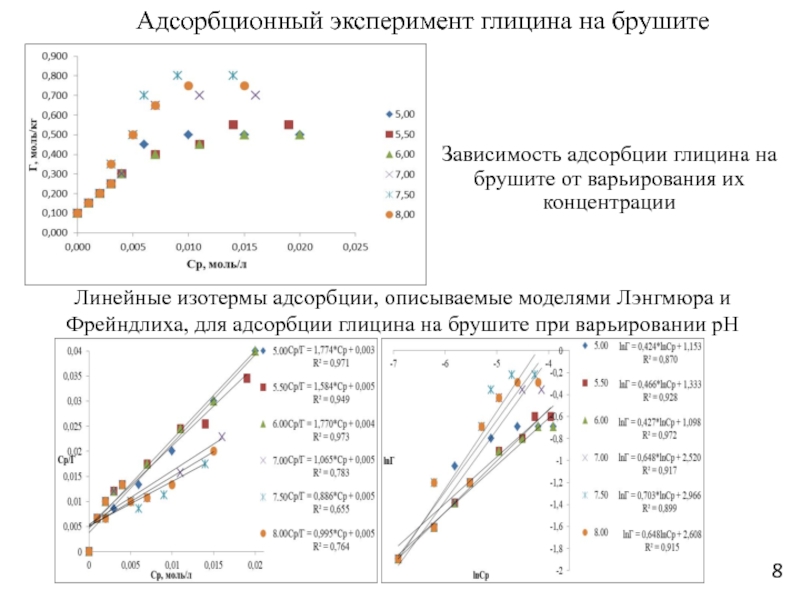
Слайд 8Зависимость адсорбции глицина на брушите от варьирования их концентрации
Линейные изотермы
адсорбции, описываемые моделями Лэнгмюра и Фрейндлиха, для адсорбции глицина на
брушите при варьировании pН
Адсорбционный эксперимент глицина на брушите
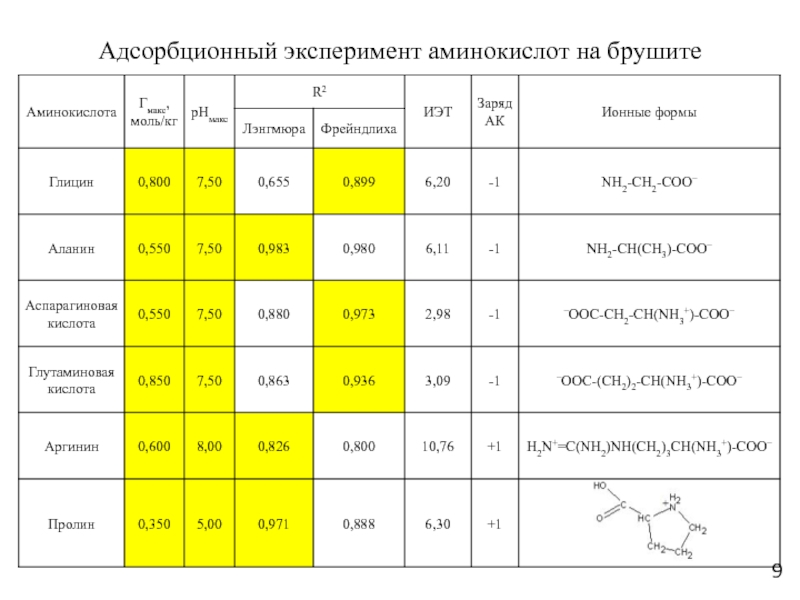
Слайд 9Адсорбционный эксперимент аминокислот на брушите
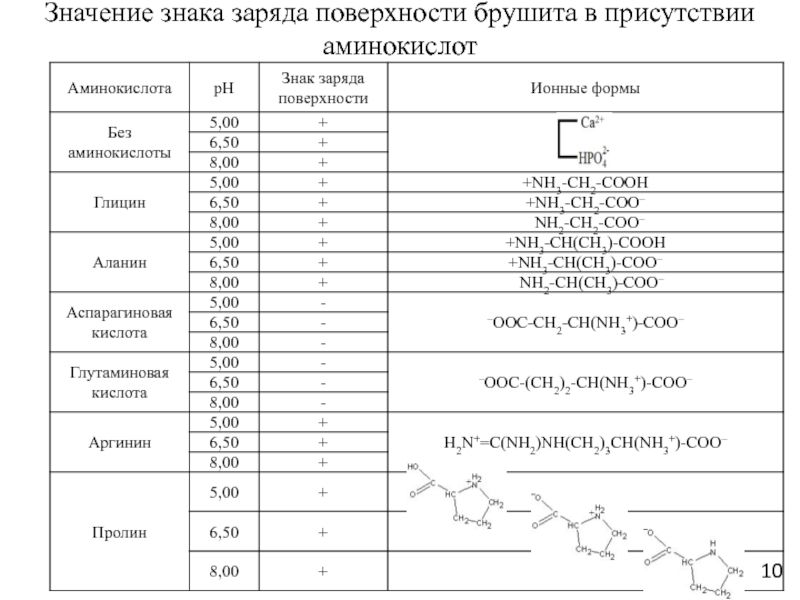
Слайд 10Значение знака заряда поверхности брушита в присутствии аминокислот
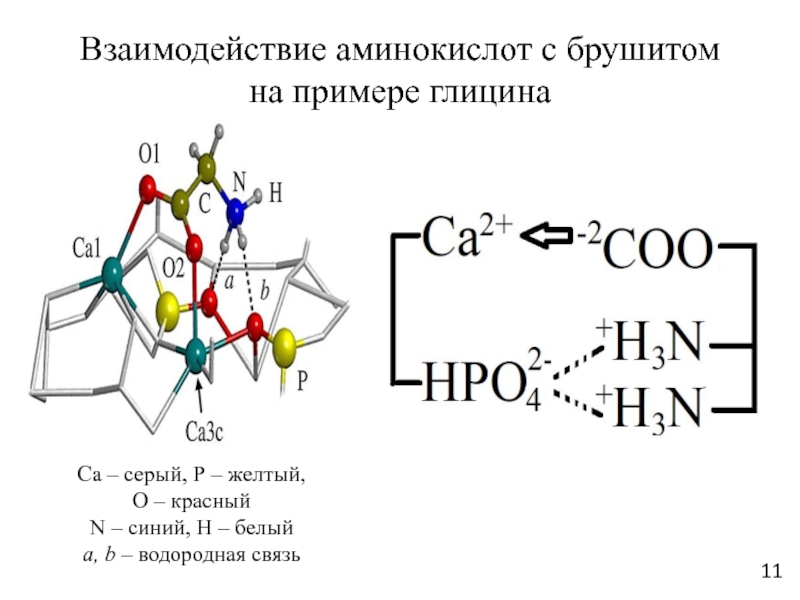
Слайд 11Взаимодействие аминокислот с брушитом
на примере глицина
Са – серый, Р –
желтый,
О – красный
N – синий, Н – белый
а, b
– водородная связь
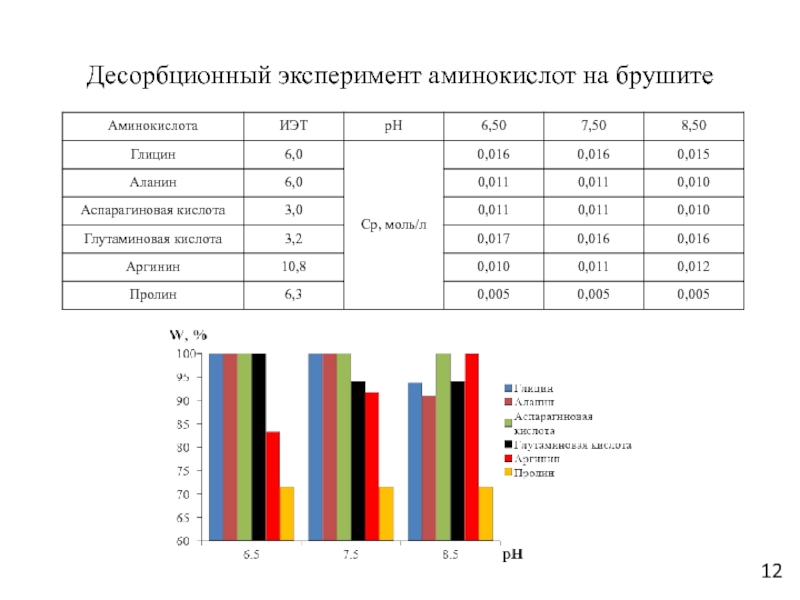
Слайд 12Десорбционный эксперимент аминокислот на брушите
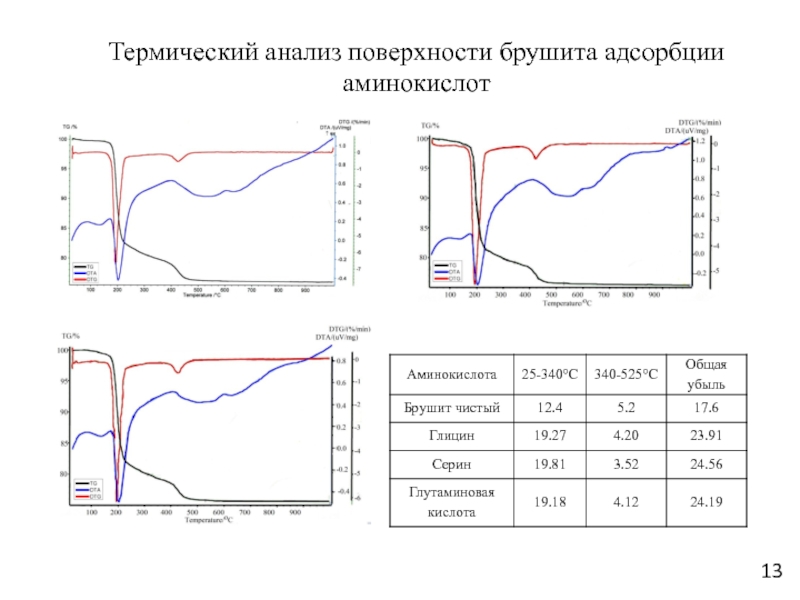
Слайд 13Термический анализ поверхности брушита адсорбции аминокислот
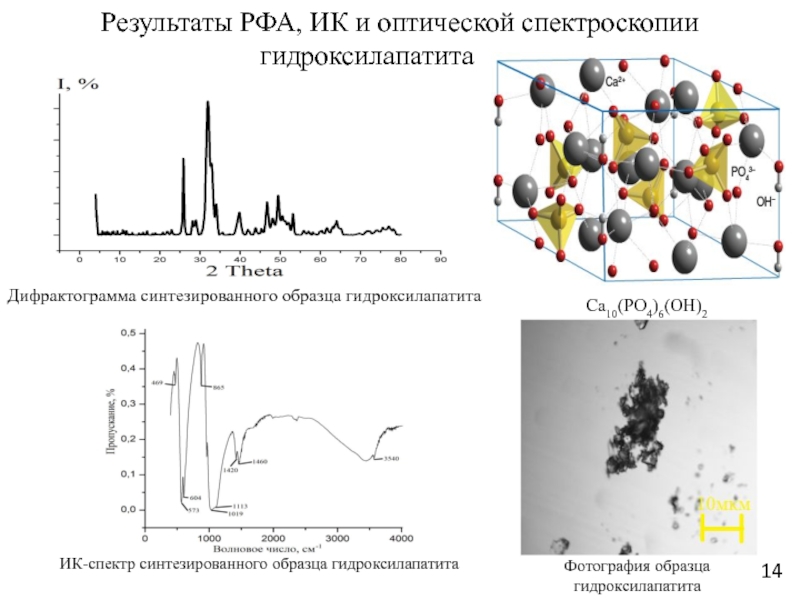
Слайд 14Результаты РФА, ИК и оптической спектроскопии гидроксилапатита
ИК-спектр синтезированного образца
гидроксилапатита
Фотография образца гидроксилапатита
Са10(РО4)6(ОН)2
Дифрактограмма синтезированного образца гидроксилапатита
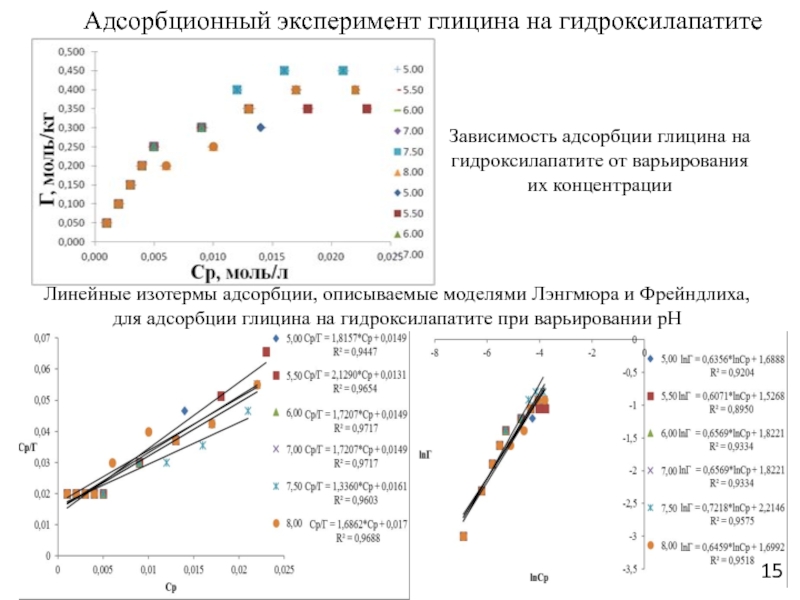
Слайд 15Зависимость адсорбции глицина на гидроксилапатите от варьирования их концентрации
Линейные изотермы
адсорбции, описываемые моделями Лэнгмюра и Фрейндлиха, для адсорбции глицина на
гидроксилапатите при варьировании pН
Адсорбционный эксперимент глицина на гидроксилапатите
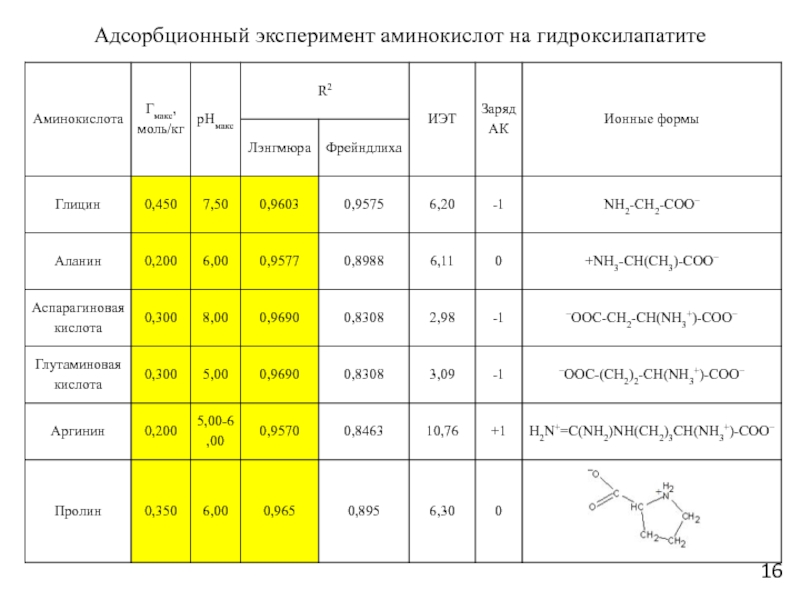
Слайд 16Адсорбционный эксперимент аминокислот на гидроксилапатите
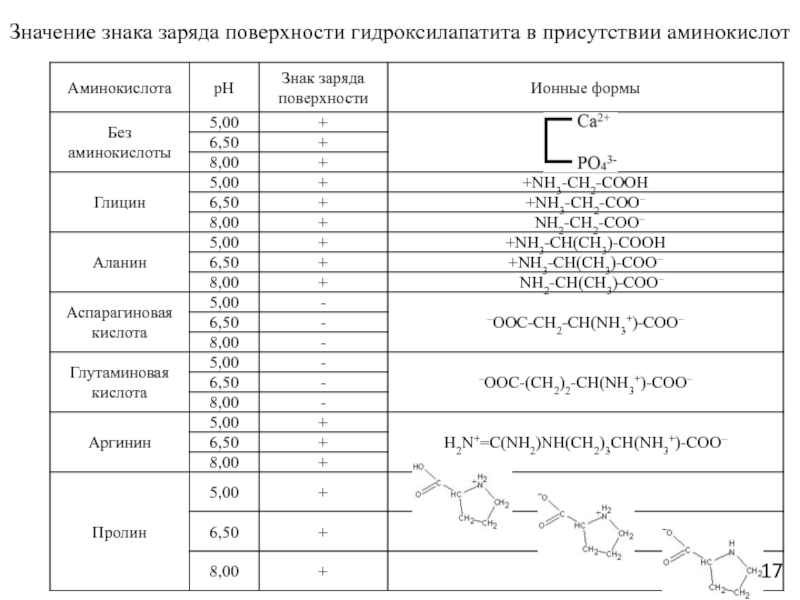
Слайд 17Значение знака заряда поверхности гидроксилапатита в присутствии аминокислот
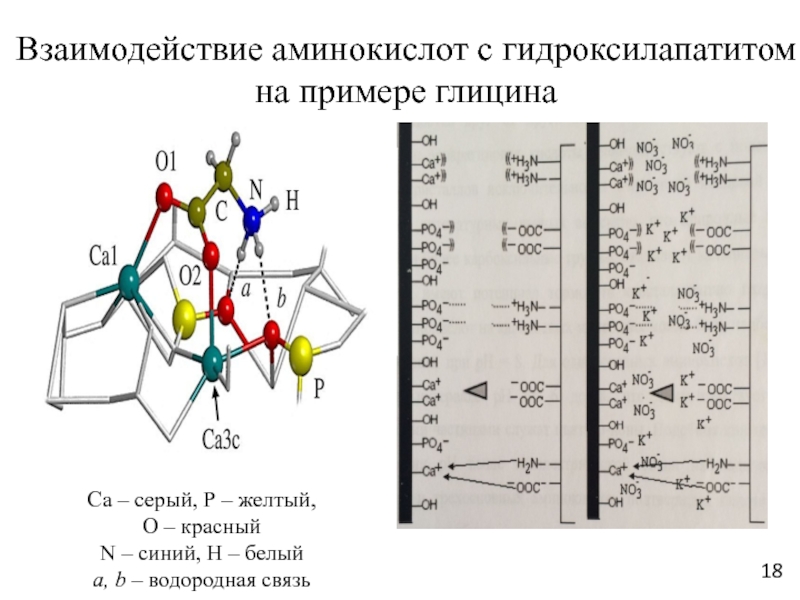
Слайд 18Взаимодействие аминокислот с гидроксилапатитом
на примере глицина
Са – серый, Р –
желтый,
О – красный
N – синий, Н – белый
а, b
– водородная связь
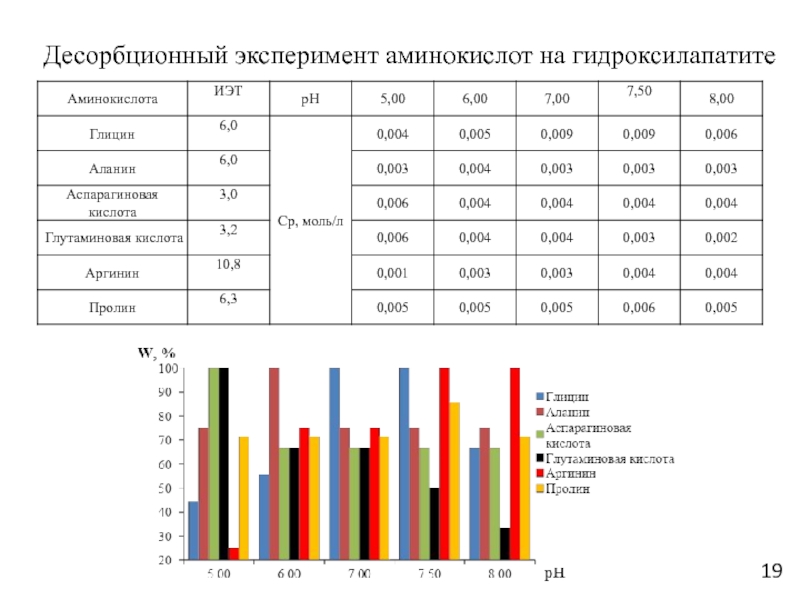
Слайд 19Десорбционный эксперимент аминокислот на гидроксилапатите
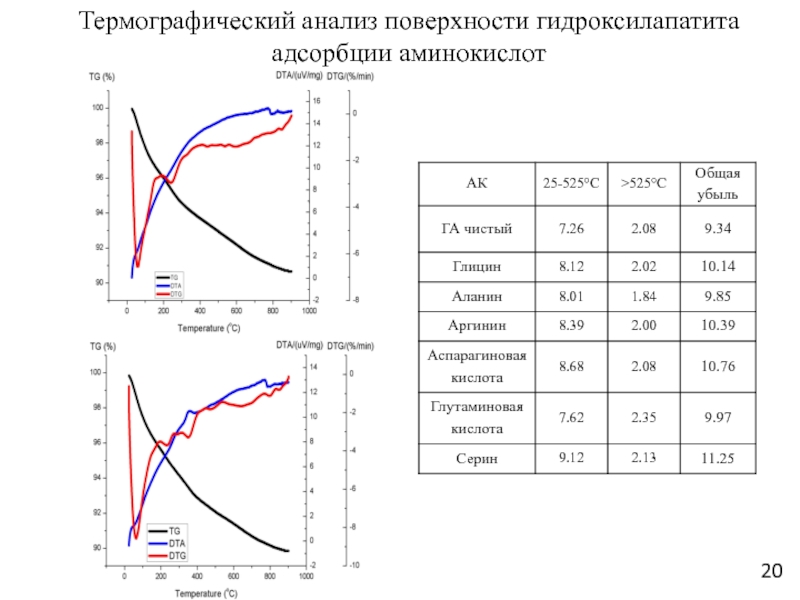
Слайд 20Термографический анализ поверхности гидроксилапатита адсорбции аминокислот
Слайд 21Сравнение адсорбционно-десорбционного взаимодействия аминокислот с поверхностями брушита и гидроксилапатита
Брушит адсорбция:
пролин
кислота<глицин.
Гидроксилапатит десорбция: глутаминовая кислота< аспарагиновая кислота<аланин<пролин<аргинин=глицин.
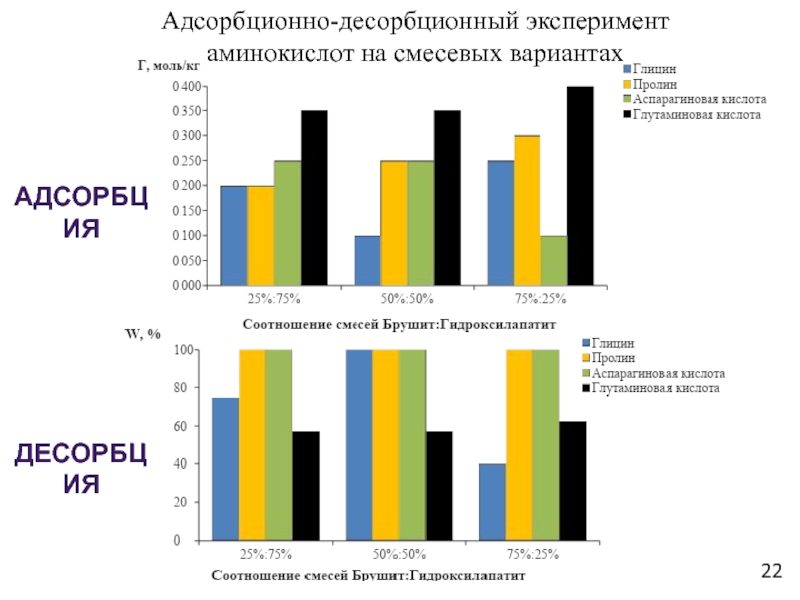
Слайд 22Адсорбционно-десорбционный эксперимент
аминокислот на смесевых вариантах
Десорбция
Адсорбция
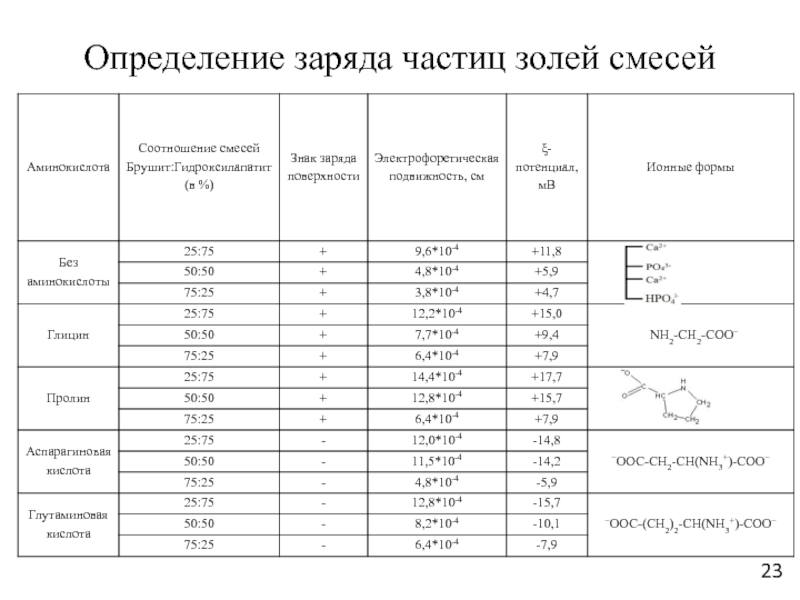
Слайд 23Определение заряда частиц золей смесей
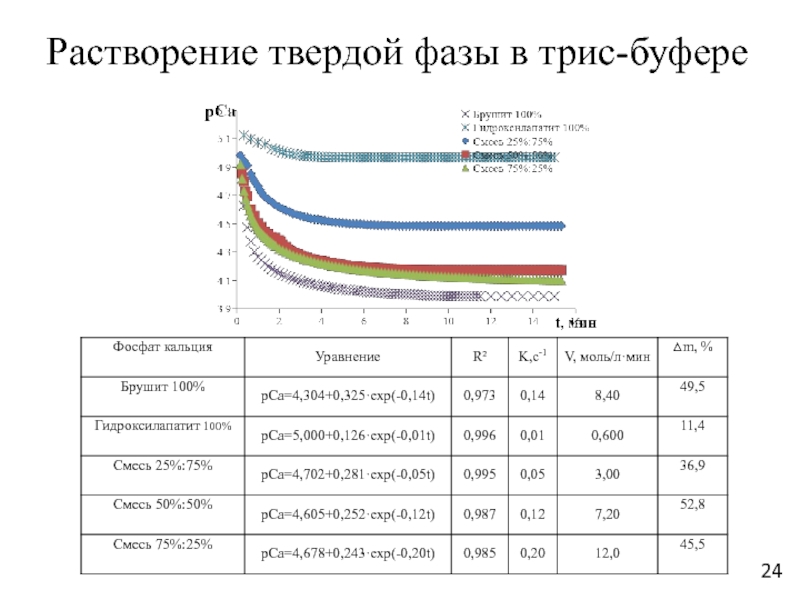
Слайд 24Растворение твердой фазы в трис-буфере
Слайд 25Выводы
Осуществлен синтез брушита, строение которого подтверждено методами РФА и ИК-спектроскопии.
Определен знака заряда поверхности брушита методом электрофореза – положительный. Изучено
его динамическое растворение в трис-буфере.
Исследована адсорбция аминокислот на брушите и показано, что для глицина, аланина, аспарагиновой и глутаминовой кислот максимальная адсорбция происходит при рН = 7,50 ± 0,05, а для аргинина при рН= 8,00 ± 0,05, пролина при рН = 5,00 ± 0,05.
Установлено, что адсорбция глицина, аспарагиновой и глутаминовой кислот адсорбция описывается моделью Фрейндлиха; а аланина, пролина и аргинина адсорбция - моделью Лэнгмюра. Рассчитанные значения энергии Гиббса адсорбции согласуются со значениями максимальной адсорбции.
Проведена десорбция аминокислот с поверхности брушита, установлено, что десорбция достигает предела при рН близком к изоэлектрической точке аминокислоты.
Осуществлен синтез гидроксилапатита, строение которого подтверждено методами РФА и ИК-спектроскопии. Определены их параметры кристаллических решеток: a = 9.426±0.002 Å, с = 6.892±0.002 Å и рассчитаны размеры кристаллитов D = 15,3 нм. Определен знака заряда поверхности гидроксилапатита методом электрофореза – положительный. Изучено его динамическое растворение в трис-буфере.

Слайд 26Исследована адсорбция аминокислот на гидроксилапатите и показано, что максимальная адсорбция
для глицина происходит при рН = 7,50 ± 0,05; аланина
и пролина при рН = 6,00 ± 0,05; аргинина при рН = 5,00-6,00 ± 0,05; аспарагиновой кислоты при рН = 8,00 ± 0,05; глутаминовой кислоты при рН = 5,00 ± 0,05.
Установлено, что адсорбция аминокислот описывается моделью Лэнгмюра. Рассчитанные значения энергии Гиббса адсорбции согласуются со значениями максимальной адсорбции.
Проведена десорбция аминокислот с поверхности гидроксилапатита, установлено, что десорбция достигает предела при рН близком к изоэлектрической точке аминокислоты.
Проведен адсорбционный эксперимент аминокислот на поверхностях смесей на основе брушита и гидроксилапатита при рН = 7,40 ± 0,05 и установлено, что для глицина, пролина и глутаминовой кислоты максимальная адсорбция наступает при соотношении брушита : гидроксилапатита равном 75%:25%, а для аспарагиновой кислоты при соотношениях брушита и гидроксилапатита равных 25%:75% и 50%:50%.
Проведен адсорбционно-десорбционный эксперимент аминокислот на поверхностях смесей на основе брушита и гидроксилапатита при рН = 7,40 ± 0,05 и установлено, что десорбция пролина и аспарагиновой кислоты, а также глицина при соотношении смеси 50:50 достигают предельного значения.
Получено, что скорость растворения смесей брушит : гидроксилапатит в трис-буфере увеличивается, при увеличении содержания брушита в смеси.

Слайд 28 в г
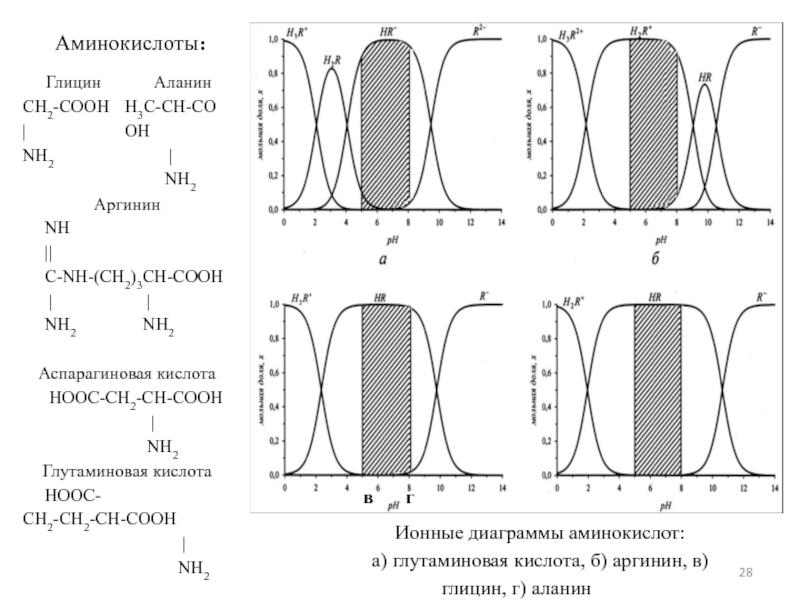
Ионные диаграммы аминокислот:
а) глутаминовая кислота, б) аргинин,
в) глицин, г) аланин
Аминокислоты:
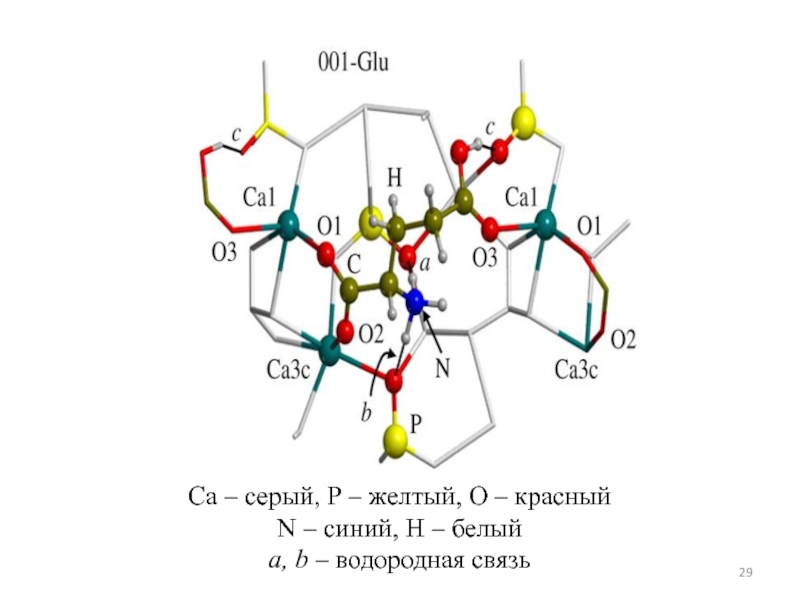
Слайд 29Са – серый, Р – желтый, О – красный
N –
синий, Н – белый
а, b – водородная связь
Слайд 33Концентрации кальция и магния в растворе рассчитывают по формулам
Слайд 34Содержание ортофосфатов в растворе определяют по формуле