Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
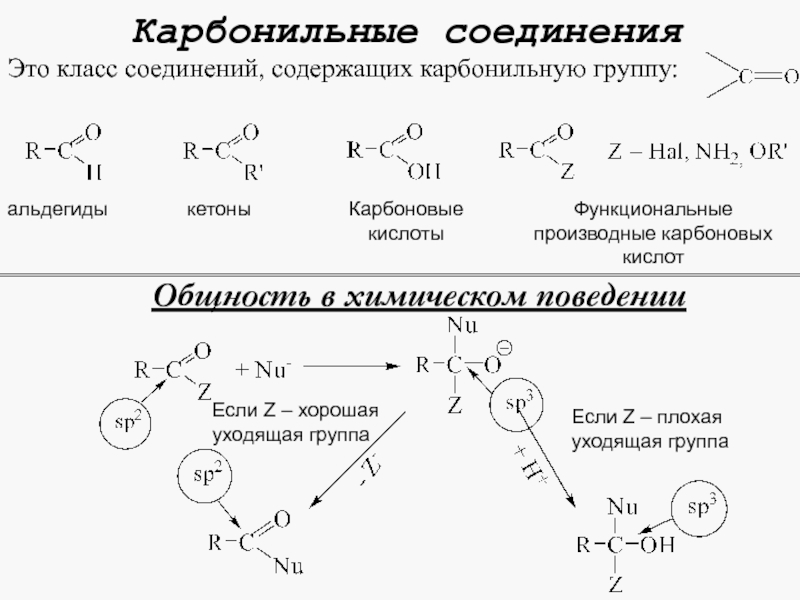
Карбонильные соединения Это класс соединений, содержащих карбонильную
Содержание
- 1. Карбонильные соединения Это класс соединений, содержащих карбонильную
- 2. Альдегиды и кетоныМетоды получения изучали ранее:Окисление спиртов;Озонолиз
- 3. 2. Синтезы на основе реактива Гриньяра: Амид карбоновой кислоты2. Восстановление хлорангидридов карбоновых кислот (по Розенмунду):
- 4. Химические свойства карбонильных соединенийС = С связь
- 5. Реакции присоединения к карбонильной группеNu атакует С=О
- 6. Электроноакцепторные заместители облегчают атаку нуклеофила:1. Образование циангидринов:ацетонциангидринα-метилакрилонитрил2-гидрокси-2-метил-пропионовая кислота
- 7. Д.З. Провести полимеризацию метакриловой кислоты:БензальдегидМиндальная кислотаПрисоединение бисульфита натрия к карбонильным соединениям:Нуклеофильный центр
- 8. Бисульфит ацетонаСоль растворима в воде, но не
- 9. Имин (кето- или альдоимин)а) Реакции с аммиаком (R = H):
- 10. Альдимидоаммиак (вулкацит) tпл.= 850CФормальдегид реагирует иначеГексаметилентетрамин (уротропин)Гексаген (RDX)Вновь в реакцию
- 11. б) Реакция с гидроксиламином:оксимРеакция используется для количественного определения карбонильных соединений (титрование выделяющейся HCl).ацетальдоксимацетонооксимГораздо токсичнее фосгена!фосген
- 12. Для оксимов возможна изомерия:Анти-tпл = 128-1300ССин-tпл =
- 13. Качественные реакции (образуются осадки).фенилгидразон2,4-динитрофенилгидразонсемикарбазонИспользуются в синтезе гетероцикловсемикарбазид2,4-динитрофенилгидразинфенилгидразин
- 14. 4. Реакци с реактивом Гриньяра (рассматривали механизм
- 15. 6. Реакции с водойВоду присоединяют только самые
- 16. Реакция катализируется кислотами и основаниями. Кислотный катализ:Основный катализ:
- 17. Образование полных ацеталей катализируется только кислотами:Кетали так
- 18. Альдегиды и кетоны реагируют с тиолами:
- 19. триоксиметилентримеризациятетрамеризацияпаральдегидснаролметальдегид
- 20. Реакции окисления карбонильных соединений:[O] – KMnO4; CrO2; H2SO4;H2O2; RCOOH.Реакция серебряного зеркала:
- 21. Окисление альдегидов кислородом воздуха в присутствии активных радикалов:Надбензойная кислотаБензойная кислота
- 22. Кетоны окисляются значительно труднее. Нужны
- 23. Реакция Каницарро. Характерна для альдегидов, не содержащих атомов водорода у α-углеродного атома:Метилат-анион
- 24. Бензиловый спиртНатриевая соль бензойной кислотыРеакции, связанные с
- 25. В нейтральной среде:ацетонЕнольная форма ацетона~0,004%Кето-енольная таутомерия –
- 26. Енолят-анионffπ, σб) Енолизация, катализируемая кислотой:fS
- 27. в) Галоформная реакция:В щелочной середе идет исчерпывающее
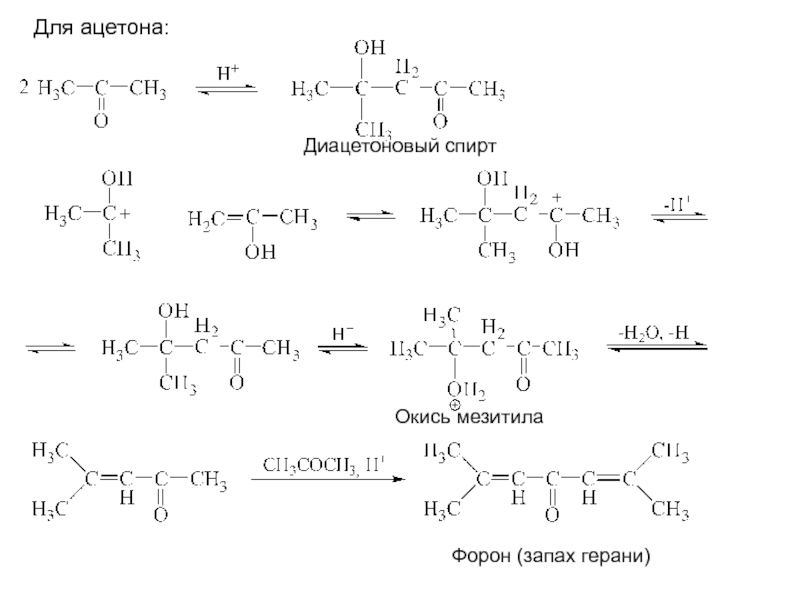
- 28. Реакции конденсации1. Альдольная конденсация:Енолят-аниональдолькротоновый альдегид
- 29. 2. Кротоновая конденсация (идет в кислой среде и при нагревании):Кротоновый альдегид
- 30. Для ацетона:Форон (запах герани)Окись мезитилаДиацетоновый спирт
- 31. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Карбонильные соединения
Это класс соединений, содержащих карбонильную группу:
альдегиды
кетоны
Карбоновые кислоты
Функциональные производные карбоновых
кислот
Z – плохая уходящая группаСлайд 2Альдегиды и кетоны
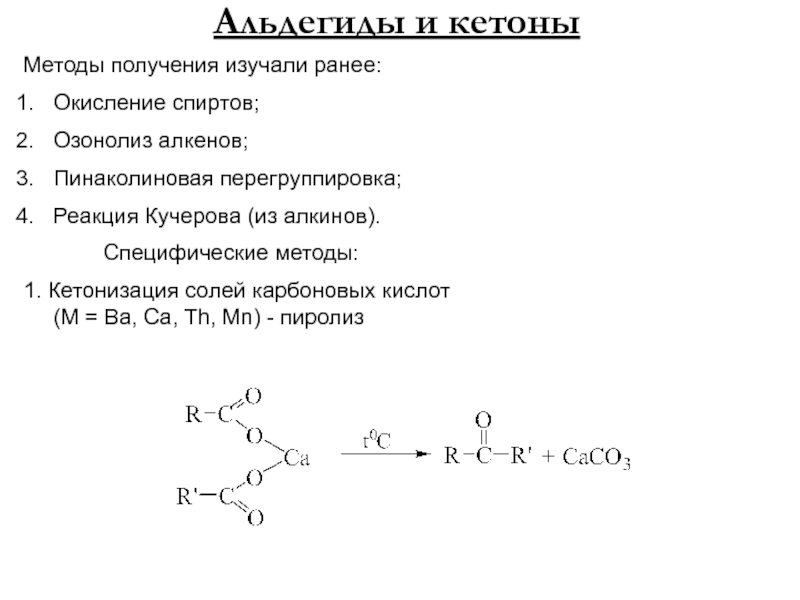
Методы получения изучали ранее:
Окисление спиртов;
Озонолиз алкенов;
Пинаколиновая перегруппировка;
Реакция Кучерова
(из алкинов).
Специфические методы:
1. Кетонизация солей карбоновых кислот (М = Ba,
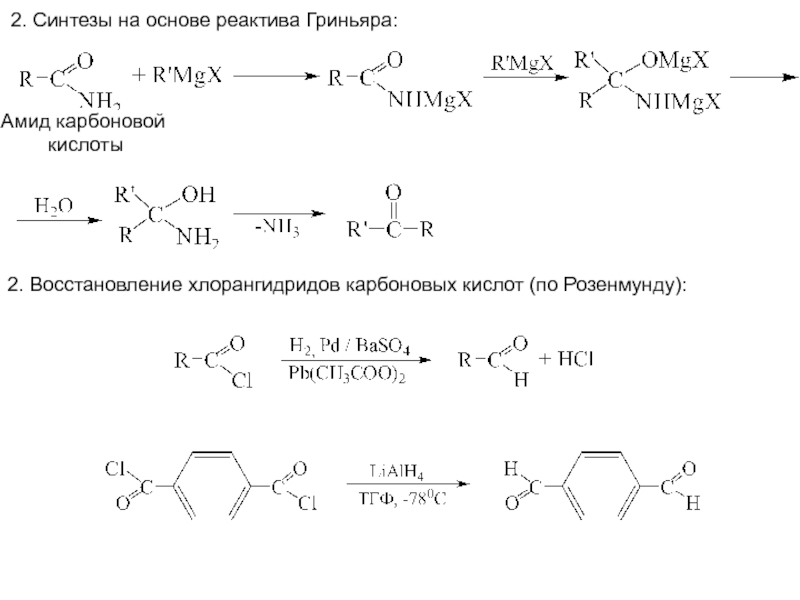
Ca, Th, Mn) - пиролизСлайд 32. Синтезы на основе реактива Гриньяра:
Амид карбоновой
кислоты
2. Восстановление
хлорангидридов карбоновых кислот (по Розенмунду):
Слайд 4Химические свойства карбонильных соединений
С = С связь менее прочная (145,8
ккал/моль), чем две С – С связи.
-связь более прочная (179
ккал/моль).Атака по кислороду - чаще всего протоном, т.е. альдегиды и кетоны – слабые основания
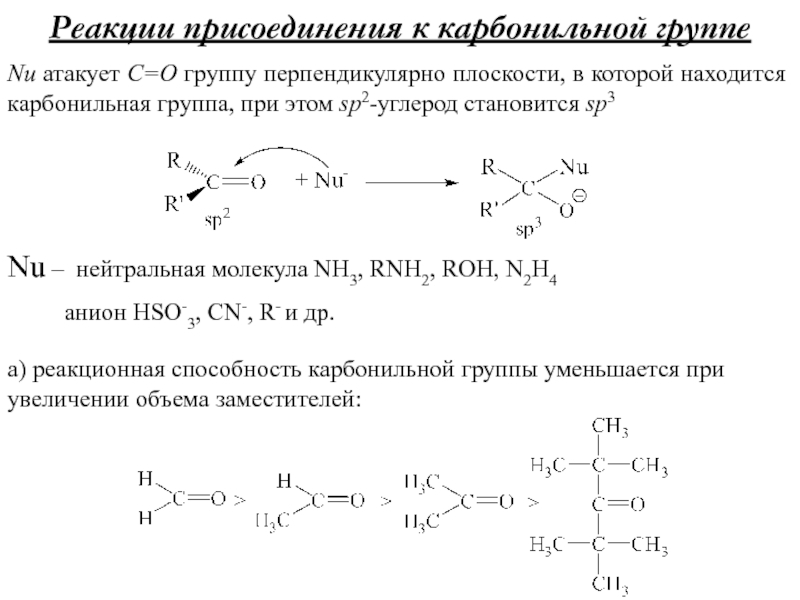
Слайд 5Реакции присоединения к карбонильной группе
Nu атакует С=О группу перпендикулярно плоскости,
в которой находится карбонильная группа, при этом sp2-углерод становится sp3
Nu
– нейтральная молекула NH3, RNH2, ROH, N2H4анион HSO-3, CN-, R- и др.
а) реакционная способность карбонильной группы уменьшается при увеличении объема заместителей:
Слайд 6Электроноакцепторные заместители облегчают атаку нуклеофила:
1. Образование циангидринов:
ацетонциангидрин
α-метилакрилонитрил
2-гидрокси-2-метил-пропионовая кислота
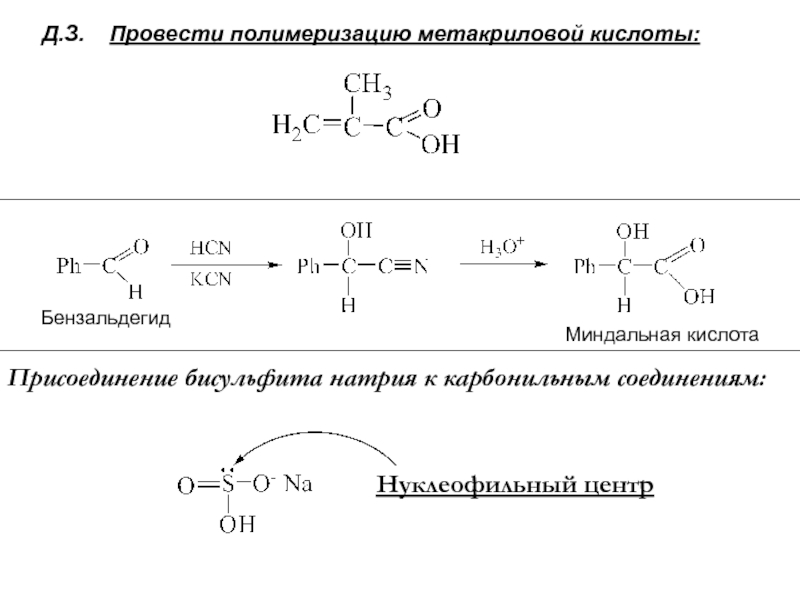
Слайд 7Д.З. Провести полимеризацию метакриловой кислоты:
Бензальдегид
Миндальная кислота
Присоединение бисульфита натрия к
карбонильным соединениям:
Нуклеофильный центр
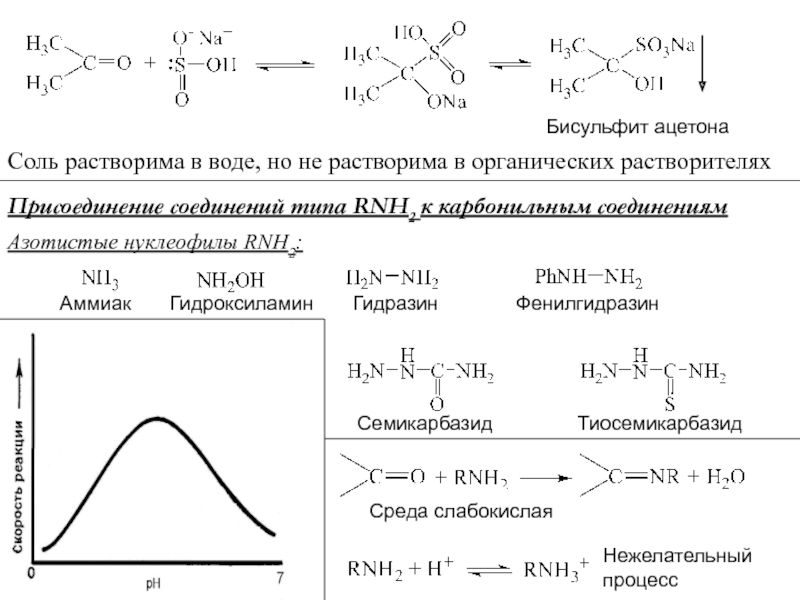
Слайд 8Бисульфит ацетона
Соль растворима в воде, но не растворима в органических
растворителях
Присоединение соединений типа RNH2 к карбонильным соединениям
Азотистые нуклеофилы RNH2:
Аммиак
Гидроксиламин Гидразин Фенилгидразин Семикарбазид
Тиосемикарбазид
Среда слабокислая
Нежелательный процесс
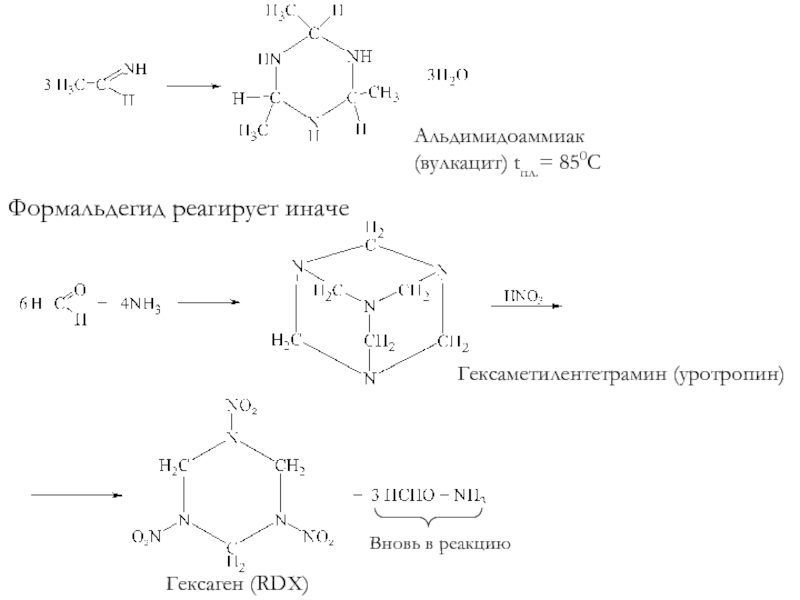
Слайд 10Альдимидоаммиак (вулкацит) tпл.= 850C
Формальдегид реагирует иначе
Гексаметилентетрамин (уротропин)
Гексаген (RDX)
Вновь в реакцию
Слайд 11б) Реакция с гидроксиламином:
оксим
Реакция используется для количественного определения карбонильных соединений
(титрование выделяющейся HCl).
ацетальдоксим
ацетонооксим
Гораздо токсичнее фосгена!
фосген
Слайд 12Для оксимов возможна изомерия:
Анти-
tпл = 128-1300С
Син-
tпл = 340С
в) Реакция с
гидразином:
азин
гидразон
Гидразоны используются для превращения карбонильных соединений
в предельные углеводороды (реакция
Кижнера):Слайд 13Качественные реакции (образуются осадки).
фенилгидразон
2,4-динитрофенилгидразон
семикарбазон
Используются в синтезе гетероциклов
семикарбазид
2,4-динитрофенилгидразин
фенилгидразин
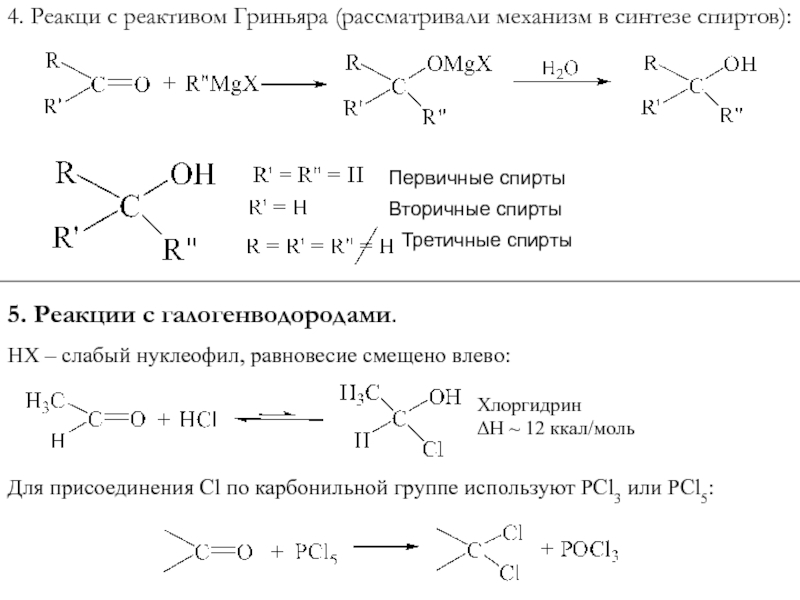
Слайд 144. Реакци с реактивом Гриньяра (рассматривали механизм в синтезе спиртов):
Первичные
спирты
Вторичные спирты
Третичные спирты
5. Реакции с галогенводородами.
НХ –
слабый нуклеофил, равновесие смещено влево:Хлоргидрин
ΔН ~ 12 ккал/моль
Для присоединения Cl по карбонильной группе используют PCl3 или PCl5:
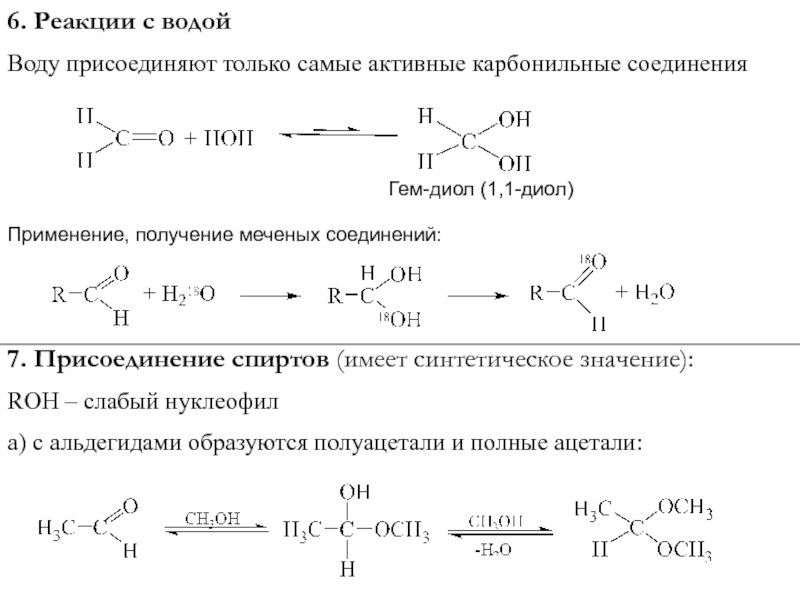
Слайд 156. Реакции с водой
Воду присоединяют только самые активные карбонильные соединения
Гем-диол
(1,1-диол)
Применение, получение меченых соединений:
7. Присоединение спиртов (имеет синтетическое значение):
ROH –
слабый нуклеофила) с альдегидами образуются полуацетали и полные ацетали:
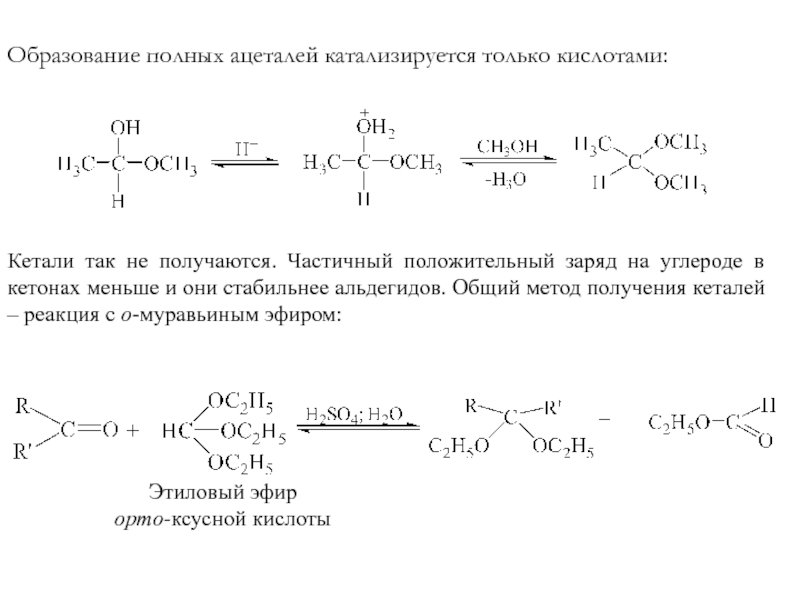
Слайд 17Образование полных ацеталей катализируется только кислотами:
Кетали так не получаются. Частичный
положительный заряд на углероде в кетонах меньше и они стабильнее
альдегидов. Общий метод получения кеталей – реакция с о-муравьиным эфиром:Этиловый эфир
орто-ксусной кислоты
Слайд 18Альдегиды и кетоны реагируют с тиолами:
Полимеризация альдегидов.
Характерна только
для альдегидов – образуются линейные и циклические полимеры.
Параформ
(Фирма «Du pont»)
Слайд 20Реакции окисления карбонильных соединений:
[O] – KMnO4; CrO2; H2SO4;
H2O2; RCOOH.
Реакция серебряного
зеркала:
Слайд 21Окисление альдегидов кислородом воздуха в присутствии
активных радикалов:
Надбензойная
кислота
Бензойная
кислота
Слайд 22 Кетоны окисляются значительно труднее. Нужны сильные
окислители, при
этом рвется связь по обе стороны карбонильной
группы, образуется смесь
кислот (пр. Попова)Масляная кислота
Уксусная
кислота
Пропионовая
кислота
Валериановая
кислота
Адипиновая кислота
Циклогексанон
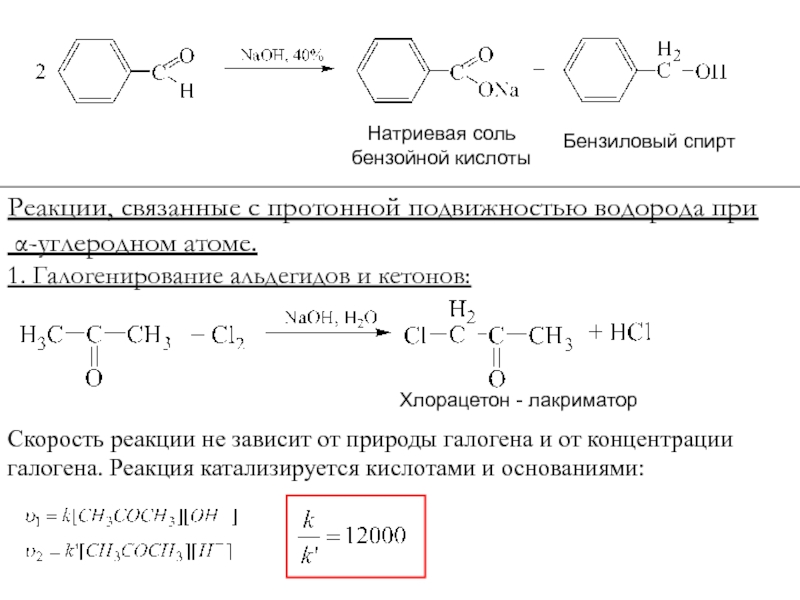
Слайд 23Реакция Каницарро. Характерна для альдегидов, не содержащих
атомов водорода у
α-углеродного атома:
Метилат-анион
Слайд 24Бензиловый спирт
Натриевая соль
бензойной кислоты
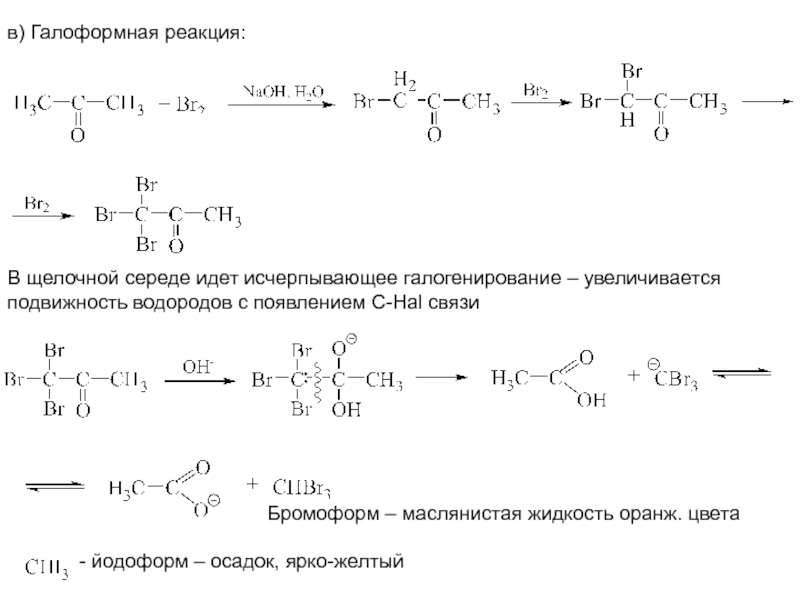
Реакции, связанные с протонной подвижностью водорода
при
α-углеродном атоме.
1. Галогенирование альдегидов и кетонов:
Хлорацетон - лакриматор
Скорость
реакции не зависит от природы галогена и от концентрациигалогена. Реакция катализируется кислотами и основаниями:
Слайд 25В нейтральной среде:
ацетон
Енольная форма ацетона
~0,004%
Кето-енольная таутомерия – вид изомерии, где
кетонная и енольная формы
различаются положением атома водорода, двойной и
простой связей. Енолизация, катализируемая основаниями:
Енолят-анионы амбидентны – 2 реакционных центра
енол
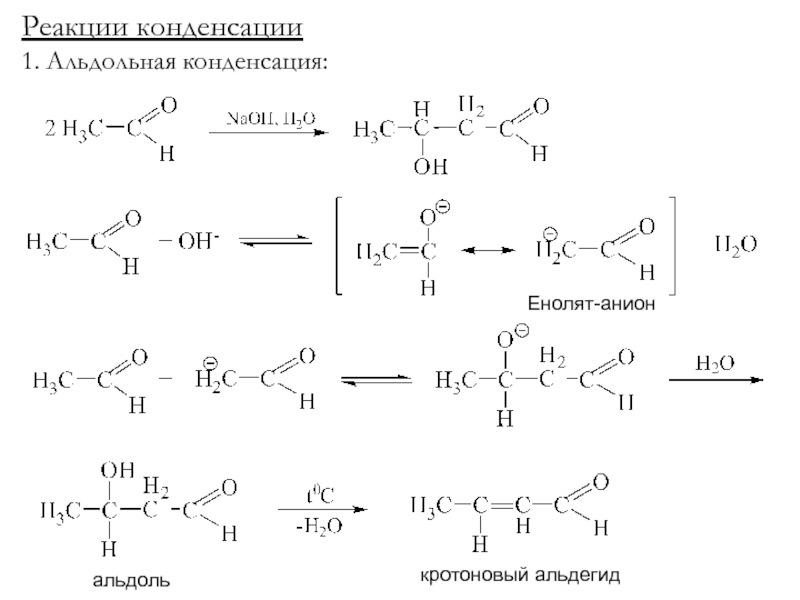
Слайд 27в) Галоформная реакция:
В щелочной середе идет исчерпывающее галогенирование – увеличивается
подвижность водородов с появлением С-Hal связи
Бромоформ – маслянистая жидкость оранж.
цвета - йодоформ – осадок, ярко-желтый









![Карбонильные соединения
Это класс соединений, содержащих карбонильную Реакции окисления карбонильных соединений:[O] – KMnO4; CrO2; H2SO4;H2O2; RCOOH.Реакция серебряного зеркала: Реакции окисления карбонильных соединений:[O] – KMnO4; CrO2; H2SO4;H2O2; RCOOH.Реакция серебряного зеркала:](/img/thumbs/740e3dd5955da95a81b4e81ce2d9072c-800x.jpg)