Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Клиническая фармакология Основы фармакокинетики и фармакодинамики
Содержание
- 1. Клиническая фармакология Основы фармакокинетики и фармакодинамики
- 2. Слайд 2
- 3. Определение класса доказанности рекомендаций по диагностике и лечению
- 4. Определение уровня доказанности рекомендаций по диагностике и лечению
- 5. Клиническая фармакология – наука, изучающая особенности
- 6. Разделы клинической фармакологииФармакокинетика и биоэквивалентность ЛСФармакодинамикаФармакогенетикаФармакоэкономикаФармакоэпидемиологияФармакомониторинг ПЭ ЛСКлинические испытания ЛС
- 7. ФармакокинетикаРаздел клинической фармакологии, изучающий пути поступления ЛС
- 8. Фармакодинамика Раздел клинической фармакологии, изучающий совокупность
- 9. ФармакодинамикаИзучает взаимодействие лекарственного вещества с молекулярными мишенями
- 10. Критерии клинической эффективности лекарственных средствКритерии клинической эффективности
- 11. Основные принципы рациональной фармакотерапииОбоснованностьМинимизацияРациональностьЭкономичностьКонтролируемостьИндивидуализированность
- 12. Комплаентность Приверженность пациента к соблюдению выполнения режима
- 13. Механизмы действия лекарственных средствДействие на специфические рецепторыВлияние
- 14. Рецепторы клетокМакромолекулярные структуры, избирательно чувствительные к определенным химическим соединениям.
- 15. Агонисты рецепторовВещества прямо возбуждающие или повышающие функциональную активность рецепторов.
- 16. Антагонисты рецепторовВещества, препятствующие действию специфических агонистов, или блокирующие рецепторы.
- 17. Конкурентный антагонизмЛекарственное вещество конкурирует с агонистом за одни и те же специфические рецепторы.
- 18. Неконкурентный антагонизмЛекарственное вещество занимает другие участки макромолекулы, не относящиеся к специфическому рецептору.
- 19. Рецепторы разделяют по чувствительности
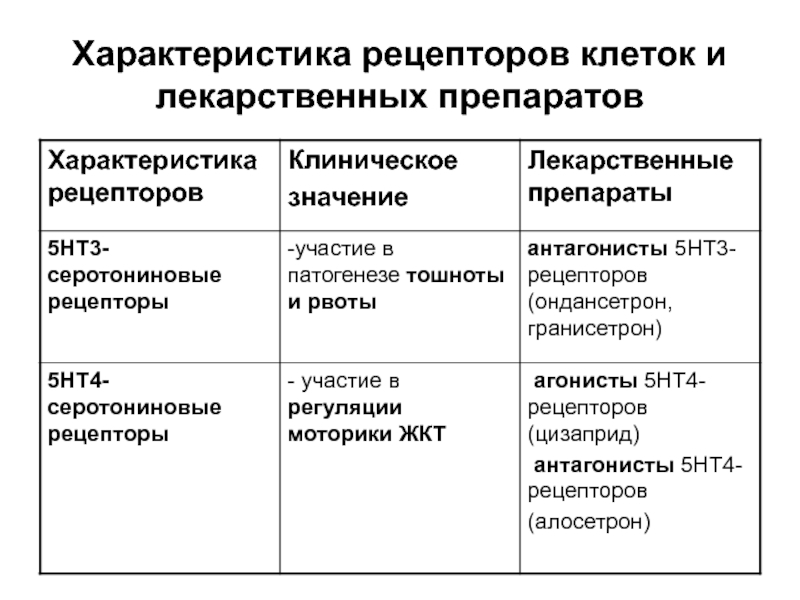
- 20. Характеристика рецепторов клеток и лекарственных препаратов
- 21. Характеристика рецепторов клеток и лекарственных препаратов
- 22. Характеристика рецепторов клеток и лекарственных препаратов
- 23. Характеристика рецепторов клеток и лекарственных препаратов
- 24. Характеристика рецепторов клеток и лекарственных препаратов
- 25. Характеристика рецепторов клеток и лекарственных препаратов
- 26. Характеристика рецепторов клеток и лекарственных препаратов
- 27. Характеристика рецепторов клеток и лекарственных препаратов
- 28. Механизмы действия лекарственных средствДействие на специфические рецепторыВлияние
- 29. Влияние на активность ферментовПротивовирусное действие Рибавирина:
- 30. Фармакокинетика Раздел клинической фармакологии, предметом которого
- 31. Основные фармакокинетические процессыВсасываниеРаспределениеБиотрансформация (метаболизм)Выведение (экскреция)
- 32. Фармакокинетическая криваяКонцентрацияТоксическая концентрация’Терапевтический диапазонНачало действияКонец действия
- 33. Фармакокинетическая криваяОписывает изменение концентрации лекарственного вещества во времени.
- 34. Биодоступность – часть лекарственного вещества, достигшая системного кровотока после внесосудистого введения.
- 35. Биодоступность зависитОт пресистемного метаболизма (кишечного и печеночного)От всасываемости (полноты всасывания) лекарственного вещества
- 36. Всасывание - процесс поступления лекарственного вещества из места введения в кровь
- 37. ВсасываниеИз кислой среды ЛВ с кислыми свойствамиИз щелочной среды (тонкий кишечник) слабых оснований
- 38. Пути поступления ЛСЧерез тканевые барьерыЧерез клеточные мембраныЧерез межкклеточные поры
- 39. Механизмы чрезмембранного транспортаПростая диффузияОблегченная диффузияАктивный транспорт
- 40. Простая диффузияПеренос лекарственного вещества по гради-
- 41. Скорость простой диффузии Прямо пропорциональна трансмембранному концентрационному
- 42. Облегченная диффузияПеренос лекарственного вещества по электрохимическому градиенту
- 43. Активный транспортПеренос лекарственного вещества против концентрационного или
- 44. Использование белка-переносчика определяет:НасыщаемостьСпецифичность белка-переносчика к определенной конформации молекулы ЛС Конкурентное ингибирование
- 45. ФильтрацияОбеспечивается гидростатическим градиентом через полярные поры мембран без затрат энергииВодаГидрофильные вещества
- 46. Транспорт растворимых в воде ЛСМежклеточныйМежду эндотелиальными клетками
- 47. Транспорт жирорастворимых ЛСПассивный вид транспорта – диффузия:простая
- 48. Пассивный вид мембранного транспорта жирорастворимых ЛСПростая диффузия
- 49. Активный вид мембранного транспорта жирорастворимых ЛСИдет против
- 50. Показатели всасыванияПолнота всасывания - количество (%) всосавшегося
- 51. Показатели всасыванияПериод полуабсорбции (Т1/2а) – время, необходимое
- 52. Факторы, влияющие на всасывание слабых электролитовСтепень их
- 53. Клеточная мембрана – обязательный универсальный биобарьер для
- 54. Свойства клеточной мембраныМембраны разных клеток различаются по
- 55. Мембранные белки выполняют функцииРецепторовИонных каналов и переносчиков (восприятия и передачи химических и электрических сигналов)Мишени для ЛС
- 56. Распределение лекарственных средствПроникновение лекарственного вещества из системного
- 57. Распределение лекарственных средств включает:Связывание с белками (альбумины,
- 58. Распределение - проникновение препарата из системного кровотока
- 59. Факторы, влияющие на распределение ЛСИнтенсивность регионального кровотокаСтепень
- 60. Факторы, влияющие на объем распределенияСодержание белка в
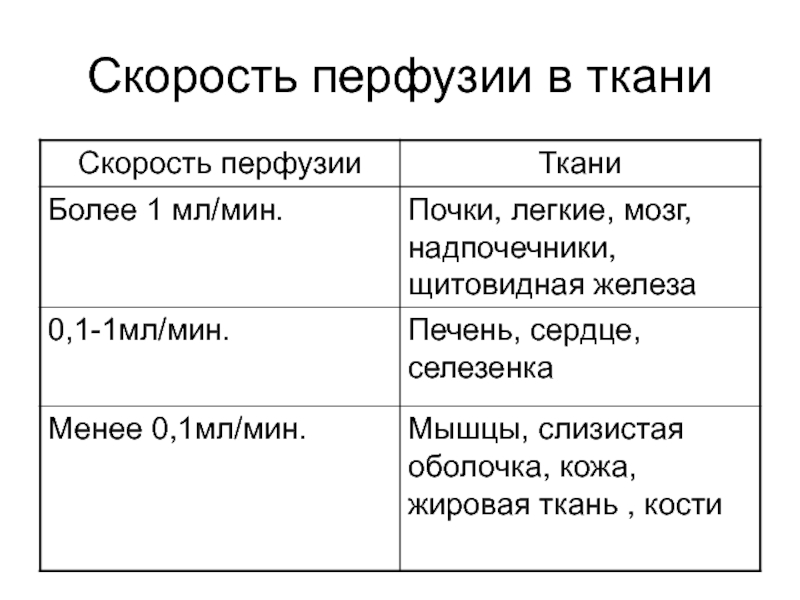
- 61. Скорость перфузии в ткани
- 62. Объем распределения (Vd)
- 63. Объем распределения (Vd)Используется для характеристики степени распределения
- 64. Vd = D / Co х M
- 65. Значения Vd
- 66. Объем распределения ЛВ
- 67. Объем распределения препаратаГидрофильные ЛС имеют малый объем
- 68. Объем распределения препаратаЛипофильные ЛС имеют большой объем
- 69. Показатели распределенияКажущаяся начальная концентрация (Со) – концентрация
- 70. Показатели распределенияМаксимум (пик) концентрации лекарственного вещества в
- 71. Показатели распределенияСтационарная равновесная концентрация (Сss) – концентрация
- 72. Период полураспредения (Т1/2α)Характеризует время, необходимое для достижения концентрации ЛС в крови, равной 50% от равновесной.
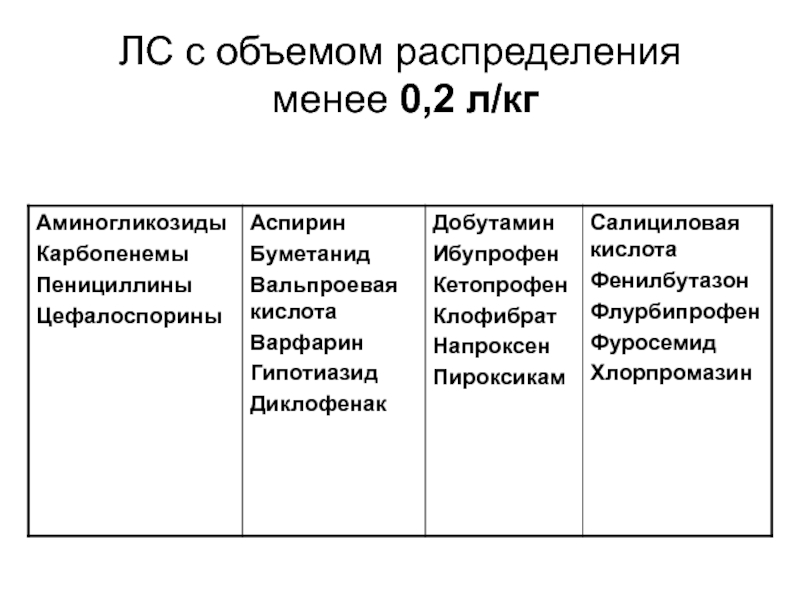
- 73. ЛС с объемом распределения менее 0,2 л/кг
- 74. Связывание ЛВ с белкомАктивным ЛВ является НЕСВЯЗАННАЯ
- 75. Сывороточный альбуминОбладает универсальной способностью связывать практически все
- 76. Связывание некоторых ЛВ с альбуминами (% свободной фракции - %СФ)
- 77. Причины гипоальбуминемииСнижение синтеза альбумина (голодание, нарушение всасывания,
- 78. Р-гликопротеин – мембранный белок-переносчикВ гепатоцитахВ кишечникеВ почечных
- 79. Элиминация ЛСБиотрансформация – препарат превращается в неактивные метаболитыЭкскреция – препарат физически выводится из организма
- 80. Показатели, характеризующие процессы элиминацииОбщий клиренс (CLt)Константа скорости
- 81. Значение показателей, характеризующих процессы элиминацииТ1/2 = 0,693/
- 82. Удерживание уровня концентрации ЛС на постоянном
- 83. Удерживание уровня концентрации ЛС на постоянном
- 84. Удерживание уровня концентрации ЛС на постоянном
- 85. Общий клиренс (CLt)Фармакокинетический показатель скорости элимининации.Определяется как
- 86. Метаболизм (биотрансформация лекарственных средств – ЛС)
- 87. Эффект первичного прохождения через печень (fist pass
- 88. Пресистемный метаболизм ЛС включает:Активный метаболизм на уровне кишечникаЭффект первого прохождения через печень
- 89. Пролекарства (pro-drugs)Вещества, которые подвергаясь пресистемному метаболизму, превращаются в активные вещества, вызывающие фармакологические эффекты (ИАПФ).
- 90. Механизмы биотрансформации ЛВ в печениI фаза биотрансформации
- 91. Фазы метаболизма ЛС, цель – создание полярных,
- 92. Печеночный клиренсВысокий: - высокая степень экстракции ЛС
- 93. Преимущественно печеночная биотрансформация с высоким клиренсом
- 94. С низким клиренсом и высокой способностью к связыванию с белками
- 95. С низким клиренсом и малой способностью к связыванию с белками
- 96. Система CYP450
- 97. Система CYP450
- 98. Генетический полиморфизмЯвление существования в популяции различных наследуемых
- 99. Распространенность генотипов «медленных» метаболизаторов в России
- 100. «Медленные» мутантные аллели гена изофермента цитохрома Р450 2D6
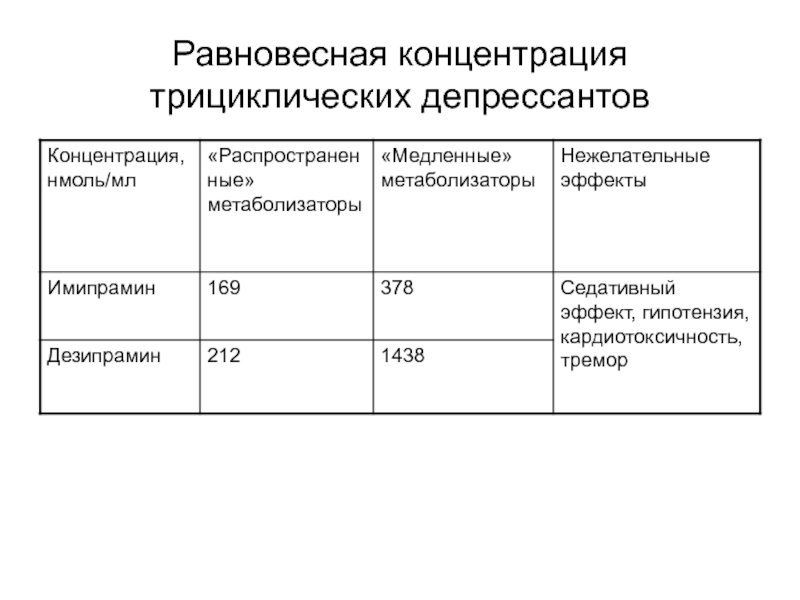
- 101. Равновесная концентрация трициклических депрессантов
- 102. Дозирование антикоагулянтов
- 103. Клинический пример: Больная Р. 65 лет. Диагноз:
- 104. На биодоступность влияют:Пути введения лекарственного веществаИндивидуальные особенности
- 105. Показатели биодоступностиАбсолютная биодоступность (f) – часть дозы
- 106. Слайд 106
- 107. Выделение ЛВ почкамиКлубочковая фильтрация, канальцевая секреция и
- 108. Выделение ЛВ почками
- 109. Зависимость от рН мочи?Слабые кислоты (барбитураты, пенициллины,
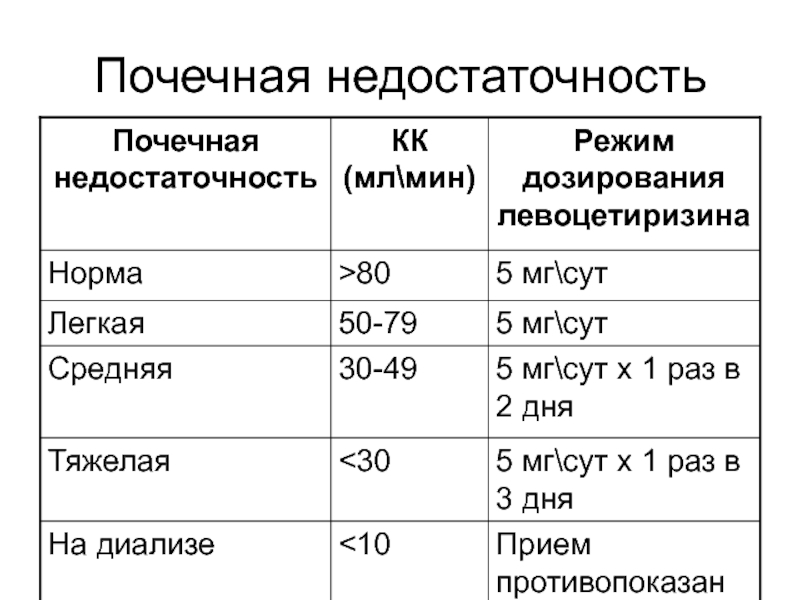
- 110. Почечная недостаточность
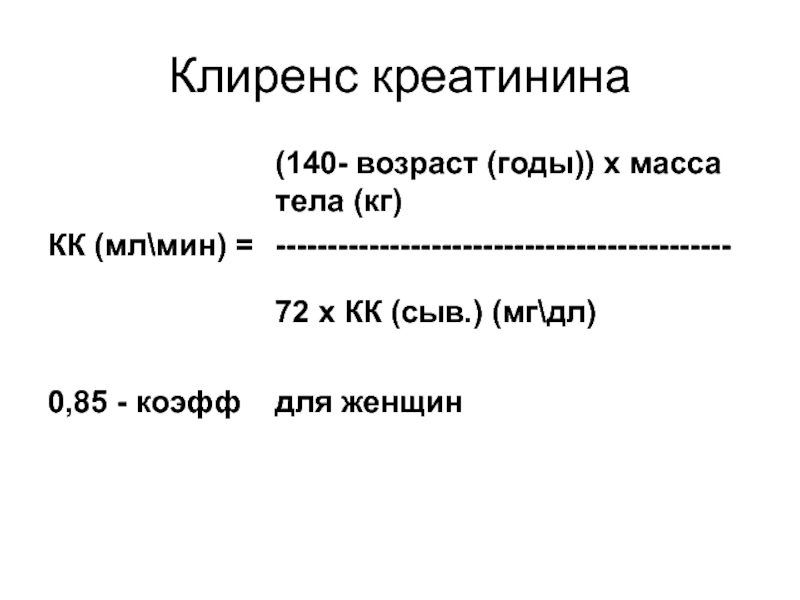
- 111. Клиренс креатинина
- 112. ХПННарушается почечная экскрецияНеобходим перерасчет режима введения препаратов
- 113. При ХПН нефротоксичныГентамицинКарбенициллинЦефазолинВанкомицин
- 114. Коррекция дозы ЛС при почечной недостаточностиЛС с
- 115. При циррозе печени↓ пресистемный метаболизм ↓ связь с белком↑ Т1\2↑ биодоступность
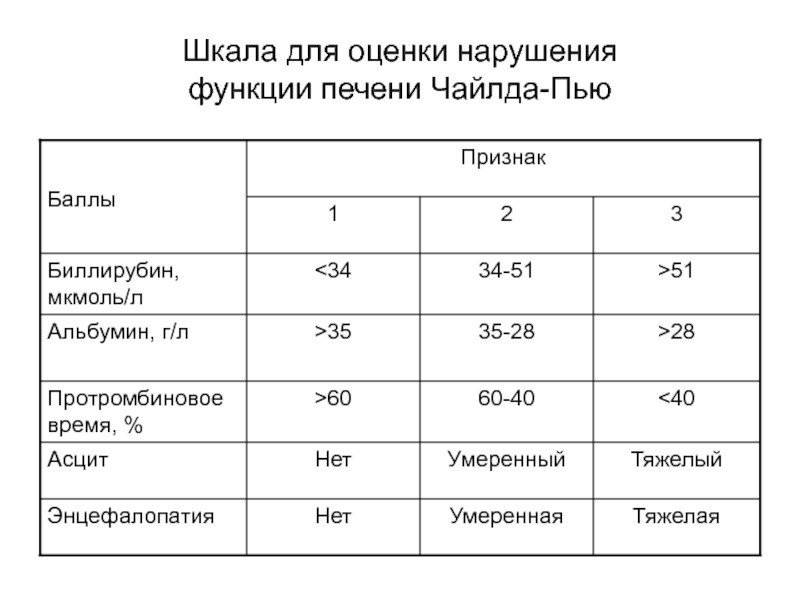
- 116. Шкала для оценки нарушения функции печени Чайлда-Пью
- 117. Коррекция дозы ЛС метаболизирующихся в печени
- 118. Коррекция дозы ЛС при заболевании печени по
- 119. Основные фармакокинетические параметрыОбъем распределенияБиодоступностьПериод полувыведенияКлиренсБиоэквивалентность
- 120. Биоэквивалентные лекарственные средстваФармацевтически эквивалентные препараты (содержат одни
- 121. Показатели биоэквивалентности лекарственных форм
- 122. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Клиническая фармакология
Основы фармакокинетики и фармакодинамики
Доцент
Егорова Наталья Анатольевна
Слайд 5Клиническая фармакология – наука, изучающая особенности эффективности и безопасности лекарственных
Слайд 6Разделы клинической фармакологии
Фармакокинетика и биоэквивалентность ЛС
Фармакодинамика
Фармакогенетика
Фармакоэкономика
Фармакоэпидемиология
Фармакомониторинг ПЭ ЛС
Клинические испытания ЛС
Слайд 7Фармакокинетика
Раздел клинической фармакологии, изучающий пути поступления ЛС в организм человека,
всасывание, распределение, биотрансформацию и выведение ЛС из организма.
Слайд 8Фармакодинамика
Раздел клинической фармакологии, изучающий совокупность эффектов лекарственных средств
(желаемых и побочных) и механизмы их развития
Слайд 9Фармакодинамика
Изучает взаимодействие лекарственного вещества с молекулярными мишенями действия в органах
и тканях организма, определяюшее терапевтический и побочный эффекты данного лекарственного
препарата.Слайд 10Критерии клинической эффективности лекарственных средств
Критерии клинической эффективности при однократном применении
лекарственного препарата. Острый фармакологический тест.
Критерии клинической эффективности лекарственного препарата при
длительном применении. Влияние на качество жизни.Слайд 11Основные принципы рациональной фармакотерапии
Обоснованность
Минимизация
Рациональность
Экономичность
Контролируемость
Индивидуализированность
Слайд 12Комплаентность
Приверженность пациента к соблюдению выполнения режима применения назначенного лекарственного
препарата
Влияющие факторы: степень дискомфорта синдрома заболевания в состоянии пациента, приемлемость
выбранной лекарственной формы препарата и т.д.Слайд 13Механизмы действия лекарственных средств
Действие на специфические рецепторы
Влияние на активность ферментов
Физико-химическое
действие на мембраны клеток
Прямое химическое воздействие (цитотоксическое)
Слайд 14Рецепторы клеток
Макромолекулярные структуры, избирательно чувствительные к определенным химическим соединениям.
Слайд 15Агонисты рецепторов
Вещества прямо возбуждающие или повышающие функциональную активность рецепторов.
Слайд 16Антагонисты рецепторов
Вещества, препятствующие действию специфических агонистов, или блокирующие рецепторы.
Слайд 17Конкурентный антагонизм
Лекарственное вещество конкурирует с агонистом за одни и те
же специфические рецепторы.
Слайд 18Неконкурентный антагонизм
Лекарственное вещество занимает другие участки макромолекулы, не относящиеся к
специфическому рецептору.
Слайд 28Механизмы действия лекарственных средств
Действие на специфические рецепторы
Влияние на активность ферментов
Физико-химическое
действие на мембраны клеток
Прямое химическое воздействие (цитотоксическое)
Слайд 29Влияние на активность ферментов
Противовирусное действие Рибавирина:
конкурентное ингибирование
инозин-монофосфат-дегидрогеназы приводит к ↓ внутриклеточного ГТФ→
↓ синтеза РНК и ДНК вирусов- изменение синтеза РНК с последующим нарушением транскрипции вируса
- прямое угнетающее влияние на активность полимеразы вирусов
Слайд 30Фармакокинетика
Раздел клинической фармакологии, предметом которого является изучение процессов
всасывания, распределения, биотрансформации и выведения лекарственных веществ.
Слайд 31Основные фармакокинетические процессы
Всасывание
Распределение
Биотрансформация (метаболизм)
Выведение (экскреция)
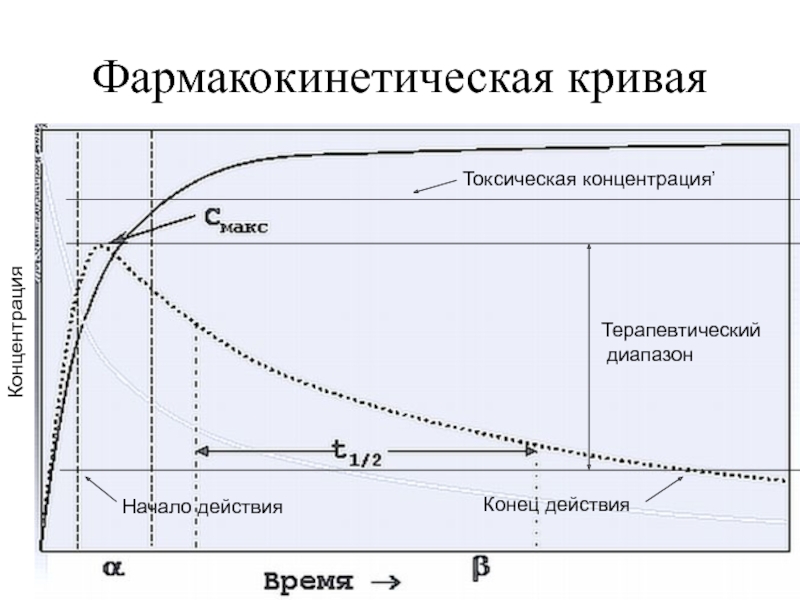
Слайд 32Фармакокинетическая кривая
Концентрация
Токсическая концентрация’
Терапевтический
диапазон
Начало действия
Конец действия
Слайд 33Фармакокинетическая кривая
Описывает изменение концентрации лекарственного вещества во времени.
Слайд 34Биодоступность – часть лекарственного вещества, достигшая системного кровотока после внесосудистого
введения.
Слайд 35Биодоступность зависит
От пресистемного метаболизма (кишечного и печеночного)
От всасываемости (полноты всасывания)
лекарственного вещества
Слайд 37Всасывание
Из кислой среды ЛВ с кислыми свойствами
Из щелочной среды (тонкий
кишечник) слабых оснований
Слайд 40Простая диффузия
Перенос лекарственного вещества по гради-
енту концентраций или
по осмотическому градиенту без затрат метаболической энергии
Липофильные (жирорастворимые) вещества с высоким молекулярным весом
Водорастворимые (гирофильные) вещества с небольшим молекулярным весом
Вещества, диффундирующие с током воды
Слайд 41Скорость простой диффузии
Прямо пропорциональна трансмембранному концентрационному градиенту
Коэффициенту распределения ЛС
между липидной и водной фазами
Площади диффузионной поверхности
Слайд 42Облегченная диффузия
Перенос лекарственного вещества по электрохимическому градиенту с помощью белка-переносчика
без затрат метаболической энергии
Липофильные и гидрофильные ЛС, скорость простой диффузии
которых слишком мала.Слайд 43Активный транспорт
Перенос лекарственного вещества против концентрационного или электрохимическго градиента с
помощью белка-переносчика с затратой метаболической энергии
Липофильные вещества с высоким молекулярным
весомГидрофильные вещества
Слайд 44Использование белка-переносчика определяет:
Насыщаемость
Специфичность белка-переносчика к определенной конформации молекулы ЛС
Конкурентное
ингибирование
Слайд 45Фильтрация
Обеспечивается гидростатическим градиентом через полярные поры мембран без затрат энергии
Вода
Гидрофильные
вещества
Слайд 46Транспорт растворимых в воде ЛС
Межклеточный
Между эндотелиальными клетками большинства капилляров с
током воды
Фильтрация по градиенту гидростатического давления
Только для свободных от белка
ЛСЗависит от активности кровотока
Важная роль в почечном фильтрационном барьере
Ч/з мембрану клетки
Многие эпителиальные ткани, капилляры ЦНС
Диффузия по градиенту осмотического давления
Только для растворимых в воде молекул
Молекулярная масса не должна превышать 100-200
Слайд 47Транспорт жирорастворимых ЛС
Пассивный вид транспорта – диффузия:
простая диффузия (наиболее распространенный
механизм мембранного транспорта, п/к, в/м)
облегченная диффузия
Активный вид транспорта
Слайд 48Пассивный вид мембранного транспорта жирорастворимых ЛС
Простая диффузия
По градиенту концентрации
Пропорциональна
величине трансмембранного концентрационного градиента
Пропорциональна коэффициенту распределения препарата между липидной и
водной фазамиПропорциональна площади диффузионной поверхности
Облегченная диффузия
По градиенту концентрации или электрохимическому градиенту
С помощью белка-переносчика
Не требует затрат энергии
Характеризуется:
насыщением,
специфичностью,
конкурентным ингибированием
Слайд 49Активный вид мембранного транспорта жирорастворимых ЛС
Идет против концентрационного или электрохимического
градиента
Осуществляется с помощью белка –переносчика
Требует затрат энергии
Характеризуется насыщением, специфичностью, конкурентным
ингибированиемСлайд 50Показатели всасывания
Полнота всасывания - количество (%) всосавшегося вещества.
Время достижения максимальной
концентрации (Тmax) – скорость всасывания лекарственного вещества и скорость наступления
терапевтического эффектаКонстанта скорости абсорбции (Ка) – скорость поступления препарата в кровь из места введения
Слайд 51Показатели всасывания
Период полуабсорбции (Т1/2а) – время, необходимое для поступления в
кровеносное русло половины дозы препарата из места введения; обратно пропорционально
константе скорости абсорбции (Т1\2а =0,693/Ка).Слайд 52Факторы, влияющие на всасывание слабых электролитов
Степень их ионизации (диффузия для
недиссоциированных, фильтрация для диссоциированных молекул).
РН среды (кислоты легче всасываются в
желудке – рН 1-2; основания в тонкой и толстой кишке – рН – 4- 8,5)Процессы в ЖКТ (ферменты, соли ЖК, моторика, состав, объем пищи и др.)
Слайд 53Клеточная мембрана – обязательный универсальный биобарьер для ЛС
Двойной слой амфифильных
липидов
Гидрофобные углеводородные хвосты обращены внутрь
Гидрофильные углеводородные хвосты обращены наружу
Встроенные внутрь
мембраны белкиСлайд 54Свойства клеточной мембраны
Мембраны разных клеток различаются по липидному составу
Обладают текучестью
и эластичностью
Обладают высоким электрическим сопротивлением (плохо проницаемы для ионизированных соединений)
Проницаема
для слабых оснований (находятся преимущественно в неионизированном состоянии в крови)Слайд 55Мембранные белки выполняют функции
Рецепторов
Ионных каналов и переносчиков (восприятия и передачи
химических и электрических сигналов)
Мишени для ЛС
Слайд 56Распределение лекарственных средств
Проникновение лекарственного вещества из системного кровотока в различные
ткани, органы и жидкие среды организма.
Степень накопления лекарственного вещества
определяет выраженность фармакодинамического эффекта.Слайд 57Распределение лекарственных средств включает:
Связывание с белками (альбумины, альфа-1 кислый гликопротеин,
глобулины, липопротеиды) и форменными элементами крови
Проникновение в эфферентные ткани и
взаимодействие с молекулами-мишенямиПоступление в органы, осуществляющие химическую модификацию (метаболизм) и выведение ЛВ
Слайд 58Распределение - проникновение препарата из системного кровотока в ткани
Размер молекулы
вещества
Фактор жирорастворимости
Степень и прочность связи с белками плазмы крови
Связь с
компонентами тканейГрадиент pH (для слабых кислот и оснований)
Слайд 59Факторы, влияющие на распределение ЛС
Интенсивность регионального кровотока
Степень связывания с белками
плазмы крови и тканевыми структурами
Растворимость в липидах
Скорость диффузии в ткани
Слайд 60Факторы, влияющие на объем распределения
Содержание белка в плазме крови –
гипоальбуминемия для ЛС, связывающихся с альбуминами более чем на 95%
(в норме альбумин 33-55 г/л)Содержание мышечной ткани (для водорастворимых ЛС) и жировой ткани (для жирорастворимых ЛС)
Состояния – беременность, возраст, заболевания
Слайд 63Объем распределения (Vd)
Используется для характеристики степени распределения ЛС в тканях
Определяется
как отношение массы ЛС, находящегося в организме , к его
концентрации в плазме крови, рассчитанное на единицу массы тела.Слайд 67Объем распределения препарата
Гидрофильные ЛС имеют малый объем распределения – менее
0,2 л/кг, хорошо распространяются только во внеклеточном пространстве, но не
проникают в мозг и другие органы, ограниченные гистогематическими барьерамиСлайд 68Объем распределения препарата
Липофильные ЛС имеют большой объем распределения – более
0,2 л/кг, быстро распределяются по всему организму, одинаково хорошо проникают
во внеклеточные и внутриклеточные области.Слайд 69Показатели распределения
Кажущаяся начальная концентрация (Со) – концентрация препарата, которая была
бы достигнута в плазме крови при внутривенном его введении и
мгновенном распределении по органам и тканям.Слайд 70Показатели распределения
Максимум (пик) концентрации лекарственного вещества в крови (Сmax) –
максимальная концентрация лекарственного вещества в системном кровотоке после парентерального или
перорального введения.Слайд 71Показатели распределения
Стационарная равновесная концентрация (Сss) – концентрация препарата, которая установится
в плазме крови при поступлении его в организм с постоянной
скоростью.Отражает состояние равновесия между кровью и тканями (steady state)
Максимальная (Сss max) и минимальная (Сss min) равновесные концентрации.
Слайд 72Период полураспредения (Т1/2α)
Характеризует время, необходимое для достижения концентрации ЛС в
крови, равной 50% от равновесной.
Слайд 74Связывание ЛВ с белком
Активным ЛВ является НЕСВЯЗАННАЯ с белком фракция
ЛВ
Чем больше степень связывания, тем меньше свободного препарата находится в
плазме крови и тем меньше вызываемый им терапевтический эффектСвязанный с белком-переносчиком препарат не может взаимодействовать с эффекторными системами
Белок выполняет роль депо ЛВ
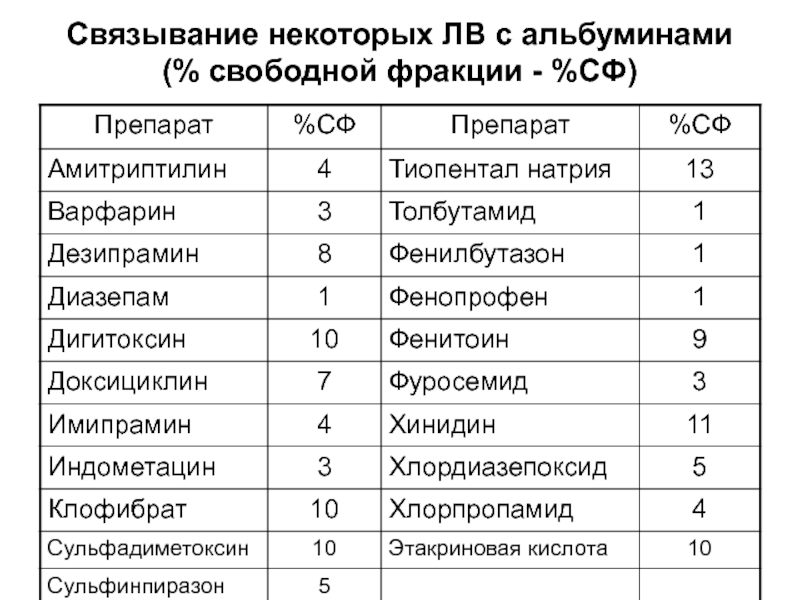
Слайд 75Сывороточный альбумин
Обладает универсальной способностью связывать практически все экзогенные и эндогенные
низкомолекулярные ЛВ
Связывающая емкость альбумина значительно выше других транспортных белков (β-глобулины,
кислые гликопротеины)Гипоальбуминемия приводит к выраженному нарушению связывания ЛВ
Слайд 77Причины гипоальбуминемии
Снижение синтеза альбумина (голодание, нарушение всасывания, заболевания печени)
Увеличение объема
распределения альбумина (избыточная гидратация перфузионной терапии, повышенная проницаемость капилляров, беременность)
Увеличение
выведения или метаболизма альбумина (нефротический синдром, энтеропатии, сопровождающиеся потерей белков, ожоги, катаболические состояния – сепсис, лихорадка, травма, кахексия и т.д.)Слайд 78Р-гликопротеин – мембранный белок-переносчик
В гепатоцитах
В кишечнике
В почечных канальцах
В эндотелии капилляров
головного мозга
В тестикулах
В плаценте
Отвечает за выведение ЛС из клетки
Слайд 79Элиминация ЛС
Биотрансформация – препарат превращается в неактивные метаболиты
Экскреция – препарат
физически выводится из организма
Слайд 80Показатели, характеризующие процессы элиминации
Общий клиренс (CLt)
Константа скорости элиминации (Kel) –характеризует
скорость исчезновения ЛС из организма.
Период полувыведения (Т1/2) – время, необходимое
для уменьшения вдвое концентрации препарата в крови. Слайд 81Значение показателей, характеризующих процессы элиминации
Т1/2 = 0,693/ Kel, показатели важны
для выбора интервала между дозами.
Т1/2 служит для определения промежутка времени
необходимого для достижения равновесной концентрации при многократном введении ЛС (обычно 3-5 Т1/2)За один Т1/2 из организма выводится 50% ЛС, за два –75%, за три – 87%.
Слайд 82Удерживание уровня концентрации ЛС
на постоянном уровне
Кинетика I порядка: при
линейной зависимости между и скоростью элиминации – чем выше содержание
ЛС в плазме, тем выше скорость элиминации.Кинетика 0 порядка: изменение концентрации ЛС происходит непропорционально дозе и определяется истощением механизмов, обеспечивающих элиминацию ЛС
Слайд 83Удерживание уровня концентрации ЛС
на постоянном уровне
Кинетика I порядка:
1)
Т1/2 не зависит от дозы ЛС
2) Т1/2 не зависит
от концентрации ЛС в плазме3) Т1/2 не зависит от пути введения ЛС
4) Плазменная концентрации ЛС меняется пропорционально дозе ЛС, что обеспечивает предсказуемость ФК-параметров при изменении режима дозирования.
Кинетика 0 порядка:
1) кинетика насыщения целиком определяется вводимой дозой ЛС
2) более медленное достижение нового стационарного состояния при изменении режима дозирования
3) непредсказуемое (непопорциональное) изменение средней концентрации в стационарном состоянии
Слайд 84Удерживание уровня концентрации ЛС
на постоянном уровне
-
Кинетика 0 порядка:
4) Т1/2
не имеют единого значения - Т1/2 изменяется в зависимости от
концентрации ЛС в крови.5) трудность контроля удержания концентрации ведет к чередованию периодов неэффективности и НЭ для фенитоина, парацетамола, АСК, пропафенона, эуфиллина, этанола и др.
Слайд 85Общий клиренс (CLt)
Фармакокинетический показатель скорости элимининации.
Определяется как объем плазмы, очищающийся
от ЛС за единицу времени (мл/мин.) путем метаболизма и экскреции.
Выделяют
почечный клиренс (KLr) и вне почечный клиренс (KLer).Печеночный клиренс: сумма метаболических процессов в печени и процессов экскреции ЛС с желчью.
Определение CLt необходимо для подбора поддерживающей дозы, позволяющей достичь равновесной концентрации в крови (Сss).
Слайд 86Метаболизм (биотрансформация
лекарственных средств – ЛС)
Под биотрансформацией, или метаболизмом
ЛС , понимают комплекс физико-химических и биохимических превращений ЛС, в
процессе которых образуются полярные водорастворимые вещества (метаболиты), которые легче выводятся из организма.Слайд 87Эффект первичного прохождения
через печень (fist pass metabolism)
Биотрансформация веществ при первичном
прохождении через печень в процессе всасывания (антагонисты кальция, липофильные бета-адреноблокаторы,
нитраты, ИАПФ)Интенсивность эффекта зависит от активности ферментов печени
Слайд 88Пресистемный метаболизм ЛС включает:
Активный метаболизм на уровне кишечника
Эффект первого прохождения
через печень
Слайд 89Пролекарства (pro-drugs)
Вещества, которые подвергаясь пресистемному метаболизму, превращаются в активные вещества,
вызывающие фармакологические эффекты (ИАПФ).
Слайд 90Механизмы биотрансформации ЛВ в печени
I фаза биотрансформации – несинтетическая: окисление,
восстановление, гидролиз или сходная модификация ЛВ для способности к коньюгации
II
фаза – биосинтетическая реакция модифицированного ЛВ с эндогенной полярной молекулой (коньюгация)Цель – полярность молекулы ЛВ для облегчения выведения
Слайд 91Фазы метаболизма ЛС, цель – создание полярных, гидрофильных метаболитов
I фаза
Присоединение
функциональной группы либо эта группа становится доступной в результате химических
превращенийКатализируется микросомальными ферментами эндоплазматического ритикулума (изоферменты цитохрома 450, дигидропи-ридимин дигидрогеназа, бутирилхолинэстераза,параоксоназа)
II фаза
Образование ковалентной связи между функциональной группой и эндогенными соединениями (глтатионовая кислота, сульфат, ацетат, глутатион,аминокислоты)
Катализируется цитозольными ферментами (N-ацетилтрансфераза, тиопурин S-метилтранфераза, эпоксид гидролаза)
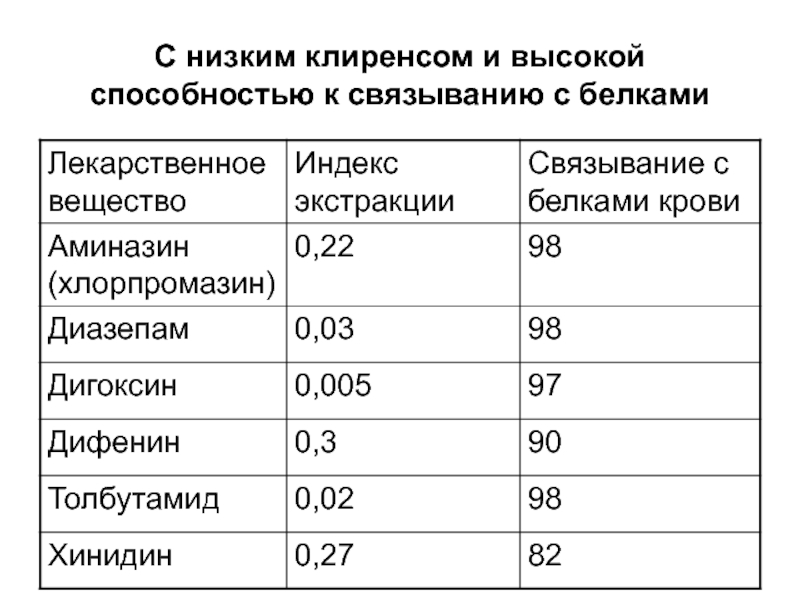
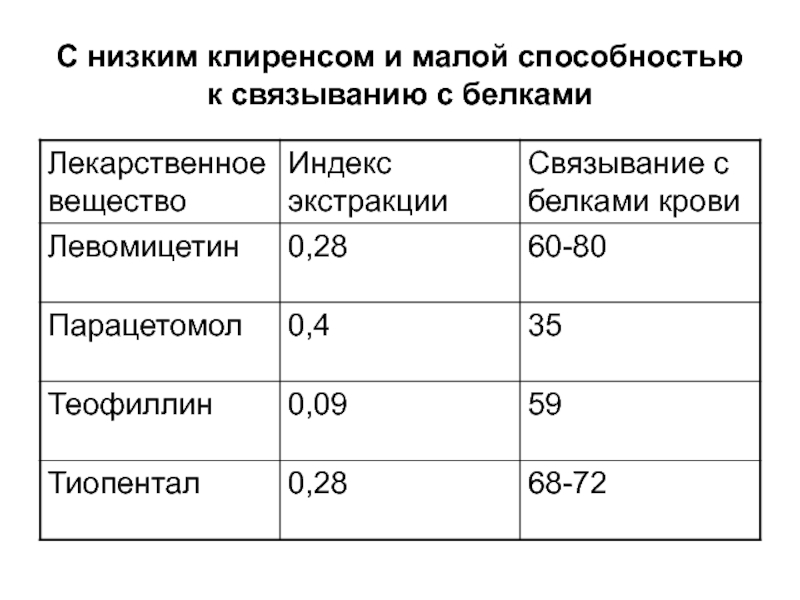
Слайд 92Печеночный клиренс
Высокий:
- высокая степень экстракции ЛС гепатоцитами из крови;
-
метаболизм ЛС зависит от скорости кровотока
Низкий:
- невысокая степень экстракции ЛС
гепатоцитами из крови;- метаболизм ЛС зависит от емкости ферментых систем печени и степени связи с белками крови
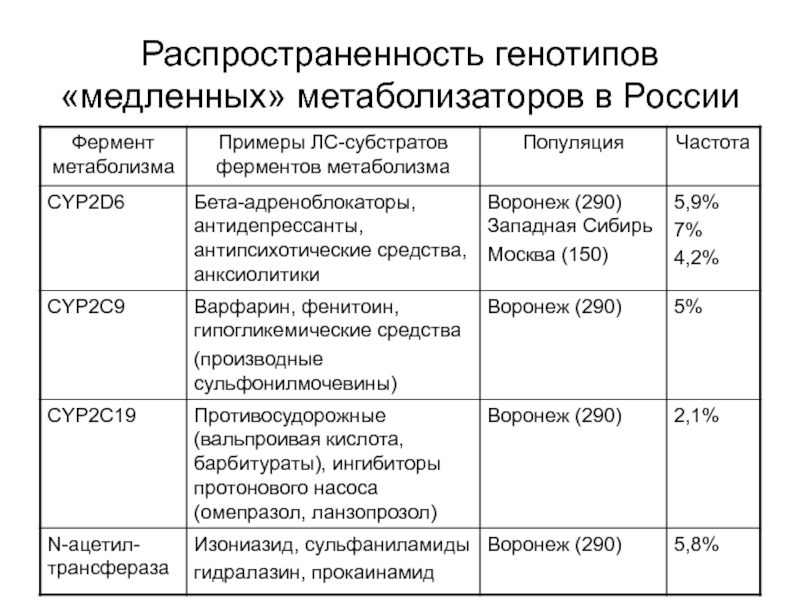
Слайд 98Генетический полиморфизм
Явление существования в популяции различных наследуемых изменений (аллельных –
функционально дефектных вариантов) одного и того же гена, контролирующего синтез
белков организма (неактивных, отсутствие синтеза, усиление синтеза -носительство копий функциональных аллелей), носит название генетического полиморфизма.Гены, для которых известен множественный аллелизм, называются полиморфными маркерами.
Существуют ассоциации полиморфного маркера с фенотипическим признаком.
Слайд 103Клинический пример: Больная Р. 65 лет. Диагноз: ИБС. СН IIIФК,
АГ 3ст., ОВР.
МА, проксизмальная тахиформа. НКI.
При поступлении: Коагулограмма –
АЧТВ 29 мс, МНО 1, варфарин 5 мг/сут., для плановой кардиоверсии.Через 2 дня: МНО 1,5
Через 5 дней: носовое кровотечение, кровохарканье, макрогематурия. АЧТВ 42 мс, МНО 8, варфарин отменен, назначен викасол.
Генотипирование CYP2C9 методом ПЦР: больная гомозиготна по «медленному» аллелю CYP2C9*3
У больной генетически детерминированное снижение скорости метаболизма варфарина.
Слайд 104На биодоступность влияют:
Пути введения лекарственного вещества
Индивидуальные особенности организма больного, состояние
ЖКТ, сердечно-сосудистой системы, печени, почек
Биофармацевтические факторы (лекарственная форма, ее состав,
особенности технологии производства)Слайд 105Показатели биодоступности
Абсолютная биодоступность (f) – часть дозы препарата (%), которая
достигла системного кровотока после внесосудистого введения.
Относительная биодоступность (f') определяют с
целью сравнения биодоступности двух лекарственных форм для внесосудисного введения.Слайд 106
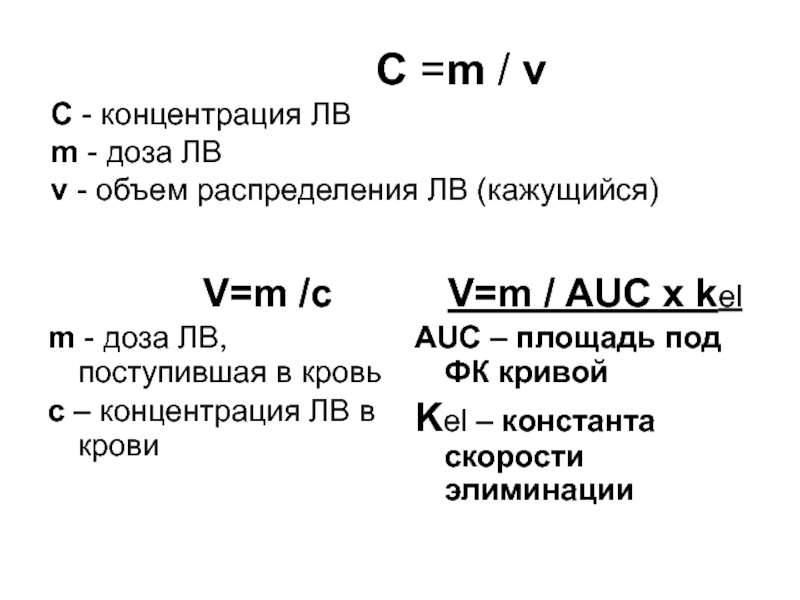
С =m / v
С - концентрация ЛВ m - доза ЛВ v - объем распределения ЛВ (кажущийся) V=m /c
m - доза ЛВ, поступившая в кровь
с – концентрация ЛВ в крови
V=m / AUC x kel
AUC – площадь под ФК кривой
Kel – константа скорости элиминации
Слайд 107Выделение ЛВ почками
Клубочковая фильтрация, канальцевая секреция и канальцевая реабсорбция –
основные механизмы почечной экскреции
Реабсорбция ЛВ из просвета канальцев зависит от
рН мочи (кислые вещества быстрее экскретируются при щелочной реакции мочи, основания – при кислой) Путем почечной экскреции удаляются преимущественно гидрофильные ЛВ или их метаболиты, т.к. они хорошо растворяются в моче
Слайд 109Зависимость от рН мочи?
Слабые кислоты (барбитураты, пенициллины, салициловая кислота, сульфаниламиды,
тетрациклины)
Слабые основания (аминогликозиды, кодеин, кокаин, хинидин, циклизин)
Слайд 112ХПН
Нарушается почечная экскреция
Необходим перерасчет режима введения препаратов с высокой степенью
экскреции в неизмененном виде
↑ концентрация ЛВ в плазме крови
↓ связь
с белками плазмы↑ Т 1\2
Слайд 114Коррекция дозы ЛС при почечной недостаточности
ЛС с узким терапевтическим диапазоном,
которые выводятся почками в неизмененном виде более 50%
ЛС не являющиеся
ЛС с узким терапевтическим диапазоном, которые выводятся почками в неизмененном виде более 75%Слайд 118Коррекция дозы ЛС при заболевании печени по уровню альбумина плазмы
При
концентрации альбумина менее 30 г/л уменьшают дозу ЛС с эффектом
«первого прохождения» на 50 %При концентрации альбумина менее 30 г/л уменьшают дозу ЛС без эффекта «первого прохождения» на 25 %