Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коллоидтық химия ДӘРІС № 13
Содержание
- 1. Коллоидтық химия ДӘРІС № 13
- 2. Сабақтың жоспары:Коллоидтық химияның негізгі нысандары мен белгіліері;Коллоидтық жүйелердің жіктелуі; Коллоидты жүйелерді алу;Коллоидты ерітінділерді тазарту әдістері.
- 3. Коллоидтық химия – дисперстік жүйелер мен фазалардың бөліну
- 4. Коллоидты химияның даму кезеңдері XIX ғ
- 5. Қазақстанда Коллоидтық химия саласындағы зерттеулер А.В. Думанскийдің жетекшілігімен 1942 – 44
- 6. Химия ғылымдары институтында Қазақстанның минералды адсорбенттері (Ш.Батталова),
- 7. Қазіргі Коллоидтық химия мына құбылыстар мен процестерді
- 8. 5) дисперстік жүйелердің молекула-кинетикалық және тасымал құбылыстарын
- 9. 9) дисперстік жүйелердің физика-химия механикасы, дисперстік жүйелердегі
- 10. Слайд 10
- 11. ДИСПЕРСТІ ЖҮЙЕЛЕРДІҢ ҚҰРАМЫДИСПЕРСТІ ФАЗА(дисперсті жүйенің майдаланған ұсақталған бөлігі)ДИСПЕРСТІК ОРТА(дисперсті жүйенің бөлінбейтін бөлігі)
- 12. Дисперстік фаза мен дисперстік ортаның агрегаттық күйіне
- 13. 2. Дисперстік ортасы газ, алдисперстік фазасы сұйық
- 14. 3. Дисперстік ортасы қатты заттар, алдисперстік фазасы
- 15. Майдалану яғни дисперстену дәрежесі бойынша ДЖ жіктеленеді:1.
- 16. Дисперстік дәрежесі әртүрлі ДЖ сипаттамалары
- 17. Коллоидтік ерітінділер немесе зольдер Ағыл. sol от лат. solutio — ерітінді —
- 18. Коллоидтық жүйелердің белгілері:
- 19. Көлденең қимасының ауданы (а) – дөнгелек бөлшектердің
- 20. Дисперстік ортаның табиғатына қарай зольдердің жіктелуіОртасы жалпы
- 21. Коллоидтық қосылыстардың жіктелуіДисперсті фаза мен дисперсті ортаның
- 22. Слайд 22
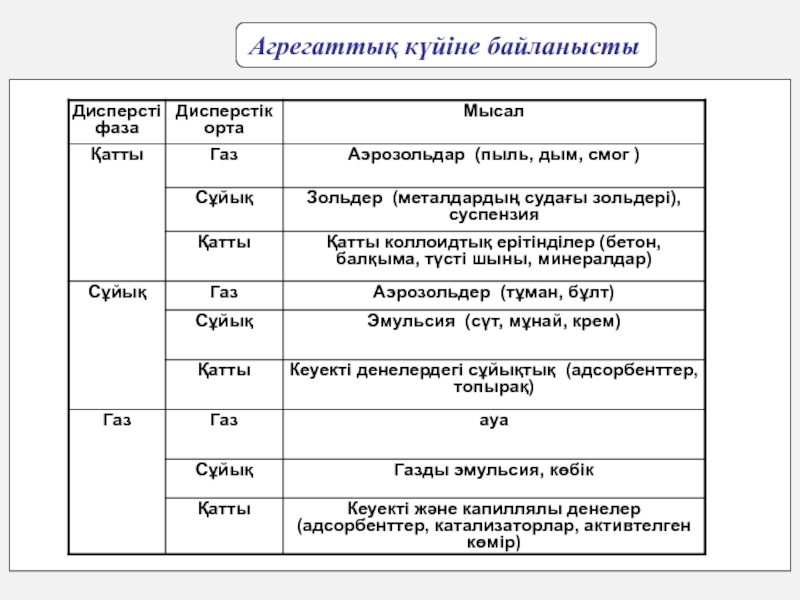
- 23. Агрегаттық күйіне байланысты
- 24. Коллоидтық қосылыстардың ерекшеліктері2. Термодинамикалық тұрақсыздық3. Туындысы болмайды4. Құрылым түзуге қабілеттілік
- 25. Дисперстік жүйелерді алуДисперстілеу – ірі бөлшектерді коллоидты-дисперстілік
- 26. Дисперстілеуді жеңілдету үшін қаттылықты төмендеткіштерді қолданады: электролиттер,
- 27. Конденсация сатылары2. Коллоидтық бөлшектің өсуі3. Стабилизатор қабатының түзілуі (ДЭҚ).
- 28. Шынайы ерітіндіден молекулаларды агрегатқа ассоциациялауға негізделген; Ірі
- 29. Физикалық конденсация әдісі
- 30. Химиялық конденсациялық әдістер
- 31. Слайд 31
- 32. 3. Тотығу реакциясы Күкірт золін алу2H2Sр-р + O2 = 2S ↓+ 2H2O Мицелланың құрылысы:
- 33. 4. Гидролиз реакциясы Темір гидроксидінің золін алу:FeCl3 + 3H2O = Fe(OH)3 ↓ + 3HCl Мицелланың құрылысы:
- 34. Слайд 34
- 35. Диализ – зольдерді жартылай өткізгіш мембрана арқылы
- 36. Өндірісте электродализ – зольдерді сыртқы электр тоғымен электролиттік қоспалардан тазарту әдісі жиі қолданады - электродиализ
- 37. Коллоидтық бөлшектің құрылысы
- 38. Мицелланың құрылысы
- 39. Мысал:
- 40. Коллоидтық жүйелердің қолданылуы мен маңызыБұлттар, тұман С/Г
- 41. Қағаз жасауда өсімдік талшығы жоғары дисперстік күйге
- 42. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Сабақтың жоспары:
Коллоидтық химияның негізгі нысандары мен белгіліері;
Коллоидтық жүйелердің жіктелуі;
Коллоидты
жүйелерді алу;
Слайд 3 Коллоидтық химия – дисперстік жүйелер мен фазалардың бөліну беттерінде болатын беттік
құбылыстарды зерттейтін ғылым саласы.
Коллоидтық химия дисперстік жүйелердің түзілу және бұзылу
жолдарын, қасиеттерін, фазалардың жанасу беттеріндегі молекулааралық әрекеттесу құбылыстарын зерттейді. Сондай-ақ, оның зерттеу нысандарына әр түрлі дисперстік жүйелер, дисперстік фазалар мен дисперстік ортаның жанасу беттері, адсорбциялық қабаттар, ламинарлық және фибриллалық жүйелер, аэрозольдер, ұнтақтар, көбіктер, эмульсиялар, жүзгіндер (суспензиялар), әр түрлі гельдер мен зольдер жатады. Золь деп коллоидтық жүйені айтады.
Слайд 4Коллоидты химияның даму кезеңдері
XIX ғ 60-жылдарында «Коллоид» түсінігін Т.Грем
алғашқы рет енгізген кезде химияның іргелі заңдары, А.М. Бутлеровтың құрылыс
теориясы мен Д.И.Менделеевтің периодттық заңы белгілі болды.1816 жылы алғаш рет П.Лаплас капилярлық қысым үшін сандық қатынастарды есептеді. 1808 жылы Мәскеу университетінің профессоры Ф.Ф. Рейсс саз балшықтың электролизін зерттей отырып, дисперсті жүйелерді электр тоғы өткенде байқалатын электрокинетикалық құбылыстарды ашты.
Слайд 5 Қазақстанда Коллоидтық химия саласындағы зерттеулер А.В. Думанскийдің жетекшілігімен 1942 – 44 ж. басталды.
Қазақ
ұлттық университетінде (Қ.Мұсабеков, Ж.Әбілев, В.П. Пальмер) үлкен молекулалы заттардың жаңа класы –
полиэлектролиттер мен кіші молекулалы беттік актив заттар (БАЗ) алынып, бұларды фазаға бөлу (С.Айдарова, К.Омарова), солюбилизация (Т.И. Юй Цун-синь) және флокуляция (Н.Түсіпбаев) процестерінде қолдану әдістері табылды.Слайд 6 Химия ғылымдары институтында Қазақстанның минералды адсорбенттері (Ш.Батталова), тұтқыр заттар қатаюының
физика-химия негіздері (С.Сүлейменова) зерттелуде, тұзды суды тұщы суға айналдыру мәселелері
шешілді (Е.Ерғожин), жаңа флокулянттар алу (Е.Шайхутдинов), пайдалы қазбалар мен өте төзімді көбіктерді флотациялық жолмен байыту (А.Байшолақов, М.Баймаханов), иониттерді алмастыра сорбциялау (А.Дадабаев) әдістері іздестірілді, беттік актив заттардың электродтық процестерге (М.Наурызбаев) және техникалық аэрозольдердің тұрақтылығына (А.А. Цыпура) тигізетін әсері анықталды. Республикада Коллоидтық химия жөніндегі зерттеулерді Қазақ ұлттық университеті үйлестіріп отырады. Петрянов-Соколов И.В., Фролов Ю.Г.Слайд 7 Қазіргі Коллоидтық химия мына құбылыстар мен процестерді қарастырады:
1) беттік
және капиллярлық құбылыстар (адсорбция және жүзу құбылыстарының термодинамикалық және кинетикалық
заңдылықтары, адсорбциялық қабаттардың қасиеттері, беттік белсенді заттардың әр түрлі фазааралық беттерге әсер ету заңдылықтары мен механизмдері);2) қатты дене беттерінің химиясы (қатты денелердің беттік қабаттарындағы кристалдың және электрондық құрылымдарының ерекшеліктері, оларда болатын сорбциялық құбылыстар заңдылықтары);
3) электрокинетикалық және электрокапиллярлық құбылыстар және ион алмасу құбылыстары (коллоидтық электрохимия);
4) дисперстік жүйелердің оптикалық қасиеттері (коллоидтық оптика);
Слайд 8 5) дисперстік жүйелердің молекула-кинетикалық және тасымал құбылыстарын зерттеп, оларды дисперсиялық
талдауға пайдалану;
6) лиофильдік және лиофобтық дисперстік жүйелердің пайда болу
(түзілу) термодинамикасы мен теориялары, оларды алу және тазарту жолдары (диализ, электрдиализ жәнеультрафильтрация); 7) лиофильдік коллоидтық жүйелер, олардың пайда болу аймақтары, екі-үш құрауышты беттік-белсенді заттары бар термодинамикалық тепе-теңдік жүйелердің құрылысын зерттеу, жұқа қабыршақтардың термодинамикасы мен физика-химия гидродинамикасы, қабыршақтардың жұқалану заңдылықтары;
8) дисперстік жүйелердің тұрақтылық теориясы, тұрақтылық факторлары, дисперстік фаза бөлшектерінің коагуляциясы (флокуляциясы), коалесценция және олардың заңдылықтары;
Слайд 9 9) дисперстік жүйелердің физика-химия механикасы, дисперстік жүйелердегі құрылым түзілу, олардың
түрлері және заңдылықтары, реологиялық зерттеулер.
Коллоидтық химия құрылыс материалдары мен силикаттар,
бояу мен пигменттер және қатты заттарды ұнтақтап майдалау технологиясының, флотация әдісі мен кен байыту технологиясының, жуу процестерінің негізін құрайды. Мұнайдағы өте майда су эмульсиясын бұзу арқылы оны су мен тұздан тазарту, көбіктерді өрт сөндіруге қолдану, т.б. маңызды мәселелер Коллоидтық химия негізінде шешіледі. Коллоидтық химияның биология, геология, медицина және т.б. ғылымдар үшін де маңызы зор.
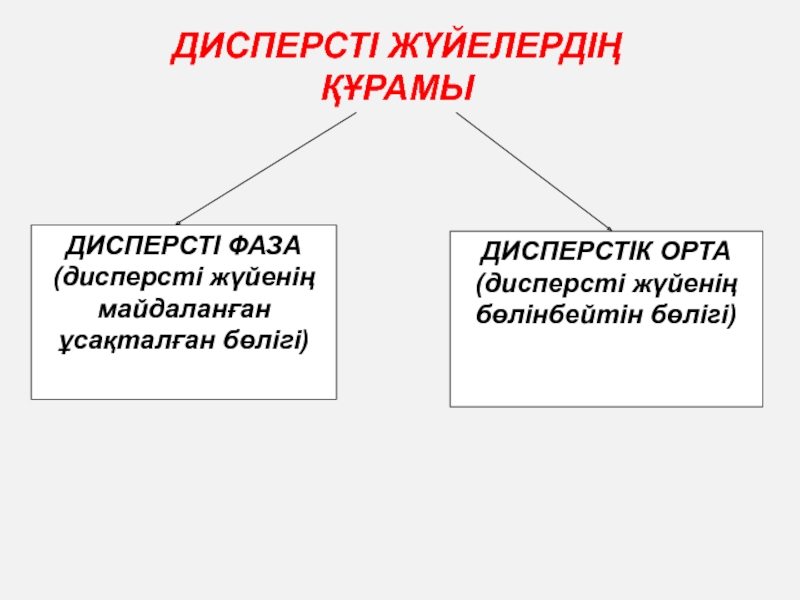
Слайд 11ДИСПЕРСТІ ЖҮЙЕЛЕРДІҢ ҚҰРАМЫ
ДИСПЕРСТІ ФАЗА
(дисперсті жүйенің майдаланған ұсақталған бөлігі)
ДИСПЕРСТІК ОРТА
(дисперсті жүйенің
бөлінбейтін бөлігі)
Слайд 12 Дисперстік фаза мен дисперстік ортаның агрегаттық күйіне қарай дисперстік жүйелер
келесідей жіктеленеді:
1. Дисперстік ортасы сұйық, ал
дисперстік фазасы газ болып келетін
жүйелер көбіктер деп аталады;дисперстік фазасы сұйық болып келетін жүйелер эмульсиялар деп аталады;
дисперстік фазасы қатты заттар болып келетін жүйелер суспензиялар деп аталады.
Слайд 132. Дисперстік ортасы газ, ал
дисперстік фазасы сұйық болып келетін жүйелер
аэрозольдер деп аталады;
дисперстік фазасы ұсақталған қатты заттар болып келетін жүйелерге
ұнтақтар, түтін, әртүрлі заттардың шаңдары жатады.Слайд 143. Дисперстік ортасы қатты заттар, ал
дисперстік фазасы газ болып келетін
жүйелер қатты көбіктер деп аталады;
дисперстік фазасы сұйық болып келетін жүйелерге
сұйық қоспалары бар табиғи минералдар – қатты эмульсиялар: маржан тас, опал және т.б. жатады:дисперстік фазасы қатты заттар болып келетін жүйелерге – қатты суспензияларға металдың балқымалары, бағалы тастар, түсті шынылар, көк тас тұзы және т.б. жатады.
Слайд 15Майдалану яғни дисперстену дәрежесі бойынша ДЖ жіктеленеді:
1. Ірідисперсті жүйелердің бөлшектерінің
ұсақталған өлшемі:
>10-7 м немесе >100 нм
2. Коллоидтік-дисперсті жүйелер:
≈ 10-7
- 10-9 м, 1 - 100 нм3. Молекулалық-иондық (шынайы ерітінділер) жүйелер:
< 10-9 м, < 1 нм
Слайд 17Коллоидтік ерітінділер немесе зольдер
Ағыл. sol от лат. solutio — ерітінді — сұйық немесе газды дисперстік
ортасының көлемінде дисперстік фаза бөлшектері көпіршіктер, тамшылар не ұнтақтар түрінде
таралған жоғарыдисперстік жүйе (коллоидтік ерітінді)Клейстер
Томат шырыны
Клеи
Слайд 19 Көлденең қимасының ауданы (а) – дөнгелек бөлшектердің диаметрі (d) и
куб тәрізді бөлшектердің ені (l).
Дисперстілік (D) – бөлшектің көлденең қимасына
кері шама: D=1/a. Меншікті беттік аудан (Sм) – дисперстік фазаның массасы мен көлеміне сәйкес келетін фаза аралық беттік қабат:
Слайд 20Дисперстік ортаның табиғатына қарай зольдердің жіктелуі
Ортасы жалпы сұйық болатын жүйелере
– лиозольдер деп аталады;
Ортасы су болса – гидрозоль;
Ортасы спирт болса
– алкозоль;Ортасы бензол болса – бензозоль;
Ортасы эфир болса – этерозоль;
Ортасы газ болса – аэрозоль.
Слайд 21Коллоидтық қосылыстардың жіктелуі
Дисперсті фаза мен дисперсті ортаның өзара әрекеттесуі б-ша:
1.
Лиофильді (гидрофильді) жүйелер дисперсті фаза мен дисперсті орта бөлшектері арасындағы
әрекеттесулер өте жоғары.2. Лиофобты (гидрофобты) жүйелер – екі фаза арасындағы молекулааралық әрекеттесу нашар өтеді.
Слайд 24Коллоидтық қосылыстардың ерекшеліктері
2. Термодинамикалық тұрақсыздық
3. Туындысы болмайды
4. Құрылым түзуге қабілеттілік
Слайд 25Дисперстік жүйелерді алу
Дисперстілеу – ірі бөлшектерді коллоидты-дисперстілік дәрежесіне дейін ұнтақтау.
Конденсация
– атомдар, молекулалар, иондарды коллоидты-дисперстілік дәрежесіне дейін ірілету, біріктіру.
Слайд 26 Дисперстілеуді жеңілдету үшін қаттылықты төмендеткіштерді қолданады: электролиттер, эмульсиялар, БАЗ және
т.б.
Қаттылықты төмендеткіштер ұнтақталған заттың жалпы массасының 0,1 % қажет
энергия шығымын 2 есе төмендетеді. Слайд 28Шынайы ерітіндіден молекулаларды агрегатқа ассоциациялауға негізделген;
Ірі дисперсті жүйелерді алуда
қолданылады;
Сыртқы жұмысты қажет етпейді;
Жаңа фазаның пайда болуы аса
қанық ортада жүреді. Конденсациялық әдіс
Слайд 33 4. Гидролиз реакциясы
Темір гидроксидінің золін алу:
FeCl3 + 3H2O = Fe(OH)3
↓ + 3HCl
Мицелланың құрылысы:
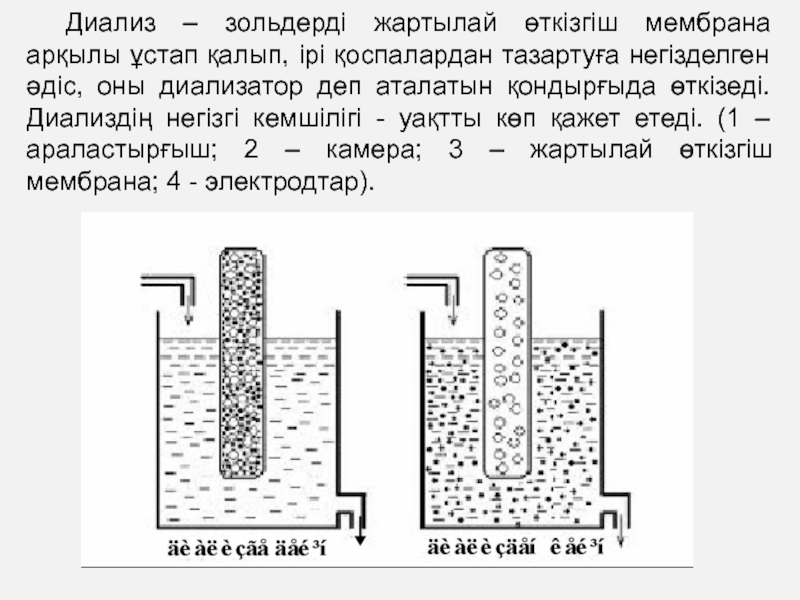
Слайд 35Диализ – зольдерді жартылай өткізгіш мембрана арқылы ұстап қалып, ірі
қоспалардан тазартуға негізделген әдіс, оны диализатор деп аталатын қондырғыда өткізеді.
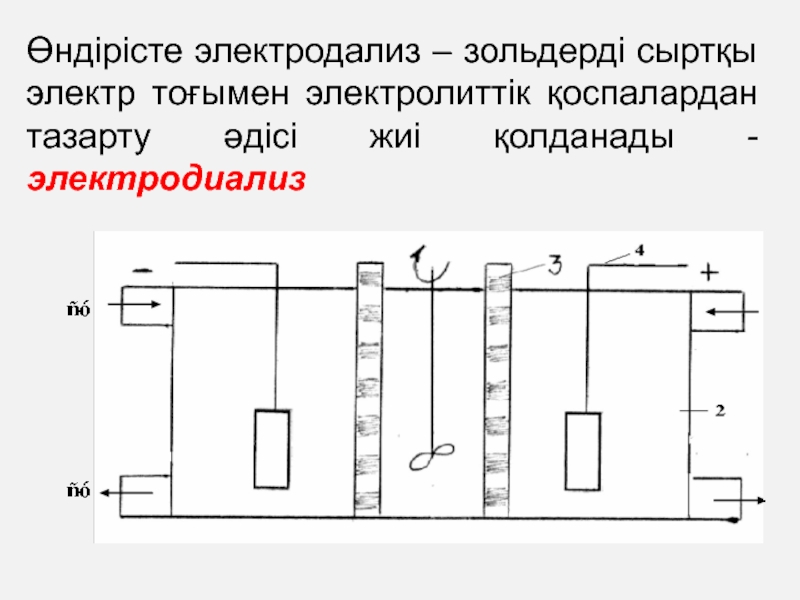
Диализдің негізгі кемшілігі - уақтты көп қажет етеді. (1 – араластырғыш; 2 – камера; 3 – жартылай өткізгіш мембрана; 4 - электродтар).Слайд 36Өндірісте электродализ – зольдерді сыртқы электр тоғымен электролиттік қоспалардан тазарту
әдісі жиі қолданады - электродиализ
Слайд 40Коллоидтық жүйелердің қолданылуы мен маңызы
Бұлттар, тұман С/Г типті коллоидты жүйелер,
ал жаңбыр, найзағай және басқа да метеорологиялық құбылыстар коллоидтық құбылыстармен
байланысты құбылыстар деп қарастырылуы керек.Керамикалық өндіріс коллоидтық химиямен тығыз байланысты. Себебі саз (керамиканың негізгі шикізаты) –гидратталған алюминий силикатының концентрлі суспензиясы болып табылады.
Минералдық шикізат негізінде жаңа құрылыстық материалдар (композициялық материалдар) жасауда колоидтық химияның маңызы өте зор.