технологического оборудования,
Санитарно-гигиенические мероприятия на предприятии и в подразделениях,
Порядок проведения
валидации/квалификации,
Порядок контроля производственной среды,
Порядок калибровки и поверки оборудования.
Порядок отбраковки продукции при производстве и контроле качества.
Порядок медицинского освидетельствования персонала.
Порядок тестирования исходных материалов и готовой продукции.
Порядок очистки и дезинфекции оборудования и помещений.
Уборка производственных помещений (отдельные инструкции для разных конкретных помещений),
Подготовка к входу в “чистые” помещения.
Порядок надевания технологической одежды.
Порядок отбора проб сырья (для каждого типа – жидкое, твердое), образцов упаковочных материалов, готовой продукции,
Порядок уничтожения и документального оформления бракованной продукции (каждого типа – ампулы, таблетки, капсулы и т.д.).
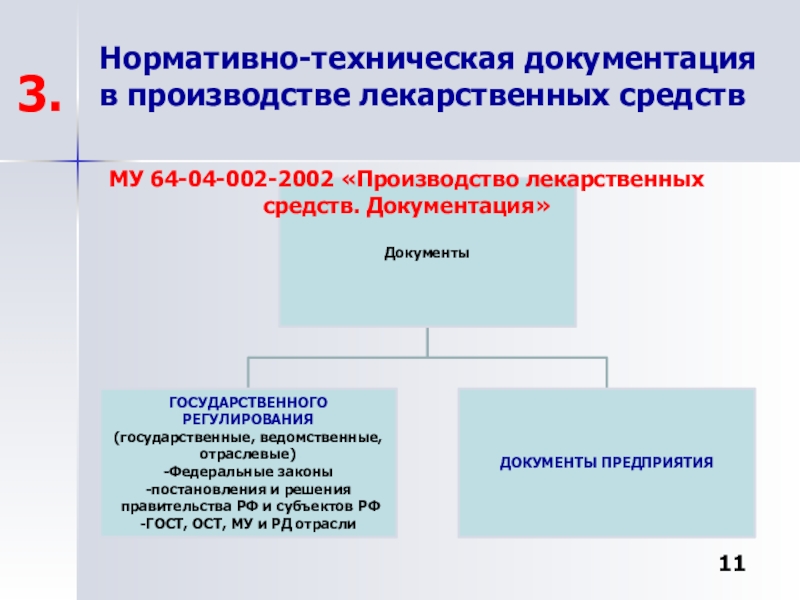
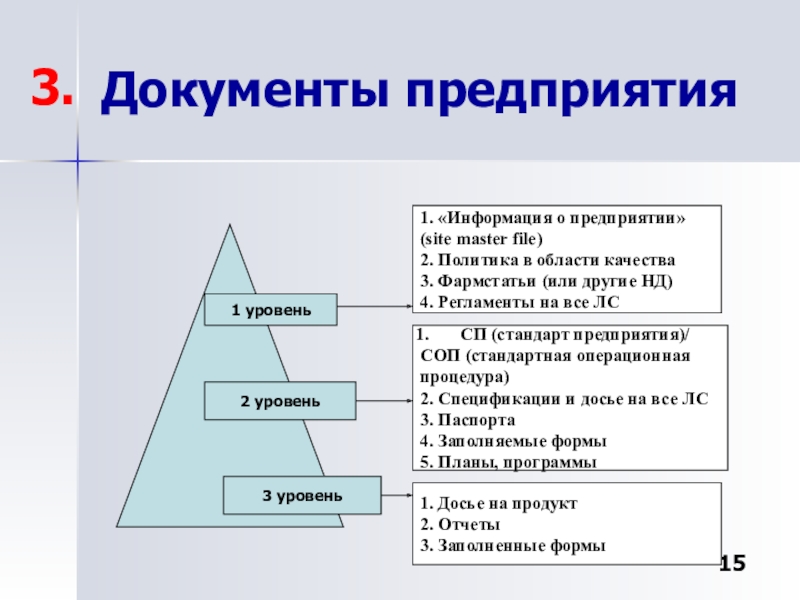
Стандартные операционные процедуры по документации.
3.