Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кристаллохимия
Содержание
- 1. Кристаллохимия
- 2. Элементы симметрииПростые оси симметрии – поворот на угол 360o/nn – порядок оси симметрии
- 3. Инверсионные оси симметрии – поворот на угол
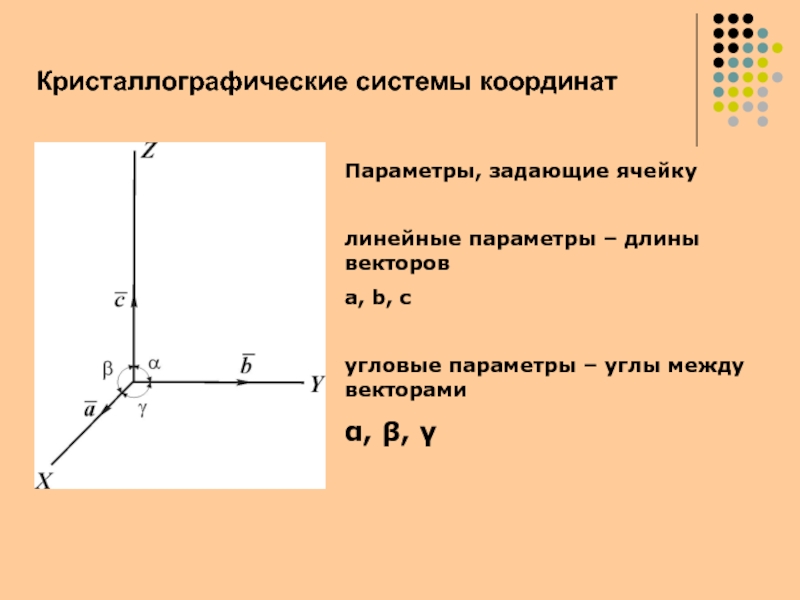
- 4. Параметры, задающие ячейкулинейные параметры – длины векторов
- 5. Кристаллографические системы координат
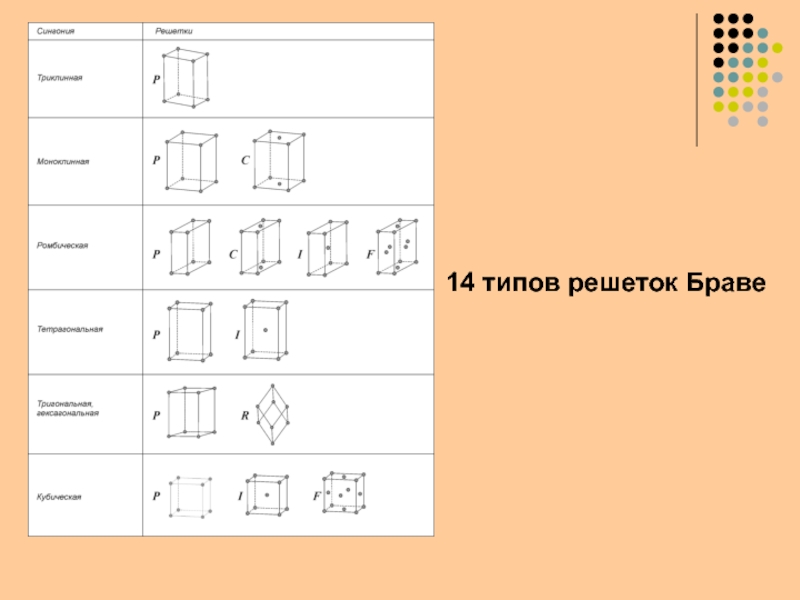
- 6. 14 типов решеток Браве
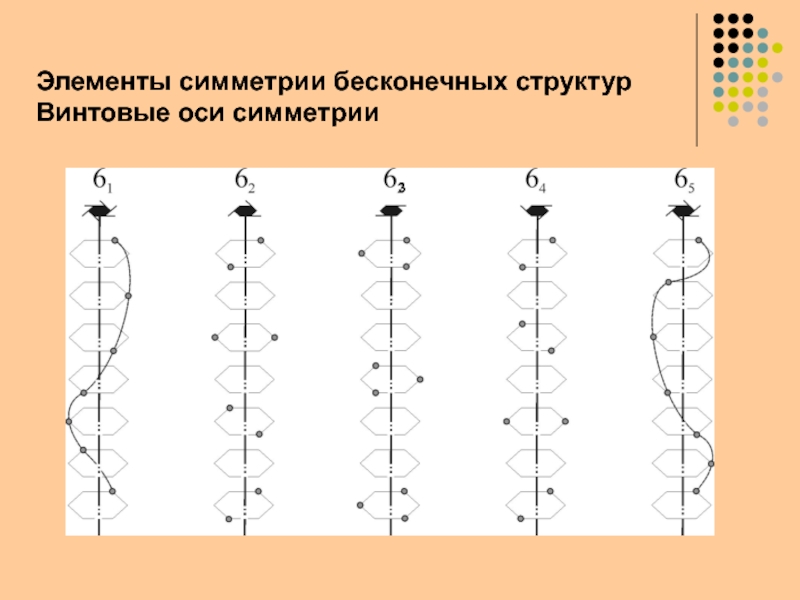
- 7. Элементы симметрии бесконечных структурВинтовые оси симметрии
- 8. Элементы симметрии бесконечных структурВинтовые оси симметрии3
- 9. Элементы симметрии бесконечных структурВинтовые оси симметрии - система обозначений
- 10. отражение + перенос вдоль плоскостиноменклатура плоскостей определяется
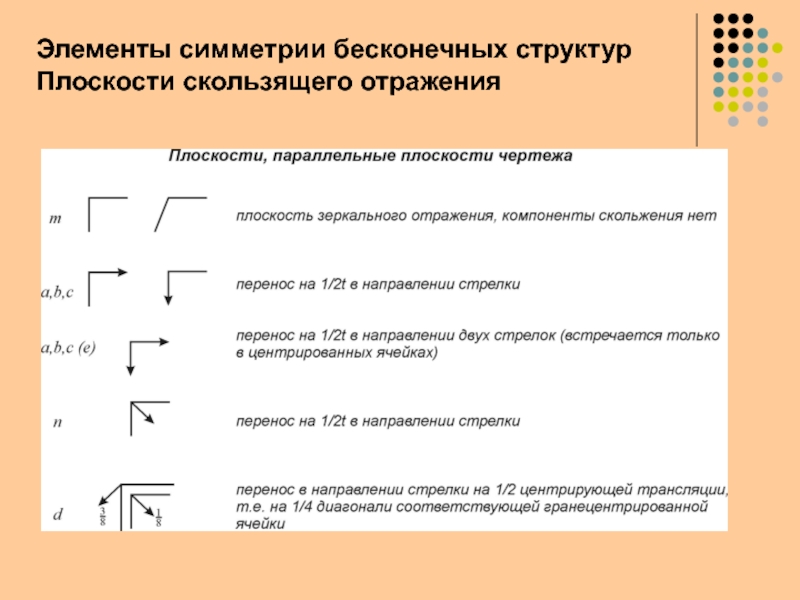
- 11. Элементы симметрии бесконечных структурПлоскости скользящего отражения
- 12. Элементы симметрии бесконечных структурПлоскости скользящего отражения
- 13. Правила записи пространственных группТриклинная сингония:1. Тип решетки
- 14. Тетрагональная сингония:1. Тип решетки Браве2. Направление [001]
- 15. Правила записи пространственных группКубическая сингония:1. Тип решетки
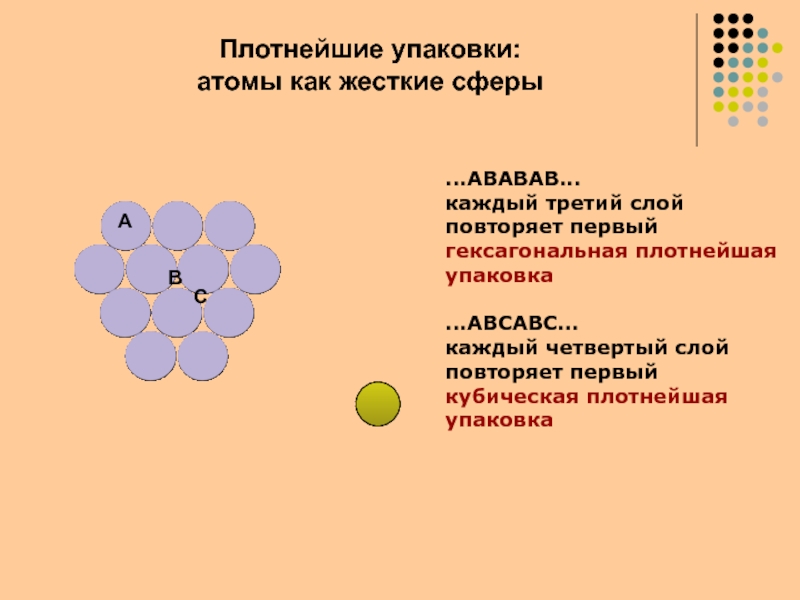
- 16. ...ABABAB...каждый третий слойповторяет первыйгексагональная плотнейшаяупаковка...ABCABC...каждый четвертый слойповторяет первыйкубическая плотнейшая упаковкаABCПлотнейшие упаковки: атомы как жесткие сферы
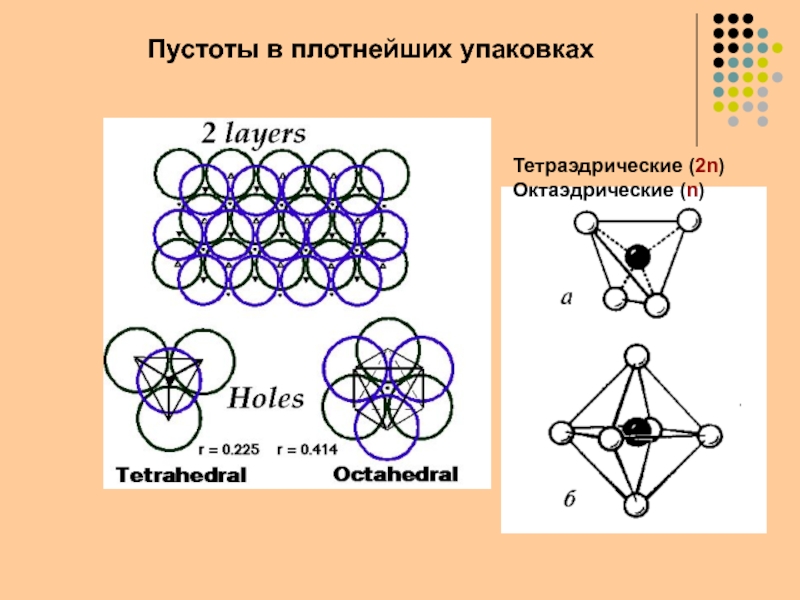
- 17. Пустоты в плотнейших упаковкахТетраэдрические (2n)Октаэдрические (n)
- 18. Теорема Кеплера:в трехмерном пространстве плотнейшая упаковкашаров имеет
- 19. КЧ – это число ближайших к данному
- 20. Z – количество элементарных формул соединения в
- 21. Простые вещества и галогениды:АлмазГрафитalfa-железоМедьМагний (Цинк)NaClCsClCaF2CdI2Необходимо:Определение и запись пространственной группыПлотнейшая упаковка, пустотыКЧКПZ
- 22. Простые вещества и галогениды:АлмазFd-3m кубическая сингонияКЧ =
- 23. Простые вещества и галогениды:Mg (Zn)P63/mmcгексагональная сингонияКЧ =
- 24. Простые вещества и галогениды:α-железоIm-3m кубическая сингонияКЧ =
- 25. Простые вещества и галогениды:CsClPm-3m кубическая сингонияКЧ (Cs)
- 26. Простые вещества и галогениды:CdI2P-3m1 тригональная (ромбоэдрическая) сингонияКЧ
- 27. Оксиды и сульфиды:КупритРутилПеровскитШпинельБруситСфалеритВюрцитПиритПирротинНикелин
- 28. Оксиды и сульфиды:Куприт Cu2OPn-3m кубическая сингонияКЧ (Cu)
- 29. Оксиды и сульфиды:Перовскит CaTiO3Pm3mкубическая сингонияКЧ (Ti) =
- 30. Оксиды и сульфиды:Брусит Mg(OH)2P-3m1 тригональная сингонияструктура аналогична
- 31. Оксиды и сульфиды:Сфалерит ZnSF-43m кубическая сингонияКЧ (Zn)
- 32. Оксиды и сульфиды:Пирит FeS2Pa3 кубическая сингонияZ =
- 33. Карбонаты:КальцитАрагонитОртосиликаты:ЦирконОливинКольцевые силикаты:Берилл
- 34. Кальцит CaCO3Тригональная сингония Ромбоэдрическая структураR-3cК.ч. (Ca) =
- 35. Циркон ZrSiO4ТетрагональнаясингонияI41/amd Z = 4 К.ч. (Si) = 4, тетраэдрК.ч. (Zr) = 8
- 36. Оливин (Mg,Fe)2SiO4Ромбическая сингонияPbnm, Z = 4 К.ч.
- 37. Берилл Be3Al2Si6O18Гексагональная сингонияP6/mcc К.ч. (Be) = 4, тетраэдрК.ч. (Al) = 6, октаэдр
- 38. Цепочечные силикаты:Диопсид (пироксены)Ленточные силикаты:Тремолит (амфиболы)Слоистые силикаты:КаолинитМусковитКаркасные силикаты:КварцТридимимтКристобалитСанидинСульфаты:БаритАнгидрит
- 39. Пироксены СТ Диопсид Ca(Mg,Fe)2Si2O6M2M1(Si2O6)Моноклинная сингонияС2/c, Z =
- 40. ПироксеныСТ Диопсид Ca(Mg,Fe)2Si2O6M2M1(Si2O6)Слои из полиэдров (M1 и M2), соединяют цепочки Si2O6, вытянутые вдоль оси с
- 41. АмфиболыСТ ТремолитCa2Mg5[Si4O11]2(OH)2 R2R5[Si4O11]2(OH)2Моноклинная сингонияС2/m, Z = 2, c
- 42. АмфиболыСТ Тремолит R2R5[Si4O11]2(OH)2
- 43. Слоистые силикатыбрусит Mg(OH)2триоктаэдрическийслойгиббсит Al(OH)3диоктаэдрическийслойКомбинация октаэдрических и тетраэдрических сеток порождает разнообразие слоистых силикатов
- 44. Слоистые силикатыВарианты укладки:2:1
- 45. триоктадиокта2:1
- 46. КаолинитAl2[Si2O5](OH)4P-1диоктаэдрический1:1
- 47. МусковитKAl2[AlSi3O10](OH)2C2/cдиоктаэдрический2:1наличие межслоевого катиона
- 48. Политипия слюдРазличное расположение слоевдруг относительно друга –в
- 49. Каркасные силикатыSiO2 кварц Тригональная сингонияP3121 (P3221)Объединение через
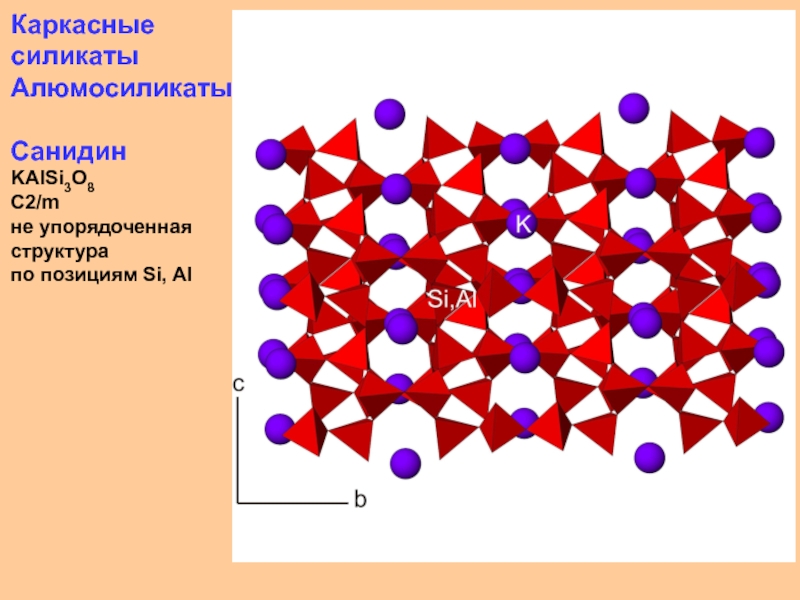
- 50. Каркасные силикатыАлюмосиликатыСанидин KAlSi3O8C2/mне упорядоченная структура по позициям Si, Al
- 51. СульфатыБарит BaSO4Ромбическая сингонияPnma baZ=4Псевдотетрагональная структураТетраэдры SO4 связаны CaК.ч. (Ca) = 8
- 52. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Инверсионные оси симметрии – поворот на угол 360o/n
плюс отражение в
точке инверсии
n – порядок оси симметрии
Элементы симметрии
Слайд 4Параметры, задающие ячейку
линейные параметры – длины векторов
a,
b, c
угловые параметры – углы между векторами
, ,
Кристаллографические системы
координатСлайд 10отражение + перенос вдоль плоскости
номенклатура плоскостей
определяется направлением переноса
например,
плоскость a
– перенос вдоль вектора a
(т.е. вдоль оси X)
Элементы симметрии бесконечных
структурПлоскости скользящего отражения
Слайд 13Правила записи пространственных групп
Триклинная сингония:
1. Тип решетки Браве (всегда P-ячейка
при стандартной установке)
2. P1 или P-1
Моноклинная сингония:
1. Тип решетки Браве
2.
Ось 2-го порядка или перпендикулярная ей плоскостьПримеры: P21/c, P2, Cc
Ромбическая сингония:
1. Тип решетки Браве
2. Ось симметрии, совпадающая с первой кристаллографической осью (x) и перпендикулярная ей плоскость
3. Ось симметрии, совпадающая со второй кристаллографической осью (y) и перпендикулярная ей плоскость
4. Ось симметрии, совпадающая с третей кристаллографической осью (z) и перпендикулярная ей плоскость
Примеры: Ibam, P2221, Cma2
Слайд 14Тетрагональная сингония:
1. Тип решетки Браве
2. Направление [001] – ось симметрии,
совпадающая с z и перпендикулярная ему плоскость
3. Направление [100] =
[010] и перпендикулярная ему плоскость4. Диагональное направление [110] и перпендикулярная ему плоскость
Примеры: I41/a, P-42m, I41/amd
Тригональная и гексагональная сингония:
1. Тип решетки Браве
2. Направление [0001] – ось симметрии, совпадающая с z и перпендикулярная ему плоскость
3. Большая диагональ: плоскость, проходящая вдоль большой диагонали и (или) перпендикулярная ей ось
4. Малая диагональ: плоскость, проходящая вдоль малой диагонали и (или) перпендикулярная ей ось
Примеры: P63/mc, P63/mcm, P63221
Правила записи пространственных групп
Слайд 15Правила записи пространственных групп
Кубическая сингония:
1. Тип решетки Браве
2. Координатное направление
[100] = [010] = [001] и перпендикулярная ему плоскость
3. Направление
[111] – ось 3-го порядка4. Диагональное направление [110] и перпендикулярная ему плоскость
Примеры: Fm-3m, F-43m, Pn-3m, Pa-3, P213
Слайд 16...ABABAB...
каждый третий слой
повторяет первый
гексагональная плотнейшая
упаковка
...ABCABC...
каждый четвертый слой
повторяет первый
кубическая плотнейшая
упаковка
A
B
C
Плотнейшие
упаковки:
атомы как жесткие сферы
Слайд 18Теорема Кеплера:
в трехмерном пространстве плотнейшая упаковка
шаров имеет максимальную плотность 74.08%.
(кубическая,
гексагональная плотнейшие упаковки
и их варианты).
Доказана только в 2005 году!
Слайд 19КЧ – это число ближайших к данному атому соседних атомов
(лиганды) в структуре кристалла независимо от того, являются они атомами
того же сорта, что и центральный, или иного.NaCl КЧ(Na) = КЧ(Cl) =
Координационные числа (КЧ), координационные полиэдры (КП),
число формульных единиц (Z)
6
6
КП – геометрия расположения лигандов вокруг центрального атома.
Слайд 20Z – количество элементарных формул соединения в одной ячейки.
Ca: 1/8*8
+ ½*6 = 4
F: 1*8 = 8
Ca4F8 = 4 (CaF2)
– Z = 4a
б
в
г
д
ж
е
з
и
к
Некоторые координационные полиэдры, встречающиеся в кристаллических структурах:
а — гантель (КЧ = 2); б — треугольник (КЧ = 3); в — квадрат (КЧ = 4)
г — тетраэдр (КЧ = 4); д — тригоиальная призма (КЧ = 6);
е — октаэдр (КЧ = 6); ж — куб (КЧ = 8); з — томсоновский куб (КЧ = 8)
и — архимедов кубооктаэдр (КЧ = 12)
к — гексагональный аналог кубооктаэдра (КЧ = 12).
Слайд 21Простые вещества и галогениды:
Алмаз
Графит
alfa-железо
Медь
Магний (Цинк)
NaCl
CsCl
CaF2
CdI2
Необходимо:
Определение и запись пространственной группы
Плотнейшая упаковка,
пустоты
КЧ
КП
Z
Слайд 22Простые вещества и галогениды:
Алмаз
Fd-3m
кубическая сингония
КЧ = 4
КП – тетраэдр
Z
= 8
степень заполнения пр-ва 32%
Графит
P63/mmc
гексагональная сингония
КЧ = 3
КП –
треугольникZ = 4
степень заполнения пр-ва 21%
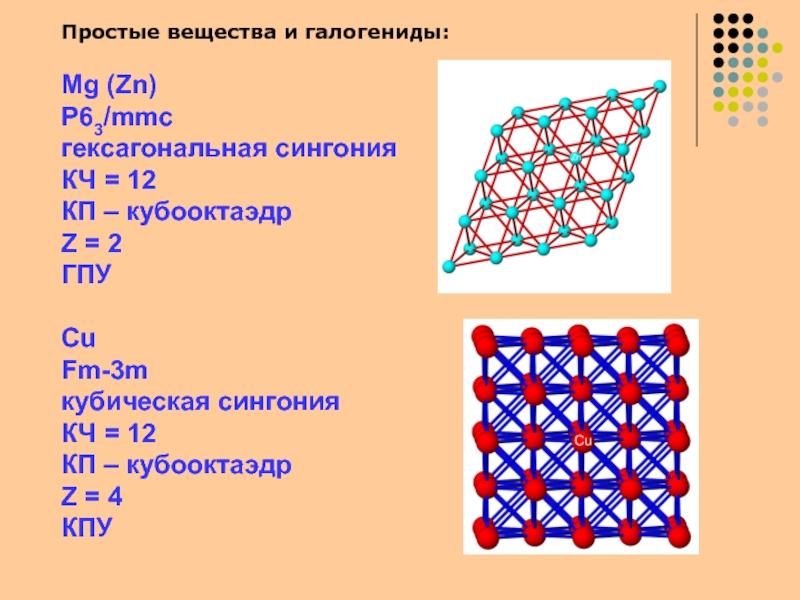
Слайд 23Простые вещества и галогениды:
Mg (Zn)
P63/mmc
гексагональная сингония
КЧ = 12
КП – кубооктаэдр
Z
= 2
ГПУ
Cu
Fm-3m
кубическая сингония
КЧ = 12
КП – кубооктаэдр
Z = 4
КПУ
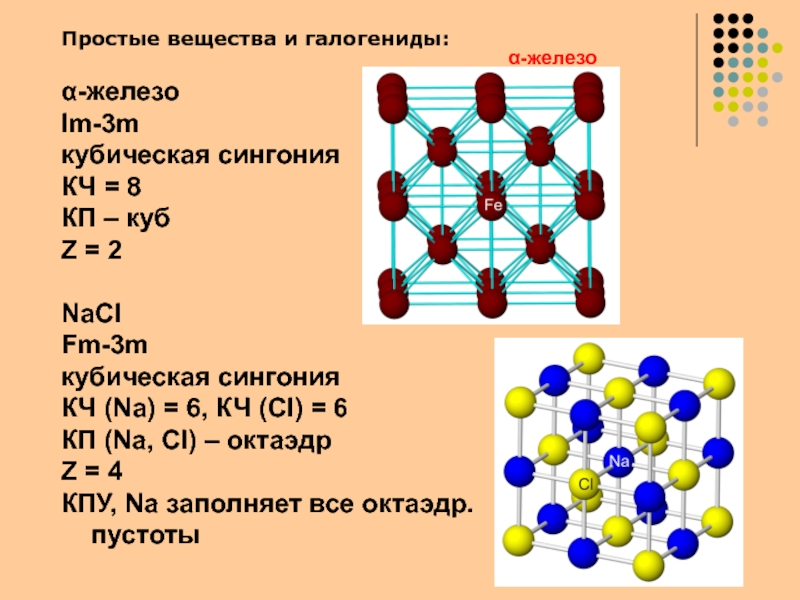
Слайд 24Простые вещества и галогениды:
α-железо
Im-3m
кубическая сингония
КЧ = 8
КП – куб
Z
= 2
NaCl
Fm-3m
кубическая сингония
КЧ (Na) = 6, КЧ (Cl) =
6КП (Na, Cl) – октаэдр
Z = 4
КПУ, Na заполняет все октаэдр. пустоты
α-железо
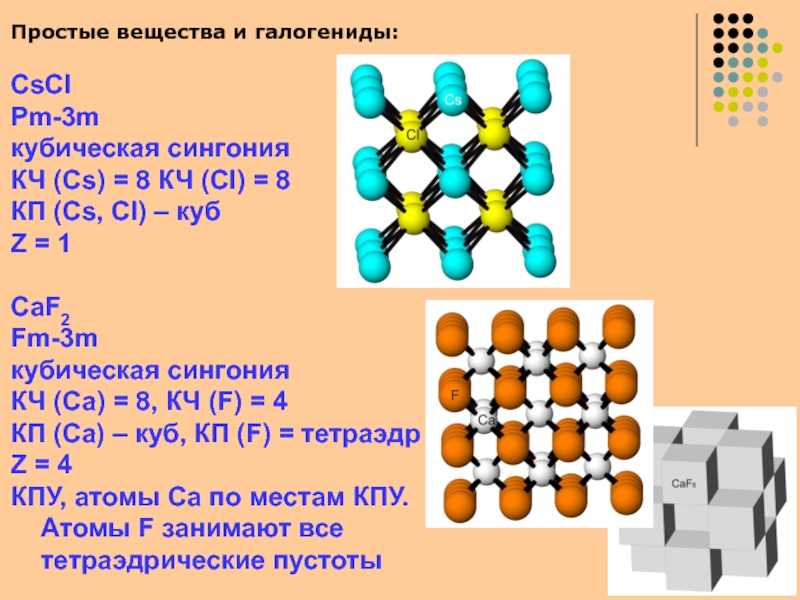
Слайд 25Простые вещества и галогениды:
CsCl
Pm-3m
кубическая сингония
КЧ (Cs) = 8 КЧ
(Cl) = 8
КП (Cs, Cl) – куб
Z = 1
CaF2
Fm-3m
кубическая
сингонияКЧ (Ca) = 8, КЧ (F) = 4
КП (Ca) – куб, КП (F) = тетраэдр
Z = 4
КПУ, атомы Ca по местам КПУ. Атомы F занимают все тетраэдрические пустоты
Слайд 26Простые вещества и галогениды:
CdI2
P-3m1
тригональная (ромбоэдрическая) сингония
КЧ (Cd) = 6
КП
(Cd) – октаэдр
Z = 1
Атомы I образуют ГПУ
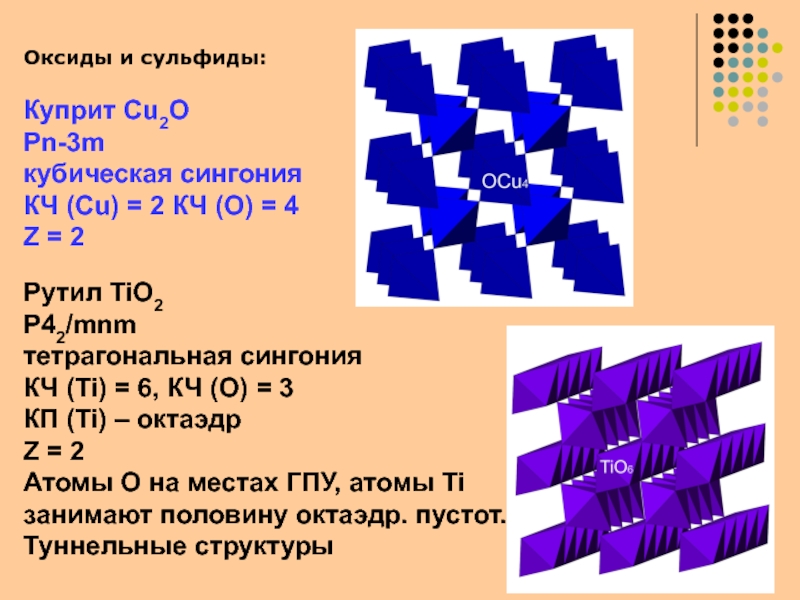
Слайд 28Оксиды и сульфиды:
Куприт Cu2O
Pn-3m
кубическая сингония
КЧ (Cu) = 2 КЧ
(O) = 4
Z = 2
Рутил TiO2
P42/mnm
тетрагональная сингония
КЧ (Ti) =
6, КЧ (O) = 3КП (Ti) – октаэдр
Z = 2
Атомы О на местах ГПУ, атомы Ti
занимают половину октаэдр. пустот.
Туннельные структуры
Слайд 29Оксиды и сульфиды:
Перовскит CaTiO3
Pm3m
кубическая сингония
КЧ (Ti) = 6
КП (Ti) –
октаэдр
TiO6 объединяются через вершины в каркас
(колонны), Ca в пустотах.
Шпинель прямая
Mg2+[4]Al3+[6] 2O4Fd-3m
кубическая сингония
прямая шпинель: большой атом (R) занимает
меньшую пустоту
Fe3+[4]Fe3+[6]Fe2+[6]O4 – обращенная (магнетит)
Mg2+ 0.72; Al3+ 0.53; Fe2+ 0.63; Fe3+ 0.55
Слайд 30Оксиды и сульфиды:
Брусит Mg(OH)2
P-3m1
тригональная сингония
структура аналогична CdI2
КЧ (Mg) =
6 КП (Mg) – октаэдр
OH группы образуют ГПУ, Mg в
октаэдрических пустотах. Триоктаэдрическая структура – октаэдры связаны через общие ребра, все 3 октаэдрические позиции занятыСлайд 31Оксиды и сульфиды:
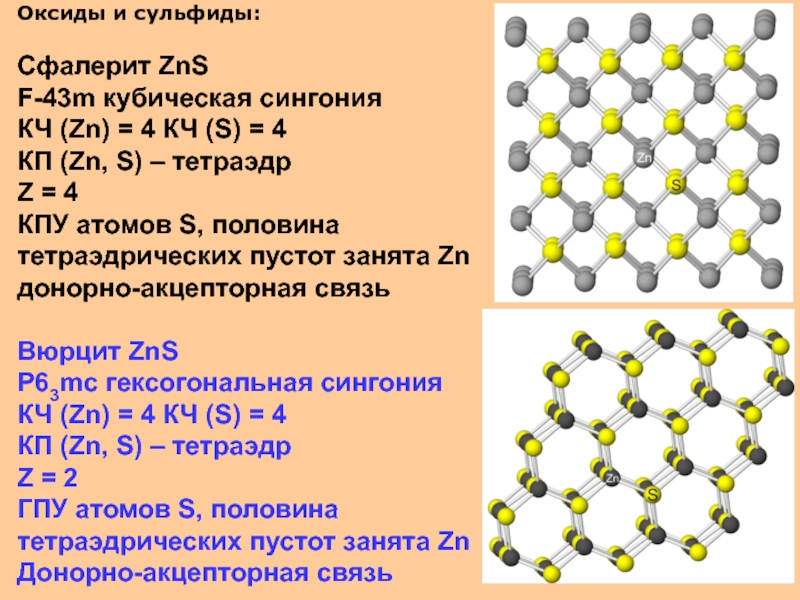
Сфалерит ZnS
F-43m кубическая сингония
КЧ (Zn) = 4 КЧ
(S) = 4
КП (Zn, S) – тетраэдр
Z = 4
КПУ атомов
S, половина тетраэдрических пустот занята Zn
донорно-акцепторная связь
Вюрцит ZnS
P63mc гексогональная сингония
КЧ (Zn) = 4 КЧ (S) = 4
КП (Zn, S) – тетраэдр
Z = 2
ГПУ атомов S, половина
тетраэдрических пустот занята Zn
Донорно-акцепторная связь
Слайд 32Оксиды и сульфиды:
Пирит FeS2
Pa3 кубическая сингония
Z = 4
связь S2 –
ковалентная,
связь Fe-S – донорно-акцепторная
Пирротин FeS, Никелин NiAs
P63/mmc гексагональная
сингонияКЧ (Fe, Ni) = 6 КЧ (S, As) = 6
КП (Fe, Ni) – октаэдр
Z = 2
ГПУ атомов S (As), октаэдрические
пустоты занята Fe (Ni).
Донорно-акцепторная связь Fe-S
FeS6 октаэдры образуют колонки,
связь в колонках металлическая
Слайд 34Кальцит CaCO3
Тригональная сингония
Ромбоэдрическая структура
R-3c
К.ч. (Ca) = 6
К.ч. (O)
= 3
Арагонит CaCO3
Ромбическая сингония
К.ч. (Ca) = 9 К.ч. (C) =
3 Z = 4
Pmcn a
двухслойную плотнейшую
упаковку, Ca окружен 6 группами
CO3, но 9 атомами O
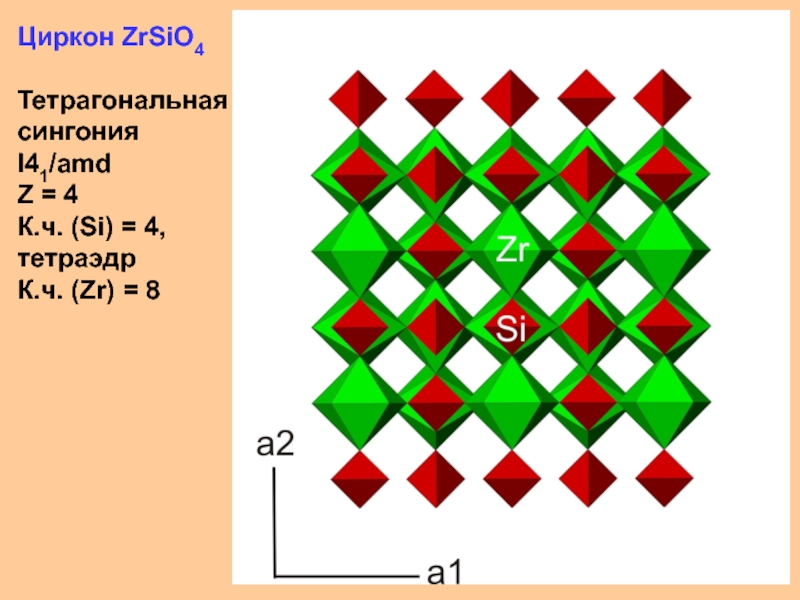
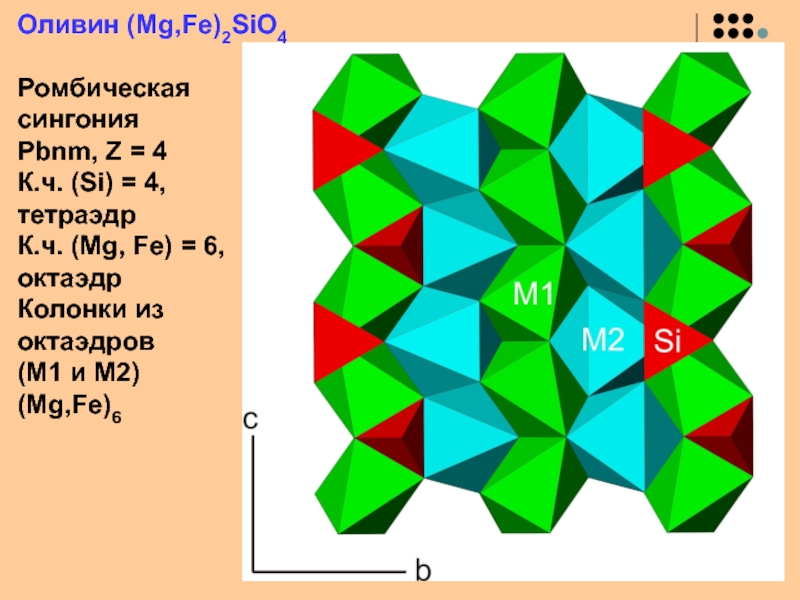
Слайд 36Оливин (Mg,Fe)2SiO4
Ромбическая
сингония
Pbnm, Z = 4
К.ч. (Si) = 4,
тетраэдр
К.ч. (Mg, Fe) = 6,
октаэдр
Колонки из
октаэдров
(M1 и
M2) (Mg,Fe)6
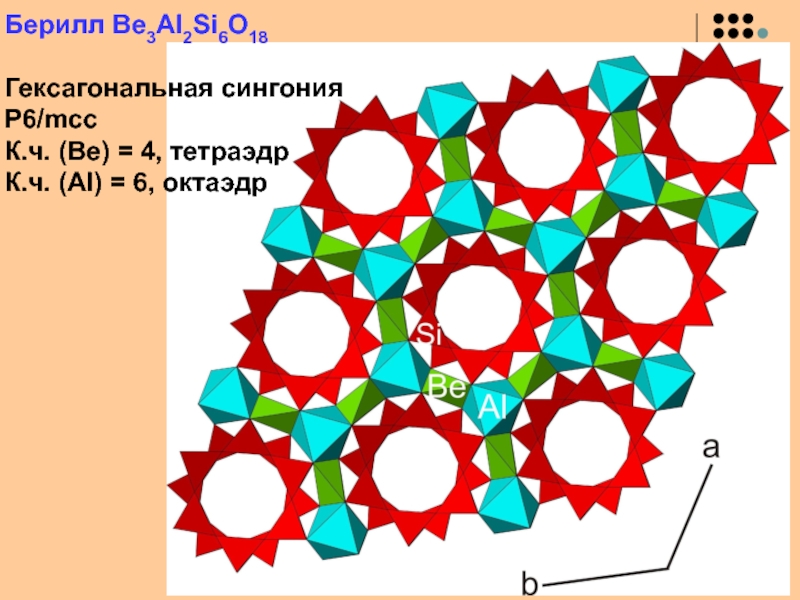
Слайд 37Берилл Be3Al2Si6O18
Гексагональная сингония
P6/mcc
К.ч. (Be) = 4, тетраэдр
К.ч. (Al) =
6, октаэдр
Слайд 38Цепочечные силикаты:
Диопсид (пироксены)
Ленточные силикаты:
Тремолит (амфиболы)
Слоистые силикаты:
Каолинит
Мусковит
Каркасные силикаты:
Кварц
Тридимимт
Кристобалит
Санидин
Сульфаты:
Барит
Ангидрит
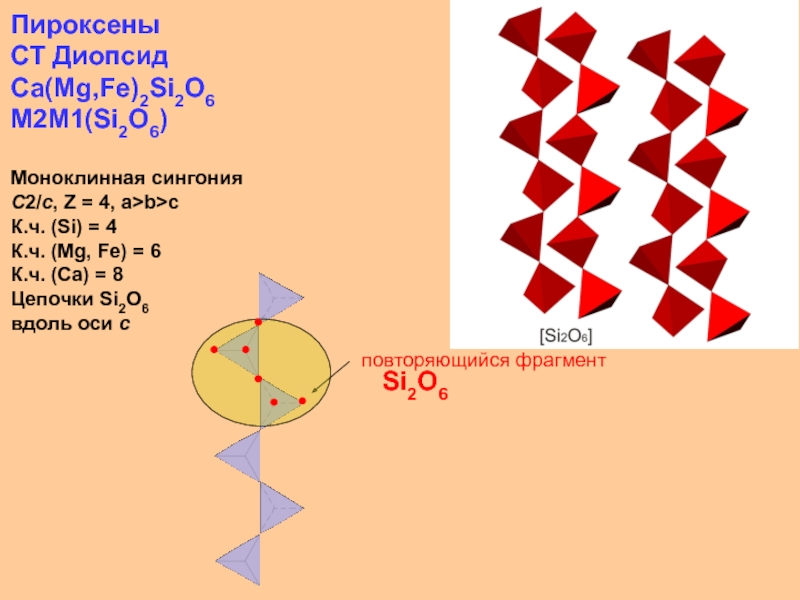
Слайд 39Пироксены
СТ Диопсид
Ca(Mg,Fe)2Si2O6
M2M1(Si2O6)
Моноклинная сингония
С2/c, Z = 4, a>b>c
К.ч.
(Si) = 4
К.ч. (Mg, Fe) = 6
К.ч. (Ca) = 8
Цепочки
Si2O6 вдоль оси с
Si2O6
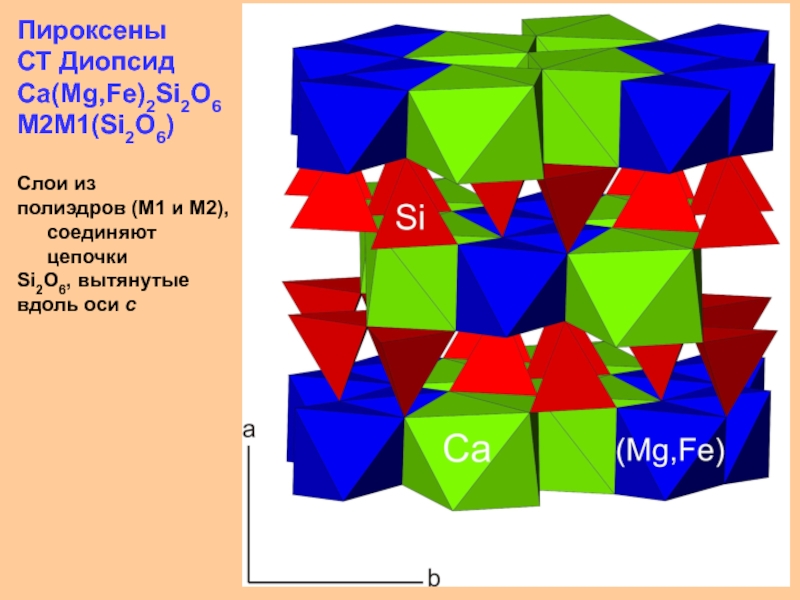
Слайд 40Пироксены
СТ Диопсид
Ca(Mg,Fe)2Si2O6
M2M1(Si2O6)
Слои из
полиэдров (M1 и M2), соединяют цепочки
Si2O6, вытянутые
вдоль оси с
Слайд 41Амфиболы
СТ Тремолит
Ca2Mg5[Si4O11]2(OH)2
R2R5[Si4O11]2(OH)2
Моноклинная сингония
С2/m, Z = 2, c
= 4
К.ч. (Mg, Fe) = 6
К.ч. (Ca) = 8
Сдвоенные цепочки
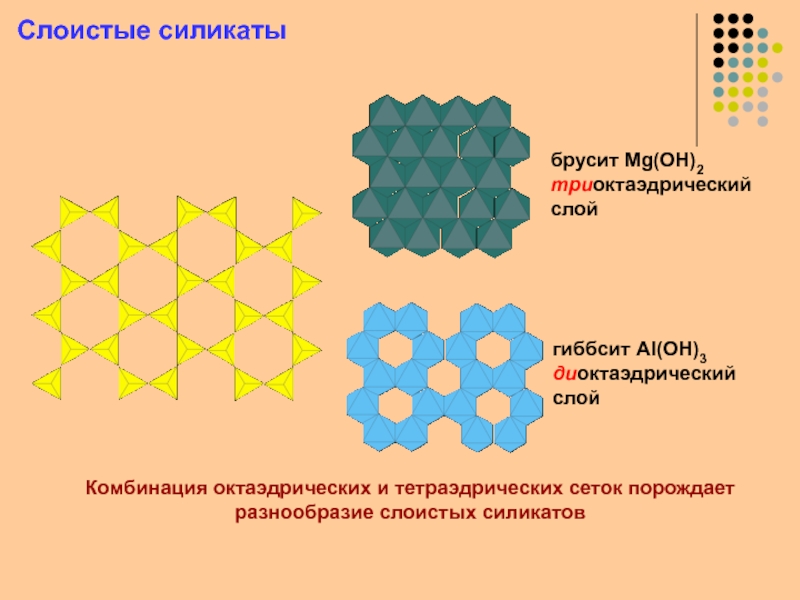
Si4O11 вдоль оси с, между которыми расположены октаэдры Fe и Mg. Октаэдры Fe и Mg образуют колонки, сшитые в стенки, вытянутые вдоль оси сСлайд 43Слоистые силикаты
брусит Mg(OH)2
триоктаэдрический
слой
гиббсит Al(OH)3
диоктаэдрический
слой
Комбинация октаэдрических и тетраэдрических сеток порождает
разнообразие
слоистых силикатов
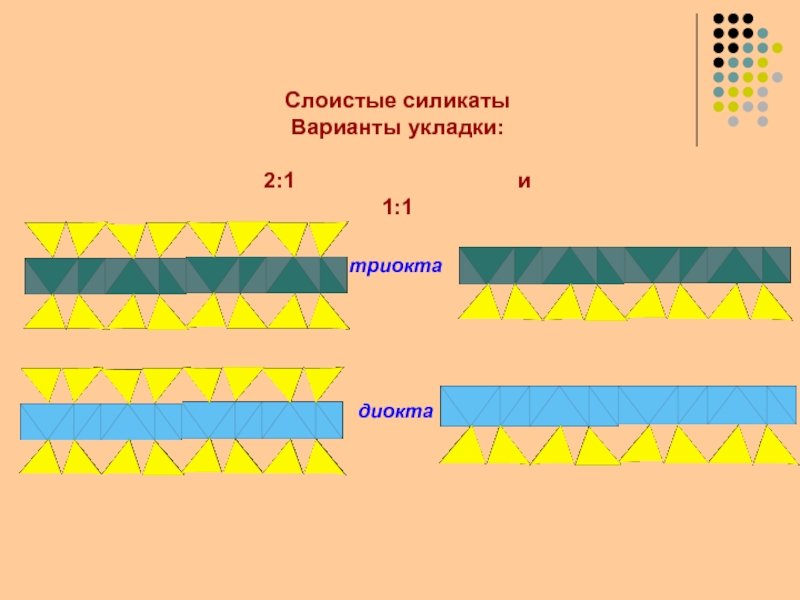
Слайд 45триокта
диокта
2:1
1:1
тальк
Mg3[Si2O5]2(OH)2
пирофиллит
Al2[Si2O5]2(OH)2
лизардит и хризотил
Mg3[Si2O5](OH)4
каолинит
Al2[Si2O5](OH)4
Слайд 48
Политипия слюд
Различное расположение слоев
друг относительно друга –
в упорядоченных политипах может
быть
описано по расположению
межслоевых катионов (напр., K+)
при взгляде на слой
сверху, т.е.прямо перпендикулярно слою
Слайд 49Каркасные силикаты
SiO2 кварц
Тригональная сингония
P3121 (P3221)
Объединение через все общие
вершины
тетраэдров SiO4
SiO2 Тридимит
Гексагональная сингония
P63/mmc
SiO2 Кристаболит
Кубическая сингония
Fd3m
Слайд 50Каркасные
силикаты
Алюмосиликаты
Санидин
KAlSi3O8
C2/m
не упорядоченная
структура
по позициям Si, Al
Слайд 51Сульфаты
Барит BaSO4
Ромбическая сингония
Pnma
b
и окружают 7 SO4 групп
Ангидрит CaSO4
Ромбическая сингония
Сmcm
c>b>a
Z=4
Псевдотетрагональная структура
Тетраэдры SO4
связаны CaК.ч. (Ca) = 8








![Кристаллохимия Тетрагональная сингония:1. Тип решетки Браве2. Направление [001] – ось симметрии, совпадающая Тетрагональная сингония:1. Тип решетки Браве2. Направление [001] – ось симметрии, совпадающая с z и перпендикулярная ему плоскость3.](/img/thumbs/bfc1d09dcb909613a1ff82dd8edc5f03-800x.jpg)
![Кристаллохимия Правила записи пространственных группКубическая сингония:1. Тип решетки Браве2. Координатное направление [100] Правила записи пространственных группКубическая сингония:1. Тип решетки Браве2. Координатное направление [100] = [010] = [001] и перпендикулярная](/img/thumbs/e60e4843788393948092de020d64884c-800x.jpg)













![Кристаллохимия АмфиболыСТ ТремолитCa2Mg5[Si4O11]2(OH)2 R2R5[Si4O11]2(OH)2Моноклинная сингонияС2/m, Z = 2, c АмфиболыСТ ТремолитCa2Mg5[Si4O11]2(OH)2 R2R5[Si4O11]2(OH)2Моноклинная сингонияС2/m, Z = 2, c](/img/thumbs/521e817e2cba5eb5ff231cd9f05269b5-800x.jpg)
![Кристаллохимия АмфиболыСТ Тремолит R2R5[Si4O11]2(OH)2 АмфиболыСТ Тремолит R2R5[Si4O11]2(OH)2](/img/thumbs/f0221f5cbda1611e6fbde41d0129de3d-800x.jpg)
![Кристаллохимия триоктадиокта2:1 1:1талькMg3[Si2O5]2(OH)2пирофиллитAl2[Si2O5]2(OH)2лизардит и хризотилMg3[Si2O5](OH)4каолинитAl2[Si2O5](OH)4 триоктадиокта2:1](/img/thumbs/70ec04c2acf3871488dfa3f0de8d4e64-800x.jpg)
4P-1диоктаэдрический1:1 КаолинитAl2[Si2O5](OH)4P-1диоктаэдрический1:1](/img/thumbs/f99ca6473b3adfc287b0a6502a59cb20-800x.jpg)
2C2/cдиоктаэдрический2:1наличие межслоевого катиона МусковитKAl2[AlSi3O10](OH)2C2/cдиоктаэдрический2:1наличие межслоевого катиона](/img/thumbs/1f72ca829e85ca215f3fb2334e7817ae-800x.jpg)