Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лабораторная №2
Содержание
- 1. Лабораторная №2
- 2. Карбоновыми кислотаминазывают производные углеводородов, в молекулах которых
- 3. В этой сложной функциональной группе соединены друг
- 4. Насыщенные одноосновные кислотыНасыщенные кислоты являются производными насыщенных
- 5. Номенклатура Карбоксильная группа, как и альдегидная, может быть образована лишь первичным углеродным атомом.
- 6. Для простейших кислот широко используются тривиальные названия,
- 7. В молекулах всех других одноосновных кислот карбоксильная
- 8. Для насыщенных одноосновных кислот более точной является
- 9. Слайд 9
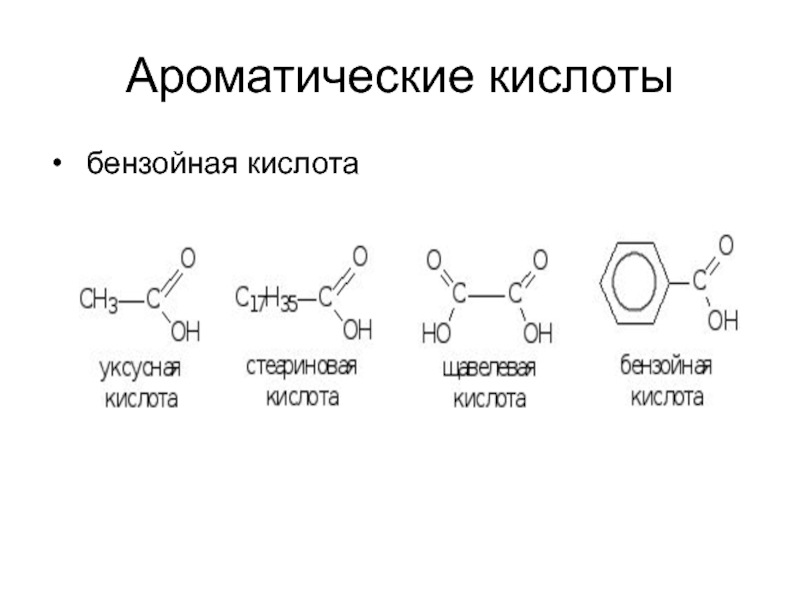
- 10. Ароматические кислоты бензойная кислота
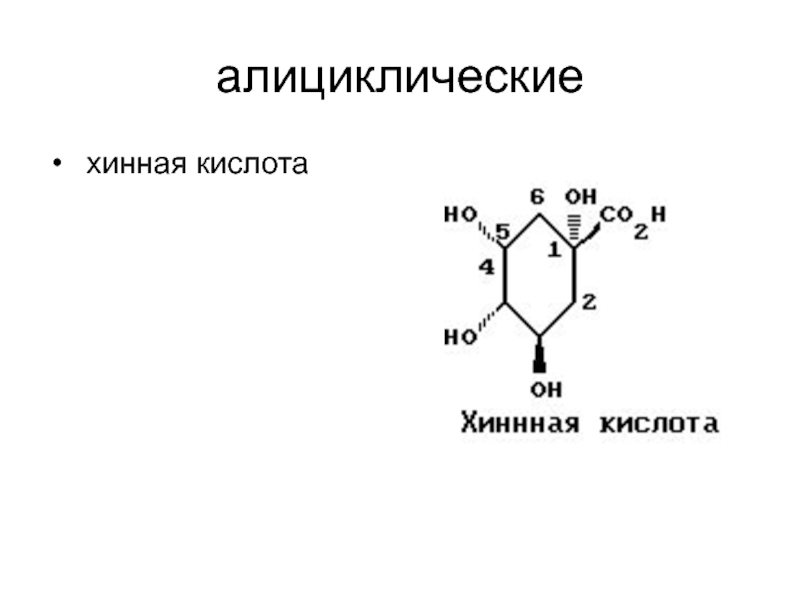
- 11. алициклические хинная кислота
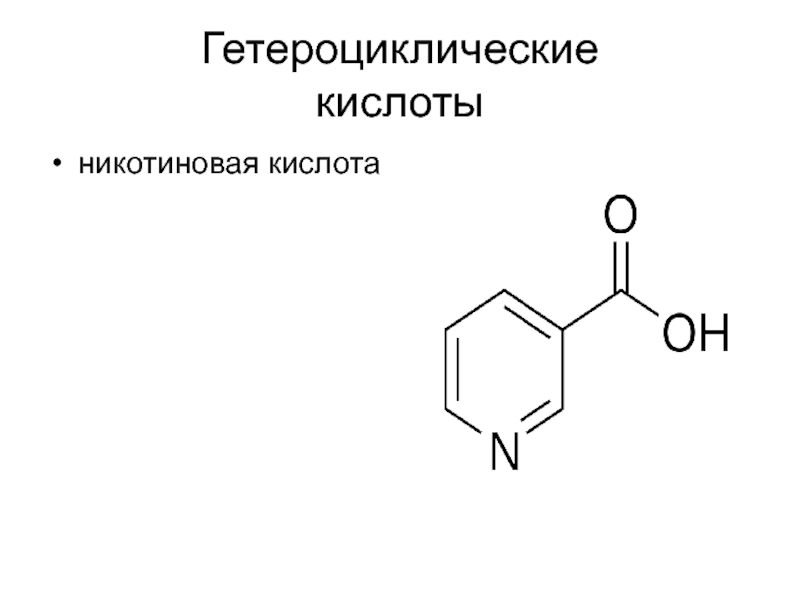
- 12. Гетероциклические кислотыникотиновая кислота
- 13. Кислоты называют, образуя прилагательное из заместительного названия,
- 14. Физические свойства предельных одноосновных кислотПервые три представителя
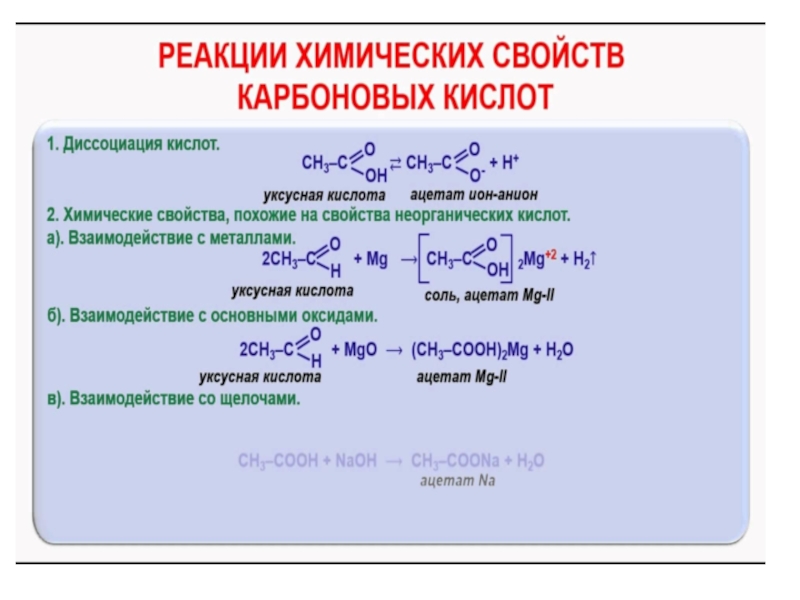
- 15. Химические свойстваХимические свойства карбоновых кислот определяются свойствами
- 16. Подвижность водорода карбоксильной группы (диссоциация карбоновых кислот)Подобно
- 17. Слайд 17
- 18. растворимые в воде карбоновые кислоты окрашивают лакмус
- 19. Образование солейПри взаимодействии с основаниями (реакция нейтрализации),
- 20. Соли карбоновых кислот и щелочных металлов как
- 21. Слайд 21
- 22. Скачать презентанцию
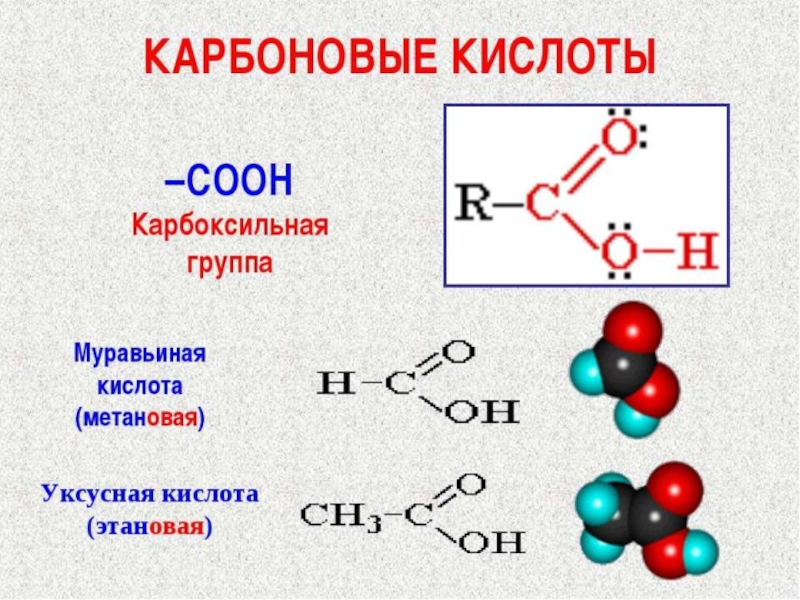
Карбоновыми кислотаминазывают производные углеводородов, в молекулах которых один или несколько углеродных атомов образуют карбоксильную группу или карбоксил
Слайды и текст этой презентации
Слайд 2Карбоновыми кислотами
называют производные углеводородов, в молекулах которых один или несколько
углеродных атомов образуют карбоксильную группу или карбоксил
Слайд 3В этой сложной функциональной группе соединены друг с другом две
простые кислородсодержащие группы: карбонильная - СО и гидроксильная (или окси
группа) –ОН; отсюда и происходит название – карбоксильная группа. Водород гидроксильной группы, входящей в карбоксильную группу, обуславливает кислотные свойства карбоновых кислот; поэтому число карбоксильных групп характеризует основность кислоты. В молекулах одноосновных (монокарбоновых) кислот – одна карбоксильная группа, двухосновных (дикарбоновых) кислот – две карбоксильные группы.Слайд 4Насыщенные одноосновные кислоты
Насыщенные кислоты являются производными насыщенных углеводородов. Высшие гомологи
этих кислот впервые были выделены из природных жиров, поэтому их,
а затем и все другие кислоты с открытой целью углеродных атомов назвали жирными кислотами.Слайд 5Номенклатура
Карбоксильная группа, как и альдегидная, может быть образована лишь
первичным углеродным атомом.
Слайд 6Для простейших кислот широко используются тривиальные названия, происходящие от названий
природных продуктов, из которых та или иная кислота была впервые
получена.Простейший представитель гомологического ряда насыщенных одноосновных кислот – муравьиная кислота, она была впервые обнаружена в выделениях муравьев, откуда и происходит ее название. В молекуле муравьиной кислоты имеется единственный углеродный атом, который и образует карбоксильную группу, соединенную с атомом водорода
Слайд 7В молекулах всех других одноосновных кислот карбоксильная группа соединена не
с водородом, а с тем или иным углеводородным остатком; их
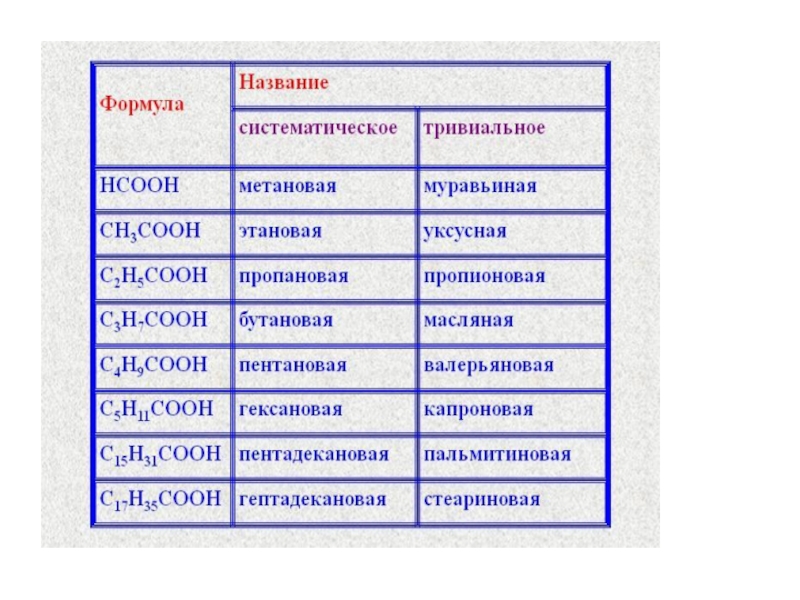
строение можно представить общей формулой R-C-OОHСлайд 8Для насыщенных одноосновных кислот более точной является общая формула CnH2n+1COOH,
показывающая, что в этих кислотах карбоксил соединен с остатками насыщенных
углеводородов.Слайд 13Кислоты называют, образуя прилагательное из заместительного названия, соответствующего по числу
атомов углерода и по строению углеводорода. Так, заместительное название муравьиной
кислоты–метановая кислота, уксусной - этановая, масляной – бутановая, изомасляной – 2-метилпропановая. Таким образом, для заместительных названий одноосных кислот характерно окончание – овая кислота.Слайд 14Физические свойства предельных одноосновных кислот
Первые три представителя предельных одноосновных кислот
– жидкости с острым характерным запахом. Они смешиваются с водой
во всех отношениях. Масляная кислота и следующие за ней гомологи – маслянистые, неприятно пахнущие жидкости, хуже растворимые в воде.Высшие кислоты – твердые, не растворимые в воде вещества. В органических растворителях (спирт, эфир) большинство кислот растворяются хорошо.
Температуры кипения жирных кислот нормального строения закономерно возрастают по мере увеличения числа углеродных атомов. Установлено, что молекулы кислот ассоциированы подобно тому, как ассоциированы молекулы воды или спиртов. Низшие кислоты хорошо перегоняются с водяным паром, поэтому их обычно называют летучими жирными кислотами.