Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА НАСЛЕДСТВЕННЫХ БОЛЕЗНЕЙ
Содержание
- 1. ЛЕЧЕНИЕ И ПРОФИЛАКТИКА НАСЛЕДСТВЕННЫХ БОЛЕЗНЕЙ
- 2. Основной принцип - индивидуализированное лечение (лечить
- 3. Методы лечения1. Симптоматическое2.Хирургическое3.Патогенетическое4. Этиологическое
- 4. Симптоматическое лечение Лекарственная симптоматическая терапия - наиболее
- 5. Симптоматическое лечениеМногие физические методы лечения (климатотерапия, бальнеолечение,
- 6. Хирургическое лечениеВыделяют три формы хирургической помощи: удаление,коррекция,ТрансплантацияОсобое
- 7. Патогенетическое лечение- это лечение по принципу вмешательства
- 8. Примеры патогенетического леченияКоррекция на уровне субстратаПри фенилкетонурии
- 9. Пример Увеличение внеклеточного белка недостаточность альфа-1 антитрипсинаМожет корректироваться ингаляциями альфа-1 антитрипсина
- 10. ПРИМЕРЫ терапия малыми молекуламиКуркумин в лечении муковисцидозаПри
- 11. Терапия малыми молекулами, приводящая к пропуску
- 12. Этиологическое лечение воздействие непосредственно на причину заболевания
- 13. Слайд 13
- 14. Слайд 14
- 15. Есть и третий подход- активация собственных генов
- 16. Историческая справкаПервым моногенным наследственным заболеванием, к которому
- 17. Слайд 17
- 18. Генная терапия СПИДаМутация гена CCR5, встречающаяся примерно
- 19. Введение геновВирусные векторыРЕТРОВИРУС: клетки-мишени: Фибробласты , Эндотелиальные
- 20. АДЕНОВИРУСклетки-мишени: Гепатоциты , Эпителий верхних дыхательных путей
- 21. АДЕНО-АССОЦИИРОВАННЫЙ ВИРУСклетки-мишени: Гематопоэтические клетки , Фибробласты ,
- 22. ГЕРПЕС ВИРУС (HSV) клетки-мишени: Неделящиеся клетки ,
- 23. Невирусные векторыкатионные липидсвязанные комплексы с ДНК в
- 24. Клетки-мишениГематопоэтические стволовые клеткиОдной из наиболее реальных мишеней
- 25. Клетки печениЭксперименты по генной терапии наследственной гиперхолестеролэмии
- 26. В настоящее времяСтадия клинических испытаний: иммунодефицит, гемофилия
- 27. РИСКИ генотерапии1. Неблагоприятный ответ на вектор(например, реакция
- 28. Не генная, но тоже очень перспективная терапияРазработаны
- 29. Важное направление -Плюрипотентные клеткиВ 2012 г. Нобелевскую
- 30. Слайд 30
- 31. Слайд 31
- 32. Слайд 32
- 33. ZFNs-«дизайнерские» ферменты адресно «собираются» под определенные гены-мишени
- 34. Карл Джун (Carl June) и Пабло Тебас
- 35. Transcription Activator-Like Effector Nucleases (TALENs) are artificial
- 36. CRISPR/Cas9 от англ. clustered regularly interspaced short palindromic repeats — короткие палиндромные повторы, регулярно расположенные группам
- 37. Rodolphe Barrangou, John van der Oost.
- 38. Для редактирования генома с помощью системы CRISPR/Cas9
- 39. ПрофилактикаПервичная профилактика– система мер, которые должны предупредить
- 40. Вторичная профилактика-это коррекция проявления патологических генов. При
- 41. Скачать презентанцию
Основной принцип - индивидуализированное лечение (лечить не болезнь, а болезнь у конкретного человека). Этот принцип особенно важен, поскольку наследственные болезни обладают гетерогенностью и с одной и той же клинической картиной
Слайды и текст этой презентации
Слайд 2 Основной принцип - индивидуализированное лечение (лечить не болезнь, а
болезнь у конкретного человека).
болезни обладают гетерогенностью и с одной и той же клинической картиной могут протекать разные наследственные заболевания с разным патогенезомСлайд 4Симптоматическое лечение
Лекарственная симптоматическая терапия - наиболее часто используемый метод. Например,
симптоматическая терапия миопатии включает в себя - витамины С, В,
антихолинэстеразные препараты, АТФ, аминокислоты, анаболические гормоны и другие средства, способствующие улучшению метаболизма в мышцах. Успехи этого раздела терапии связаны с прогрессом фармакологии, обеспечивающим все более широкий выбор лекарств. Вместе с тем расшифровка патогенеза каждой болезни позволяет понять причину возникновения симптома, а на этой основе становиться возможной более тонкая лекарственная коррекция.Слайд 5Симптоматическое лечение
Многие физические методы лечения (климатотерапия, бальнеолечение, разные виды электротерапии,
теплолечение) применяются при наследственных болезнях нервной системы, обмена веществ, заболеваниях
скелета.У больных после курсов такой терапии улучшается самочувствие, увеличивается продолжительность жизни. Практически при всех наследственных болезнях показано физиотерапевтическое лечение. Например, лекарственная терапия муковисцидоза постоянно дополняется многообразными физиотерапевтическими процедурами (ингаляции, массаж и другие). К симптоматическому можно отнести рентгенорадиологическое лечение при наследственно обусловленных опухолях. Симптоматическое лечение (особенно лекарственное и диетическое) широко применяется и будет использоваться в будущем наряду с самым совершенным патогенетическим и этиотропным лечением наследственных болезней.
Слайд 6Хирургическое лечение
Выделяют три формы хирургической помощи:
удаление,
коррекция,
Трансплантация
Особое значение имеет реконструктивная
хирургия, которая применяется при незаращении губы и нёба, атрезии ЖКТ,
коррекции костно-мышечной системыСлайд 7Патогенетическое лечение
- это лечение по принципу вмешательства в патогенез болезни.
При
этом исходят из того, что у больных либо образуется аномальный
белок, либо белка образуется недостаточно. За этими событиями следуют изменения цепи превращения субстрата или его продукта. Знание этих принципов позволяет разрабатывать схемы лечения.Слайд 8Примеры патогенетического лечения
Коррекция на уровне субстрата
При фенилкетонурии диета , ограничивающая
содержание фенилаланина в пище позволяет избежать тяжелых поражений нервной системы
Коррекция
на уровне фермента-поставка в организм недостающих ферментов или введение кофактора (кобаламин, биотин, пиридоксин, аскорбат) или модификация активности фермента (например, введение даназола в течение 30-дней существенно повышает уровень α1-антитрипсина, что предупреждает развитие легочных осложнений
Коррекция на уровне продукта гена
Для многих болезней установлена патогенетическая значимость отсутствия некоторых веществ в развитии болезни (инсулин, гормоны роста, антигемофильный глобулин и др.). Возмещение недостающего продукта приводит к коррекции обмена
Слайд 9Пример
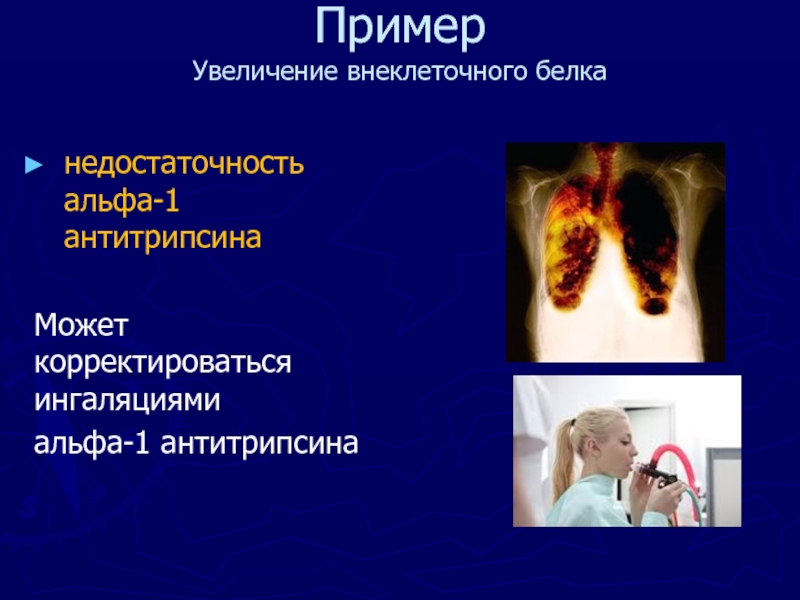
Увеличение внеклеточного белка
недостаточность альфа-1 антитрипсина
Может корректироваться ингаляциями
альфа-1 антитрипсина
Слайд 10ПРИМЕРЫ
терапия малыми молекулами
Куркумин в лечении муковисцидоза
При назначении куркумина мышам -
гомозиготам по мутации delF508, происходило торможение кальциевого насоса в ЭПС,
что приводило к нормализации у них транспорта хлоридов в назальном и кишечном эпителииСлайд 11Терапия малыми молекулами,
приводящая к пропуску
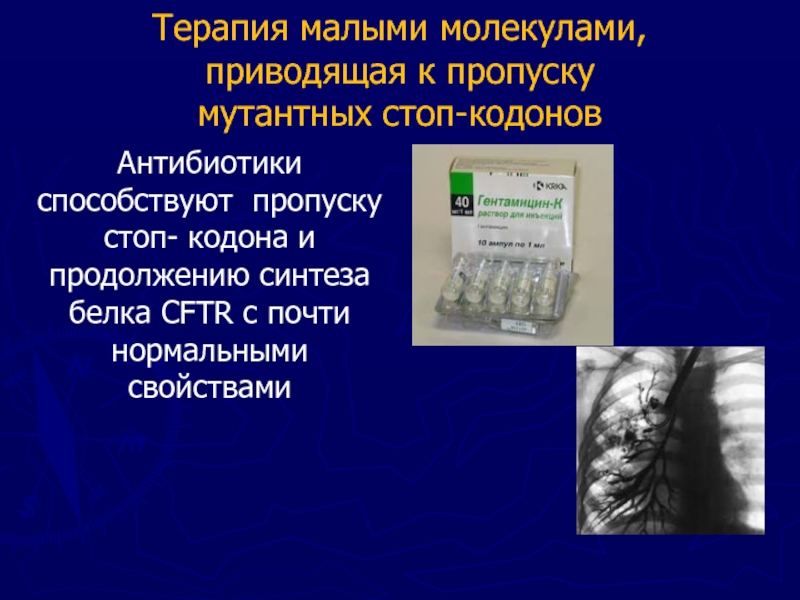
мутантных стоп-кодонов
Антибиотики способствуют пропуску стоп-
кодона и продолжению синтеза белка CFTR с почти нормальными свойствами
Слайд 15Есть и третий подход
- активация собственных генов организма с целью
полного или частичного преодоления действия мутантного гена.
Яркий пример такого
подхода - использование гидроксимочевины (уменьшает метилирование ДНК) для активации синтеза фетального гемоглобина F у больных с серповидноклеточной анемией и талассемиями.Слайд 16Историческая справка
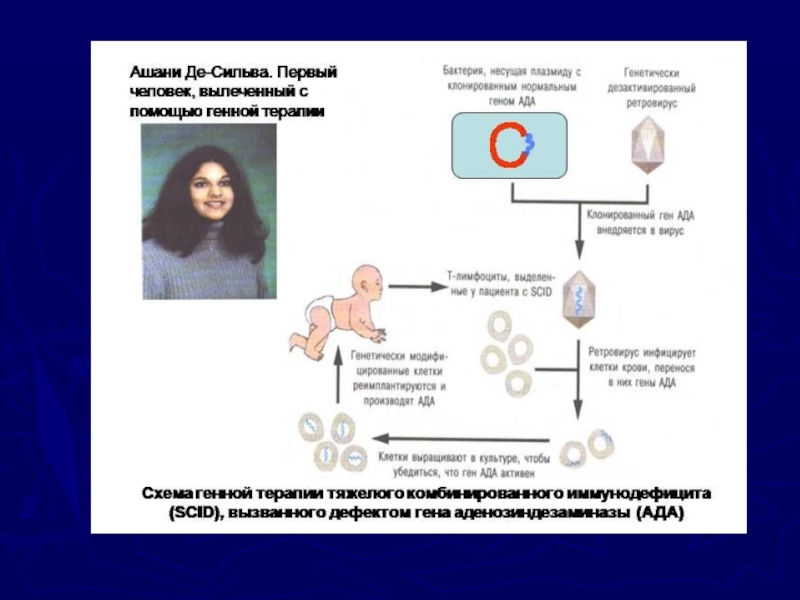
Первым моногенным наследственным заболеванием, к которому применили методы генной
терапии, стал наследственный иммунодефицит, обусловленный мутацией в гене фермента аденозиндезаминазы.
14-го сентября 1990 года в Бетесде (США) четырёхлетней девочке, страдающей этой достаточно редкой патологией (1:100000) пересадили её собственные лимфоциты, которые предварительно трансформировали in vitro геном АДА (ген АДА + ген neo + ретровирусный вектор). Лечебный эффект наблюдался в течение нескольких месяцев, после чего процедуру повторяли с интервалом в 3-5 месяцев. В результате лечения состояние пациентки настолько улучшилось, что она смогла вести нормальный образ жизни и не бояться случайных инфекций.Слайд 18Генная терапия СПИДа
Мутация гена CCR5, встречающаяся примерно у трех процентов
европейцев, делает их невосприимчивым ко всем известным штаммам ВИЧ. Эта
мутация затрагивает структуру кодируемого CCR5 белка-рецептора, с помощью которого вирус связывается с иммунными клетками организма-хозяина.Тимоти Рей Браун, которого также называют «берлинским пациентом», улучшил свое состояние благодаря двум пересадкам клеток костного мозга от донора, имевшего врожденную невосприимчивость к ВИЧ (мутация в гене CCR5). Это случилось в 2007-2008 годах. Полагается, что клетки с генной мутацией заселили иммунную систему Тимоти и позволили ему перестать принимать лекарства. Впрочем, то, что «берлинский пациент» живет без антиретровирусной терапии и не испытывает проблем со здоровьем, не значит, что ВИЧ-инфекция была полностью побеждена. Не исключено, что вирус затаился и лишь значительно снизил активность.
Пациент из города Трентон (США, штат Нью-Джерси) также смог перестать принимать лекарства, однако для этого ему не пришлось проходить через сложную и рискованную операцию (летальность при трансплантации костного мозга — 30%). Вместо этого ученые поработали с его собственными генами: на лейкоциты пациента воздействовали по специальной технологии, благодаря которой они стали производить протеин, разрушающий ген CCR5 (мутация этого гена делает людей невосприимчивыми к ВИЧ). Эксперимент оказался удачным, и инфицированный человек смог обходиться без терапии. Но не все однозначно. Подобная манипуляция с генами еще пятерых людей не привела к ожидаемому результату. Возможно, предполагают эксперты, каждый второй ген CCR5 пациента из Трентона мог иметь унаследованную мутацию, что упростило задачу.
Слайд 19Введение генов
Вирусные векторы
РЕТРОВИРУС:
клетки-мишени: Фибробласты , Эндотелиальные клетки , Миобласты
, Гладкомышечные клетки , Гепатоциты , Гематопоэтические клетки , Стволовые
клеткиПОЛОЖИТЕЛЬНЫЕ СВОЙСТВА:
Непатогенен, Интегрирует в геном, Относительно простое манипулирование, Биология хорошо изучена
ОТРИЦАТЕЛЬНЫЕ СВОЙСТВА:
Относительно низкие вирусные титры, Ограниченная емкость для внедрения трансгена ((10 кб), Не инфицирует неделящиеся клетки, Экспрессия трансгена м.б. непродолжительной
Не очень хорош для in vivo терапии
Слайд 20АДЕНОВИРУС
клетки-мишени: Гепатоциты , Эпителий верхних дыхательных путей , Лимфоидные ,
гематопоэтические и миелоидные клетки
ПОЛОЖИТЕЛЬНЫЕ СВОЙСТВА:
Доступны непатогенные дефектные мутанты, Человек
- природный хозяин, Высокие титры, Высокая эффективность при in vivo инфекции, Инфицирует как делящиеся так и неделящиеся клетки, неинфицируемые ретровирусами, Биология хорошо изучена, Существуют паковочные клеточные линии ОТРИЦАТЕЛЬНЫЕ СВОЙСТВА:
Не интегрирует в геном, Конструкция вектора более сложна, чем у ретровирусов, Может рекомбинировать с природными аденовирусами.
Слайд 21АДЕНО-АССОЦИИРОВАННЫЙ ВИРУС
клетки-мишени: Гематопоэтические клетки , Фибробласты , эпителиальные клетки
ПОЛОЖИТЕЛЬНЫЕ СВОЙСТВА:
Непатогенен, нецитотоксичен, Человек - природный хозяин, Предпочтительный сайт интеграции на
хромосоме 19, Способен устанавливать латентное состояние, Относительно простое конструирование ветора.
ОТРИЦАТЕЛЬНЫЕ СВОЙСТВА:
Относительно низкие титры, Малая емкость (4кб), Инфекционность относительно низка, Требует аденовирус в качестве помощника для инфекции, Биология не очень хорошо изучена.
Слайд 22ГЕРПЕС ВИРУС (HSV)
клетки-мишени: Неделящиеся клетки , дифференцированные нейроны ,
Дифференцированные гепатоциты
ПОЛОЖИТЕЛЬНЫЕ СВОЙСТВА:
Доступны мутанты дефектные по репликации, доступны пакующие
системы, Высокие титры, Широкий спектр клеток-хозяев, Высокая эффективность инфекции, Инфицирует клетки, неинфицируемые ретровирусами, Биология хорошо изучена, Высокая емкость - до 30кб.
ОТРИЦАТЕЛЬНЫЕ СВОЙСТВА:
Упаковка происходит с низкой эффективностью, Репликационно-дефектные мутанты цитотоксичны,
С вирусным геномом трудно создавать векторные конструкции, Сложная регуляция.
Слайд 23Невирусные векторы
катионные липидсвязанные комплексы с ДНК в составе липосом
полимеры
В этом случае ДНК вводят в комплекс с поликатионом
(например, полилизином), лигандом для связывания с клеткой и эндоцитоза (таким лигандом может быть, например, трансферрин или антитело, специфичное к какому-либо поверхностному белку клетки) и специальным агентом, облегчающим высвобождение ДНК из этого комплекса и эндосом в цитоплазме. Такие агенты называют эндосомолитическим . Ими могут служить репликационно-дефектные аденовирусные частицы, влючаемые в комплексискусственные хромосомы
Физические методы (микроинъекция, электропорация, лазерная микроинъекция
Слияние клеток (микроклеток)
Слайд 24Клетки-мишени
Гематопоэтические стволовые клетки
Одной из наиболее реальных мишеней для генной терапии
являются гематопоэтические стволовые клетки , т.е. клетки-предшественники зрелых клеток крови.
Трансплантации костного мозга широко применяются в медицине , а костный мозг и есть одно из мест, где эти стволовые клетки существуют.Лимфоциты
В лимфоциты больной с недостаточностью аденозиндезаминазы был введен ген АДА. Модифицированные лимфоциты были возвращены в кровоток. В результате было восстановлено функционирование иммунной системы ребенка.
Слайд 25Клетки печени
Эксперименты по генной терапии наследственной гиперхолестеролэмии демонстрируют возможность использования
гепатоцитов , в качестве мишеней для ex vivo геной терапии
. Найдена модель, которая позволяет избежать низкой эффективности введения генов в клетки печени и делает генную терапию, нацеленную на печень, существенно более реальной.Слайд 26В настоящее время
Стадия клинических испытаний: иммунодефицит, гемофилия В, болезнь Гоше,
муковисцидоз.
Стадия экспериментальных разработок: гемофилия А, эмфизема лёгких, фенилкетонурия, мышечная дистрофия
Дюшенна, талассемия, серповидноклеточная анемия, болезнь Альцгеймера, болезнь Паркинсона, хронический грануломатоз, респираторный дистресс-синдром.Слайд 27РИСКИ
генотерапии
1. Неблагоприятный ответ на вектор
(например, реакция на аденовирус при дефекте
цикла мочевины)
2. Инсерционный мутагенез, приводящий к злокачественным новообразованиям
3.Инсерционная инактивация важного
для жизнеспособности гена.Слайд 28Не генная, но тоже очень перспективная терапия
Разработаны препараты для лечения
-на основе siRNA
(малая интерферирующая РНК; Silensing-глушение генов), которые способны
разрушать РНК, гомологичные им по последовательности. Таким образом, разрушаются только «нужные» мРНК. С помощью этих синтетических siRNA можно подавлять экспрессию любых генов в том числе, вирусных и «опухолевых». Пример:
Лечение макулодистрофии сетчатки
Макула- центральный участок сетчатки, который обеспечивает человеку ~80% зрения. При возрастной дегенерации (обычно в 70-80 лет, но все чаще теперь и в 40-60 лет) сначала в поле зрения появляются точечные дефекты, потом изображение в центре просто исчезает). В настоящее время разработан препарат SIRNA-27-первое из лекарств серии интерферирующих РНК, допущенных до клинических испытаний.
В живых клетках существуют аналоги siRNA, так называемые микроРНК, которые снижают активность экспрессии некоторых клеточных генов. Снять такую микроРНК-блокаду важных клеточных генов помогут антоганисты РНК (antagomiRNA) – антисмысловые молекулы, инактивирующие клеточные микроРНК).Сняв блокаду можно ген заставить работать быстрее.
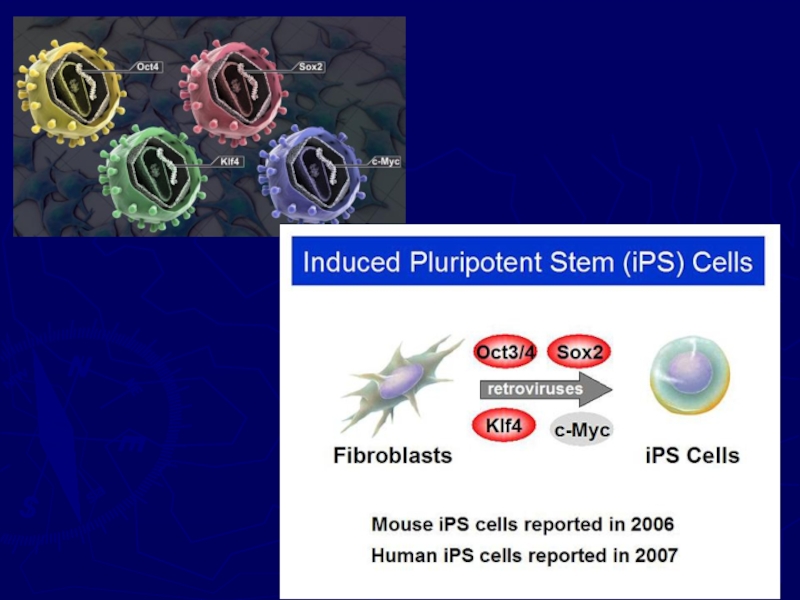
Слайд 29Важное направление -Плюрипотентные клетки
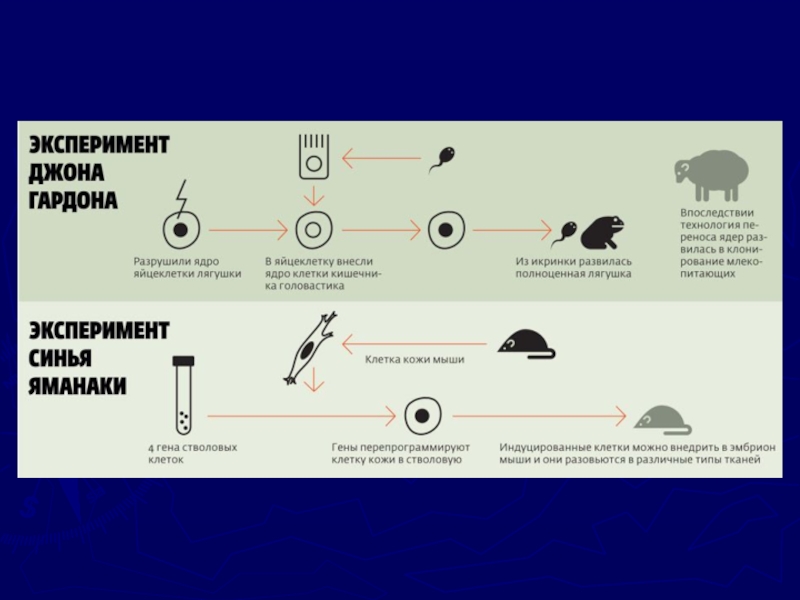
В 2012 г. Нобелевскую премию в области
физиологии и медицины получили John B.Gordon и Shinya Yamanaka
за открытие возможности перепрограммирования зрелых клеток в плюрипотентные (iPSCs).Слайд 33ZFNs-
«дизайнерские» ферменты адресно «собираются» под определенные гены-мишени и фактически представляют
собой инструмент, позволяющий манипулировать клеточным геномом – инактивировать, восстанавливать или
изменять определенные последовательности ДНК.Слайд 34Карл Джун (Carl June) и Пабло Тебас (Pablo Tebas), 2013г
zinc-finger
nucleases - ZFNs
«цинковые пальцы» - синтетические цинкосодержащие белки-нуклеазы
Слайд 35Transcription Activator-Like Effector Nucleases (TALENs)
are artificial fusion proteins composed
of an engineered DNA binding domain fused to a non-specific
nuclease domain from the FokI restriction enzyme.“Method of the Year” for 2011»
Zinc finger and transcription activator-like effector repeat domains with customized specificities can be joined together into arrays capable of binding to extended DNA sequences.
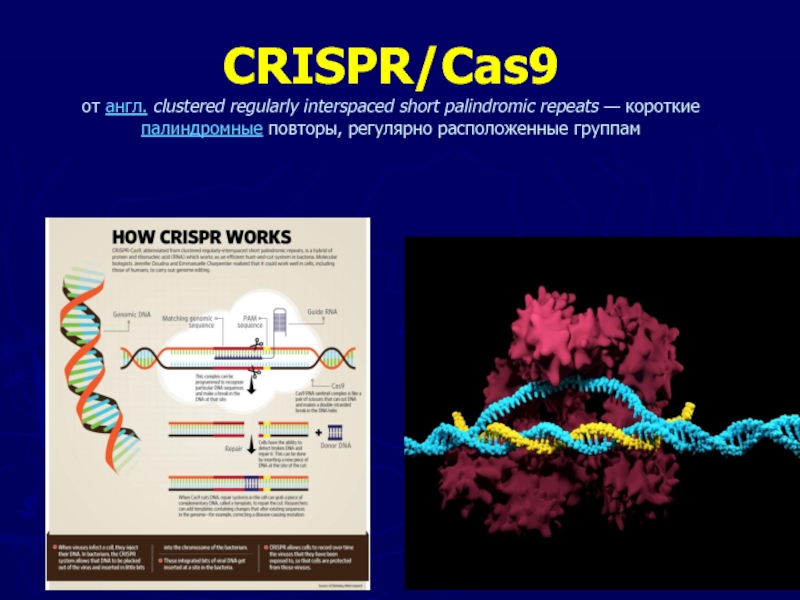
Слайд 36CRISPR/Cas9 от англ. clustered regularly interspaced short palindromic repeats — короткие палиндромные повторы,
регулярно расположенные группам
Слайд 37 Rodolphe Barrangou, John van der Oost.
Barrangou R, et
al. CRISPR provides acquired resistance against viruses in prokaryotes. Science.
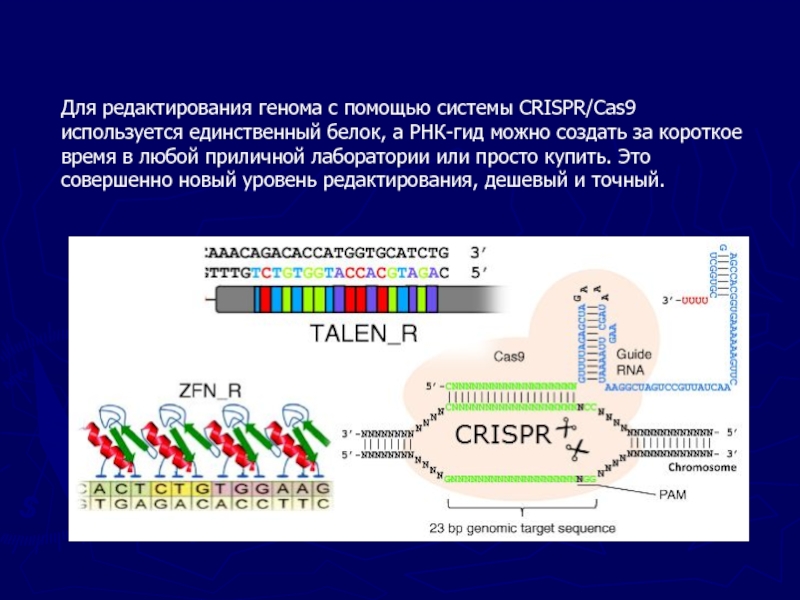
2007;315:1709–1712Слайд 38Для редактирования генома с помощью системы CRISPR/Cas9 используется единственный белок,
а РНК-гид можно создать за короткое время в любой приличной
лаборатории или просто купить. Это совершенно новый уровень редактирования, дешевый и точный.Слайд 39Профилактика
Первичная профилактика– система мер, которые должны предупредить зачатие или рождение
больного ребенка. К таким мерам относятся:
Исключение контакта с генотоксикантами
Планирование семьи
Разновидностью
природной профилактики считают механизм спонтанных абортов, позволяющий элиминировать больной плодИспользование методов пренатальной диагностики