Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция 3
Содержание
- 1. Лекция 3
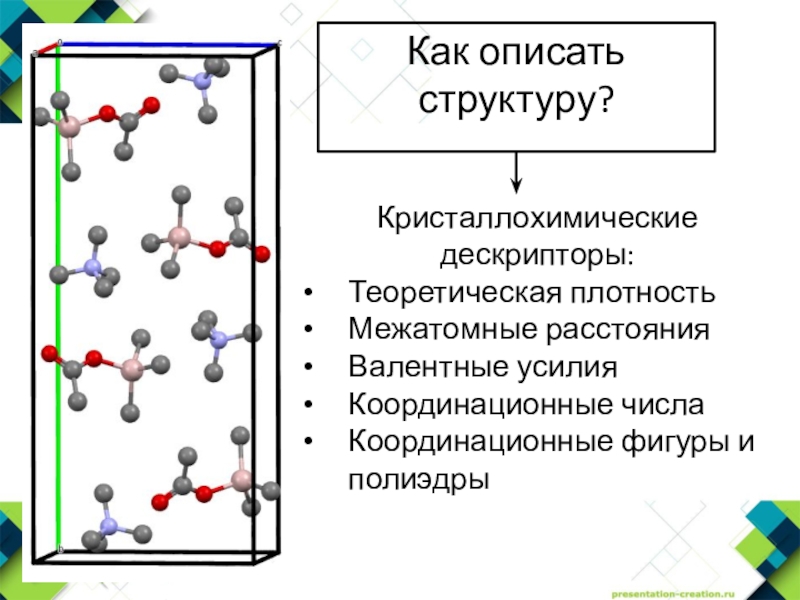
- 2. Кристаллохимические дескрипторы:Теоретическая плотностьМежатомные расстоянияВалентные усилияКоординационные числаКоординационные фигуры и полиэдрыКак описать структуру?
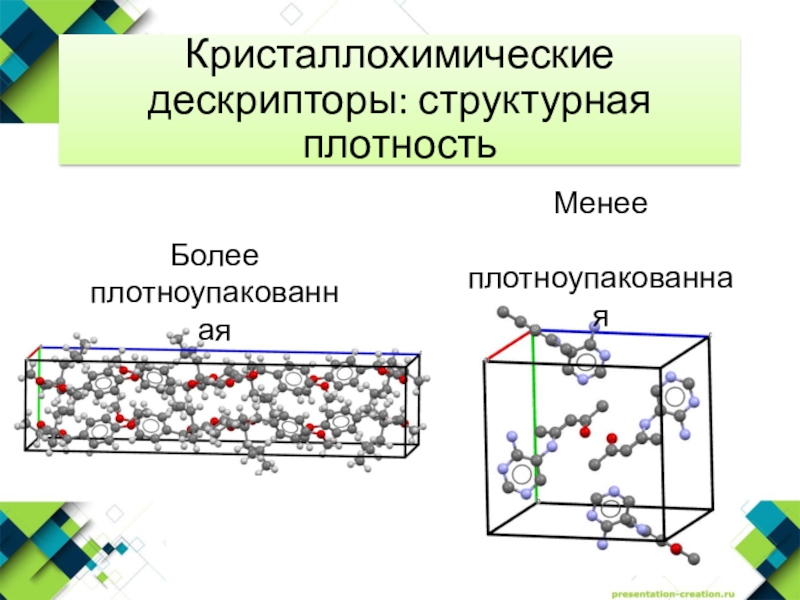
- 3. Кристаллохимические дескрипторы: структурная плотность
- 4. Кристаллохимические дескрипторы: теоретическая плотностьZ – число формульных
- 5. M(H2O)=At(H)·2+At(O)=1·2+16=18M(CCl4)=At(C)+At(Cl)·4=12+35.5·4=154M(CO2)=?M(CO2)=At(C)+At(O)·2=44Молекулярная масса
- 6. Кристаллохимические дескрипторы: межатомные расстояния
- 7. Кристаллохимические дескрипторы: межатомные расстояния
- 8. S – сила связи; R0 – типичная
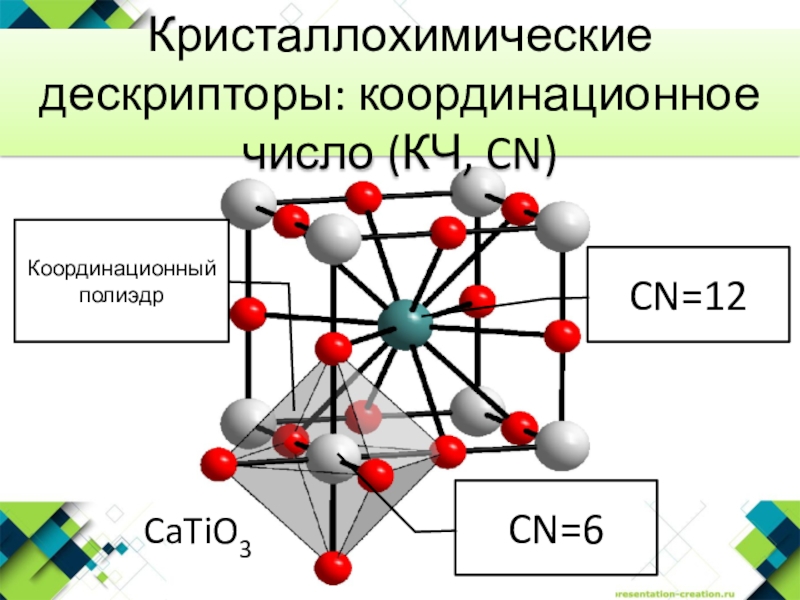
- 9. CaTiO3Кристаллохимические дескрипторы: координационное число (КЧ, CN)
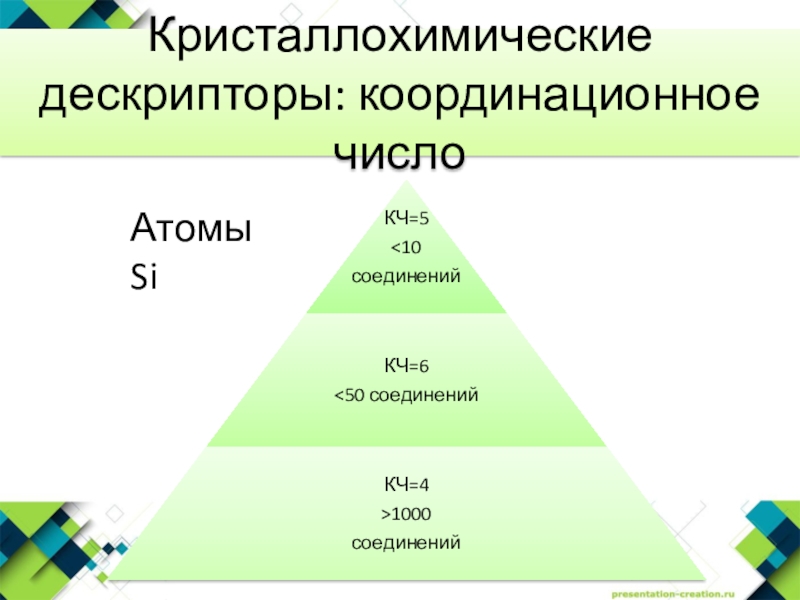
- 10. Кристаллохимические дескрипторы: координационное числоАтомы Si
- 11. CO2Линейная(гантель)УголковаяH2OКристаллохимические дескрипторы: координационный полиэдр и координационная фигураКЧ=2
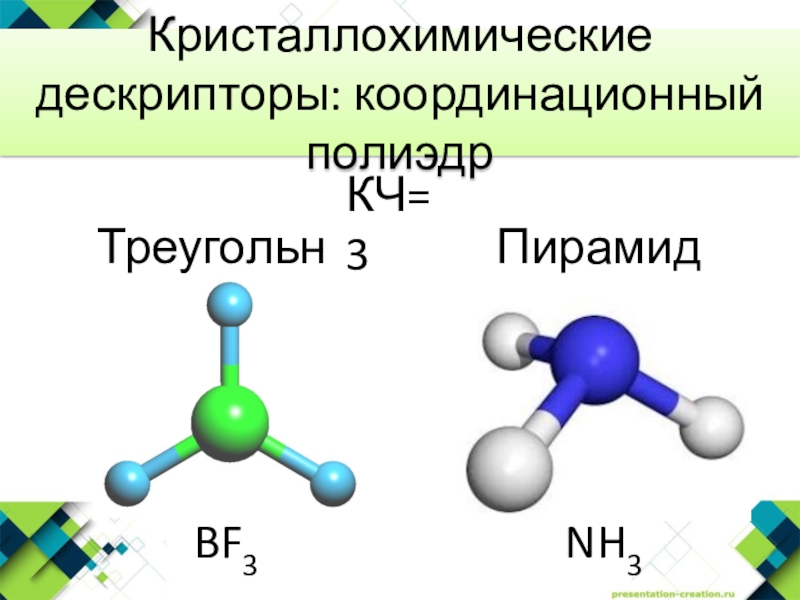
- 12. BF3ТреугольникNH3ПирамидаКристаллохимические дескрипторы: координационный полиэдрКЧ=3
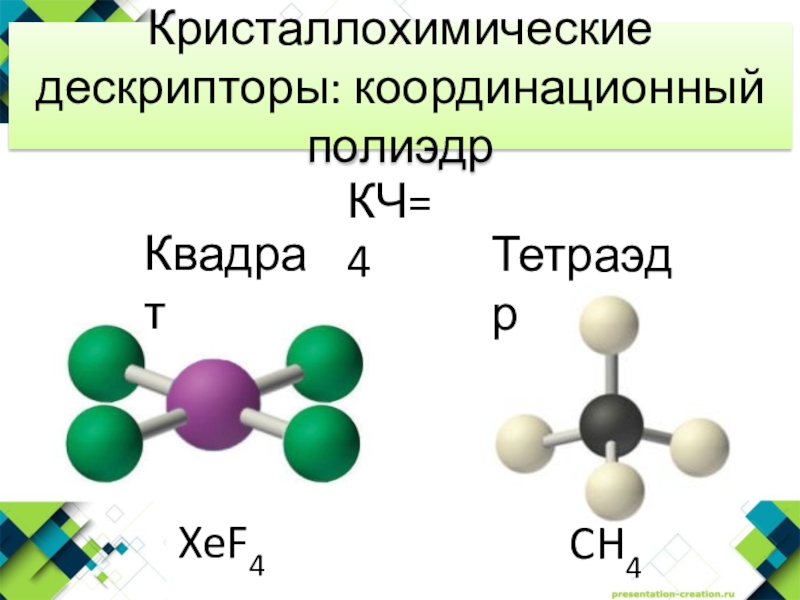
- 13. XeF4КвадратCH4ТетраэдрКристаллохимические дескрипторы: координационный полиэдрКЧ=4
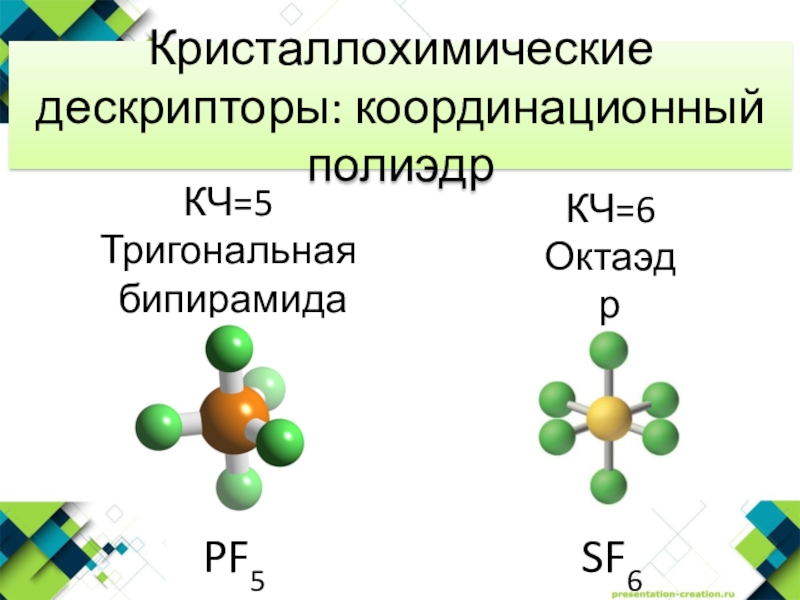
- 14. SF6КЧ=6ОктаэдрPF5КЧ=5Тригональная бипирамидаКристаллохимические дескрипторы: координационный полиэдр
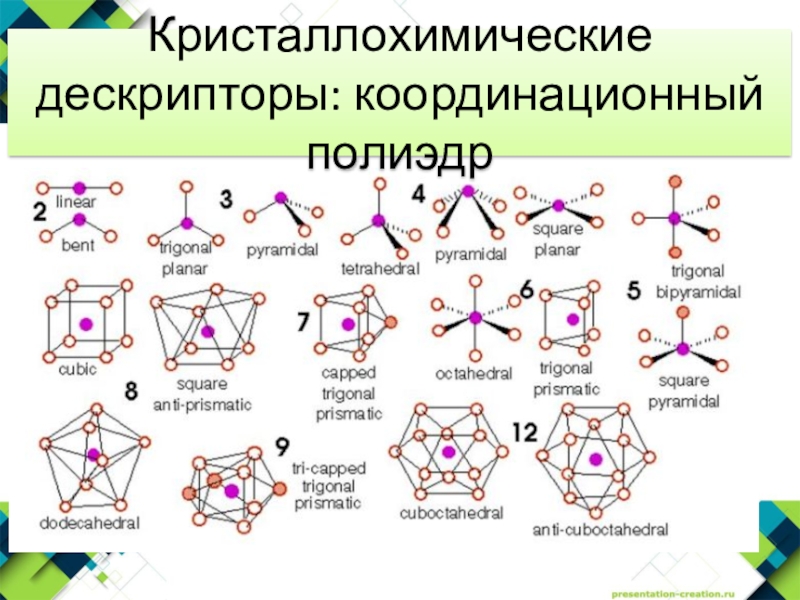
- 15. Кристаллохимические дескрипторы: координационный полиэдр
- 16. Радиусы атомов
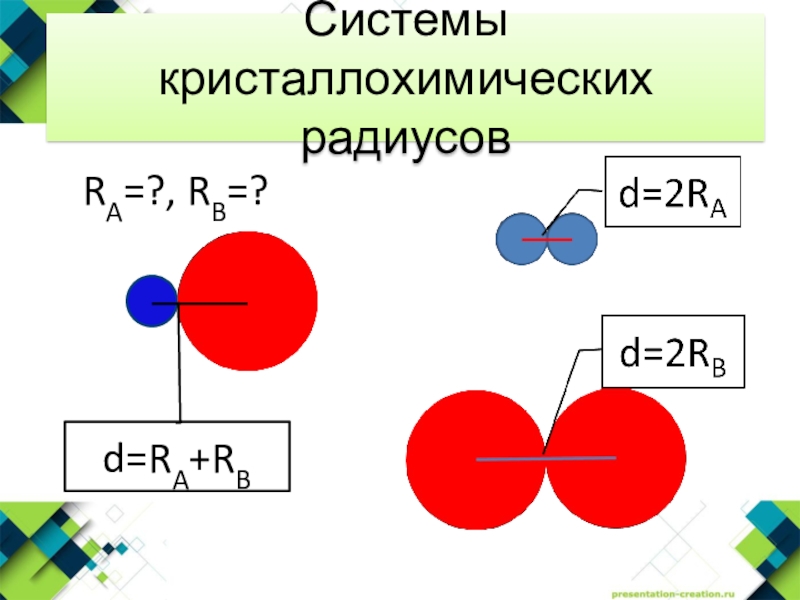
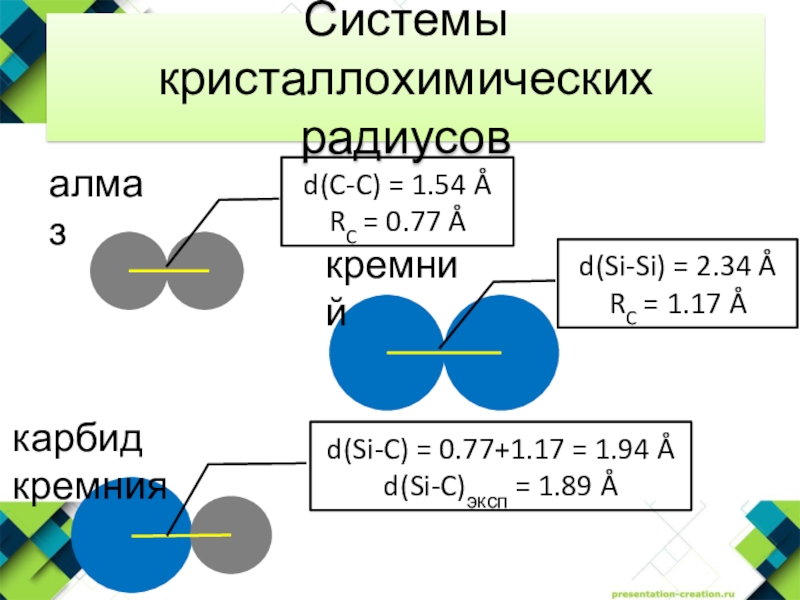
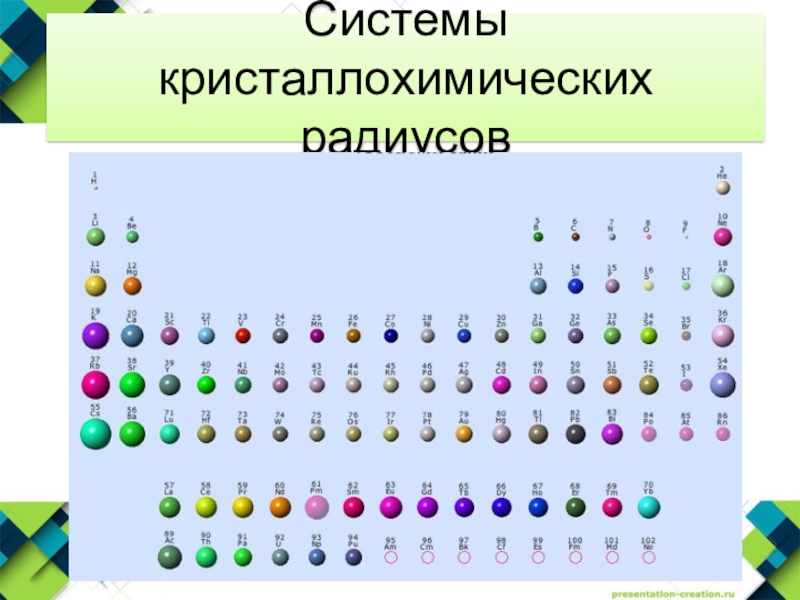
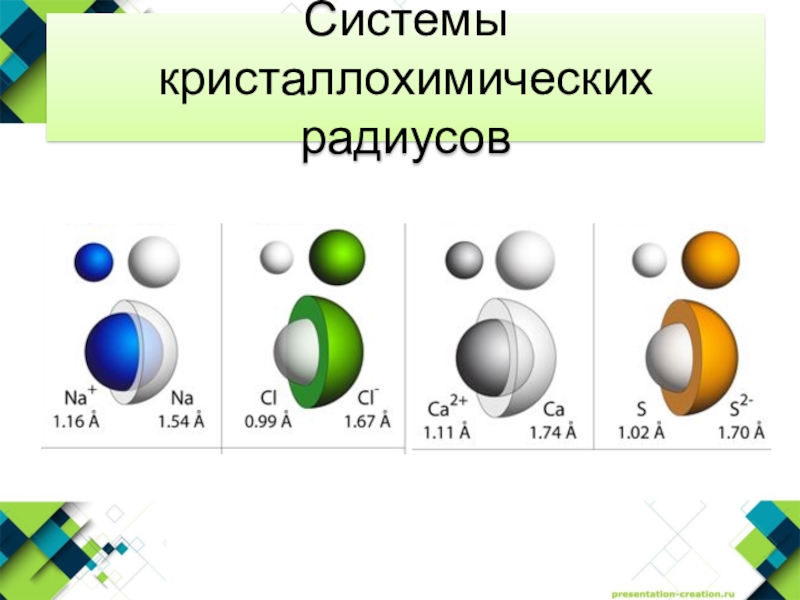
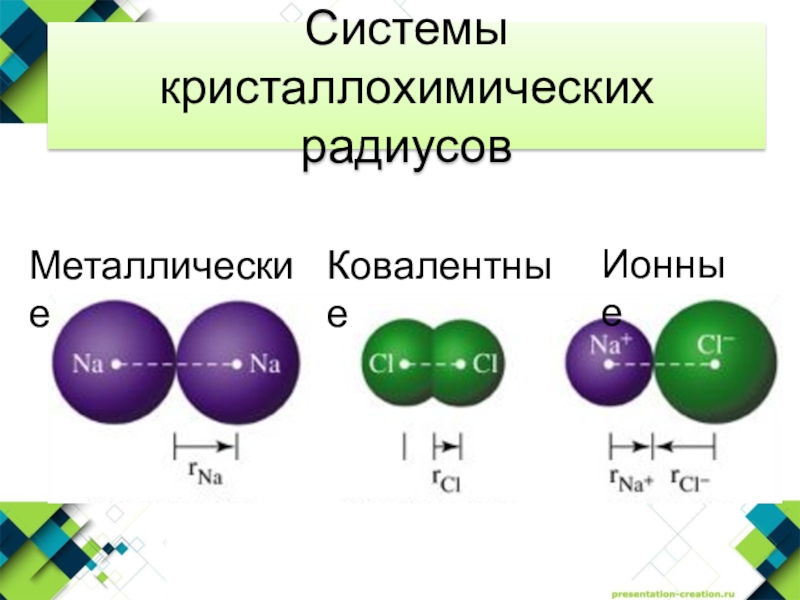
- 17. Системы кристаллохимических радиусов
- 18. Системы кристаллохимических радиусов
- 19. Системы кристаллохимических радиусов
- 20. Системы кристаллохимических радиусов
- 21. Системы кристаллохимических радиусов
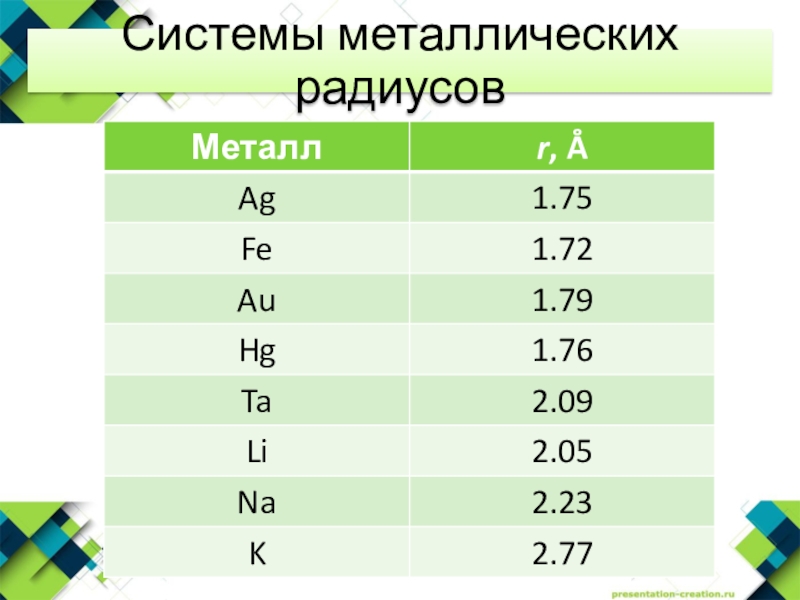
- 22. Системы металлических радиусов
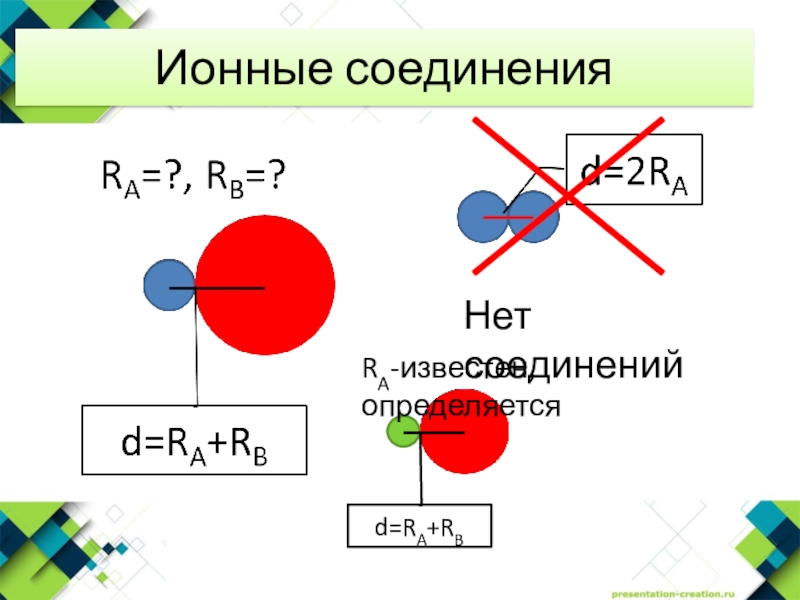
- 23. Ионные соединения
- 24. Слайд 24
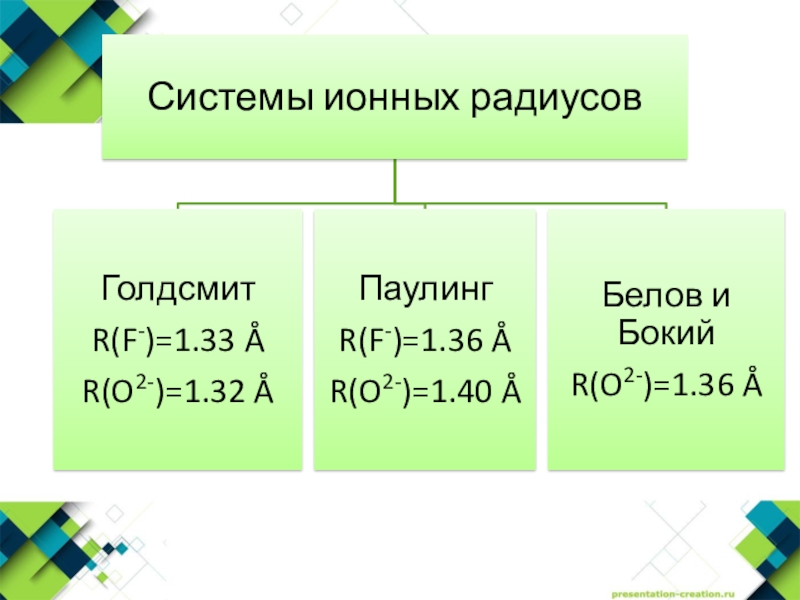
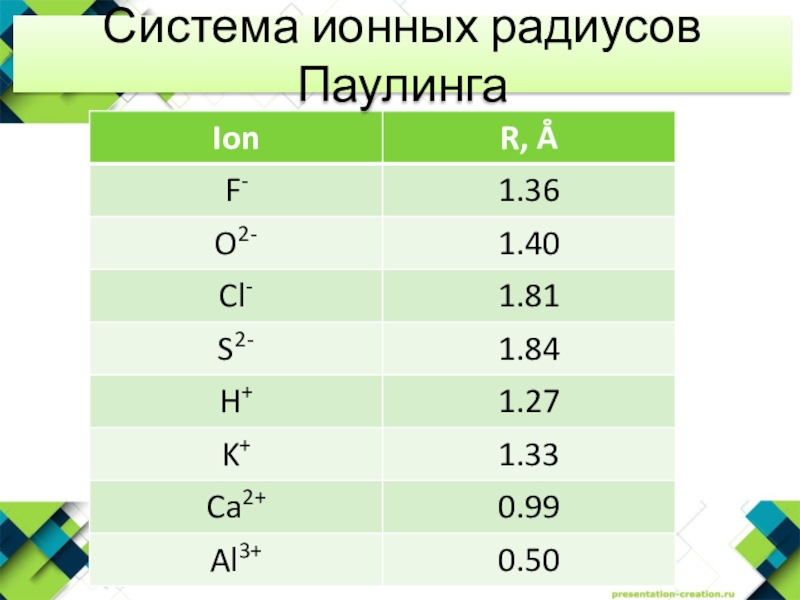
- 25. Система ионных радиусов Паулинга
- 26. Слайд 26
- 27. Спасибо за внимание
- 28. Скачать презентанцию
Кристаллохимические дескрипторы:Теоретическая плотностьМежатомные расстоянияВалентные усилияКоординационные числаКоординационные фигуры и полиэдрыКак описать структуру?
Слайды и текст этой презентации
Слайд 1Лекция 3
Кристаллохимические дескрипторы: структурная плотность, межатомные расстояния, координационные числа и
полиэдры; системы межатомных и атомных радиусов
Слайд 2Кристаллохимические дескрипторы:
Теоретическая плотность
Межатомные расстояния
Валентные усилия
Координационные числа
Координационные фигуры и полиэдры
Как описать
структуру?
Слайд 4Кристаллохимические дескрипторы: теоретическая плотность
Z – число формульных единиц в элементарной
ячейке
Na = 6.02·1023 число Авогадро
M – молекулярная масса
Слайд 5M(H2O)=At(H)·2+At(O)=1·2+16=18
M(CCl4)=At(C)+At(Cl)·4=12+35.5·4=154
M(CO2)=?
M(CO2)=At(C)+At(O)·2=44
Молекулярная масса
Слайд 8S – сила связи; R0 – типичная длина связи
Mn+2-O=1.79 Å
Mn+3-O=1.76 Å Mn+4-O=1.753 Å
Mn+2-F=1.698 Å; Mn+2-Cl=2.133 Å
Altermatt, D.; Brown, I.
D. (1985)Кристаллохимические дескрипторы: валентные усилия