Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция 3 Естественные факторы защиты организма. Механизмы иммунной защиты
Содержание
- 1. Лекция 3 Естественные факторы защиты организма. Механизмы иммунной защиты
- 2. Естественные (неспецифические) факторы защиты организма - это
- 3. Естественные (неспецифические) факторы защиты организма Естественные барьеры:
- 4. Естественные (неспецифические) факторы защиты организма Естественные барьеры:
- 5. Естественные (неспецифические) факторы защиты организма Cистема фагоцитов
- 6. Естественные (неспецифические) факторы защиты организма Cистема фагоцитов
- 7. Естественные (неспецифические) факторы защиты организма 4.Борются с
- 8. Естественные (неспецифические) факторы защиты организма Фагоцитоз —
- 9. Естественные (неспецифические) факторы защиты организма Этапы фагоцитоза:1.
- 10. Естественные (неспецифические) факторы защиты организма Возможные три
- 11. Естественные (неспецифические) факторы защиты организма Возможные три
- 12. Естественные (неспецифические) факторы защиты организма Возможные три
- 13. факторы защиты организма Гуморальные неспецифические факторы защиты
- 14. факторы защиты организма Функции:1. Облегчение адгезии микробной
- 15. факторы защиты организма Результатом данного процесса
- 16. факторы защиты организма Факторы системы комплемента :1.
- 17. факторы защиты организма Пути активизации системы комплементаКлассическийАльтернативный
- 18. Классический путь активизации системы комплементаПусковой механизм -
- 19. Слайд 19
- 20. Классический путь активизации системы комплементаУчастие комплемента в
- 21. факторы защиты организма
- 22. факторы защиты организма
- 23. АЛЬТЕРНАТИВНЫЙ путь активизации системы комплементаАктивизация системы комплемента
- 24. факторы защиты организМА Биологические эффекты системы комплемента:
- 25. факторы защиты организМА Бактерицидные гуморальные факторы, ограничивающие
- 26. факторы защиты организма Интерфероны — белки, продуцирующиеся
- 27. факторы защиты организма 3 вида: 1. Лейкоцитарный
- 28. Механизм биологического действия интерферона
- 29. факторы защиты организма Синтез интерферонов начинается с
- 30. факторы защиты организма Противовирусное действием интерферонов проявляется
- 31. факторы защиты организма Интерфероны обладают:1. Антибактериальными свойствами
- 32. факторы защиты организма Нормальные киллеры (NK) —
- 33. факторы защиты организма Рис. 1. Контакты мононуклеарных
- 34. Механизмы иммунной (специфической) защиты Специфический иммунный ответ,
- 35. Механизмы иммунной (специфической) защиты Взаимодействие клеток в
- 36. Схема кооперативного взаимодействия макрофагов, Т- и В-лимфоцитов и выдачи иммунного ответа
- 37. Схема кооперативного взаимодействия макрофагов,
- 38. Механизмы иммунной (специфической) защиты Образуются иммунные комплексы,
- 39. Механизмы противовирусного иммунитетаГуморальный механизм противовирусного иммунитета опосредован
- 40. Механизмы антибактериального иммунитетаКомплемент разрушает клеточную стенку бактерий,
- 41. Механизмы антибактериального иммунитетаЗащитную роль в системе антибактериального
- 42. Механизмы антибактериального иммунитетаКлеточный иммунитет является основой против
- 43. Скачать презентанцию
Естественные (неспецифические) факторы защиты организма - это факторы, действие которых не зависит от специфичности проникающего в организм антигенаДанный механизм защиты является генетически детерминированным и способствует элиминации чужеродного агента. Факторы естественной защиты
Слайды и текст этой презентации
Слайд 1Лекция 3 Естественные факторы защиты организма. Механизмы иммунной защиты. Механизмы противовирусного
и антибактериального иммунитета
Слайд 2Естественные (неспецифические) факторы защиты организма
- это факторы, действие которых
не зависит от специфичности проникающего в организм антигена
Данный механизм защиты
является генетически детерминированным и способствует элиминации чужеродного агента. Факторы естественной защиты являются чаще всего первым барьером при поступлении в организм инфекционного агента.
Слайд 3Естественные (неспецифические) факторы защиты организма
Естественные барьеры: кожа и слизистые
Защита:
1.
Способность кожи к десквамации клеток обеспечивает механическое удаление инфекционного агента;
2.Воздействие
молочной кислоты и жирных кислот, содержащихся в поте и секрете сальных желез является губительным для микроорганизма. 3. Секрет бронхов, желудка, кишечника действует как защитный барьер, препятствуя механическому прикреплению бактерий к эпителиальным клеткам и удаляя их за счет движения ресничек.
Слайд 4Естественные (неспецифические) факторы защиты организма
Естественные барьеры: кожа и слизистые
Защита:
4.
Слеза, слюна, моча оказывают вымывающее действие на патогенные микроорганизмы.
5.
Во многих биологических жидкостях организма содержатся вещества, обладающие бактерицидными свойствами (например, соляная кислота желудочного сока; спермин и цинк в сперме; лизоцим в слезах; лактопероксидаза в молоке). 6. Бактериальная микрофлора кишечника угнетается рост потенциально патогенных бактерий и грибов вследствие конкуренции за питательные вещества или выработки кислот.
Слайд 5Естественные (неспецифические) факторы защиты организма
Cистема фагоцитов (микро- и макрофагов)
1.
Микрофаги (полиморфно-ядерные нейтрофилы)
Родоначальник - стволовая клетка костного мозга. Это
короткоживущая неделящаяся клетка, основной функциональной особенностью которой является защита от гноеродных бактерий. Слайд 6Естественные (неспецифические) факторы защиты организма
Cистема фагоцитов (микро- и макрофагов)
2.
Макрофаги (моноциты)
Родоначальник - клетка костного мозга (стволовая клетка
монобласт промоноцит моноцит костного мозга моноцит периферической крови тканевой макрофаг).Функции:
1. Формируют систему мононуклеарных фагоцитов
в тканях.
2. Присутствуют в соединительной ткани, в базальных мембранах мелких кровеносных сосудов, в легких (альвеолярные макрофаги), печени (клетки Купфера), среди клеток почечных клубочков, клеток мозга и костной ткани.
3. Отфильтровывают чужеродный материал в селезенке и лимфатических узлах
Слайд 7Естественные (неспецифические) факторы защиты организма
4.Борются с бактериями, вирусами и
простейшими, которые способны выживать внутри клетки хозяина.
5. Секретируют биологически
активные соединения (простагландинов, некоторых компонентов системы комплемента — С2, С3, С4, С5, фактор некроза опухолей и т.п.) 6. Перерабатывают антиген и представляют его с участием белков 2-го класса главного комплекса гистосовместимости иммунокомпетентным клеткам, принимающим участие в формировании иммунного ответа.
7. Синтезируют интерлейкины, которые являются клеточными медиаторами и участвуют в регуляции разных форм иммунного ответа.
Слайд 8Естественные (неспецифические) факторы защиты организма
Фагоцитоз — процесс адгезии микроба
на поверхности макрофага, его поглощения и переваривания внутри макрофага.
В случае,
когда размеры микроорганизма превосходят размеры макрофага, в силу вступают механизмы внешнего фагоцитоза — уничтожение бактерий путем выделения во внешнюю среду биологически активных веществ. Илья Ильич Мечников
Слайд 9Естественные (неспецифические) факторы защиты организма
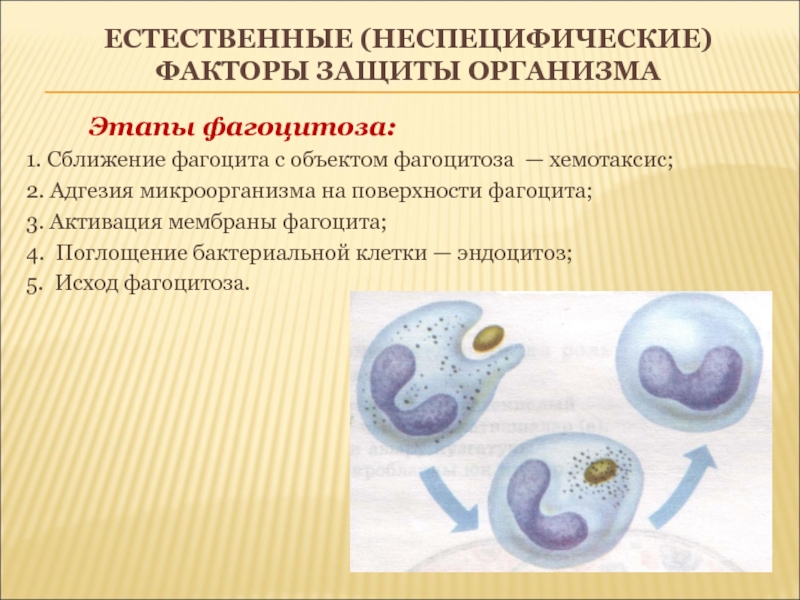
Этапы фагоцитоза:
1. Сближение фагоцита с
объектом фагоцитоза — хемотаксис;
2. Адгезия микроорганизма на поверхности фагоцита;
3.
Активация мембраны фагоцита;4. Поглощение бактериальной клетки — эндоцитоз;
5. Исход фагоцитоза.
Слайд 10Естественные (неспецифические) факторы защиты организма
Возможные три исхода фагоцитоза:
1. Полное
внутриклеточное переваривание микробных клеток — завершенный фагоцитоз.
В процессе фагоцитоза
происходит «окислительный» взрыв, который приводит к образованию активных форм кислорода, обусловливающих бактерицидный эффект. Кроме того, важную роль играют катионные белки, разрушающие бактериальную мембрану. Убитые клетки далее подвергаются действию ферментов лизосом.Слайд 11Естественные (неспецифические) факторы защиты организма
Возможные три исхода фагоцитоза:
2. Приживление
и активное размножение бактерий внутри макрофага — незавершенный фагоцитоз.
Многие
вирулентные бактерии часто не погибают и могут длительно персистировать внутри макрофага. Выживание фагоцитированных микроорганизмов обеспечивается различными механизмами: препятствием слияния лизосом с фагосомами, устойчивостью к лизосомным ферментам и бактерицидным факторам и т.п. и выталкивание микробов из фагоцитов обратно во внешнюю среду.
Слайд 12Естественные (неспецифические) факторы защиты организма
Возможные три исхода фагоцитоза:
3. Внешний
фагоцитоз — процесс уничтожения бактерий, находящихся вне клеток, в ближайшем
окружении.Данный процесс осуществляется благодаря синтезу фагоцитами веществ, обладающих эффекторной активностью: антибактериальной, антивирусной и цитотоксической. Это кислородные радикалы, компоненты комплемента, лизоцим, лизосомные ферменты, интерферон.
Этими же продуктами может быть опосредовано и цитотоксическое действие фагоцитов в реализации иммунного ответа при развитии опухолей, трансплантации органов и тканей, развитии аллергических реакций.
Слайд 13факторы защиты организма
Гуморальные неспецифические факторы защиты
- система комплемента
— сложный комплекс быстро и каскадно действующих сывороточных белков, последовательно
активизирующихсяСлайд 14факторы защиты организма
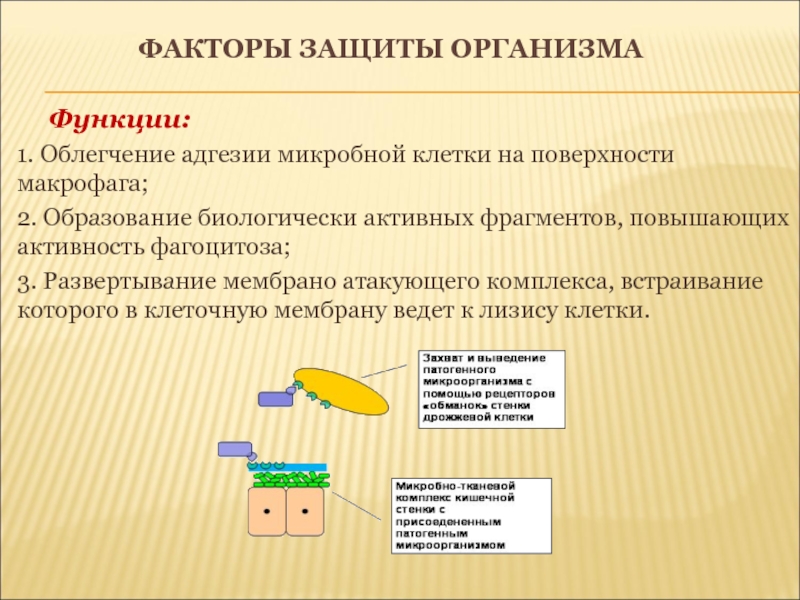
Функции:
1. Облегчение адгезии микробной клетки на поверхности
макрофага;
2. Образование биологически активных фрагментов, повышающих активность фагоцитоза;
3.
Развертывание мембрано атакующего комплекса, встраивание которого в клеточную мембрану ведет к лизису клетки.Слайд 15факторы защиты организма
Результатом данного процесса является
бактериолизис или
цитолиз
Образование компонентов системы комплемента (С) происходит преимущественно в печени, костном
мозге и селезенке, возможно, эпителии тонкого кишечника. Из общего числа сывороточных белков на систему комплемента приходится 10%.
Слайд 16факторы защиты организма
Факторы системы комплемента :
1. Девять белков, составляющих
собственно комплемент: С1, С2…С9
С1-компонент состоит из 3 белковых субъединиц (С1q,
С1r, С1s), остальные - представляют собой единичные белковые молекулы. В составе молекулы С1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела.
Антитела, относящиеся к иммуноглобулинам различных классов, взаимодействуют с комплементом с различной степенью активности. Белки С5, С6, С7, С8, С9 участвуют в организации мембрано атакующего комплекса.
2. Регуляторные белки: С1Е1, С44bp, фактор Н, фактор 1, белок S.
3. Факторы, участвующие в альтернативном пути активации системы комплемента: фактор В (протеиназа), фактор D (гликопротеин), фактор Р (пропердин).
Слайд 18Классический путь активизации системы комплемента
Пусковой механизм - образование комплекса
антиген
— антитело.
Антитела принадлежат классам IgG или IgM и связывают
С1q фракцию системы комплемента, обеспечивая образование фермента С1-эстеразы.В присутствии ионов Са2+ возникает комплекс антиген + антитело + С1 и запускается механизм последовательной активации системы комплемента:
- вначале данный комплекс взаимодействует с С4 фактором;
- затем к комплексу присоединяется компонент С2;
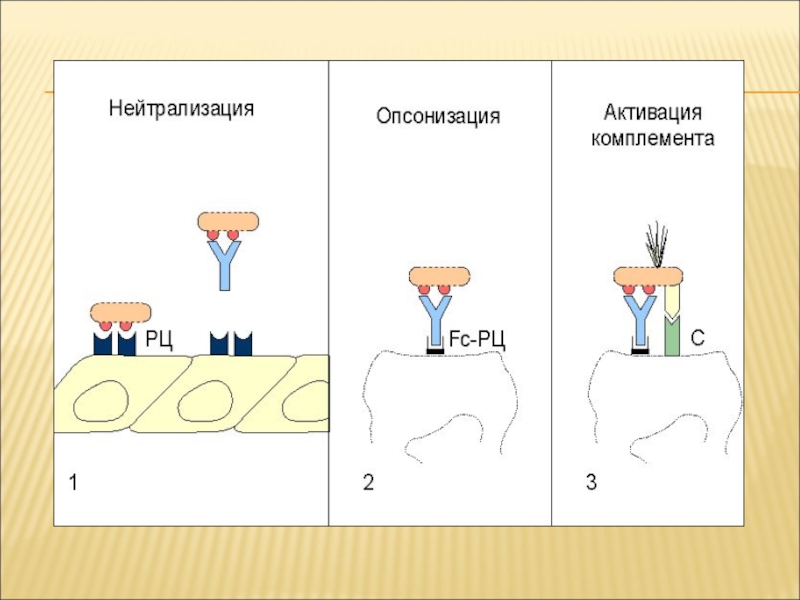
- при дальнейшем присоединении С3 фактора комплекс приобретает способность прилипать к различным клеткам, в том числе к эритроцитам и фагоцитам.
Чужеродное вещество под влиянием этого комплекса опсонизируется, т.е. подвергается более активному фагоцитозу и цитотоксическому действию.
Слайд 20Классический путь активизации системы комплемента
Участие комплемента в защите от микроорганизмов
вовлекает три различных механизма:
1. Лизис бактерий;
2. Активизацию всего аппарата
макрофагов;3. Воспаление.
Начало синтеза компонентов С5—С9 является сигналом для образования мембраноатакующего комплекса, ведущего к лизису бактерий. Этот комплекс погружается в двойной липидный слой мембраны и формирует канал, по которому в клетку проникает вода; клетка набухает и лопается. В инициации воспаления и активации фагоцитоза участвует белок С3 и его два биологически активных фрагмента — С3а и С3b. Фиксация С3b на бактериальной клетке обусловливает эффект иммунного прилипания, в результате которого к клетке начинают присоединяться фагоциты и, выделяя гидролитические ферменты, убивают клетку. Компонент С3а участвует в данном процессе, вызывая хемотаксис фагоцитов.
Слайд 23АЛЬТЕРНАТИВНЫЙ путь активизации системы комплемента
Активизация системы комплемента альтернативным путем осуществляется
липополисахаридами клеточной стенки грамотрицательных бактерий и любыми другими микробными антигенами
(вирусными, бактериальными, антигенами грибов, простейших).Этот механизм активизируется тогда, когда нет еще антител к данному возбудителю.
В инициации и контроле активации по альтернативному пути участвуют не менее 6 белков:
фактор В, фактор D, пропердин, а также регуляторные белки (фактор Н, фактор 1 и компонент С3).
В данном случае сывороточные белки активизируют систему, минуя образование первых трех факторов (С1, С4, С2), сразу через С3-фактор системы комплемента.
Слайд 24факторы защиты организМА
Биологические эффекты системы комплемента:
1. Лизис чужеродных
клеток, включая бактерии;
2. Опсонизация чужеродных клеток, которые становятся более доступными
для макрофагов; 3. Стимуляция хемотаксиса;
4. Стимуляция фагоцитоза (С1q и С1b);
5. Повышение сосудистой проницаемости (С5а, С3а);
6. Стимуляция анафилотоксинами (С5а, С3а) внутриклеточных процессов, в результате которых выбрасываются биологически активные соединения (гистамин, брадикинин, серотонин, лейкотриеныи т.п.), которые обусловливают развитие воспаления.
Слайд 25факторы защиты организМА
Бактерицидные гуморальные факторы, ограничивающие распространение инфекции:
1. Фермент
лизоцим, расщепляющий клеточную стенку и способствующий лизису бактерий. Лизоцим присутствует
в слюне, слезной жидкости, ликворе, сыворотке крови. Синтезируется микро- и макрофагами.2. Фибронектин — белок плазмы и тканевой жидкости, связывающий микроорганизмы и другие частицы с мембраной фагоцитов. Синтезируется макрофагами.
Слайд 26факторы защиты организма
Интерфероны — белки, продуцирующиеся лимфоцитами.
Интерфероны, синтезируемые
в клетках организма человека, различаются:
1. По своим физико-химическим свойствам;
2. Рецепторам,
с помощью которых они взаимодействуют с клетками; 3. Кислоточувствительности;
4. Антигенной специфичности.
По своей природе интерфероны являются гликопротеидами
Слайд 27факторы защиты организма
3 вида:
1. Лейкоцитарный (б-интерферон) обладает противовирусной
и противоопухолевой активностью в системе неспецифической защиты организма.
2. Фибробластный (в-интерферон)
только противоопухолевый.3. Иммунный гамма-интерферон (г-интерферон) имеет специфическое иммуномодулирующее действие на организм человека; стимулирует образование молекул 2-го класса системы HLA; участвует в процессе запуска активации и дифференцировки В-лимфоцитов.
Биологическая активность различных интерферонов выражена в разной степени:
б- и в- интерфероны обладают более высокой противовирусной активностью, чем г-интерферон, однако последний имеет во много раз большую иммуномодулирующую активность.
Слайд 29факторы защиты организма
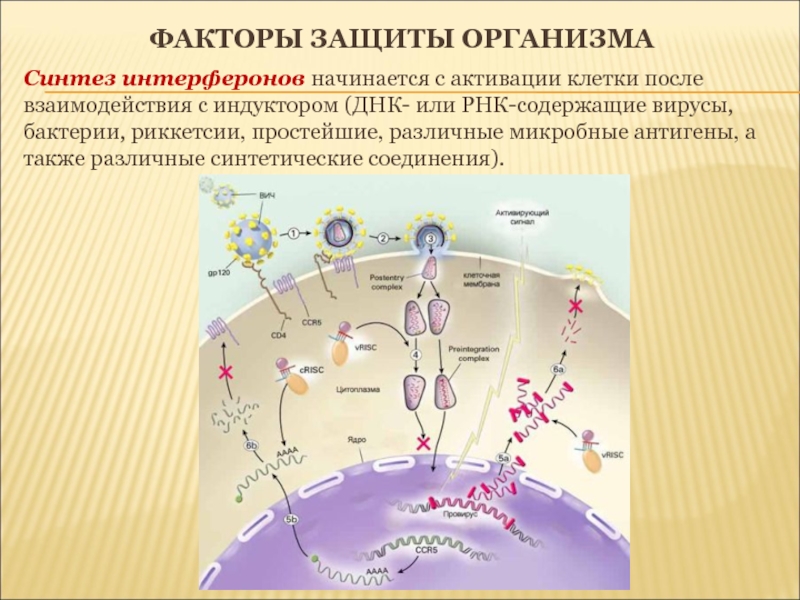
Синтез интерферонов начинается с активации клетки после
взаимодействия с индуктором (ДНК- или РНК-содержащие вирусы, бактерии, риккетсии, простейшие,
различные микробные антигены, а также различные синтетические соединения).Слайд 30факторы защиты организма
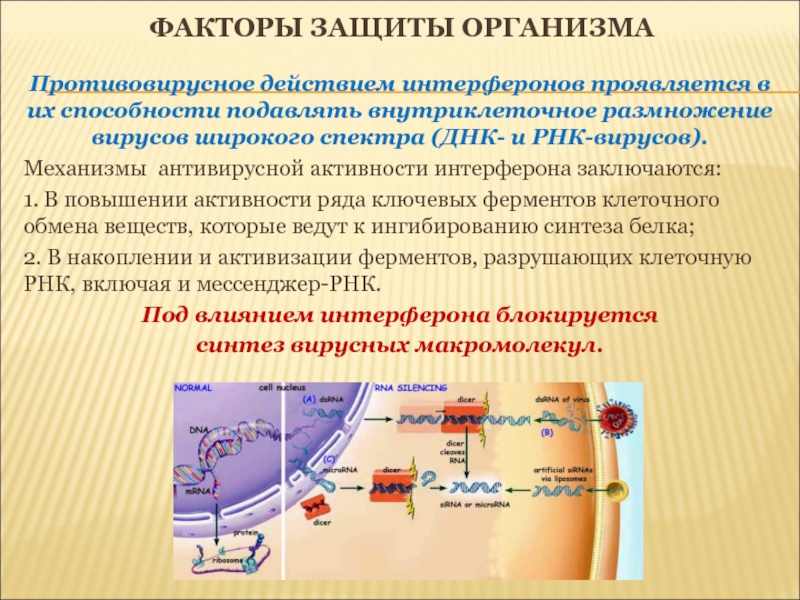
Противовирусное действием интерферонов проявляется в их способности
подавлять внутриклеточное размножение вирусов широкого спектра (ДНК- и РНК-вирусов).
Механизмы
антивирусной активности интерферона заключаются:1. В повышении активности ряда ключевых ферментов клеточного обмена веществ, которые ведут к ингибированию синтеза белка;
2. В накоплении и активизации ферментов, разрушающих клеточную РНК, включая и мессенджер-РНК.
Под влиянием интерферона блокируется
синтез вирусных макромолекул.
Слайд 31факторы защиты организма
Интерфероны обладают:
1. Антибактериальными свойствами (высокую чувствительность к
интерферону проявляют грамположительные и несколько меньшую — грамотрицательные бактерии);
2. Противоопухолевым
действием;3. Иммуномодулирующим свойством (они воздействуют на системы видового иммунитета и системы специфической иммунной защиты).
Интерфероны:
- стимулируют активность естественных киллеров и цитотоксических Т-лимфоцитов;
- повышают чувствительность к ним клеток-мишеней, стимулируют фагоцитоз, антителообразование, фиксацию комплемента.
Молекулы интерферонов синтезируются первыми в ответ на получение клетками неспецифического сигнала чужеродности.
Им принадлежит важная роль в поддержании гомеостаза не только в клетках и тканях, но и на уровне целостного организма.
Слайд 32факторы защиты организма
Нормальные киллеры (NK) — большие зернистые лимфоциты
— осуществляют защиту организма от вирусной инфекции.
Основная функция —
уничтожение клеток-мишеней, зараженных вирусами. Интерфероны усиливают цитотоксическое действие нормальных киллеров. Крупные паразиты типа гельминтов не могут быть фагоцитированы физически. Чтобы справиться с ними, на помощь приходят эозинофилы, осуществляющие внеклеточное уничтожение.
После связывания эозинофила при помощи системы комплемента к поверхности гельминта происходит высвобождение их главного основного белка, который повреждает мембрану паразита.
Слайд 33факторы защиты организма
Рис. 1. Контакты мононуклеарных клеток из крови
человека с клетками-мишенями: КЭ — клетка эффектор; КМ — клетка-мишень.
Ув.: а — 24 000; б— 16 000.Рис. 2. Изменение ультраструктуры клетки-мишени в результате взаимодействия с клеткой-эффектором: а — после 30-минутной инкубации при 37 °С; б — после 1,5-часовой инкубации при 37 °С.
Слайд 34Механизмы иммунной (специфической) защиты
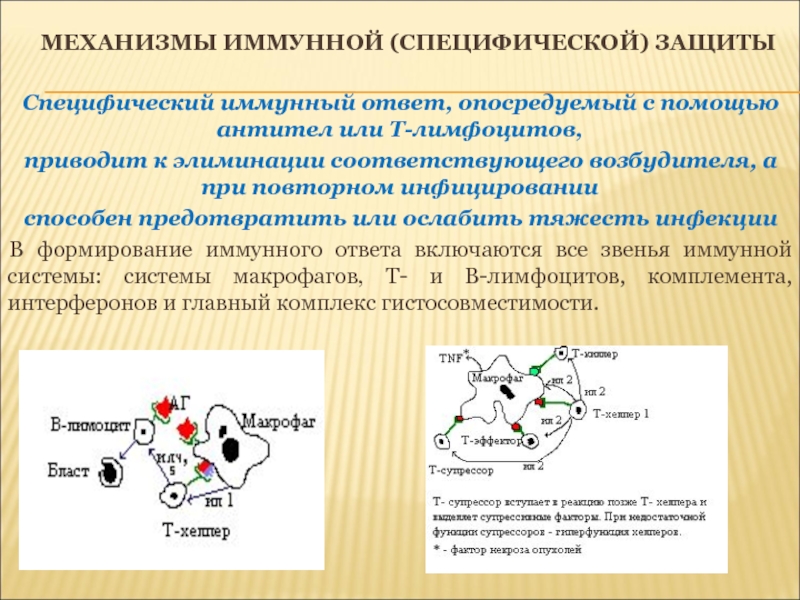
Специфический иммунный ответ, опосредуемый с помощью антител
или Т-лимфоцитов,
приводит к элиминации соответствующего возбудителя, а при повторном
инфицировании способен предотвратить или ослабить тяжесть инфекции
В формирование иммунного ответа включаются все звенья иммунной системы: системы макрофагов, Т- и В-лимфоцитов, комплемента, интерферонов и главный комплекс гистосовместимости.
Слайд 35Механизмы иммунной (специфической) защиты
Взаимодействие клеток в иммунном ответе
Процессинг антигена -
это переработка антигенпредставляющими клетками, в результате которой обнажаются и связываются
с белками главного комплекса гистосовместимости 1 или 2-го класса пептидные фрагменты антигена, необходимые для представления другим иммунокомпетентным клеткам.Функции процессинга и представления антигена в комплексе с белками 2-го класса комплекса гистосовместимости выполняют активированные макрофаги, В-лимфоциты, дендритные клетки селезенки, а также эпителиальные, эндотелиальные клетки, астроциты, клетки Лангерганса кожи и купферовские клетки печени (антигенпредставляющие).
Основная роль в процессинге и представлении антигена принадлежит макрофагам. В структуре молекулы 2-го класса главного комплекса гистосовместимости имеется специальный центр, способный связывать чужеродные антигены.
Образование комплекса белок 2-го класса МНС + антиген происходит внутри клетки, где подвергается процессингу, а представление процессированного антигена белками 2-го класса происходит на мембране макрофага.
Слайд 36 Схема кооперативного взаимодействия макрофагов, Т- и В-лимфоцитов и выдачи иммунного
ответа
Слайд 37 Схема кооперативного взаимодействия макрофагов, Т- и В-лимфоцитов и выдачи иммунного
ответа
1. Антиген поглощается макрофагом.
2. Макрофаг осуществляет процессинг антигена.
3. Макрофаг с
помощью белков 2-го класса МНС представляет процессированный антиген Т-хелперам.4. Т-хелпер узнает процессированный антиген с помощью собственного белка 2-го класса МНС и активизируется (синтезирует факторы роста, дифференцировки для других субпопуляций Т-клеток и В-лимфоцитов).
5. Антиген распознается В-лимфоцитом, который также несет процессированный антиген и активируется (на его мембране синтезируются рецепторы для различных интерлейкинов: факторов роста, активации, дифференцировки и других).
6. Активированный В-лимфоцит размножается и дифференцируется в антителообразующие клетки и клетки памяти. Клон антителообразующих клеток синтезирует антитела в большом количестве.
7. Антитела связываются с антигеном и таким образом маркируют его для узнавания другими компонентами иммунной системы.
Слайд 38Механизмы иммунной (специфической) защиты
Образуются иммунные комплексы, благодаря которым антигены выводятся
из организма.
Разрушение бактерий осуществляется благодаря системе комплемента. Формируется очаг
воспаления, происходит активирование других макрофагов. Феномен иммунной адгезии (иммунного прилипания) повышает активность макрофагов, которые синтезируя отдельные компоненты системы комплемента, усиливают его активность.
В работу включаются главный комплекс гистосовместимости и его третий локус, отвечающий за синтез некоторых компонентов системы комплемента.
При участии белков 1-го класса МНС Т-киллерам представляются чужеродные бактериальные, вирусные и другие антигены. Т-киллеры распознают эти комплексы, атакуют и разрушают инфицированные чужеродными агентами клетки.
Слайд 39Механизмы противовирусного иммунитета
Гуморальный механизм противовирусного иммунитета опосредован антителами (Ig M,
Ig G, Ig A, Ig D, Ig E).
Антитела (Ig
A, Ig E) осуществляют местную защиту — по месту входных ворот инфекции (слизистые оболочки дыхательных путей и желудочно-кишечного тракта).Клеточный иммунный ответ при вирусных инфекциях направлен против вирусов, проникших в клетку.
Т-лимфоциты человека обладают непосредственной цитотоксичностью в отношении клеток, зараженных вирусными частицами. Специфические Т-киллеры появляются в организме человека уже через 1—3 дня после заражения вирусом.
Если вирус не удается обезвредить подобным образом, и он все же выходит из клетки, к процессу подключаются Т-хелперы.
Важную роль в противовирусном приобретенном иммунитете играют Т-эффекторы, которые распознают вирусный антиген и выделяют медиаторы клеточного иммунитета.
Макрофаги фагоцитируют инфицированные вирусами живые и распадающиеся клетки.
Стойкость вирусного иммунитета вариабельна.
Слайд 40Механизмы антибактериального иммунитета
Комплемент разрушает клеточную стенку бактерий, образуя в ней
отверстия.
Сывороточный лизоцим получает доступ к внутреннему слою бактериальной стенки,
что приводит к ее гибели. Активация системы комплемента обеспечивает также приток нейтрофилов (полиморфно-ядерных лейкоцитов), осуществляющих фагоцитоз - клеточноопосредованный антителозависимый бактериолиз.
Взаимодействия не всегда заканчиваются гибелью бактериальной клетки (например, микобактерии туберкулеза способны размножаться внутриклеточно). Это зависит от массивности инфекции и устойчивости возбудителя.
Гуморальные механизмы. Специфический иммунитет против инфекций, вызванных инкапсулированными бактериями (пневмококки, стрептококки гр.А; менингококки и т.д.), зависит от уровня антител против клеточной капсулы.
Слайд 41Механизмы антибактериального иммунитета
Защитную роль в системе антибактериального иммунитета играет секреторная
иммунная система.
Ig A предотвращает адгезию бактерий на слизистой.
Если
инфекционный агент преодолевает этот барьер, он встречается со следующей защитной линией, представленной IgE. Большая часть IgE синтезируется плазматическими клетками слизистых оболочек и дренирующих их лимфоузлов.
Контакт бактериальной клетки с IgE приводит к высвобождению медиаторов, которые привлекают эффекторные клетки и клетки иммунного ответа (IgG, факторы системы комплемента, нейтрофилы, эозинофилы).
Слайд 42Механизмы антибактериального иммунитета
Клеточный иммунитет является основой против инфекций, возбудители которых
имеют внутриклеточный путь размножения (туберкулез, сальмонеллез, туляремия, токсоплазмоз).
Для этих
инфекций характерно развитие аллергических состояний. В механизме антибактериального иммунитета большую роль играют цитотоксические Т-лимфоциты, уничтожающие клетки, содержащие бактерии, и выделение специфических медиаторов лимфокинов, которые активизируют действие макрофагов.
Реакции клеточного иммунитета сохраняются в организме после перенесенной инфекции в течение многих лет.