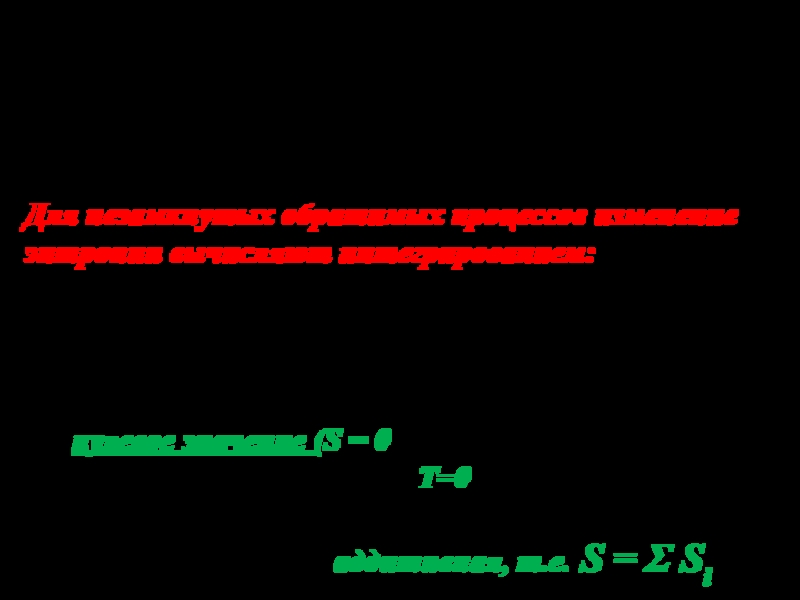Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция № 10. Тепловая машина Карно. Второе начало термодинамики
Содержание
- 1. Лекция № 10. Тепловая машина Карно. Второе начало термодинамики
- 2. Идеальная тепловая машина. Цикл КарноНаибольшим КПД при
- 3. Тепловую машину, работающую по циклу
- 4. PV = constPVγ = const
- 5. На участке АВ происходит изотермическое расширение при
- 6. Для этого в точке В газ отклю-
- 7. В точке D изотермическое сжатие заканчивается. Теперь
- 8. Работа и КПД цикла КарноВ результате цикла
- 9. Исходя из этого за КПД машины Карно
- 10. Это сформулировано в 1-ой теореме Карно: Тепловая
- 11. Холодильная машинаЭта машина работает по
- 12. Эффективность холодильной машины характеризуется ее холодильным коэффициентом,
- 13. Второе начало термодинамики Тепловой двигатель и
- 14. Появление второго начала термодинамики связано с необходимостью
- 15. Формулировка У.Томсона: «Невозможны такие процессы, единственным результатом
- 16. Для количественной характеристики степени хао- тичности
- 17. Отношение теплоты Q к температуре, при которой
- 18. Убедимся, к примеру, что это справедливо для
- 19. Можно показать, что и для любого другого обратимого кругового процессаПолученное выражение называется: равенство Клаузиуса
- 20. Напомним, если в круговом процессе
- 21. Из равенства Клаузиуса
- 22. Так кактоПосле интегрированияРассчитаем изменение энтропии в изопроцессах
- 23. Каждый из изопроцессов идеального газа характери-зуется своим
- 24. Изохорический (
- 25. Энтропия в изолированной системе при необратимых процессах.
- 26. Это означает, что для квазистатических цикличес-ких процессов
- 27. Пусть система переходит из состояния 1 в
- 28. Распишем цикл поэтапно:Для обратимого процессаТогдаЕсли система изолирована:
- 29. Основные итоги рассмотренного. При любом необратимом
- 30. Первое и второе начала термодинамики в объединенной форме имеют вид: Здесь использовано
- 31. Третье начало термодинамики.
- 32. На их основании можно считать, что при
- 33. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Лекция № 10.
Тепловая машина Карно.
Второе начало термодинамики
1. Идеальная тепловая машина.
Цикл Карно.
термодинамики. (Теорема Нернста).Слайд 2Идеальная тепловая машина. Цикл Карно
Наибольшим КПД при заданных температурах нагревателя
T1 и холодильника T2 обладает тепловой двигатель, где рабочее тело
расширяется и сжимается по циклу Карно, который состоит из двух изотерм и двух адиабат.Карно Никола Леонард Сади (1796 – 1832) – французский физик и инженер, один из создателей термодинамики
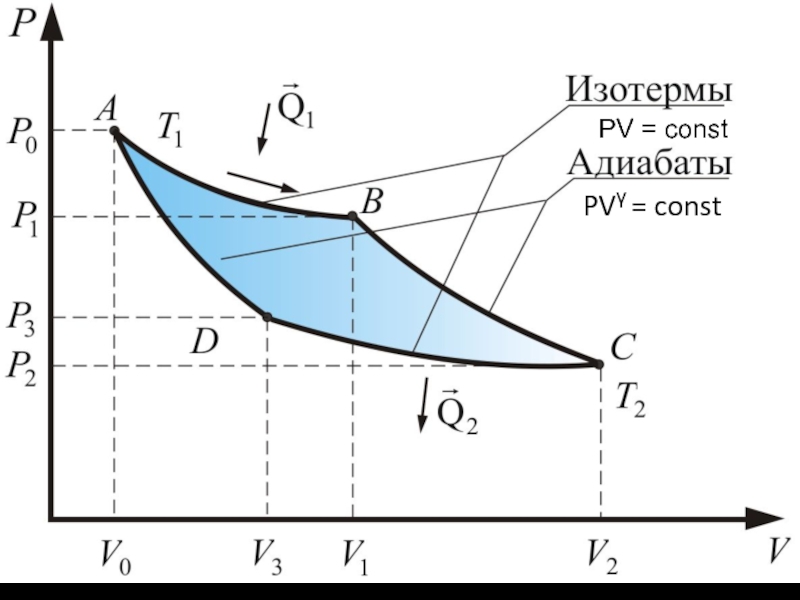
Слайд 3 Тепловую машину, работающую по циклу Карно, называют идеальной,
потому что в этом цикле отсутствуют необратимые процессы, связанные с
теплопроводностью.Рассмотрим цикл Карно.
Пусть в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Будем считать, что нагреватель и холодильник имеют бесконечную теплоемкость. Это означает, что их температуры остаются неизменными в процессе обмена теплом с рабочим телом.
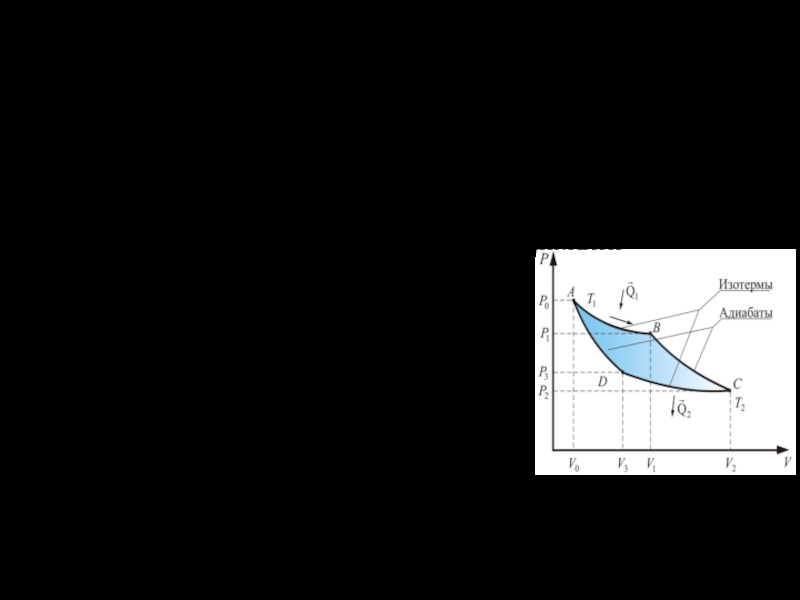
На диаграмме PV цикл Карно выглядит следующим образом.
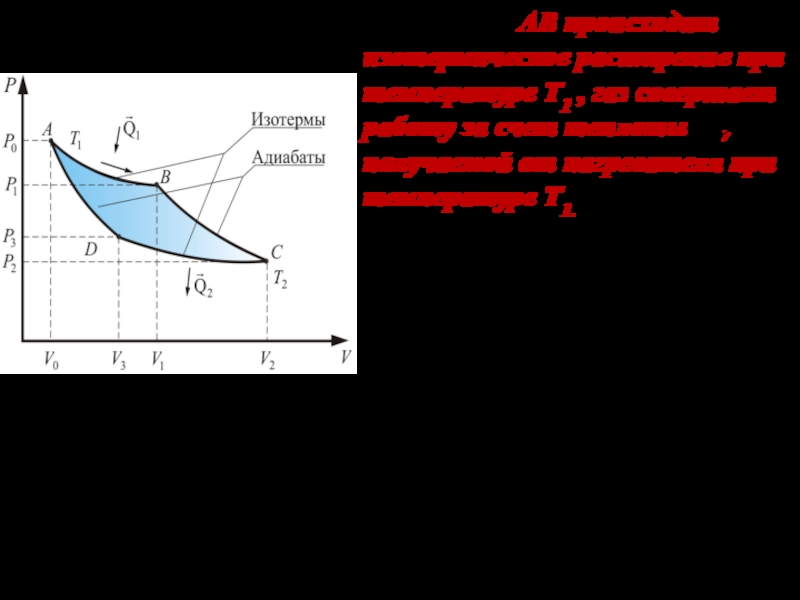
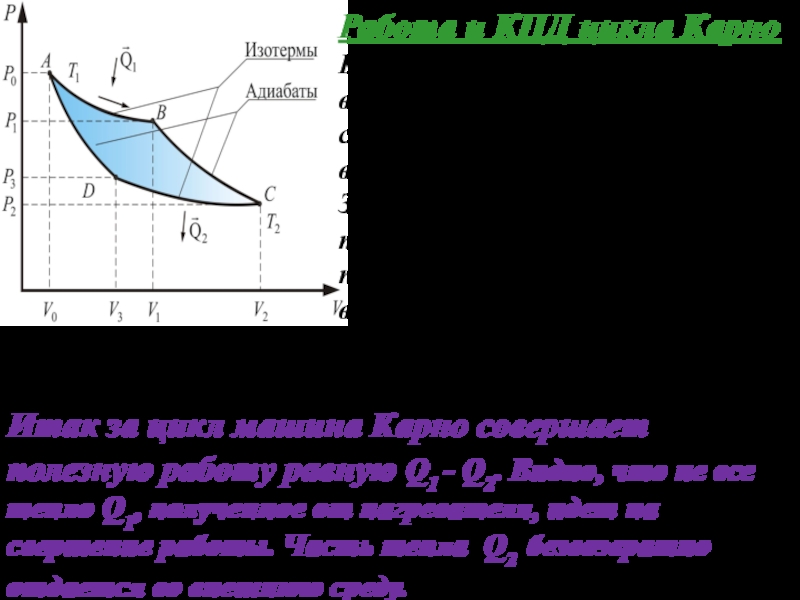
Слайд 5На участке АВ происходит изотермическое расширение при температуре Т1 ,
газ совершает работу за счет теплоты , получаемой от нагревателя при
температуре Т1. Здесь не происходит необратимой передачи тепла от более нагретого тела к менее нагретому, передаваемое тепло сразу переходит в работу. Данный процесс обратим.Как отмечалось выше, в тепловой машине в ходе расши- рения газа температура должна быть более высокой, чем при его обратном сжатии, поэтому перед сжатием газа его температуру предварительно понижают от Т1 до Т2..
Слайд 6Для этого в точке В газ отклю- чают от контакта
с нагрева- телем и совершают процесс адиабатического расширения ВС, в
ходе которого газ продолжает совершать работу, но теперь уже за счет своей внутренней энергии, убыль которой и снижает его температуру до Т2
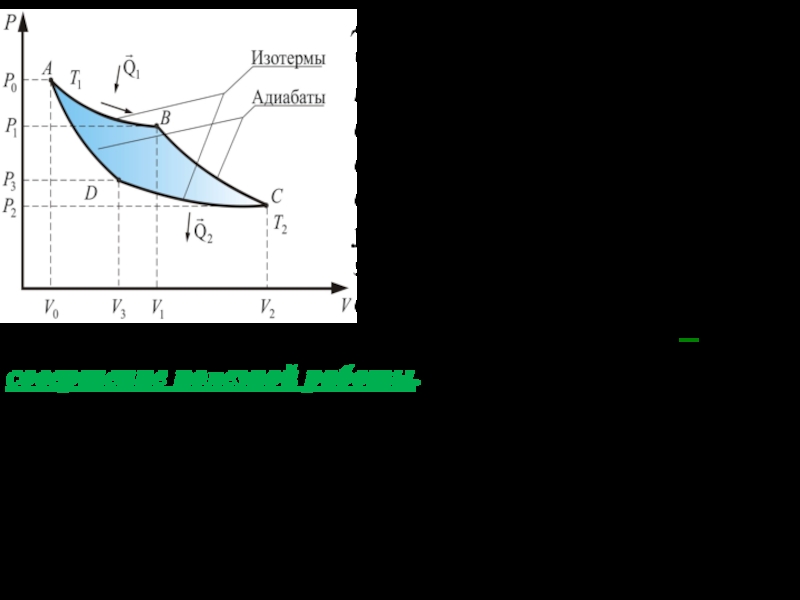
На этом заканчивается первая половина цикла – совершение полезной работы.
В точке С начинают изотермическое сжатие газа, предва- рительно приведя его в контакт с холодильником, имею-щем температуру Т2 (процесс CD). Работа внешних сил по сжатию газа переходит в его внутреннюю энергию, которая при постоянной температуре сразу отдается холодильнику в виде теплоты Q2
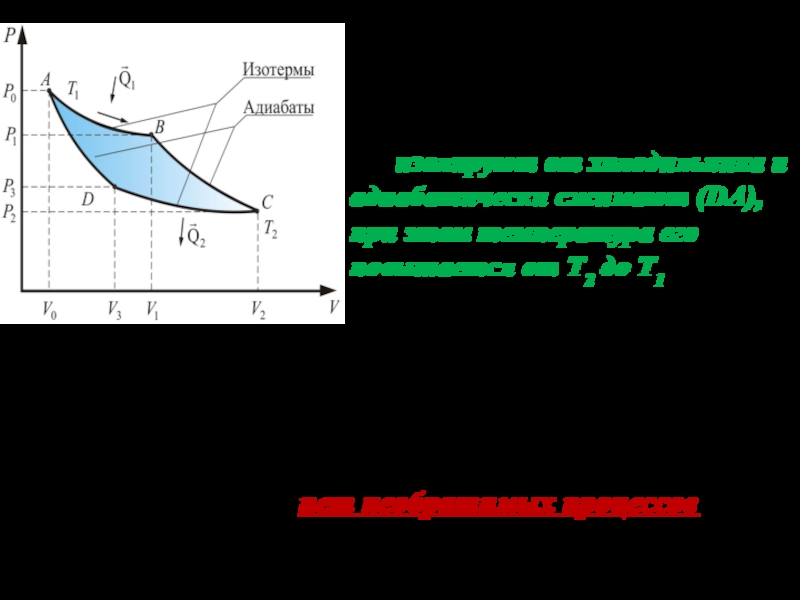
Слайд 7В точке D изотермическое сжатие заканчивается. Теперь нужно вернуть газ
в исходное состояние (точку А). Для этого его изолируют от
холодильника и адиабатически сжимают (DА), при этом температура его повышается от Т2 до Т1 за счет того, что работа, внешних сил, совершенная над газом, перехо- дит в его внутреннюю энергию и увеличивает ее.На всех стадиях этого кругового процесса нигде не допускается соприкосновение тел с разной температурой, т.е. нет необратимых процессов теплопроводности. Весь цикл проводится обратимо ( в идеале, бесконечно медленно).
Слайд 8Работа и КПД цикла Карно
В результате цикла газ возвращается в
исходное состояние, т.е. изменения его внутренней энергии нет (ΔU=0). За
цикл газ получил количество теплоты равное Q1 - Q2 . Тогда из первого начала термодинамики вся эта теплота пошла на совершение газом полезной работы А.
Итак за цикл машина Карно совершает полезную работу равную Q1 - Q2. Видно, что не все тепло Q1, полученное от нагревателя, идет на свершение работы. Часть тепла Q2 безвозвратно отдается во внешнюю среду.
Слайд 9Исходя из этого за КПД машины Карно η примем отношение
полезной работы А к теплоте Q1 , полученной от нагревателя
Цикл
Карно, рассмотренный нами, был на всех стадиях проведен так, что не было необратимых процессов, (не было соприкосновения тел с разными температурами). Поэтому здесь самый большой КПД. Больше получить в принципе невозможно.
Слайд 10Это сформулировано в 1-ой теореме Карно:
Тепловая машина, работающая при
данных
значениях температур нагревателя и холодиль-
ника, не может иметь КПД больший,
чем машина, работающая по обратимому циклу Карно при тех же значениях Т1 и Т2 .2-ая теорема Карно:
КПД тепловой машины, работающей по циклу Карно, не зависит от рода рабочего тела, а определяется только температурой нагревателя Т1 и температурой холодильника Т2 .
Из теоремы Карно следует, что , поэтому
КПД машины Карно
Слайд 11
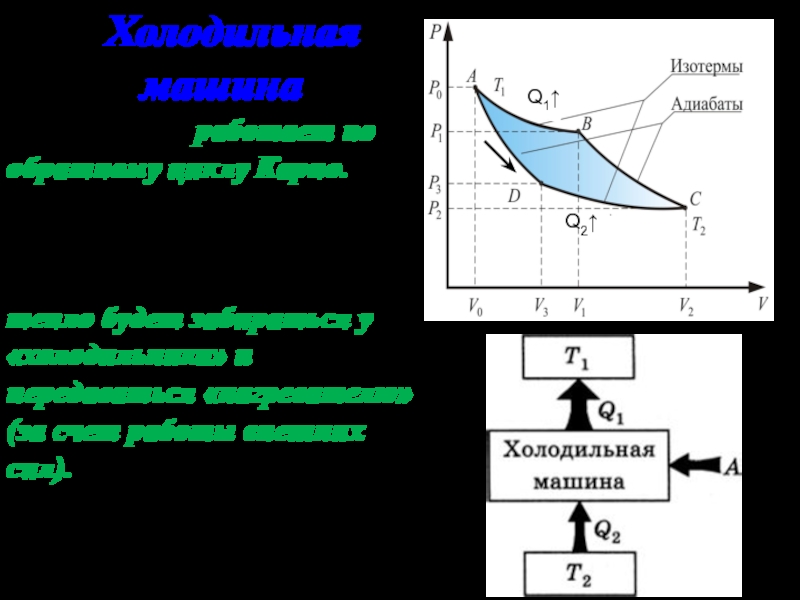
Холодильная машина
Эта машина работает по обратному циклу
Карно.
Если проводить цикл в обратном направлении, против часовой
стрелки, тепло будет забираться у «холодильника» и передаваться «нагревателю» (за счет работы внешних сил).Q2↑
Q1↑
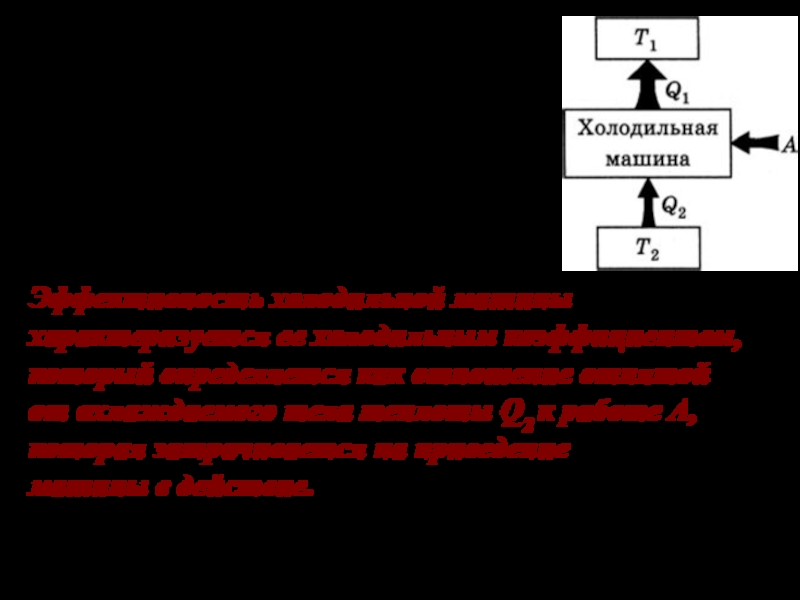
Слайд 12Эффективность холодильной машины характеризуется ее холодильным коэффициентом, который определяется как
отношение отнятой от охлаждаемого тела теплоты Q2 к работе A,
которая затрачивается на приведениемашины в действие.
Холодильная машина отбирает за цикл от холодного резервуара с темпе-ратурой T2 количество теплоты Q2 , добавляет к ней работу А, превра-щенную в тепло, и отдает резервуару с более высокой температурой T1 большее количество теплоты Q1.
Слайд 13Второе начало термодинамики
Тепловой двигатель и даже идеальная машина
Карно показали невозможность превращения всего тепла, полученного от нагревателя, в
механическую работу.Теплота обусловлена случайным хаотическим движением молекул, а механическая работа — их согласованным направленным движением. Таким образом указанное свойство термодинамических систем можно трактовать как невозможность превращения всей энергии теплового (хаотического) движения молекул в энергию направленного движения макроскопических тел (работу).
Слайд 14Появление второго начала термодинамики связано с необходимостью дать ответ на
вопрос, какие процессы в природе возможны, а какие нет. Второе
начало термодинамики дает ответ на этот вопрос. Оно определяет направление протекания термодинамических процессов.Существует несколько формулировок второго начала.
Формулировки Р. Клаузиуса: «Теплота не может самопроизвольно переходить от менее нагретого тела к более нагретому» или:
«Невозможны такие процессы, единственным результатом которых был бы переход теплоты от тела менее нагретого к телу более нагретому»
Первое начало термодинамики не позволяет устано-вить направление протекания т/д процессов.
Слайд 15Формулировка У.Томсона: «Невозможны такие процессы, единственным результатом которых
явилось бы отнятие
от некоторого тела определенного количества теплоты и превращение этой теплоты
полностью в работу» .Эта формулировка позволяет утверждать, что невозможен вечный двигатель второго рода:
такое превращение означало бы, что хаотическое тепловое движение молекул можно полностью превратить в упорядоченное движение макротел (работу).
II-е начало констатирует неуничтожимость хаотического теплового движения в изолированной системе
Слайд 16 Для количественной характеристики степени хао- тичности т/д состояния вводят
специальную функцию.
Энтропия
(греческая entropia – поворот, превращение)
Энтропия S – мера
хаотичности т/д системы. Требования к новой функции:
1) Энтропия S - функция состояния, т.е. dS - полный дифференциал
2) Энтропия S = const в изолированной системе с обратимыми процессами.
Понятие энтропии было впервые введено Клаузиусом в 1865 г.
При рассмотрении цикла Карно, он обратил внимание на отношение теплот к температурам, при которых они были получены или отданы в изотермических процессах:
Слайд 17Отношение теплоты Q к температуре, при которой происходила передача теплоты,
называется приведенной теплотой. Для квазистатического процесса элементарная приведенная теплота равна
Это
выражение является полным дифференциалом, т.е. сумма приведенных количеств теплоты для обратимого циклаСлайд 18Убедимся, к примеру, что это справедливо для обратимого цикла Карно.
Напомним
, что для цикла Карно имеем
Учтем, что получаемая газом теплота
Q1 - поло- жительна, а отдаваемая Q2- отрицательна.Суммируя приведенную теплоту на
всех участках цикла Карно, получим:
Слайд 19Можно показать, что и для любого другого обратимого кругового процесса
Полученное
выражение называется:
равенство Клаузиуса
Слайд 20 Напомним, если в круговом процессе интеграл от полного
дифференциала какой-либо функции равен нулю, то эта функция определяется только
состоянием системы и не зависит от пути, каким система пришла в это состояние, то есть она является функцией состояния (пример из механики — потенциальная энергия).Функция состояния, дифференциалом которой является величина
называется энтропией и обозначается S
Слайд 21Из равенства Клаузиуса
вытекает, что для замкнутых обратимых процессов
изменение энтропии равно нулюДля незамкнутых обратимых процессов изменение энтропии вычисляют интегрированием:
За нулевое значение (S = 0) выбирается состояние с абсолютной температурой T=0.
Энтропия – величина аддитивная, т.е. S = Σ Si
Слайд 23Каждый из изопроцессов идеального газа характери-зуется своим изменением энтропии, а
именно:
Изотермический ( ):
Изобарический
( ) :Слайд 24Изохорический ( )
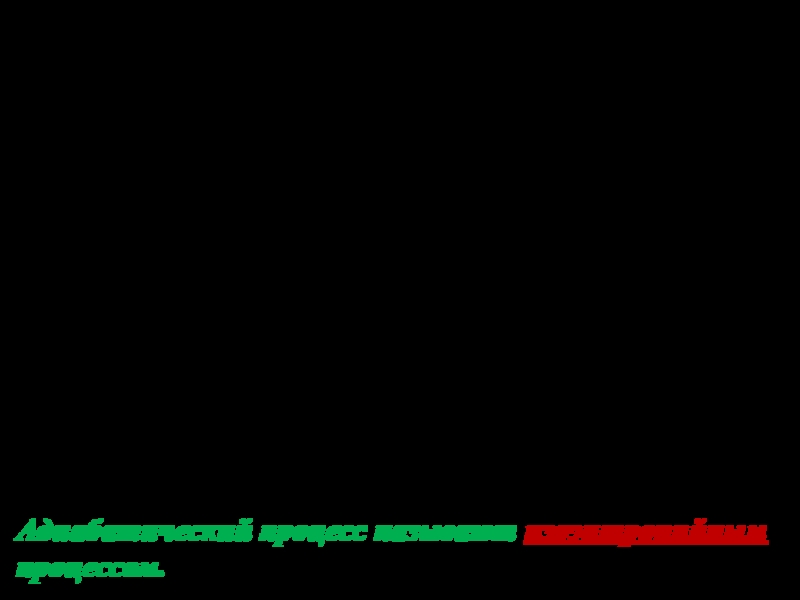
Адиабатический (
):
Адиабатический процесс
называют изоэнтропийным процессом.Слайд 25Энтропия в изолированной системе при необратимых процессах.
Из 1-ой теоремы
Карно: для любой тепловой машины, использующей любые, в том числе
необратимые процессыУчтем, что отдаваемое газом тепло отрицательно,
Тогда 1-ая теорема Карно принимает вид:
т.е. сумма приведенных количеств теплоты в любом замкнутом цикле ≤ 0 ( = 0 для обратимых циклов)
Слайд 26Это означает, что для квазистатических цикличес-ких процессов при наличии необратимых
процессов:
(Неравенство Клаузиуса)
На примере можно показать, что из этого вытекает возрастание
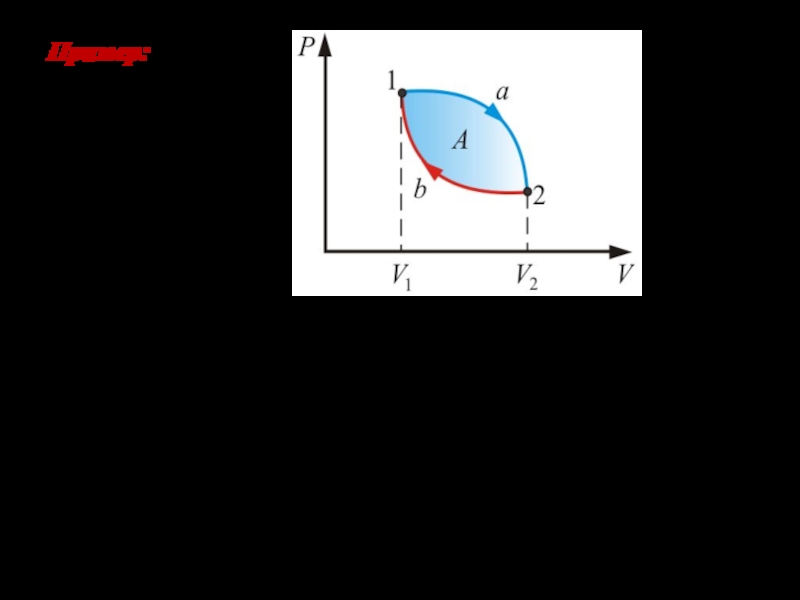
энтропии в необратимом процессе, протекающем в изолированной системе.Слайд 27Пусть система переходит из состояния 1 в состояние 2 (1а2)
в результате необратимого процесса, а возвращается из 2 в 1
(2b1) – в результате обратимого процесса. Для всего цикла справедливо неравенство Клаузиуса.Пример:
Слайд 28Распишем цикл поэтапно:
Для обратимого процесса
Тогда
Если система изолирована:
и
следовательно
Т. е. энтропия изолированной системы возрастает
Слайд 29Основные итоги рассмотренного.
При любом необратимом процессе в изолированной
системе энтропия возрастает (dS > 0).
Энтропия достигает своего
максимального значе-ния в состоянии термодинамического равновесия.
Для произвольного процесса
где, знак равенства – для обратимого процесса; знак больше > для необратимого.
– математическая запись второго начала термодинамики.
Слайд 31 Третье начало термодинамики.
Первое и второе
начала термодинамики не указывают на поведение энтропии при абсолютном нуле
Т = 0º К.На основании обобщения экспериментальных исследований различных веществ при сверхнизких температурах было сформулировано, что
1. При приближении к абсолютному нулю энтропия стремится к определенному конечному пределу;
2. Все равновесные процессы при абсолютном нуле происходят без изменения энтропии.
Эти утверждения называют теоремой Нернста или Третьим началом термодинамики.
Слайд 32На их основании можно считать, что при
Т → 0
энтропия также стремится к нулю.
(такую формулировку третьего начала термодинамики предложил
М. Планк) Энтропия с таким нулем отсчета называется абсолютной энтропией.Нулевое значение энтропии соответ- ствует отсутствию хаотического теплового движения при абсолютном нуле.