Слайд 1Лекция № 11
Клеточные механизмы запуска мышечного сокращения.
Механизмы электромеханического
сопряжения в разных типах мышечных волокон.
Курс лекций по дисциплине
«Структурные
и функциональные особенности
поперечно-полосатых и гладких мышц»
Институт теоретической и экспериментальной
биофизики РАН
(ИТЭБ РАН)
Слайд 21. Назовите три типа нитей в саркомере поперечно-полосатых мышц.
2.
Какой белок формирует третий тип нитей?
Вопросы для мини-проверки
3. Напишите
разные названия третьего типа нитей.
4. Какие функции выполняет титин/тайтин(коннектин)?
5. Каким методом был открыт титин?
6. Каким образом в лаборатории структуры и функций мышечных белков показали, что титин связывается с актином?
Слайд 3Новости науки
Раскрыта причина непобедимости рака
Ученые Калифорнийского университета в Сан-Диего
выяснили, что в опухолевых клетках в изобилии содержатся кольцевые молекулы
внехромосомной ДНК, которые играют ключевую роль в способности рака сопротивляться лечению. Об этом сообщается в пресс-релизе на сайте MedicalXpress.
Оказалось, что кольцевая ДНК в раковых клетках характеризуется высокой активностью, что способствует синтезу факторов роста и других соединений, способствующих развитию опухолей. Эта форма ДНК напоминает ДНК у бактерий и обнаруживается в 50 процентах случаев рака.
В 2014 году Пол Мишель (Paul Mischel) и его коллеги обнаружили, что ДНК играет центральную роль в лекарственной устойчивости некоторых опухолей головного мозга. При делении дефектной клетки дочерние клетки получают сразу несколько копий онкогенов, что обеспечивает более быструю эволюцию. Это отличается от обычного митоза, при котором происходит копирование только хромосом.
Слайд 4НОВЫЙ АППАРАТ ОТ TOSHIBA ПО КАПЛЕ КРОВИ ВЫЯВЛЯЕТ 13 ВИДОВ
РАКА
Эксперты из компании Toshiba создали устройство, которое может выявить 13
типов рака с точностью в 99%. И для этого потребуется всего-то одна капля крови.
Новейший тест способен выявить рак желудка, пищевода, легких, печени, поджелудочной железы, желчевыводящих путей, кишечника, яичников, простаты, мочевого пузыря, молочной железы, а также глиому (опухоль из нервных тканей, часто возникающую в головном мозге) и саркому (группа опухолей мягких тканей — жировой, мышечной и так далее).
Цена не превысит 20000 японских иен (порядка 12 тысяч рублей), что для такого широкого спектра выявляемых болезней — просто смехотворная цена.
Сам метод основан на оценке типа и концентрации молекул микро-РНК раковых клеток, циркулирующих в периферической крови человека. Дело в том, что все раковые клетки очень часто имеют разную микро-РНК (это часть клетки, которая несет ряд информации о ее особенностях и функционировании). Так вот, данный структурный элемент не просто разнится от клетки к клетке, но и при каждом виде рака концентрация микро-РНК в крови своя.

Слайд 6Три основных события, необходимых для реализации сокращения любой мышцы:
Деполяризация
мышечной мембраны и генерация потенциала действия (ПД);
Повышение концентрации свободного
ионизированного кальция в саркоплазме вблизи сократительных белков;
Кальций-зависимое взаимодействие белков актиномиозинового комплекса, приводящее к сокращению клетки.
Сложный каскад реакций от момента деполяризации мембраны до повышения уровня внутриклеточного кальция вблизи сократительных белков получил название электромеханического сопряжения (ЭМС).
Слайд 7Внутриклеточный метаболизм ионов кальция
Внутриклеточный кальций присутствует в мышечных клетках в
основном в связанном состоянии, и только небольшая его часть находится
в цитоплазме в свободном (ионизированном) состоянии.
Уровень кальция в клетке можно определить с помощью ионоселективного микроэлектрода.
Слайд 9Т.о., мышечные клетки и волокна в состоянии покоя имеют ~
одинаковый уровень ионов кальция в миоплазме = 0,1-0,3 микромоля/л, т.е.
~10 (в минус 7 степени) Моля.
Слайд 10Механизмы, поддерживающие низкий уровень кальция в покое (кстати, зачем?)
кальций-зависимая АТРаза
мембраны клетки – кальциевый насос (10 в минус восьмой Моля,
связывает ионы кальция при такой концентрации). Из миоплазмы – наружу.
кальций-зависимая АТРаза саркоплазматического ретикулума.
Натрий-кальциевый транспортер – выводит ионы кальция из клетки, но только при 10-кратном и более превышении их нормального уровня в миоплазме.
Кальций-связывающие белки цитоплазмы (напр., кальмодулин) играют роль внутриклеточных буферов кальция.
Митохондрии способны закачивать ионы кальция (до 0,6 на 10 в минус 3 степени Моля). Участвуют в закачке кальция при патологии или гипоксии.
Слайд 11Повышение уровня кальция при сокращении
В покое концентрация ионов кальция в
миоплазме = ~ 5х10 (в минус 8) – 5х10 (в
минус 7) М., а снаружи клетки – 5х10 (в минус 3) М.
Во сколько раз разница?
Откуда берется кальций?
Из цистерн саркоплазматического ретикулума (СР), а также из ядра и митохондрий (внутри клетки),
а также из наружной среды клетки по кальциевым каналам, по механочувствительным или стреч-каналам,
+ за счет инвертированной работы натрий-кальциевого транспортера.
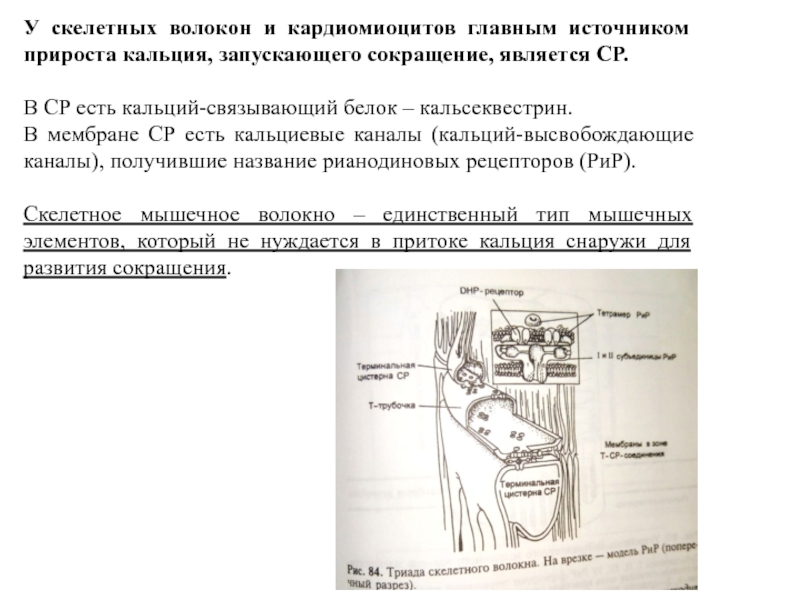
Слайд 12У скелетных волокон и кардиомиоцитов главным источником прироста кальция, запускающего
сокращение, является СР.
В СР есть кальций-связывающий белок – кальсеквестрин.
В мембране СР есть кальциевые каналы (кальций-высвобождающие каналы), получившие название рианодиновых рецепторов (РиР).
Скелетное мышечное волокно – единственный тип мышечных элементов, который не нуждается в притоке кальция снаружи для развития сокращения.
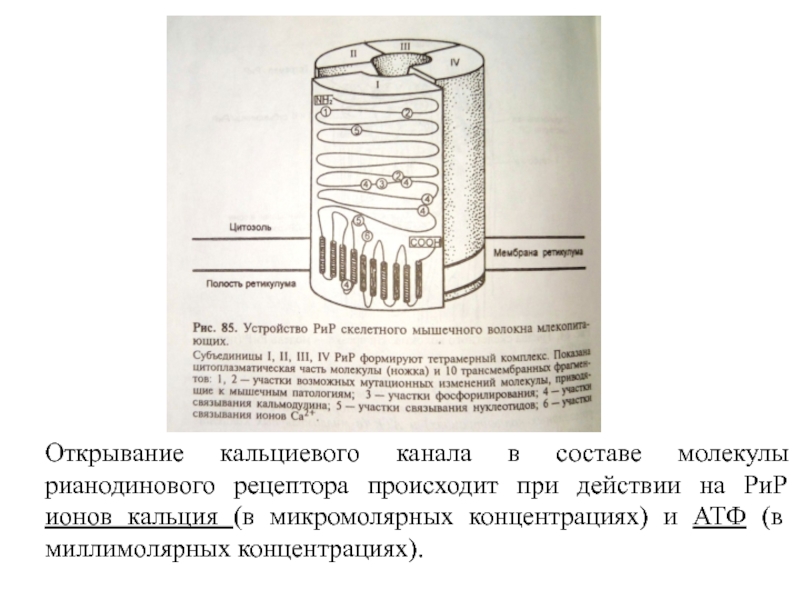
Слайд 13Открывание кальциевого канала в составе молекулы рианодинового рецептора происходит при
действии на РиР ионов кальция (в микромолярных концентрациях) и АТФ
(в миллимолярных концентрациях).
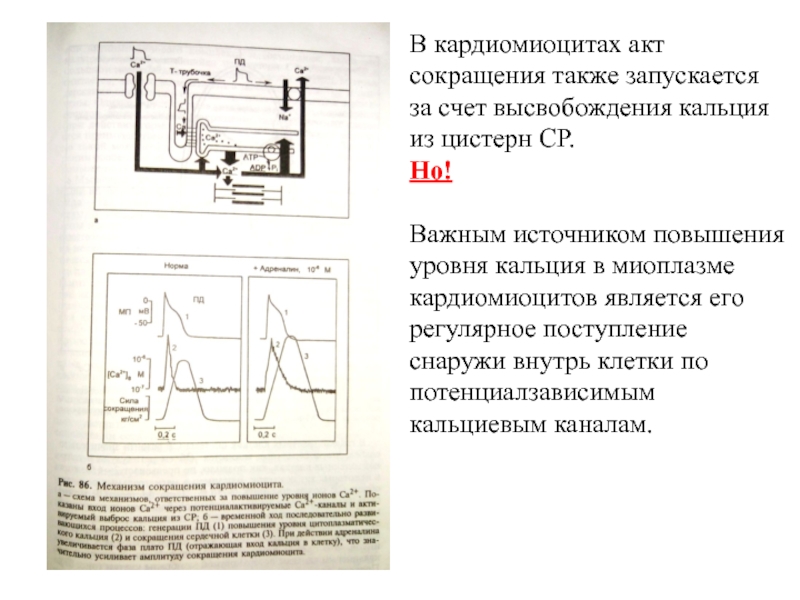
Слайд 14В кардиомиоцитах акт сокращения также запускается за счет высвобождения кальция
из цистерн СР.
Но!
Важным источником повышения уровня кальция в
миоплазме кардиомиоцитов является его регулярное поступление снаружи внутрь клетки по потенциалзависимым кальциевым каналам.
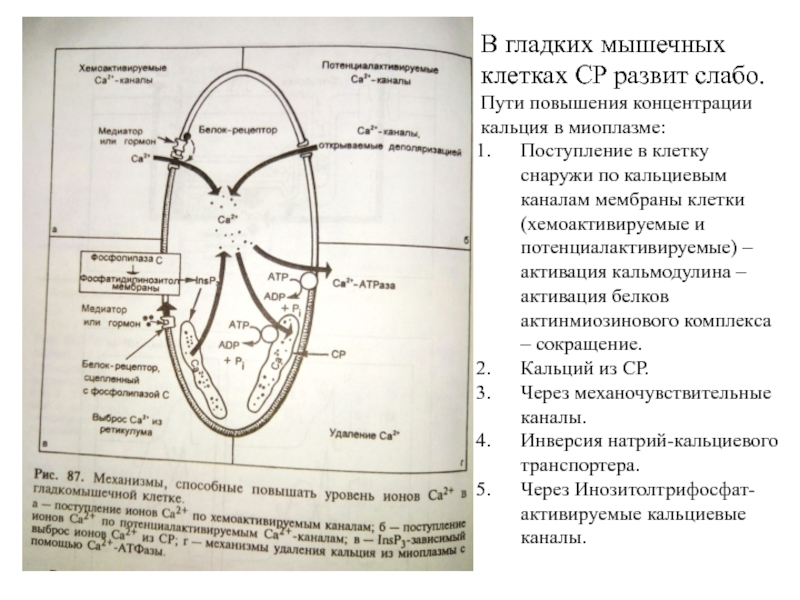
Слайд 15В гладких мышечных клетках СР развит слабо.
Пути повышения концентрации кальция
в миоплазме:
Поступление в клетку снаружи по кальциевым каналам мембраны
клетки (хемоактивируемые и потенциалактивируемые) – активация кальмодулина – активация белков актинмиозинового комплекса – сокращение.
Кальций из СР.
Через механочувствительные каналы.
Инверсия натрий-кальциевого транспортера.
Через Инозитолтрифосфат-активируемые кальциевые каналы.
Слайд 16Особенности генерации потенциала действия (ПД) в разных типах мышечных клеток
В скелетных мышечных волокнах позвоночных восходящая фаза ПД обусловлена входящим
натриевым током за счет открывания потенциалактивируемых натриевых каналов.
Вторя – нисходящая фаза ПД , вызвана выходящим калиевым током по потенциалактивируемым калиевым каналам.
Длительность ПД в скелетных мышцах = 4-6 мс.
Слайд 17В сердечных миоцитах восходящая фаза ПД обусловлена входящим натриевым током
и!!!
кальциевым током! Имеется фаза «плато ПД». В этой фазе сохраняется
долго кальциевый ток (long lasting – долго длящийся) – L-ток.
Длительность ПД = 300-400 мс.
Реполяризация мембраны сердечной клетки связана с закрытием кальциевых каналов L-типа и доминированием выходящего калиевого тока по особым кальций-активируемым калиевым каналам!
Слайд 18У гладкомышечных клеток, как и у кардиомиоцитов, ПД имеет три
фазы: деполяризацию, плато и реполяризацию.
Длительность ПД – 10-100 мс.
I фаза ПД в гладкомышечных клетках обусловлена быстрым входящим кальциевым током Т-типа, а фаза плато – кальциевым током L-типа. (но не натриевым током!!!!)
Реполяризация: закрытие кальциевых и открытие калиевых каналов, в том числе кальций-активируемых и калиевых каналов задержанного выпрямления!
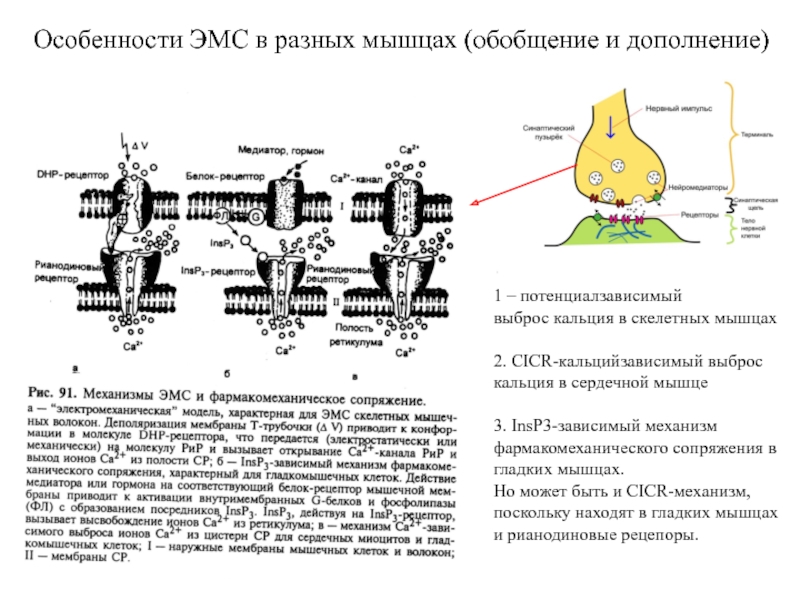
Слайд 19Особенности ЭМС в разных мышцах (обобщение и дополнение)
1 –
потенциалзависимый
выброс кальция в скелетных мышцах
2. CICR-кальцийзависимый выброс кальция в
сердечной мышце
3. InsP3-зависимый механизм фармакомеханического сопряжения в гладких мышцах.
Но может быть и CICR-механизм, поскольку находят в гладких мышцах и рианодиновые рецепоры.
Слайд 20Фармако-механическое сопряжение в гладких мышцах
Слайд 21Регуляция взаимодействия актина и миозина на уровне сократительного аппарата
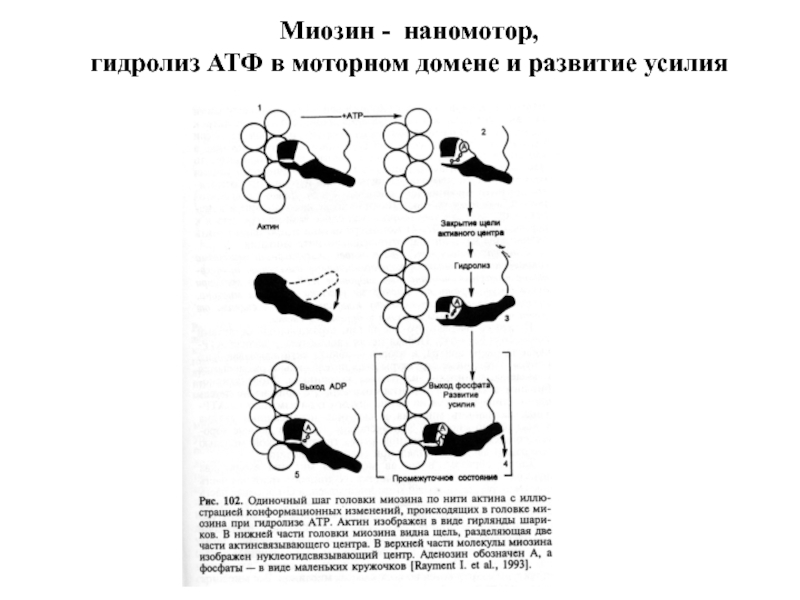
Слайд 22Миозин - наномотор,
гидролиз АТФ в моторном домене и развитие
усилия
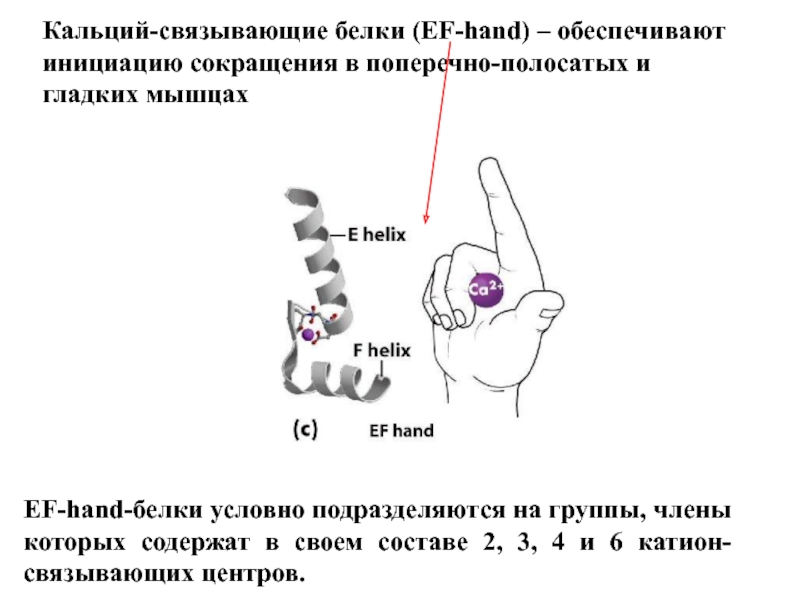
Слайд 23Кальций-связывающие белки (EF-hand) – обеспечивают
инициацию сокращения в поперечно-полосатых и
гладких
мышцах
EF-hand-белки условно подразделяются на группы, члены которых содержат в
своем составе 2, 3, 4 и 6 катион-связывающих центров.
Слайд 24Самые простые по строению кальций-связывающие белки содержат в своем составе
только 2 EF-hand домена:
S-100 (из мозга), кальтропин и кальгицарин
(гладкие мышцы);
Функции: регуляция клеточного цикла, регуляция сократительной активности;
Самая обширная группа представлена белками, содержащими в своем составе 4 кальций-связывающих центра:
Кальмодулин, тропонин С, легкие цепи миозина,
а также кальпаины – кальций-зависимые протеазы, + кальцинейрин – Са-кальмодулинзависимая протеинфосфотаза;
+ парвальбумины (в быстросокращающихся быстрых мышцах у рыб), участвуют, по-видимому, в быстром удалении ионов кальция от сократительного аппарата.
Слайд 25К EF-hand-белкам относятся также:
альфа-актинин, дистрофин!
Группа белков, содержащая 6
и более центров связывания ионов кальция – кальретинин, кальбиндин (в
кишечнике у птиц).
Вопрос?
А ионы магния могут связываться с EF-hand-белками?
Слайд 26Ионы магния имеют меньший радиус, чем ионы кальция. Вследствие этого
они менее прочно связываются в катионсвязывающих центрах и вызывают заметно
меньшие конформационные изменения в общей структуре анализируемых белков.
Слайд 27EF-hand-белки участвуют в регуляции сократительной активности поперечно-полосатых и гладких мышц!
Эти
белки связаны в мышце либо с миозином, либо с актином.
Поэтому различают 2 типа регуляции мышечного сокращения: миозиновый и актиновый
Самый простой тип миозиновой регуляции основан на связывании ионов кальция в области шейки миозина (кальций-связывающийся центр формируется при участии 2-х легких и одной тяжелой цепи миозина).
При этом происходят конформационные изменения в актин- и АТФ-связывающих центрах головки миозина в результате чего миозин способен взаимодействовать с актином.
Этот тип регуляции характерен для поперечно-полосатых мышц моллюсков.
Слайд 282 Тип миозиновой регуляции – конформационные изменения в области шейки
головки формируются путем фосфорилирования регуляторных легких цепей миозина (ЛЦ2).
Фосфорилирование
по Ser и Thr
Фосфорилирует кальций-кальмодулинзависимая киназа легких цепей миозина.
Дефосфорилируют легкие цепи – протеинфосфотазы 1 и 2А (их активность не зависит от концентрации ионов кальция).
Этот тип регуляции присущ гладким мышцам, немышечным клеткам, но и, как дополнительный (модулирующий) тип регуляции, характерен и для поперечно-полосатых мышц.
Слайд 29Актиновый тип регуляции - основной тип регуляции мышечного сокращения в
поперечно-полосатых мышцах животных. В основе этого типа сокращения лежат конформационные
изменения в тропонин-тропомиозиновом комплексе на тонких нитях.
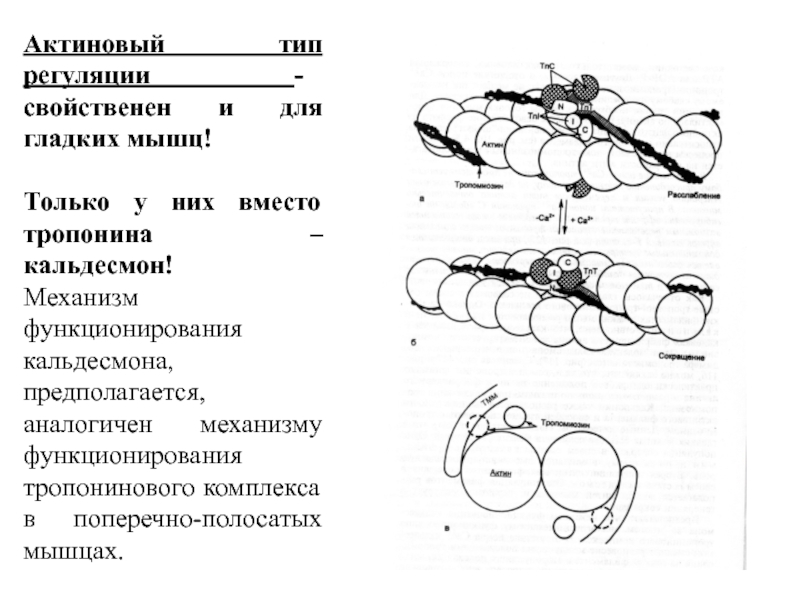
Слайд 30Актиновый тип регуляции - свойственен и для гладких мышц!
Только у
них вместо тропонина – кальдесмон!
Механизм функционирования кальдесмона, предполагается, аналогичен
механизму функционирования тропонинового комплекса в поперечно-полосатых мышцах.
Слайд 34Т.о., актиновый и миозиновый типы регуляции свойственны для всех типов
мышц!