Слайд 1Лекция № 20
ГБОУ ВПО КрасГМУ им. проф.В.Ф. Войно-Ясенецкого Минздрава
России
Фармацевтический колледж
Лектор Ростовцева Л.В., преподаватель химии
высшей квалификационной категории
Красноярск,
2013
Тема: Производные ненасыщенных
полиокси-γ-лактонов
Слайд 2План лекции:
1) Понятие о производных ненасыщенных полиокси-γ-лактонов
2) Кислота аскорбиновая
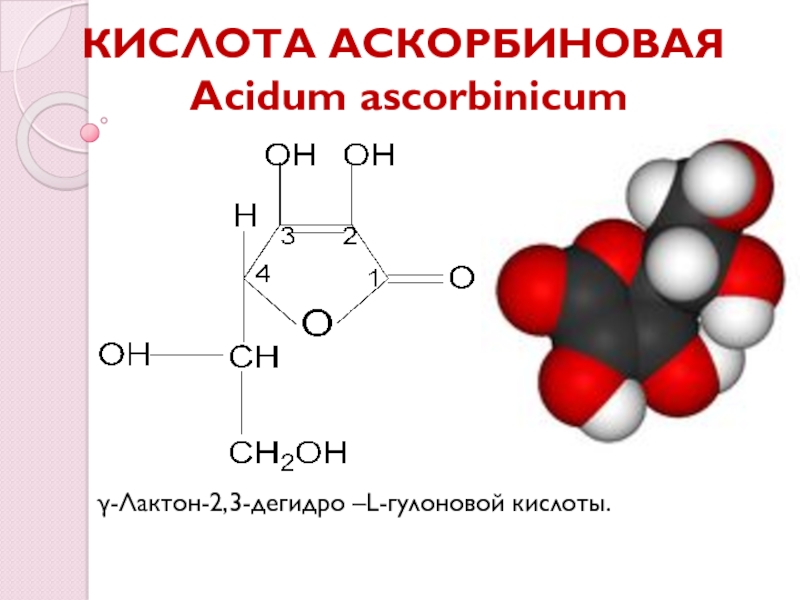
Слайд 3КИСЛОТА АСКОРБИНОВАЯ
Acidum ascorbinicum
γ-Лактон-2,3-дегидро –L-гулоновой кислоты.
Слайд 4Получение:
Впервые аскорбиновая кислота была получена из капусты Бессоновым. Синтез был
осуществлён в 1933г. В промышленности кислоту аскорбиновую получают из D-глюкозы,
которая в больших количествах получается при расщеплении крахмала серной кислотой.
Суточная потребность человека в витамине С составляет примерно 30 мг.
Природные источники: цитрусовые, ягоды, помидоры,
цветная капуста, картофель, шиповник.
Слайд 5Описание:
Кислота аскорбиновая – белый кристаллический порошок без запаха, кислого вкуса;
легко растворим в воде и спирте, нерастворим в эфире и
хлороформе. Имеет 2 ассиметрических атома углерода. Оптически активна.
Температура плавления 190°С - 193°С
Слайд 6Реакции подлинности:
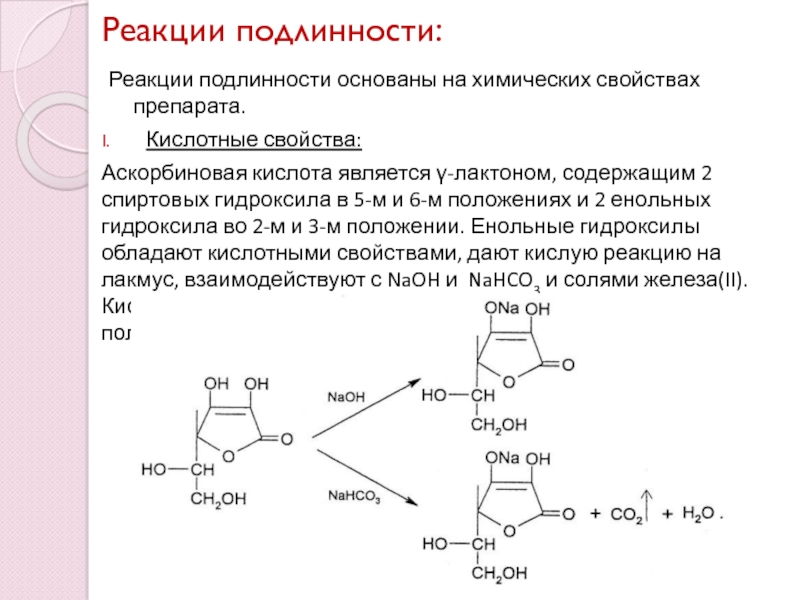
Реакции подлинности основаны на химических свойствах препарата.
Кислотные свойства:
Аскорбиновая кислота
является γ-лактоном, содержащим 2 спиртовых гидроксила в 5-м и 6-м
положениях и 2 енольных гидроксила во 2-м и 3-м положении. Енольные гидроксилы обладают кислотными свойствами, дают кислую реакцию на лакмус, взаимодействуют с NaOH и NaHCO3 и солями железа(II). Кислотные свойства более выражены у гидроксила в 3-м положении.
Слайд 7На наличии кислотных свойств основана реакция образования аскорбината железа. Аскорбиновую
кислоту переводят в натриевую соль добавлением NaHCO3, а затем добавляют
FeSO4;появляется фиолетовое окрашивание:
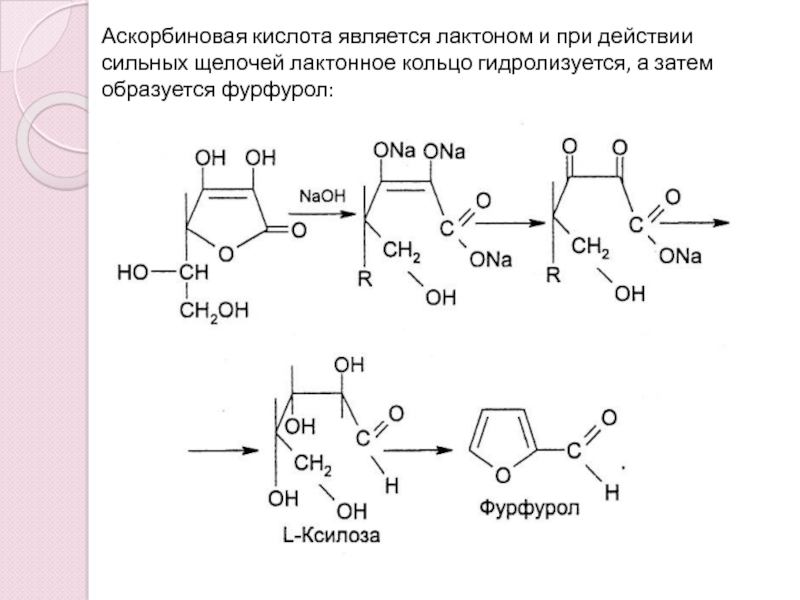
Слайд 8Аскорбиновая кислота является лактоном и при действии сильных щелочей лактонное
кольцо гидролизуется, а затем образуется фурфурол:
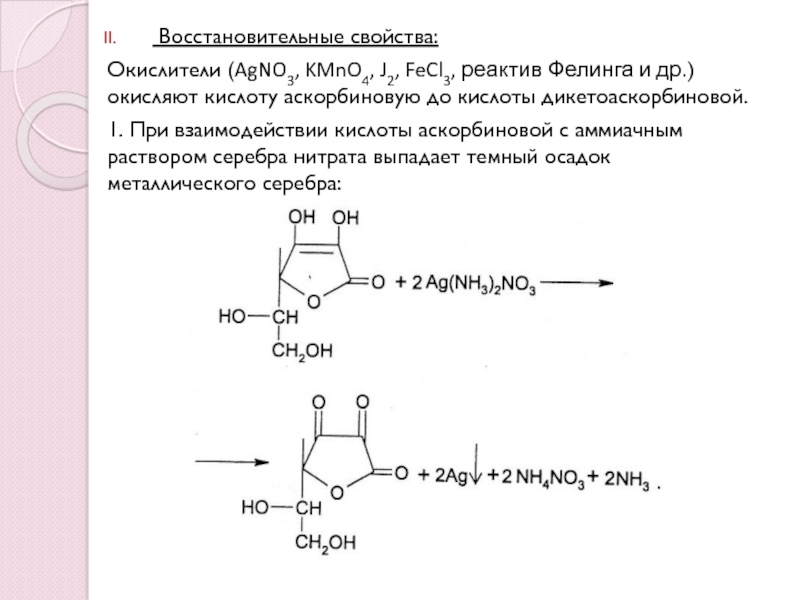
Слайд 9 Восстановительные свойства:
Окислители (AgNO3, KMnO4, J2, FeCl3, реактив Фелинга и
др.) окисляют кислоту аскорбиновую до кислоты дикетоаскорбиновой.
1. При взаимодействии кислоты
аскорбиновой с аммиачным раствором серебра нитрата выпадает темный осадок металлического серебра:
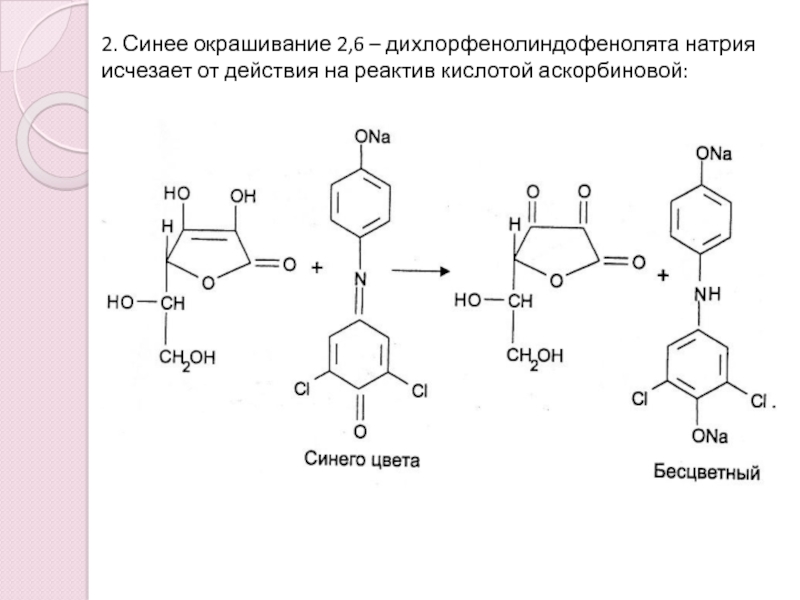
Слайд 102. Синее окрашивание 2,6 – дихлорфенолиндофенолята натрия исчезает от действия
на реактив кислотой аскорбиновой:
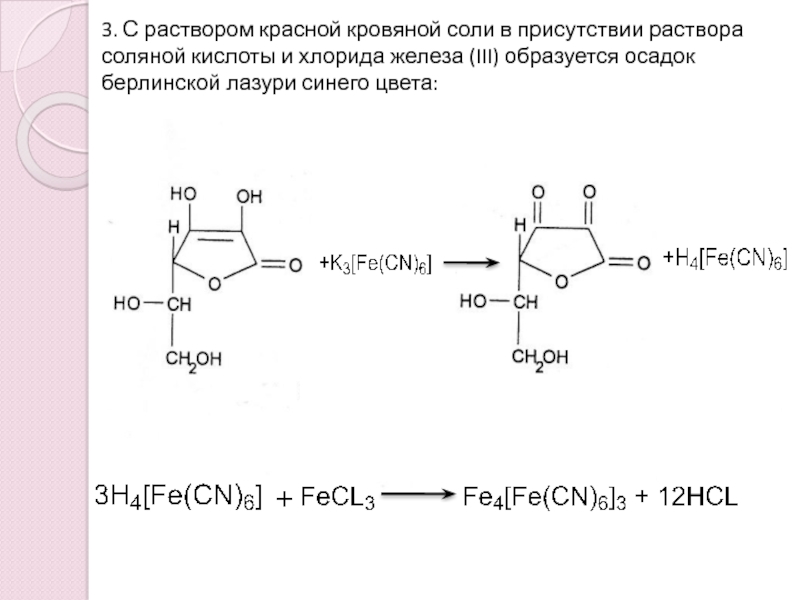
Слайд 113. С раствором красной кровяной соли в присутствии раствора соляной
кислоты и хлорида железа (III) образуется осадок берлинской лазури синего
цвета:
Слайд 12Испытание на чистоту:
В качестве допустимых примесей рассматривают сульфатную золу (не
более 0,1%) и тяжелые металлы (не более 0,001%). Содержание органических
примесей определяют после добавления к препарату концентрированной серной кислоты: окраска раствора через 30 мин не должна превышать окраску эталонного раствора, разведенного в соотношении 1:2 (ГФ). Обязателен тест на щавелевую кислоту (возможный продукт окисления).
Слайд 13Методы количественного определения:
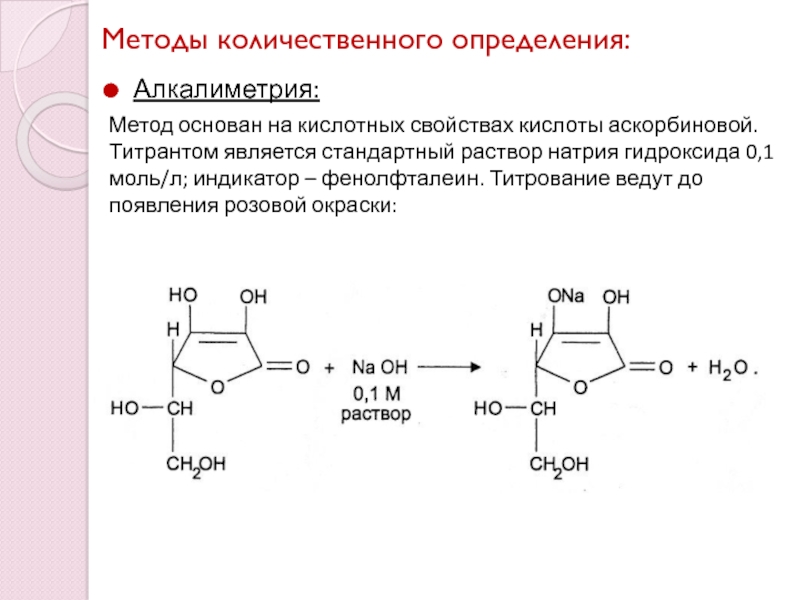
Алкалиметрия:
Метод основан на кислотных свойствах кислоты аскорбиновой. Титрантом
является стандартный раствор натрия гидроксида 0,1моль/л; индикатор – фенолфталеин. Титрование
ведут до появления розовой окраски:
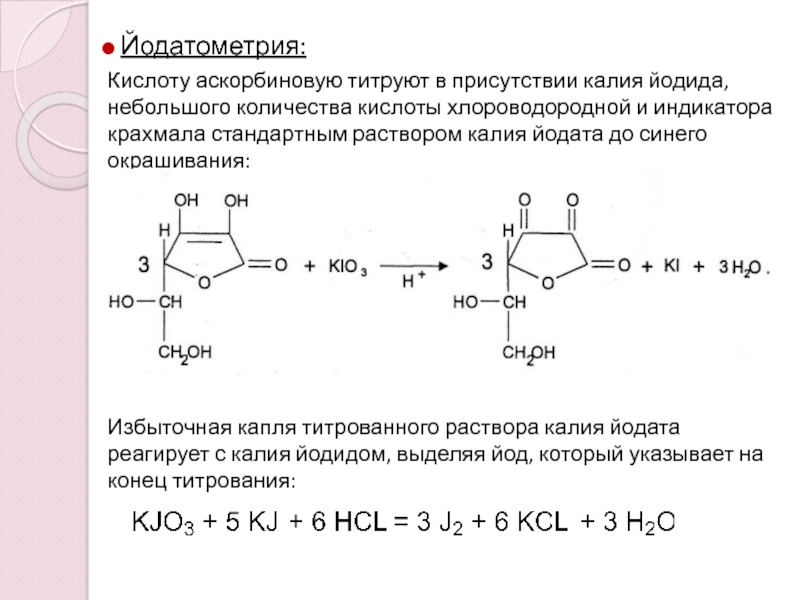
Слайд 14 Йодатометрия:
Кислоту аскорбиновую титруют в присутствии калия йодида, небольшого количества
кислоты хлороводородной и индикатора крахмала стандартным раствором калия йодата до
синего окрашивания:
Избыточная капля титрованного раствора калия йодата реагирует с калия йодидом, выделяя йод, который указывает на конец титрования:
Слайд 15 Йодометрия:
В основе метода лежат восстановительные свойства аскорбиновой кислоты. В
качестве титранта используют раствор йода 0,1моль/л; индикатор – крахмал. Титрование
ведут до устойчивой синей окраски:
Слайд 16Применение:
Витаминное средство, оказывает метаболическое действие, не образуется в организме человека,
а поступает только с пищей. Участвует в регулировании окислительно-восстановительных процессов,
углеводного обмена, свертываемости крови, регенерации тканей; повышает устойчивость организма к инфекциям, уменьшает сосудистую проницаемость, снижает потребность в витаминах B1, B2, А, Е, фолиевой кислоте, пантотеновой кислоте. Обладает антиагрегантными и выраженными антиоксидантными свойствами.
Слайд 17Формы выпуска:
порошок;
таблетки;
таблетки по с глюкозой (в профилактических целях),
5 % и 10 % растворы в ампулах по 1
и 2 мл (в лечебных целях) .
Хранение: порошок аскорбиновой кислоты - в хорошо укупоренной таре, предохраняющей от действия света, в сухом прохладном месте; таблетки и ампулы - в прохладном, защищенном от света месте.
Слайд 18Литература
Обязательная:
Глущенко Н.Н., Плетнева Т.В., Попков В.А. Фармацевтическая химия.
М.: Академия,
2004.- 384 с. 198-200
Государственная фармакопея Российской Федерации/ Издательство
«Научный центр
экспертизы средств медицинского применения»,
2008.-704с.:ил.
Дополнительная:
1. Государственная фармакопея 11 изд., вып. 2-М: Медицина, 1989. - 400 с.
2. Беликов В. Г. Фармацевтическая химия. – 3-е изд., М., МЕДпресс-информ
- 2009, 616 с.:ил.