Слайд 1Метаболизм сложных белков
Метаболизм гема
Метаболизм нуклеотидов
Слайд 2Сложные белки - протеиды
Сложные белки классифицируются по характеру
простетической группы:
Хромопротеиды ( к ним относятся гемпротеиды, простетическая группа -
гем);
Нуклеопротеиды (простетическая группа – нуклеотиды);
Гликопротеиды (простетическая группа – углеводы);
Липопротеиды ( простетическая группа – липиды);
Фосфопротеиды ( простетичеая группа – фосфорная кислота)
Белковая часть метаболизируется по уже известному нам механизму.
Слайд 3Гемпротеиды. Гем
Гемпротеиды человека представлены следующими. веществами: гемоглобин, миоглобин, цитохромы, каталаза
и др.
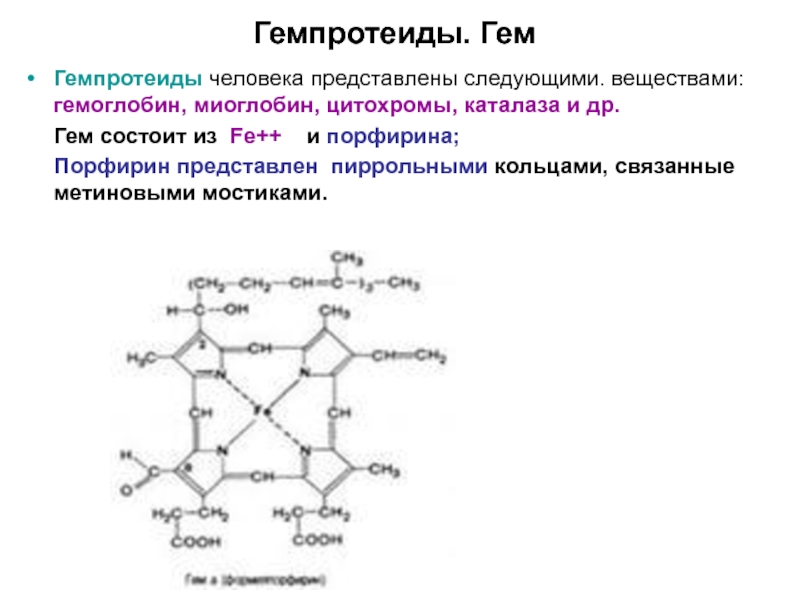
Гем состоит из Fe++ и
порфирина;
Порфирин представлен пиррольными кольцами, связанные метиновыми мостиками.
Слайд 4Гемоглобин
Молекула гемоглобина А представлена:
4 гема связаны с попарноодинаковыми пептидными
цепями 2L = 2β
Синтез на рибосомах цепей L и
β
строго контролируется (L =β )
Слайд 5Источники гема
Пищевые продукты - (экзогенный путь) не имеет значения!!.
В пищевом
рационе в составе продуктов животного происхождения (гемоглобин, миоглобин). В желудке
под действием пепсина и НСL расщепляются на гем и белковую часть. Белковая часть подвергается перевариванию по известному механизму. Гем окисляется в гематин, который не всасывается и выходит с калом.
2. Синтез de novo!!!
Слайд 6Синтез гема
Синтез de novo – источник гема!!!
Место
синтеза все ткани, основное - костный мозг
(исключение – эритроциты – нет рибосом)
Источники железа для синтеза:
а. пищевые продукты (экзогенный источник)- негеминовое железо в составе органических солей и железосодержащих негеминовых белков (говядина, гов. печень, птица, рыба, гречка, просо). Fe+++
Из пищевых продуктов Fe +++ высвобождается в кислой среде желудочного сока. Всасывается в 12-перстной кишке в виде Fe++, Fe+++ → Fe++ (аскорбиновая кислота)
Суточный рацион содержит от 10 – 30 мг железа, всасывается около 10 % от введенного.
Выводится в сутки около 1 мг. Излишнее кол-во депонируется в составе белка ферритина. Степень всасывания железа в ЖКТ контролируется ферритином энтероцитов.
Транспорт железа в крови осуществляется белком трансферрином.
б. железо, освобождающееся при постоянном распаде гемоглобина, реутилизируется вновь
Депо железа в тканях –ферритин ( наибольшее кол-во содержится в печени, селезенке, костном мозге)
Слайд 7Синтез гема
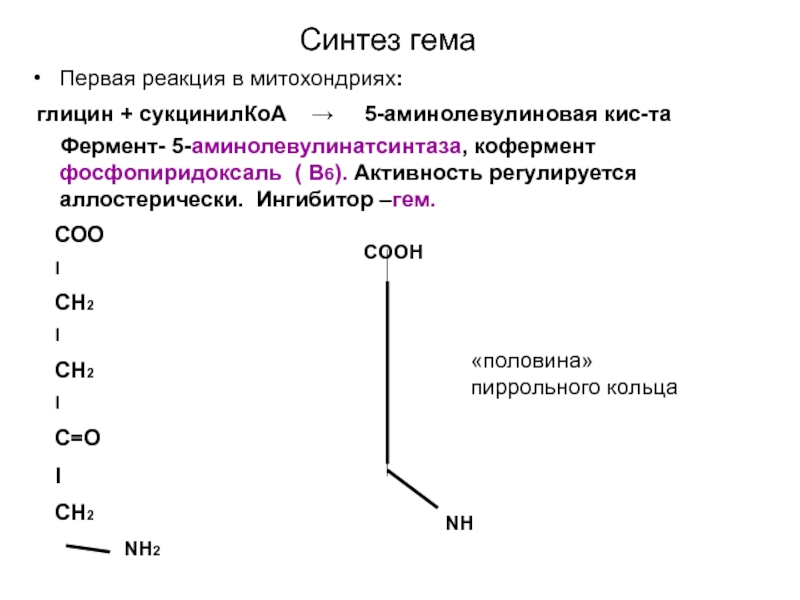
Первая реакция в митохондриях:
глицин + сукцинилКоА →
5-аминолевулиновая кис-та
Фермент- 5-аминолевулинатсинтаза, кофермент фосфопиридоксаль
( В6). Активность регулируется аллостерически. Ингибитор –гем.
СОО
I
СН2
I
СН2
I
С=O
I
СН2
Н
NH2
CООН
NH
«половина» пиррольного кольца
Слайд 8Синтез гема
Глицин + сукцинилКоА
5 аминолевулиновая кислота
Порфобилиноген
Уропорфириноген III
Копропорфириноген III
Протопорфирин IХ
Гем
аминолевулинатсинтаза
Пиррольное кольцо
Синтаза,
косинтаза
-СО2 декарбоксилаза
-СО2 декарбоксилаза
+Fe++ хелатаза
2 молекулы конденсируются
4 кольца конденсируется
Слайд 9Нарушения синтеза гема
Порфирии - (порфирин – пурпурный(греч.) сопровождаются накоплением в
крови порфириногенов и их окисленных продуктов порфиринов ( окрашенные).
Наследственные связаны
с генетическими дефектами ферментов синтеза гема: синтазы и косинтазы, декарбоксилаз:
Эритропоэтическая (снижение синтеза в костном мозге) и накопление метаболитов (порфиринов) в эритроцитах, далее в кровь, далее с мочой (Моча – красного цвета)
Печеночные – снижение синтеза в печени и накопление метаболитов (порфиринов) в гепатацитах.
Возможны нейропсихические расстройства – метаболиты- нейротоксины; фотодерматиты, нарушение функции печени
Приобретенные (часто на фоне бессимтомных наследственных) при- отравление свинцом, приеме лекарственных препаратов – индукторов синтеза 5-аминолевулинатсинтазы - диклофенак, барбитураты, стероиды.
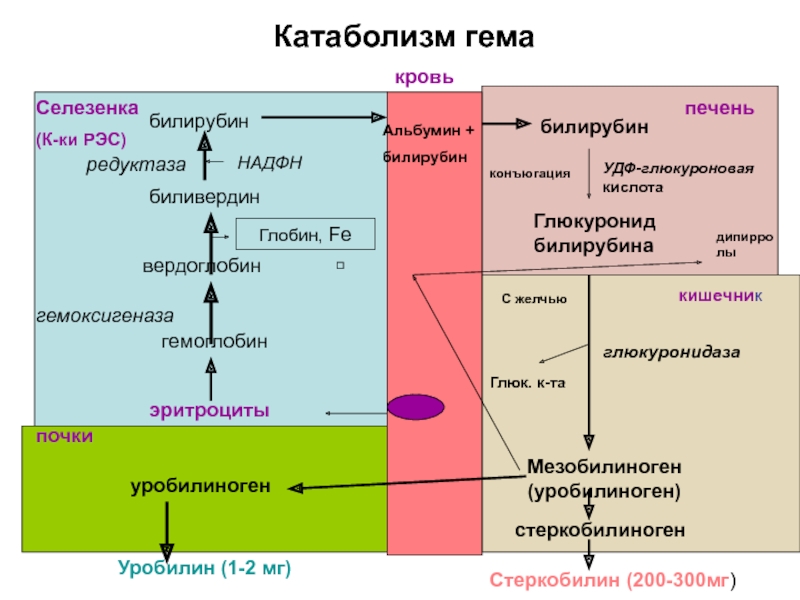
Слайд 10Катаболизм гема
Селезенка
(К-ки РЭС)
почки
печень
кишечник
эритроциты
вердоглобин
биливердин
билирубин
гемоглобин
Глобин, Fe
Альбумин +
билирубин
билирубин
УДФ-глюкуроновая кислота
конъюгация
Глюкуронид билирубина
С желчью
глюкуронидаза
Глюк. к-та
Мезобилиноген (уробилиноген)
стеркобилиноген
уробилиноген
Стеркобилин
(200-300мг)
Уробилин (1-2 мг)
дипирролы
кровь
гемоксигеназа
редуктаза
НАДФН
Слайд 11Билирубин – основной метаболит гема (гидрофобный)
В норме в крови общего
билирубина до 20 мкмоль/л
Свободный ( непрямой)- 75%;
Связанный - ( прямой)
глюкуронид- 25%
Гипербилирубинемия: может как следствие:
А.Образование билирубина в большем кол-ве (вследствие гемолиза), чем то, которое печень может поглотить;
Б. повреждение гепатоцитов, нарушающих экскрецию билирубина в кишечник;
В. закупорка желчных выводящих протоков (опухоль, камни)
В зависимости от уровня повреждения различают надпеченочная( гемолитическая), печеночная, (паренхитматозная); подпеченочная( механическая, обтурационная)
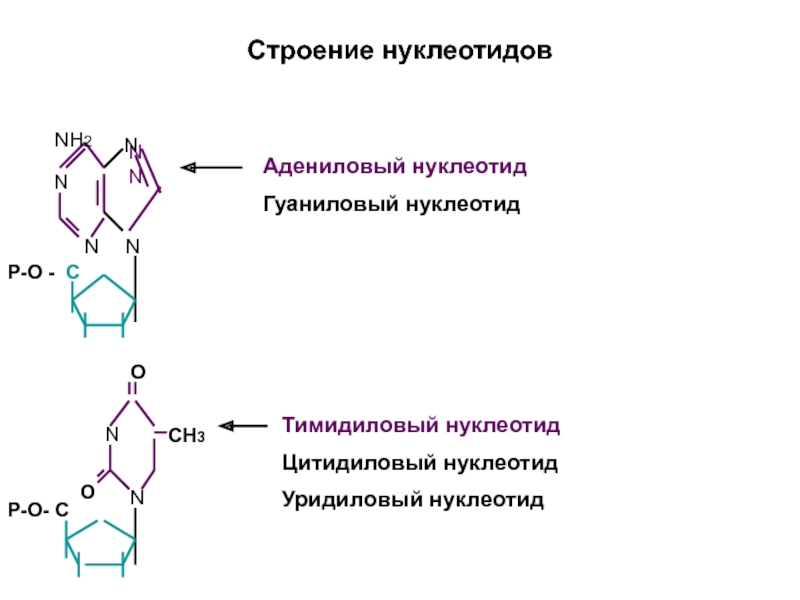
Слайд 13Строение нуклеотидов
N
N
NN
N
N
C
P-O -
N
N
P-O- C
NH2
CH3
O
O
Адениловый нуклеотид
Гуаниловый нуклеотид
Тимидиловый нуклеотид
Цитидиловый
нуклеотид
Уридиловый нуклеотид
Слайд 14Метаболизм нуклеотидов – (простетическая группа нуклеопротеидов)
Значение нуклеотидов:
Мономеры нуклеиновых кислот –
ДНК и РНК;
Нуклеотиды- трифосфаты – источники энергии;
АТФ- универсальный источник энергии; ЦТФ,ГТФ, УТФ- источники энергии в синтезах
3. Образуя активные формы сульфатов ( ФАФС), глюкуроновой кислоты (УДФ-глюкуроновая кислота), участвуют в процессах детоксикации;
4. Входят в состав коферментов дегидрогеназ (НАД, ФАД) и кофермента ацетилирования КоА;
5. Циклические формы (цАМФ,цГМФ)- вторичные посредники в проведении гормонального сигнала
Слайд 15Источники нуклеотидов
1. Биосинтез de novo (практически во всех тканях) !!!!
2.
Повторный синтез из готовых структурных компонентов нуклеотидов и нуклеиновых кислот
пищи и тканей (реутилизация азотистых оснований– « путь спасения»)
Слайд 16Превращение нуклеопротеидов пищи в ЖКТ
нуклеопротеиды
HCL
Пепсин - желудок
Трипсин - 12 перстная кишка
Нуклеиновые кислоты + белок аминокислоты
Нуклеазы -12-перстная кишка:
Рибо-, дезоксинуклеазы
Деполимеризация- разрыв фосфорноэфирных связей
нуклеотиды
Нуклеотидазы (фосфатазы)
Нуклеозиды- (могут всасываться)
Нуклеозидазы – (гликозидные связи)
Своб. азотистые основания + рибоза или дезоксирибоза (всасываются)
РР
Слайд 17Биосинтез нуклеотидов de novo !!!
Азотистые основания синтезируются из низкомолекулярных предшественников
Рибозы-
источник - пентозофосфатный путь;
Фосфорная кислота поступает с пищей
Слайд 18Биосинтез пиримидиновых нуклеотидов de novo
N
N
C
C
C
C
1
2
3
Субстраты синтеза:
Амид глутаминовой кислоты
СО2
Аспарагиновая
кислота
1 Этап –синтез пиримидинового основания (синтез оротовой кислоты):
А.Амид глутаминовой кис-ты
+ СО2 +АТФ карбомоилфосфат
Фермент- карбомоилфосфатсинтаза ( вит. Н)
Б.карбомоилфосфат + аспарагиновая кислота карбомоиласпартат
В. циклизация карбомоиласпартата оротовая кислота
Слайд 19Биосинтез пиримидиновых нуклеотидов
N
N
C=O
CH
C-COOH
O=C
Оротовая кислота -сформированное пиримидиновое кольцо
2
этап: присоединение оротовой кислоты к производному рибозы-5- фосфат – Фосфорибозилдифосфату:
А.
образование фосфорибозилпирофосфата (ФРПФ)
Рибоза-5-фосфат + АТФ фосфорибозилдифосфат
Фермент – фосфорибозилдифосфатсинтаза
Б. непосредственный перенос оротовой кислоты на фосфорибозилдифосфат с образованием нуклеотида -
Оротидин – 5- фосфат ( оротатфосфорибозилтрансфераза)
Слайд 20Биосинтез пиримидиновых нуклеотидов
Б. непосредственный перенос оротовой кислоты на фосфорибозилдифосфат с
образованием нуклеотида -
Оротидин – 5- фосфат ( оротатфосфорибозилтрансфераза
СН
С-СООН
О
ОН ОН
С-О-Р-О-Р
O
C
O
P
C-COOH
CH
+
В.
Декарбоксилирование оротовой кислоты в составе оротидин-5-фосфата ( фермент – декарбоксилаза) с образованием нуклеотида:
УМФ (уридинмонофосфат)
+ГЛУ-NH2
ЦМФ
СН3
Донор СН3 -тетрагидрофолиевая кислота (вит. ВС) Вит. В12
N
N
N
N
ТМФ
Слайд 21Нарушение синтеза пиримидиновых нуклеотидов
Оротацидурия ( генетически обусловленное)
Энзимдефекты- оротатфосфорибозилтрансфераза,
декарбоксилаза;
«Пиримидиновый голод»- мегалобластичес- кая анемия - нарушен синтез ДНК)
Дефицит витаминов:
ВС ; В12
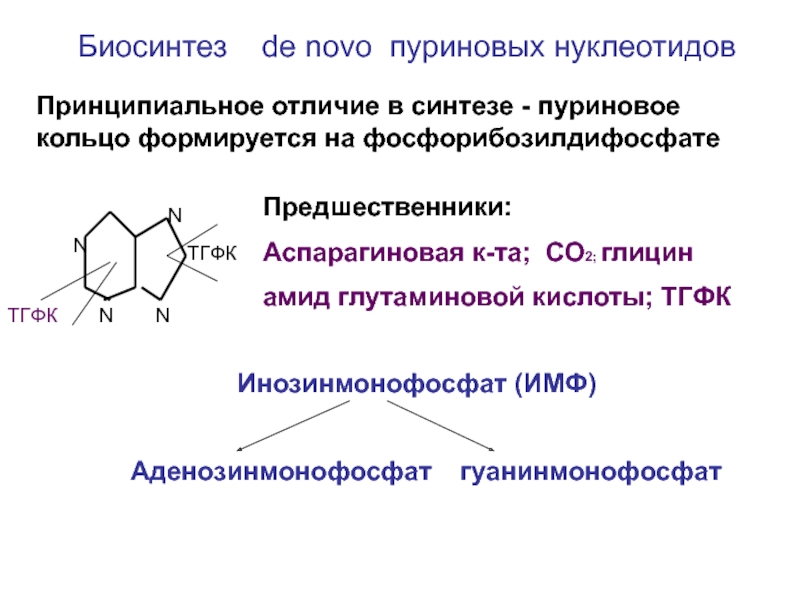
Слайд 22Биосинтез de novo пуриновых нуклеотидов
Принципиальное отличие в синтезе -
пуриновое кольцо формируется на фосфорибозилдифосфате
N
N
N
N
Предшественники:
Аспарагиновая к-та; СО2; глицин
амид глутаминовой кислоты;
ТГФК
Инозинмонофосфат (ИМФ)
Аденозинмонофосфат гуанинмонофосфат
ТГФК
ТГФК
Слайд 23Катаболизм пуриновых нуклеотидов
1 Этап: распад нуклеотида в тканях до азотистого
основания, рибозы(дезокси-),фосфорная кислота.
Ферменты : тканевые нуклеазы, нуклеотидазы;
нуклеозидазы.
2.Этап: катаболизм пуринового
основания:
Аденозин гипоксантин ксантин мочевая
кислота
Ферменты (последовательно):
Дезаминаза, ксантиноксидаза, ксантиноксидаза
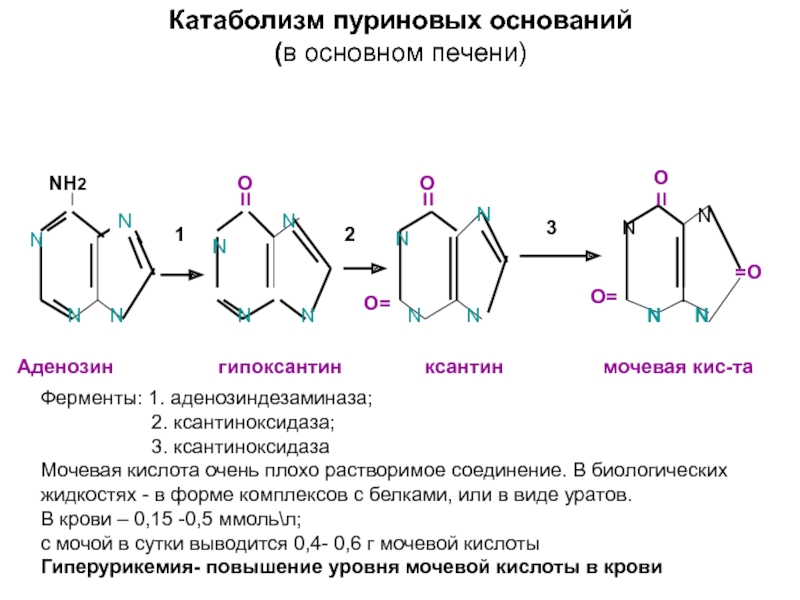
Слайд 24Катаболизм пуриновых оснований
(в основном печени)
N
NH2
N
O
N N
N
N
O
N
N
N
N
N
N
N
N N
N
O=
O
O=
=O
Аденозин
гипоксантин ксантин мочевая кис-та
1
2
3
Ферменты: 1. аденозиндезаминаза;
2. ксантиноксидаза;
3. ксантиноксидаза
Мочевая кислота очень плохо растворимое соединение. В биологических жидкостях - в форме комплексов с белками, или в виде уратов.
В крови – 0,15 -0,5 ммоль\л;
с мочой в сутки выводится 0,4- 0,6 г мочевой кислоты
Гиперурикемия- повышение уровня мочевой кислоты в крови