Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Метаболизм ядов
Содержание
- 1. Метаболизм ядов
- 2. Общая характеристика метаболизма ядов. Многие
- 3. В ходе первой фазы окислительно-восстановительного или гидролитического
- 4. Следствием химической модификации молекулы ксенобиотика могут стать:
- 5. Метаболизм многих ксенобиотиков сопровождается образованием продуктов существенно
- 6. В ряде случаев в ходе биотрансформации ксенобиотиков
- 7. Порой сам процесс метаболизма ксенобиотика является пусковым
- 8. Процесс образования токсичных продуктов метаболизма называется "токсификация",
- 9. Биоактивация далеко не всегда сопровождается повреждением биосубстрата,
- 10. Концепция l и ll фазы метаболизма ксенобиотиков
- 11. Рисунок 3. Метаболизм бензола
- 12. В ходе l фазы метаболизма обеспечивается превращение
- 13. 2. Локализация процессов биотрансформации Основным органом метаболизма
- 14. Продукты l фазы метаболизма поступают в общий
- 15. Энзимы, участвующие в метаболизме ксенобиотиков, локализованы в
- 16. Таблица 1. Энзиматические реакции метаболизма ксенобиотиков и локализация энзимов внутри гепатоцита (Первая фаза).
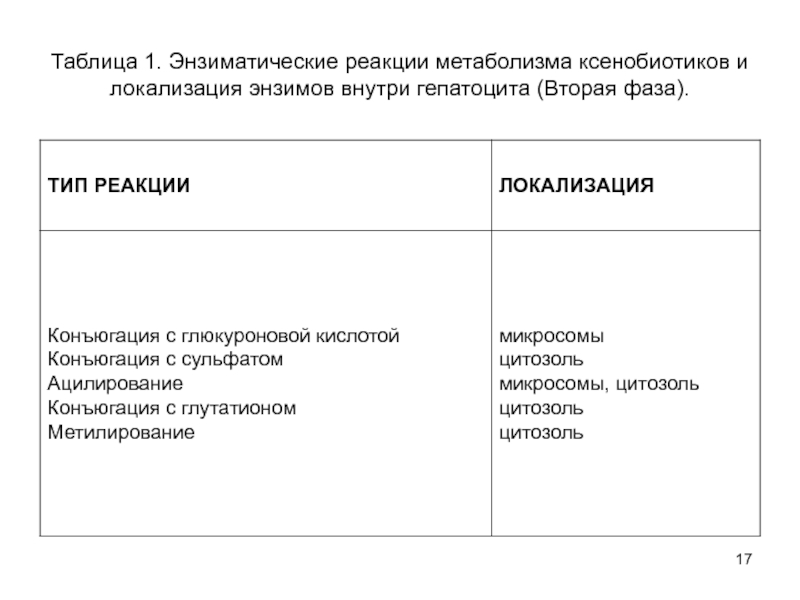
- 17. Таблица 1. Энзиматические реакции метаболизма ксенобиотиков и локализация энзимов внутри гепатоцита (Вторая фаза).
- 18. 1. Первая фаза метаболизма Энзимы l фазы,
- 19. Таблица 2. Примеры веществ, подвергающихся биотрансформации при участии энзимов l фазы
- 20. Особое значение для биотрансформации ксенобиотиков имеют микросомальные
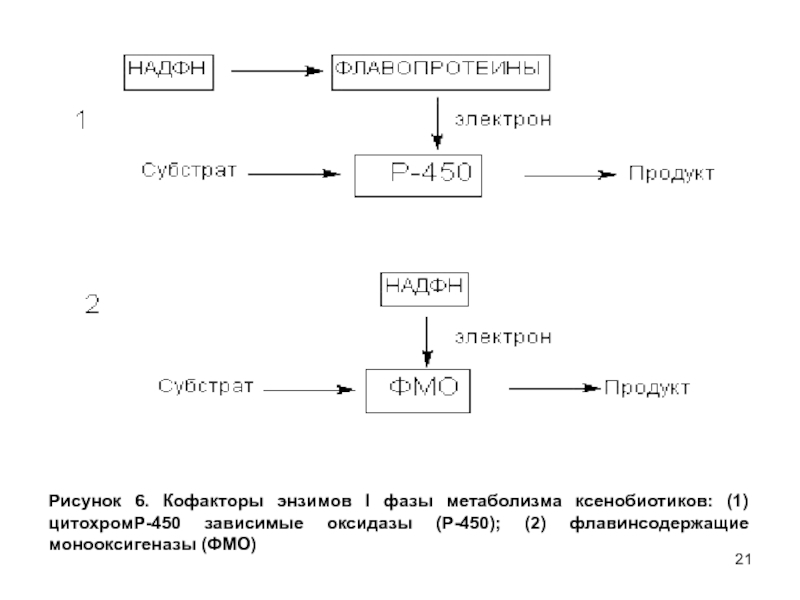
- 21. Рисунок 6. Кофакторы энзимов l фазы метаболизма
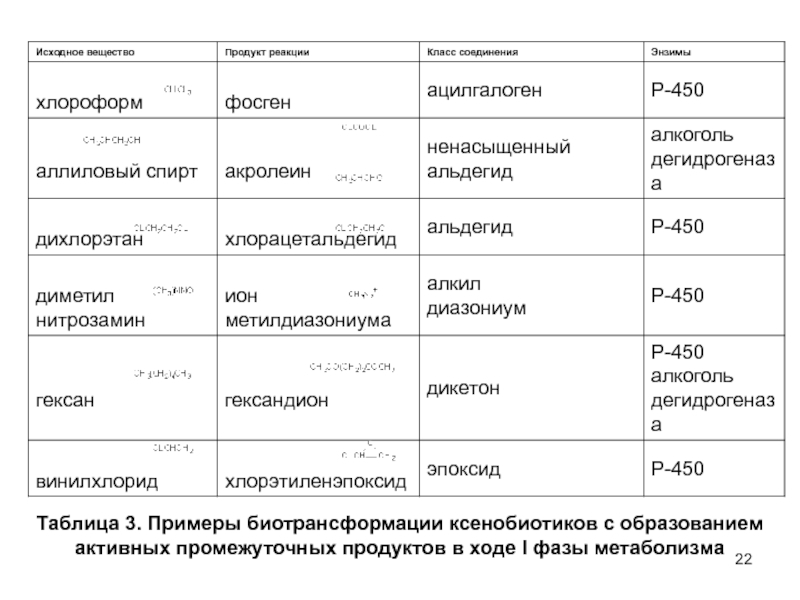
- 22. Таблица 3. Примеры биотрансформации ксенобиотиков с образованием активных промежуточных продуктов в ходе l фазы метаболизма
- 23. Окислительно-восстановительные превращения Оксидазы смешанной функции ЦитохромР-450-зависимая монооксигеназная
- 24. Р-450 представляют собой семейство энзимов, локализующихся в
- 25. Реакции микросомального окисления, протекающие при участии Р-450,
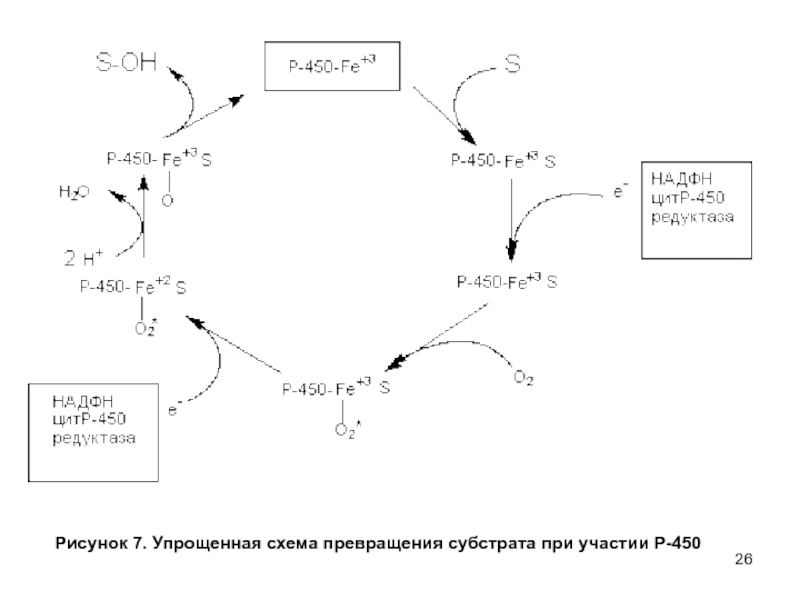
- 26. Рисунок 7. Упрощенная схема превращения субстрата при участии Р-450
- 27. Как видно из рисунка на начальном этапе
- 28. Классическим примером превращения данного типа является О-деалкилирование
- 29. Дегидрогеназы Помимо микросом, энзимы, участвующие в окислении
- 30. Среди веществ, метаболизируемых при участии рассматриваемых энзимов
- 31. Гидролитические превращения В тканях человека и животных,
- 32. 3. Вторая фаза метаболизма. Конъюгация Превращение
- 33. Рассматриваемую группу энзимов можно классифицировать следующим образом:
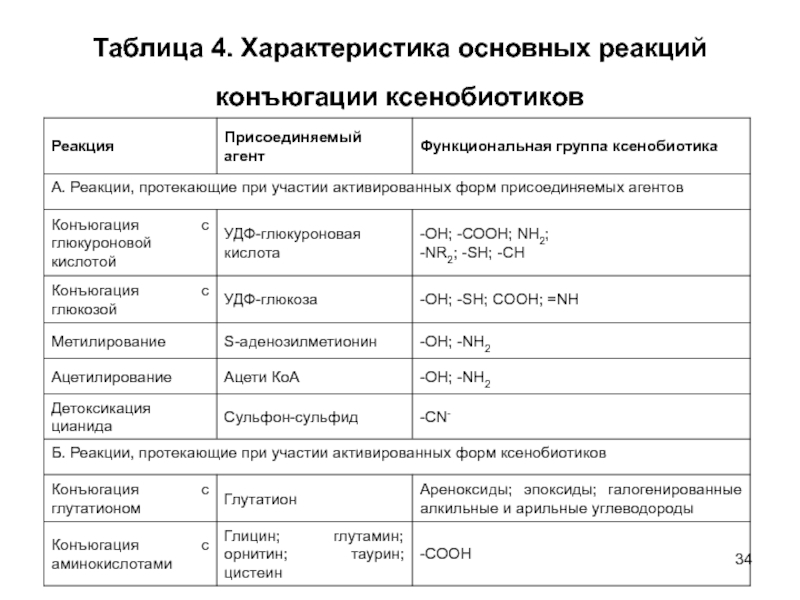
- 34. Таблица 4. Характеристика основных реакций конъюгации ксенобиотиков
- 35. Ацетилирование Аминогруппы ароматических соединений часто подвергаются ацетилированию.
- 36. Конъюгация с глюкуроновой кислотой Глюкуроновая кислота Она
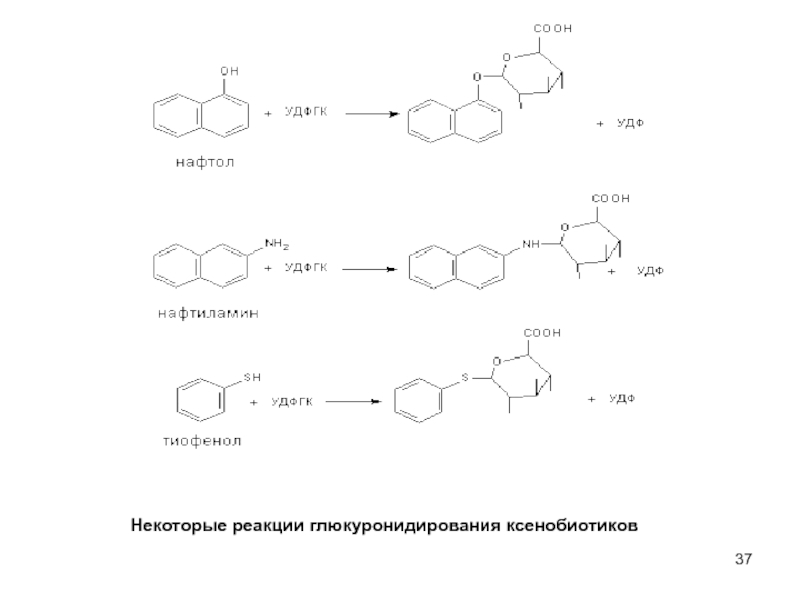
- 37. Некоторые реакции глюкуронидирования ксенобиотиков
- 38. Конъюгация с глутатионом и цистеином Органические вещества,
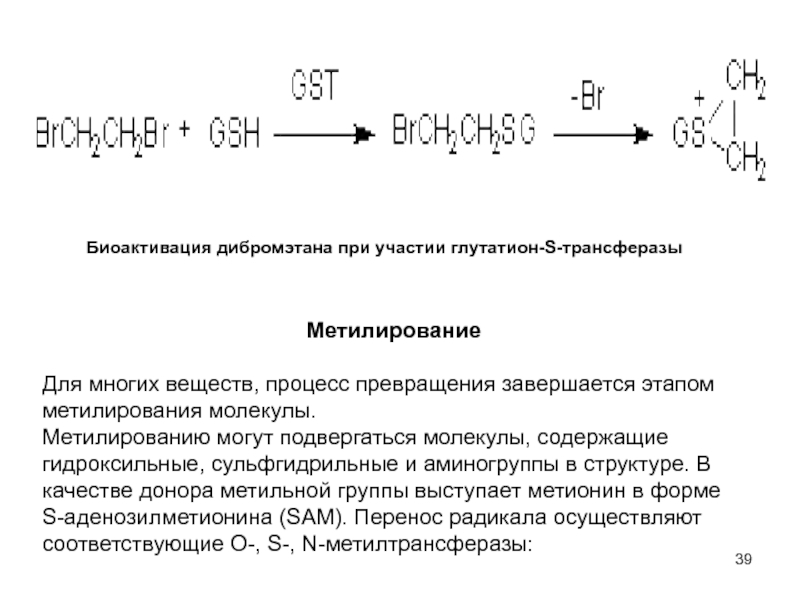
- 39. Биоактивация дибромэтана при участии глутатион-S-трансферазы Метилирование Для
- 40. Энзимы кишечной флоры При участии кишечной флоры
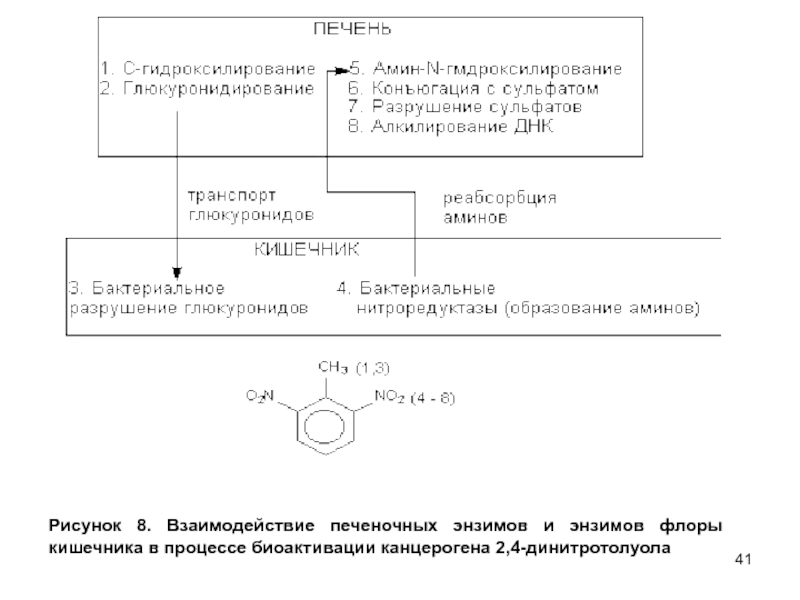
- 41. Рисунок 8. Взаимодействие печеночных энзимов и энзимов флоры кишечника в процессе биоактивации канцерогена 2,4-динитротолуола
- 42. 4. Факторы, влияющие на метаболизм ксенобиотиков Генетические
- 43. Пол и возраст В опытах на лабораторных
- 44. Влияние химических веществ Ксенобиотики, поступающие в организм,
- 45. Активные метаболиты и их роль в инициации
- 46. Модель N2. Орган мишень не в состоянии
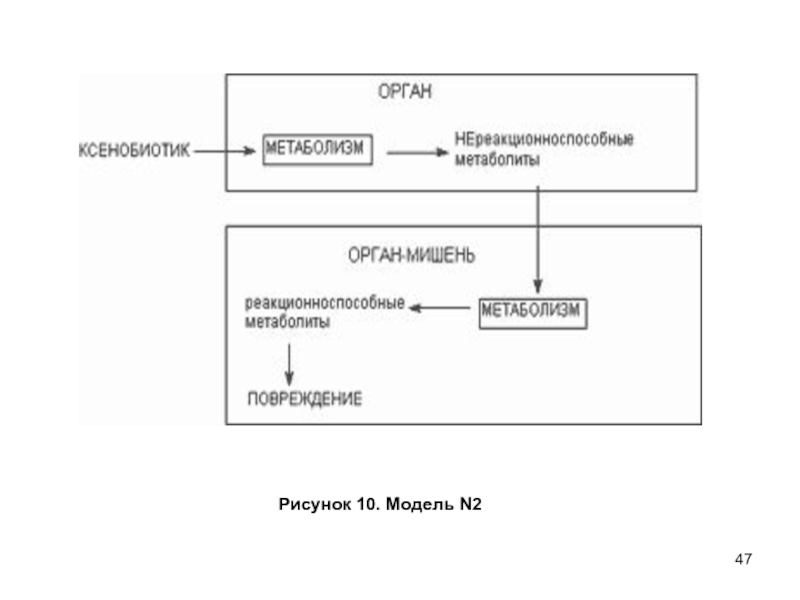
- 47. Рисунок 10. Модель N2
- 48. Модель N3. Орган-мишень может вообще не участвовать
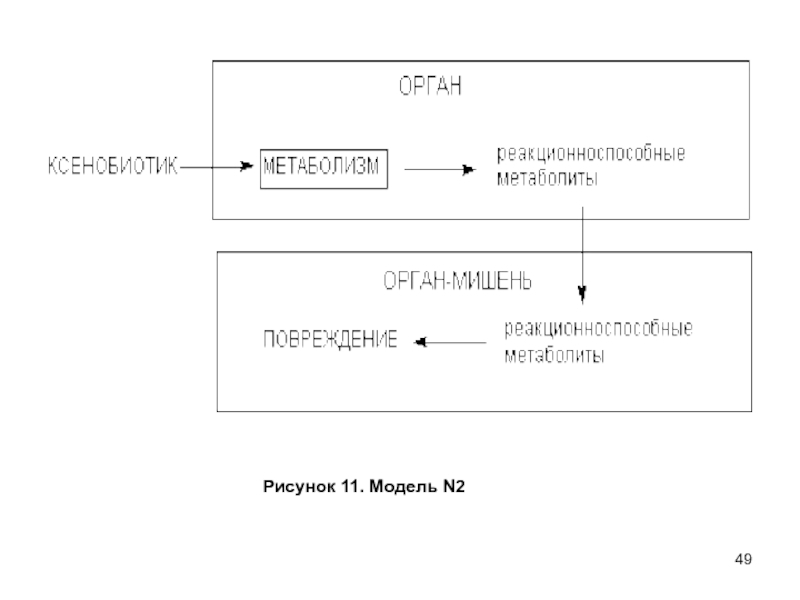
- 49. Рисунок 11. Модель N2
- 50. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Метаболизм ядов
Общая характеристика метаболизма ядов.
2. Первая фаза метаболизма ксенобиотиков.
3. Вторая
фаза метаболизма. Конъюгация.
Слайд 2Общая характеристика метаболизма ядов.
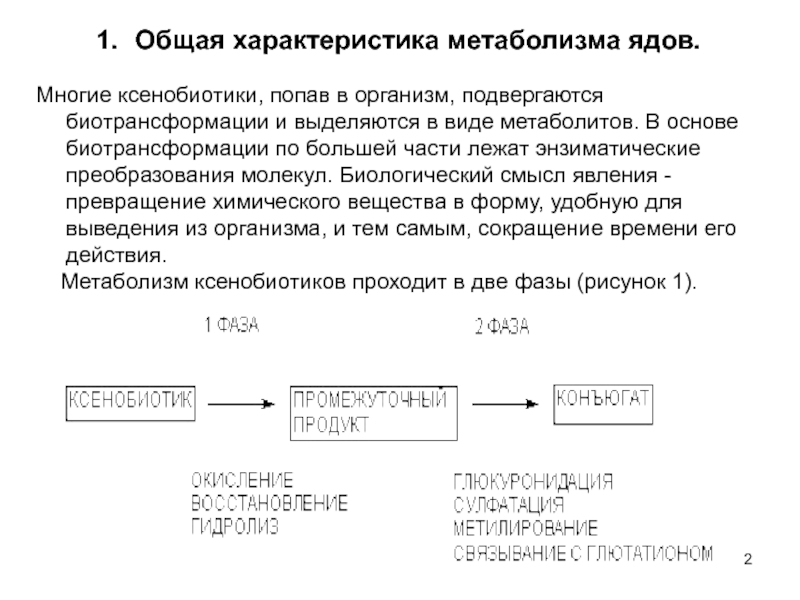
Многие ксенобиотики, попав в
организм, подвергаются биотрансформации и выделяются в виде метаболитов. В основе
биотрансформации по большей части лежат энзиматические преобразования молекул. Биологический смысл явления - превращение химического вещества в форму, удобную для выведения из организма, и тем самым, сокращение времени его действия.Метаболизм ксенобиотиков проходит в две фазы (рисунок 1).
Слайд 3В ходе первой фазы окислительно-восстановительного или гидролитического превращения молекула вещества
обогащается полярными функциональными группами, что делает ее реакционно-способной и более
растворимой в воде. Во второй фазе проходят синтетические процессы конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, в результате чего образуются полярные соединения, которые выводятся из организма с помощью специальных механизмов экскреции.Разнообразие каталитических свойств энзимов биотрансформации и их низкая субстратная специфичность позволяет организму метаболизировать вещества самого разного строения. Вместе с тем, у животных разных видов и человека метаболизм ксенобиотиков проходит далеко не одинаково, поскольку энзимы, участвующие в превращениях чужеродных веществ, часто видоспецифичны.
Слайд 4Следствием химической модификации молекулы ксенобиотика могут стать:
Ослабление токсичности;
2.
Усиление токсичности;
3. Изменение характера токсического действия;
4. Инициация токсического
процесса. Слайд 5Метаболизм многих ксенобиотиков сопровождается образованием продуктов существенно уступающих по токсичности
исходным веществам. Так, роданиды, образующиеся в процессе биопревращения цианидов, в
несколько сот раз менее токсичны, чем исходные ксенобиотики. Гидролитическое отщепление от молекул зарина, зомана, диизопропилфторфосфата иона фтора, приводит к утрате этими веществами способности угнетать активность ацетилхолинэстеразы и существенному понижению их токсичности. Процесс утраты токсикантом токсичности в результате биотрансформации обозначается как "метаболическая детоксикация".В процессе метаболизма других веществ образуются более токсичные соединения. Примером такого рода превращений является, в частности, образование в организме фторуксусной кислоты при интоксикации фторэтанолом.
Слайд 6В ряде случаев в ходе биотрансформации ксенобиотиков образуются вещества, способные
совершенно иначе действовать на организм, чем исходные агенты. Так, некоторые
спирты (этиленгликоль), действуя целой молекулой, вызывают седативно-гипнотический эффект (опьянение, наркоз). В ходе их биопревращения образуются соответствующие альдегиды и органические кислоты (щавелевая кислота), способные повреждать паренхиматозные органы и, в частности, почки.Многие низкомолекулярные вещества, являющиеся факультативными аллергенами, подвергаются в организме метаболическим превращениям с образованием реакционноспособных промежуточных продуктов. Так, соединения, содержащие в молекуле амино- или нитрогруппу в ходе метаболизма превращаются в гидроксиламины, активно взаимодействующие с протеинами крови и тканей, формируя полные антигены. При повторном поступлении таких веществ в организм помимо специфического действия развиваются аллергические реакции.
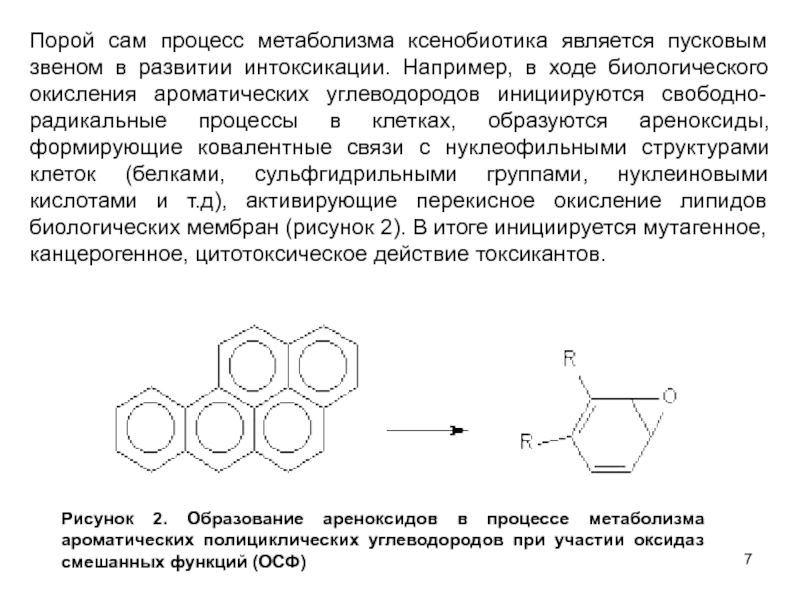
Слайд 7Порой сам процесс метаболизма ксенобиотика является пусковым звеном в развитии
интоксикации. Например, в ходе биологического окисления ароматических углеводородов инициируются свободно-радикальные
процессы в клетках, образуются ареноксиды, формирующие ковалентные связи с нуклеофильными структурами клеток (белками, сульфгидрильными группами, нуклеиновыми кислотами и т.д), активирующие перекисное окисление липидов биологических мембран (рисунок 2). В итоге инициируется мутагенное, канцерогенное, цитотоксическое действие токсикантов.Рисунок 2. Образование ареноксидов в процессе метаболизма ароматических полициклических углеводородов при участии оксидаз смешанных функций (ОСФ)
Слайд 8Процесс образования токсичных продуктов метаболизма называется "токсификация", а продукты биотрансформации,
обладающие высокой токсичностью - токсичными метаболитами. Во многих случаях токсичный
метаболит является не стабильным продуктом, подвергающимся дальнейшим превращениям. В этом случае он также называется промежуточным или реактивным метаболитом. Реактивные метаболиты это как раз те вещества, которые часто и вызывают повреждение биосистем на молекулярном уровне. Общим свойством практически всех реактивных метаболитов является их электродефицитное состояние, т.е. высокая электрофильность. Эти вещества вступают во взаимодействие с богатыми электронами (нуклеофильными) молекулами, повреждая их. К числу последних относятся макромолекулы клеток, в структуру которых входят в большом количестве атомы кислорода, азота, серы. Это, прежде всего, белки и нуклеиновые кислоты. Реактивные метаболиты либо присоединяются к нуклеофильным молекулам, образуя с ними ковалентные связи, либо вызывают их окисление. В обоих случаях структура макромолекул нарушается, следовательно, нарушаются и их функции.Слайд 9Биоактивация далеко не всегда сопровождается повреждением биосубстрата, поскольку одновременно в
организме протекают процессы детоксикации и репарации. Интенсивность этих процессов может
быть достаточной для компенсации ущерба, связанного с образованием реактивных метаболитов. Тем не менее при введении высоких доз токсиканта, повторном воздействии защитные механизмы могут оказаться несостоятельными, что и приведет к развитию токсического процесса.Слайд 10Концепция l и ll фазы метаболизма ксенобиотиков
Фаза I метаболизма
в широком смысле может быть определена, как этап биотрансформации, в
ходе которого к молекуле соединения либо присоединяются полярные функциональные группы, либо осуществляется экспрессия таких групп, находящихся в субстрате в скрытой форме. Это достигается либо путем окисления или (значительно реже) восстановления молекул с помощью оксидо-редуктаз, либо путем их гидролиза эстеразами и амидазами.Фаза ll - этап биологической конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, такими как глутатион, глюкуроновая кислота, сульфат и т.д. Специфические системы транспорта конъюгированных дериватов обеспечивают их выведение из организма.
В ходе биопревращений липофильный и, следовательно, трудновыводимый ксенобиотик становиться гидрофильным продуктом, что обусловливает возможность его быстрой экскреции.
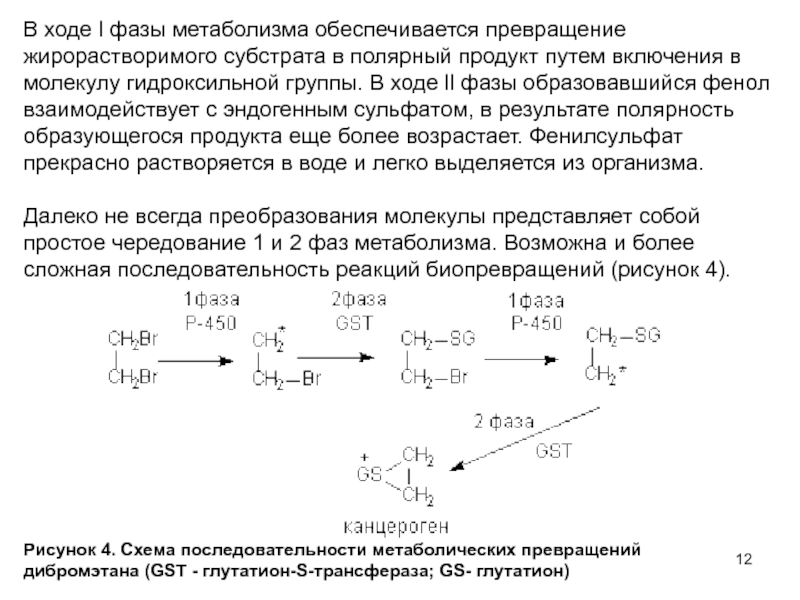
Слайд 12В ходе l фазы метаболизма обеспечивается превращение жирорастворимого субстрата в
полярный продукт путем включения в молекулу гидроксильной группы. В ходе
ll фазы образовавшийся фенол взаимодействует с эндогенным сульфатом, в результате полярность образующегося продукта еще более возрастает. Фенилсульфат прекрасно растворяется в воде и легко выделяется из организма.Далеко не всегда преобразования молекулы представляет собой простое чередование 1 и 2 фаз метаболизма. Возможна и более сложная последовательность реакций биопревращений (рисунок 4).
Рисунок 4. Схема последовательности метаболических превращений
дибромэтана (GST - глутатион-S-трансфераза; GS- глутатион)
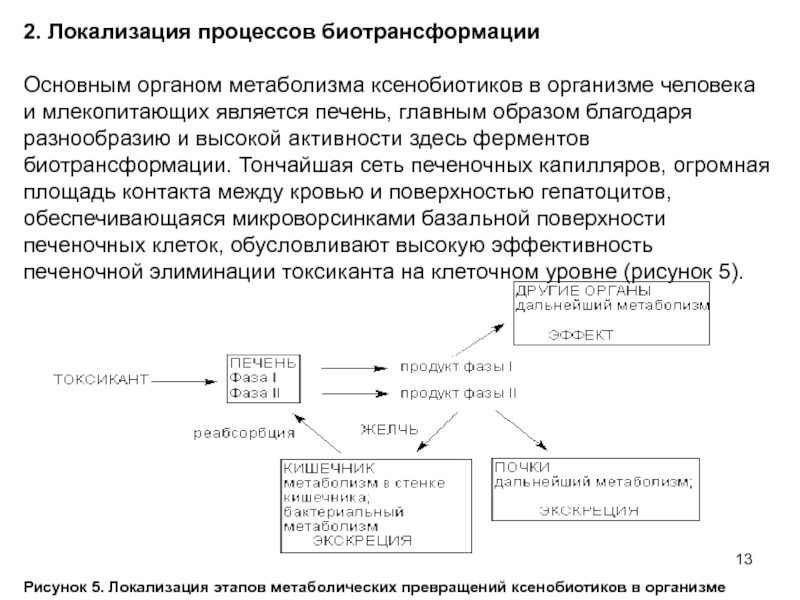
Слайд 132. Локализация процессов биотрансформации
Основным органом метаболизма ксенобиотиков в организме
человека и млекопитающих является печень, главным образом благодаря разнообразию и
высокой активности здесь ферментов биотрансформации. Тончайшая сеть печеночных капилляров, огромная площадь контакта между кровью и поверхностью гепатоцитов, обеспечивающаяся микроворсинками базальной поверхности печеночных клеток, обусловливают высокую эффективность печеночной элиминации токсиканта на клеточном уровне (рисунок 5).Рисунок 5. Локализация этапов метаболических превращений ксенобиотиков в организме
Слайд 14Продукты l фазы метаболизма поступают в общий кровоток и могут
оказывать действие на органы и системы. Печень выбрасывает в кровь
и продукты ll фазы метаболизма. Из крови продукты превращения могут захватываться почками, легкими, другими органами, повторно печенью для экскреции с желчью. С желчью метаболиты поступают в кишечник, где частично реабсорбируются и повторно поступать в печень (цикл печеночной рециркуляции).Несмотря на доминирующую роль печени в метаболизме ксенобиотиков, другие органы также принимают участие в этом процессе. Почки и легкие содержат энзимы и l и ll фаз метаболизма. Особенно велика роль почек, поскольку в этом органе имеется специфическая система захвата и катаболизма продуктов конъюгации, образующихся в печени. Активность других органов, таких как кишечник, селезенка, мышечная ткань, плацента, мозг, кровь - значительно ниже, однако наличие энзимов, катализирующих процессы биотрансформации, при отравлении токсифицирующимися ксенобиотиками, имеет ключевое значение в развитии патологических процессов в этих органах. В процессе внепеченочного метаболизма могут образовываться продукты, как аналогичные продуктам печеночного происхождения, так и отличные от них.
Слайд 15Энзимы, участвующие в метаболизме ксенобиотиков, локализованы в основном внутриклеточно. Небольшое
их количество определяется в растворимой фракции циотозоля, митохондриях, большинство же
связаны с гладким эндоплазматическим ретикулумом (таблица 1). Методом ультрацентрфугирования гладкий эндоплазматический ретикулум выделяется из исследуемых клеток в виде фрагментов мембранных структур, называемых микросомами. Поэтому основная группа ферментов, участвующих в метаболизме ксенобиотиков, получила название "микросомальные энзимы".Слайд 16Таблица 1. Энзиматические реакции метаболизма ксенобиотиков и локализация энзимов внутри
гепатоцита (Первая фаза).
Слайд 17Таблица 1. Энзиматические реакции метаболизма ксенобиотиков и локализация энзимов внутри
гепатоцита (Вторая фаза).
Слайд 181. Первая фаза метаболизма
Энзимы l фазы, участвующие в процессе
биотрансформации ксенобиотиков, можно классифицировать в соответствии с типом активируемой ими
реакции:Оксидазы смешанной функции: цитохромР-450 (Р-450) и флавинсодержащие монооксигеназы (ФМО);
2. Простогландинсинтетазы - гидропероксидазы (ПГС) и другие пероксидазы;
3. Алкогольдегидрогеназы и альдегиддегидрогеназы;
4. Флавопротеинредуктазы;
5. Эпоксидгидролазы;
6. Эстеразы и амидазы.
Слайд 20Особое значение для биотрансформации ксенобиотиков имеют микросомальные энзимы. Как уже
указывалось, морфологическим эквивалентом микросом в интактных клетках является гладкий эндоплазматический
ретикулум. Ферменты микросом не принимают участие в окислении большинства эндогенных соединений, таких как аминокислоты, нуклеотиды, сахара и т.д., для которых существуют специфические пути превращения.Однако в метаболизме некоторых эндогенных соединений (например, стероидов) микросомальные оксидазы принимают участие наряду со специфическими ферментными комплексами. Под влиянием этих энзимов могут метаболизировать некоторые жирные кислоты, простогландины и т.д. Кофакторы микросомальных монооксигеназ, принимающих участие в метаболических превращения ксенобиотиков, представлены на рисунке 6.
Слайд 21Рисунок 6. Кофакторы энзимов l фазы метаболизма ксенобиотиков: (1) цитохромР-450
зависимые оксидазы (Р-450); (2) флавинсодержащие монооксигеназы (ФМО)
Слайд 22Таблица 3. Примеры биотрансформации ксенобиотиков с образованием активных промежуточных продуктов
в ходе l фазы метаболизма
Слайд 23Окислительно-восстановительные превращения
Оксидазы смешанной функции
ЦитохромР-450-зависимая монооксигеназная система
Энзимы
рассматриваемой группы, цитохромР-450 зависимые оксидазы (Р-450), как правило, обладают низкой
субстратной специфичностью, вызывая превращения веществ самого разного строения, и потому часто называются оксидазами смешенной функции (ОСФ). Р-450 относятся к группе гемопротеинов типа цитохромов b - пигментов, активно связывающих монооксид углерода. Название "цитохромР-450" энзимы получили в силу того, что максимум поглощения света пигментом, связанным с СО, осуществляется при длине волны 450 нм.Слайд 24Р-450 представляют собой семейство энзимов, локализующихся в эндоплазматическом ретикулуме, которые
могут быть разделены с помощью иммунологических и иных методов на
несколько подсемейств. Отдельные ткани содержат несколько различных изоформ Р-450. Встречаются тканеспецифичные формы энзимов. Изоферменты Р-450 часто проявляют перекрестную субстратную специфичность, таким образом, как правило, более чем один изофермент принимает участие в метаболизме ксенобиотика. Наличие специфических форм энзимов обусловлено генетическими механизмами, а повышение содержания в тканях различных изоферментов индуцируется действием на организм различных ксенобиотиков: лекарств, ядов, экотоксикантов. Р-450 подвержены не только активации, но и инактивации, как исходными ксенобиотиками, так и их реактивными метаболитами.Слайд 25Реакции микросомального окисления, протекающие при участии Р-450, как правило, зависят
от содержания O2 и НАДФН в среде. Молекулярный кислород активируется
цитохромомР-450 (или другими цитохормами, например, Р-448). Активация осуществляется с помощью НАДФН при участии флавин-содержащего энзима НАДФН-цитохромР-450 редуктазы. Поскольку донором электронов в превращениях субстратов, катализируемых этими энзимами, является НАДФН, суммарное уравнение реакции может быть записано следующим образом:ЦитохромР-450, НАДФН-цитохромР-450 редуктаза и фосфолипиды биологических мембран, в которые встроены оба энзима, образуют микросомальный монооксигеназный комплекс. Несмотря на то, что энзимы комплекса связаны с биологическими мембранами
Слайд 27Как видно из рисунка на начальном этапе ксенобиотик (S) вступает
во взаимодействие с окисленной формой цитохромаР-450. Затем к этому комплексу
с помощью НАДФН-зависимой цитохромР-450 редуктазы присоединяется электрон, донором которого является восстановленный НАДФН. После этого комплекс взаимодействует с кислородом. После взаимодействия со вторым электроном (донор - НАДФН) происходит активация связанного с цитохромом кислорода, который приобретает способность связывать протоны и образовывать воду. Образовавшаяся при этом форма цитохромаР-450 гидроксилирует субстрат.Метаболизируемое вещество не связывается непосредственно с геминовой группой цитохромаР-450. Оно присоединяется к белковой части цитохрома. Процесс превращения ксенобиотиков чувствителен к СО, поскольку это вещество вытесняет кислород из связи с железом геминовой группы цитохромаР-450. Некоторые оксидазы резистентны к СО (образование N-оксидов).
Поскольку Р-450 - гемопротеины, их активность отчасти регулируется процессами синтеза гема, т.е. связана с метаболизмом железа. Нарушение метаболизма, голодание, понижение соотношения НАДФН/НАДФ+ могут приводить к снижению активности Р-450.
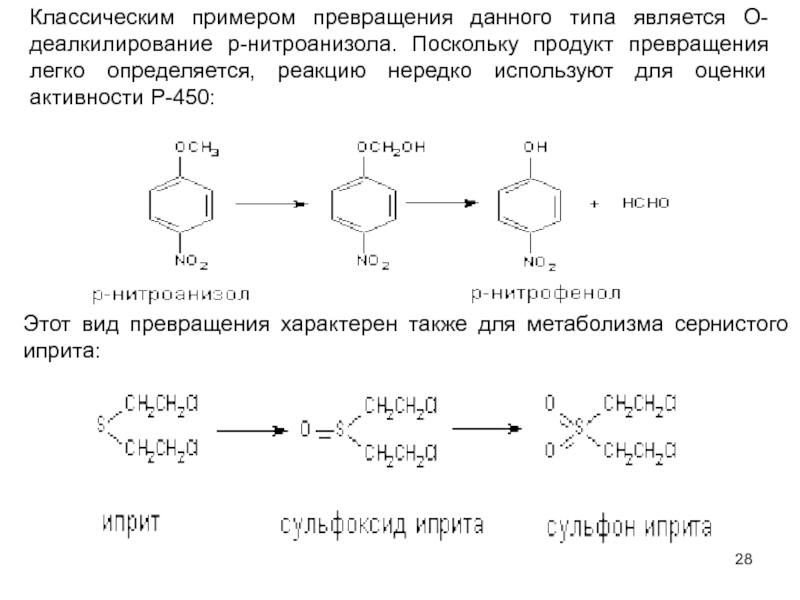
Слайд 28Классическим примером превращения данного типа является О-деалкилирование р-нитроанизола. Поскольку продукт
превращения легко определяется, реакцию нередко используют для оценки активности Р-450:
Этот вид превращения характерен также для метаболизма сернистого иприта:
Слайд 29Дегидрогеназы
Помимо микросом, энзимы, участвующие в окислении ксенобиотиков, выявляются также
в митохондриях и растворимой фазе цитозоля. Процесс дегидрирования ксенобиотиков проходит
в организме чаще в форме гидроксилирования. Среди прочих веществ такому превращению подвергаются многочисленные спирты и альдегиды при участии алкоголь- и альдегиддегидрогеназ. Благодаря высокой активности этих энзимов, печень - основной орган метаболизма спиртов. Энзимы идентифицированы также в почках и легких.НАД-зависимая алкогольдегидрогеназа печени обладает невысокой субстратной специфичностью. Так, под влиянием этого энзима метаболизируют не только первичные и вторичные алифатические спирты, но и ароматические спирты, а также такие соединения, как р-нитробензиловый спирт и т.д. В результате окисления образуются соответствующие альдегиды:
Слайд 30Среди веществ, метаболизируемых при участии рассматриваемых энзимов наибольшее токсикологическое значение
имеют метанол, этиленгликоль, аллиловый спирт. В процессе метаболизма этих веществ
образуются высоко токсичные промежуточные (формальдегид, гликолиевый альдегид) и конечные (муравьиная кислота, оксалат) продукты.Процесс дегидрирования лежит в основе превращений целого ряда ароматических соединений. Так, в ходе метаболизма бензойной кислоты образуется гиппуровая кислота. Участвующие в превращении энзимы локализуются в митохондриях.
Слайд 31Гидролитические превращения
В тканях человека и животных, а также в
жидкостях организма, например крови, содержатся энзимы, обладающие эстеразной активностью. Их
низкая специфичность обеспечивает гидролиз эфиров различного строения. Так, в плазме крови содержатся эстеразы, разрушающие эфиры холина, прокаина, производных прокаина и др. Среди наиболее изученных: карбоксилэстераза и арилэстераза. Эфиры фосфорной кислоты в крови и тканях также расщепляются эстеразами. Гидролиз эфиров изменяет биологическую активность веществ.В 1955 году Мюнтер с сотрудниками (Mounter et al.) обнаружили в разных тканях и крови млекопитающих энзим (флюорогидролаза), активирующий отщепление от атома фосфора высокотоксичных фосфорорганических соединений (ДФФ, зарин, зоман и т.д.) атом фтора. Токсичность веществ, в процессе такого превращения, резко снижается.
Слайд 32 3. Вторая фаза метаболизма. Конъюгация
Превращение молекул в первой
фазе биотрансформации усиливает их полярность, уменьшает способность растворяться в липидах.
Уже только благодаря этому целый ряд чужеродных соединений лучше выделяется с мочой. Эффект еще более усиливается, когда к образовавшимся в ходе 1 фазы метаболизма продуктам присоединяются такие эндогенные вещества, как ацетат, сульфат, глюкуроновая кислота, глутатион и т.д. Как и энзимы l фазы метаболизма ксенобиотиков, энзимы ll фазы обладают слабой субстратной специфичностью и участвуют в превращениях большой группы химических веществ.Слайд 33Рассматриваемую группу энзимов можно классифицировать следующим образом:
Энзимы, формирующие эфирные
или амидные связи с промежуточными метаболитами:
- ацетил КоА: амин
N-ацетилтрансфераза; - сульфотрансфераза;
УДФ-глюкуронозилтрансфераза.
2. Энзимы, активирующие конъюгацию веществ с глутатионом:
глутатион S-трансферазы.
3. Энзимы, активирующие конъюгацию веществ с цистеином:
- цистеин-конъюгирующие β-лиазы.
Слайд 35Ацетилирование
Аминогруппы ароматических соединений часто подвергаются ацетилированию. Уксусная кислота переносится
на аминогруппу в форме ацетил-КоА с помощью соответствующих трансфераз, в
частности - ацетил-КоА:амин-N-ацетилтрансферазы.Ацетилированию могут подвергаться сульфамидные группы, алифатические амины, группы гидразина. У людей выражены генетически обусловленные различия в способности к реакции N-ацетилирования. Замедленное ацетилирование отмечается у гомозиготных по рецессивному аллелю индивидов. Высокая активность ацетилирования отмечается у гетерозиготных индивидов или людей, гомозиготных по доминантному аллелю.
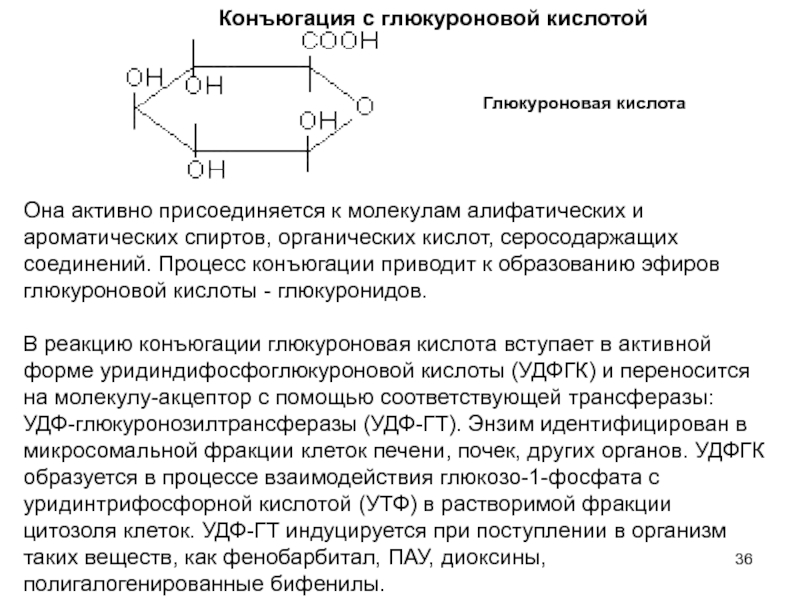
Слайд 36Конъюгация с глюкуроновой кислотой
Глюкуроновая кислота
Она активно присоединяется к
молекулам алифатических и ароматических спиртов, органических кислот, серосодаржащих соединений. Процесс
конъюгации приводит к образованию эфиров глюкуроновой кислоты - глюкуронидов.В реакцию конъюгации глюкуроновая кислота вступает в активной форме уридиндифосфоглюкуроновой кислоты (УДФГК) и переносится на молекулу-акцептор с помощью соответствующей трансферазы: УДФ-глюкуронозилтрансферазы (УДФ-ГТ). Энзим идентифицирован в микросомальной фракции клеток печени, почек, других органов. УДФГК образуется в процессе взаимодействия глюкозо-1-фосфата с уридинтрифосфорной кислотой (УТФ) в растворимой фракции цитозоля клеток. УДФ-ГТ индуцируется при поступлении в организм таких веществ, как фенобарбитал, ПАУ, диоксины, полигалогенированные бифенилы.
Слайд 38Конъюгация с глутатионом и цистеином
Органические вещества, содержащие в молекуле
лабильные атомы водорода, галогенов и др., в организме могут взаимодействовать
с SH-содержащими эндогенными соединениями: цистеином, ацетилцистеином, глутатионом и т.д.Реакции конъюгации восстановленного глутатиона с электрофильными субстратами катализируют энзимы глутатион-S-трансферазы (GST). Хотя GST обнаружены практически во всех тканях организма млекопитающих, уровень энзимов в печени - максимален. В этом органе GST составляет до 10% общего количества цитозольных протеинов. GST - большое семейство энзимов, в котором набор изоформ часто специфичен для отдельных тканей. Их активность индуцируется при поступлении в организм различных ксенобиотиков. В подавляющем большинстве случаев взаимодействие ксенобиотиков с глутатионом приводит к их детоксикации. Однако известны примеры биоактивации. Так, конъюгация глутатиона с 1,2-дигалогеналканами (дихлорэтан, дибромэтан) приводит к образованию продукта: S-(2-галогеналкан), который в дальнейшем превращается в активный циклический эписульфониум-ион (см. след. слайд)
Слайд 39Биоактивация дибромэтана при участии глутатион-S-трансферазы
Метилирование
Для многих веществ, процесс
превращения завершается этапом метилирования молекулы.
Метилированию могут подвергаться молекулы, содержащие
гидроксильные, сульфгидрильные и аминогруппы в структуре. В качестве донора метильной группы выступает метионин в форме S-аденозилметионина (SАМ). Перенос радикала осуществляют соответствующие O-, S-, N-метилтрансферазы: Слайд 40Энзимы кишечной флоры
При участии кишечной флоры также возможен метаболизм
химических соединений. Действие бактериальных энзимов сопровождается расщеплением продуктов ll фазы
метаболизма, поступающих в кишечник с желчью, и образованием исходных метаболитов. Этот процесс проходит при участии гидролаз, разрушающих глюкурониды и сульфаты. Реабсорбция образовавшихся веществ замыкает цикл внутрипеченочной рециркуляции ксенобиотиков. Кроме того, анаэробная среда кишечника обеспечивает возможность восстановления некоторых химических веществ бактериями. Например, восстановление нитроароматических соединений сопровождается образованием аминов, которые, поступая в печень, вновь подвергается метаболизму. Бактериальная β-глюкуронидаза и нитроредуктаза играют исключительно важную роль в процессе многоэтапной биоактивации 2,6-динитротолуолаСлайд 41Рисунок 8. Взаимодействие печеночных энзимов и энзимов флоры кишечника в
процессе биоактивации канцерогена 2,4-динитротолуола
Слайд 424. Факторы, влияющие на метаболизм ксенобиотиков
Генетические факторы
Особи одного
и того же вида живых существ порой значительно различаются по
способности метаболизировать ксенобиотики. Это во многом детерминировано генетически. Так, в популяции людей выявляются лица, обладающие пониженной активностью цитохромР-450 зависимых оксидаз. "Слабые метаболизанты" могут отличаться отсутствием некоторых изоэнзимов, необходимых для катализа ряда превращений ксенобиотиков.Полиморфизм метаболизма ксенобиотиков отмечен для процессов ацетилирования ароматических веществ, содержащих амино-, сульфо-, амидную группу. Лица со слабым напряжением процессов ацетилирования более подвержены некоторым аллергическим реакциям, вызываемым химическими веществами. С другой стороны, излишне напряженный процесс ацетилирования ксенобиотиков может иметь пагубные последствия в результате биоактивации арилгидразинов.
Слайд 43Пол и возраст
В опытах на лабораторных животных, в основном
грызунах, показано, что половые гормоны принимают участие в регуляции активности
энзимов метаболизма ксенобиотиков и прежде всего монооксигеназ. Так, взрослые самцы крыс быстрее метаболизируют такие вещества, как гексабарбитал, аминопирин, аминофенол и т.д. Вместе с тем анилин и его аналоги подвергаются биопревращению в организме самцов и самок с одинаковой скоростью. Кастрация нередко сопровождается снижением скорость метаболизма ксенобиотиков. У человека половые различия выражены не столь существенно.Отличия метаболизма ксенобиотиков, обусловленные возрастом, наиболее отчетливо проявляются у новорожденных и лиц пожилого возраста. Хорошо известно, что недостаточно развитая система метаболизма ксенобиотиков у новорожденных делает их особенно чувствительными к ряду токсикантов. Токсический процесс может стать следствием как накапливающихся в организме исходных продуктов, так и промежуточных метаболитов, не подвергающихся дальнейшей биотрансформации.
В старческом возрасте наблюдается снижение клиаренса ксенобиотиков отчасти обусловленное понижением интенсивности метаболизма. Нарушение метаболизма ксенобиотиков печенью в старческом возрасте может являться следствием уменьшения интенсивности печеночного кровотока, хронических патологических процессов в печени, связанного с возрастом снижения активности ферментов.
Слайд 44Влияние химических веществ
Ксенобиотики, поступающие в организм, могут оказывать влияние
на процессы метаболизма как самих этих веществ, так и других
соединений, поступающих в организм одновременно или вслед за ними. Теоретически можно выделить три группы химических соединений, по-разному влияющих на метаболизм чужеродных веществ:Практически не влияющие на активность энзимов метаболизма;
2. Повышающие активность энзимов - индукторы;
3. Угнетающие активность энзимов - ингибиторы.
Важно иметь в виду, что одно и то же вещество может выступать и как индуктор и как ингибитор метаболизма другого вещества, в зависимости от того в каком порядке ксенобиотики поступают в.
Слайд 45Активные метаболиты и их роль в инициации токсического процесса
Модель
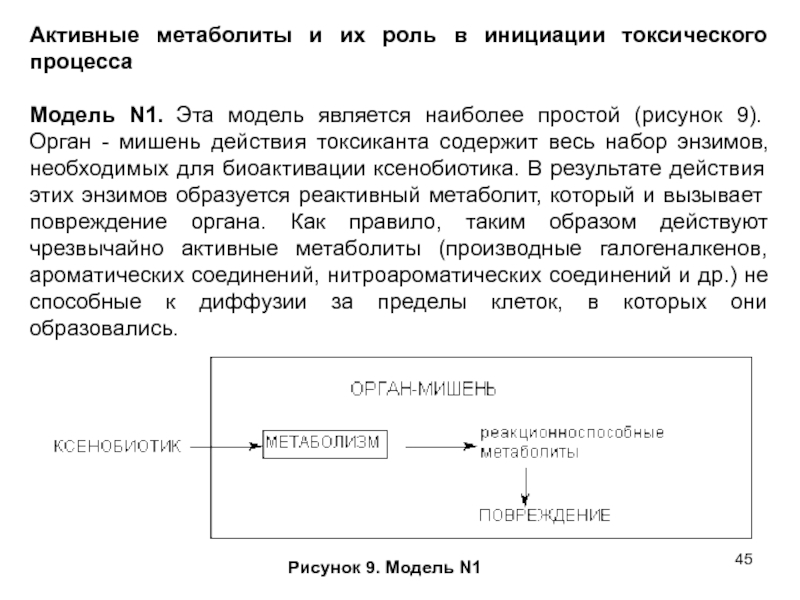
N1. Эта модель является наиболее простой (рисунок 9). Орган -
мишень действия токсиканта содержит весь набор энзимов, необходимых для биоактивации ксенобиотика. В результате действия этих энзимов образуется реактивный метаболит, который и вызывает повреждение органа. Как правило, таким образом действуют чрезвычайно активные метаболиты (производные галогеналкенов, ароматических соединений, нитроароматических соединений и др.) не способные к диффузии за пределы клеток, в которых они образовались.Рисунок 9. Модель N1
Слайд 46Модель N2. Орган мишень не в состоянии биотрансформировать исходный токсикант
в реакционноспособный метаболит, но может участвовать в биоактивации промежуточных продуктов,
образовавшихся в других органах (рисунок 10). Эта модель применима к веществам, первично метаболизируемым в печени (производные бензола, фенола, нитроароматических соединений).Однако обязательным этапом их метаболизма является превращение в других органах, например кишечнике и т.д. Орган-мишень содержит энзимы, отсутствующие в печени, например, энзимы катаболизма конъюгатов глутатиона (почки), пероксидазы (почки, лейкоциты, костный мозг), некоторые подтипы цитохромР-450. Первичные метаболиты - химически инертные вещества, вторичные - обладают высокой реакционной способностью, достаточной для того, что бы вызывать повреждение органа в котором они образуются.
Слайд 48Модель N3. Орган-мишень может вообще не участвовать в процессе биоактивации
токсиканта, но обладает при этом высокой чувствительностью к образующемуся в
других органах метаболиту (рисунок 11). Эта модель приложима к химическим соединениям, вызывающим повреждение органов и тканей либо вообще не участвующих, либо участвующих в минимальной степени, в биоактивации ксенобиотиков (многоатомные спирты, алканы, ароматические амины и др).Органами-мишенями могут быть и периферические нервные стволы, практически не содержащими энзимов метаболизма ксенобиотиков, и легкие, отличающиеся достаточно высокой метаболической активностью, и др. Общим между ними является то, что они не в состоянии метаболизировать конкретное химическое вещество, вызывающее их повреждение. Основой для развития токсического процесса являются: поступление большого количества метаболита с притекающей кровью, активный захват метаболитов, недостаточность механизмов детоксикации, высокая чувствительность клеток органа к метаболиту, недостаточность механизмов репарации повреждений. Установление такого механизма действия токсикантов требует проведения глубоких исследований.