Слайд 1МЕТОДЫ ВОССТАНОВЛЕНИЯ И ОКИСЛЕНИЯ
неразрывно связанные процессы. Если одно из двух
веществ восстанавливается, то другое окисляется.
Отнесение реакций к процессам окисления
или— к процессам восстановления определяется тем, какое вещество является в данном случае субстратом.
Восстановлением называют процесс, в результате которого атом или группа атомов приобретают электроны. Наоборот, окисление заключается в потере электронов. Речь идет об изменении плотности электронного облака, которое окружает рассматриваемую группировку атомов субстрата. При восстановлении оно увеличивается, а при окислении уменьшается.
Слайд 2Степень окисления
— это тот условный заряд атома, который возникает на
нем при условии, что электронные пары связей полностью сместятся к
более электроотрицательному атому, образующему эту связь, а электроны связи между одинаковыми атомами будут поделены пополам.
В ходе реакций окисления степень окисления атомов субстрата увеличивается. Например, при получении бензойной кислоты из толуола, степень окисления атома углерода метильной группы увеличивается от (–3) до (+3) при этом изменяется и состав молекулы:
Легкость окисления субстрата возрастает вместе с ростом его электронной плотности и нуклеофильности (N, S, O, двойные и тройные связи).
Окислители: простые вещества, оксиды элементов, пероксиды, кислородсодержащие кислоты и их соли, некоторые органические соединения (нитросоединения).
Слайд 3МЕТОДЫ ВОССТАНОВЛЕНИЯ И ОКИСЛЕНИЯ
Выбор восстановителя или окислителя определяется
целевым продуктом,
видом
сырья,
экономическими факторами,
технологичностью процесса, вопросами техники безопасности и др. критериями.
Следует отметить, что наиболее дешевым и доступным окислителем является кислород воздуха, который в настоящее время широко используется в каталитических процессах окисления.
Многочисленные методы восстановления и окисления можно разделить на четыре группы:
химические,
каталитические,
электролитические
биохимические (микробиологические).
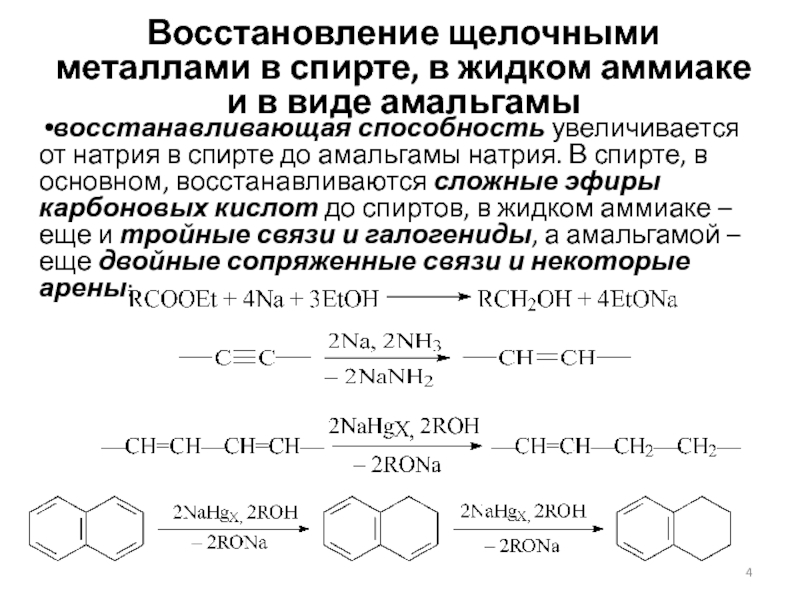
Слайд 4Восстановление щелочными металлами в спирте, в жидком аммиаке и в
виде амальгамы
восстанавливающая способность увеличивается от натрия в спирте до амальгамы
натрия. В спирте, в основном, восстанавливаются сложные эфиры карбоновых кислот до спиртов, в жидком аммиаке – еще и тройные связи и галогениды, а амальгамой – еще двойные сопряженные связи и некоторые арены:
Слайд 5Механизм восстановления натрием
во всех случаях одинаков: атомы натрия отдают
электроны, источником протонов является спирт, аммиак и вода;
Потери обусловлены непосредственной
реакцией между натрием и спиртом, аммиаком, водой (в случае амальгамы). Выделяющийся водород неактивен, а образующиеся алкоголяты вызывают образование побочных продуктов.
Слайд 6Технология восстановления щелочными металлами в спирте, в жидком аммиаке и
в виде амальгамы
Методики восстановления простые, но опасные, (к кипящему раствору
сложного эфира в спирте загружают натрий, после завершения реакции реакционную массу выливают в воду) поэтому их применяют, когда нет возможности применить другие методы.
Отвод тепла (через обратный теплообменник) при реакции в спирте является сложной технической проблемой, т.к. тепловой эффект реакции очень высок (до 520 кДж/моль), поэтому используют более высококипящие спирты, чем этанол.
Для ведения процесса в аммиаке необходима специальная аппаратура, т.к. температура кипения аммиака очень низкая (–33,5 °С). Зато натрий хорошо растворяется в аммиаке.
Амальгаму натрия получают растворением натрия в ртути, что вызывает дополнительные трудности.
Слайд 7Восстановление оловом, хлоридом олова (II) и железом в кислой среде,
цинком в кислой и щелочной средах и амальгамой цинка
простые и
давно известные способы восстановления нитро-, нитрозо-, гидроксиамино-, азо- и диазо- групп. Они широко применяются как в лабораторной практике, так и в промышленности (кроме олова).
Механизм восстановления нитрогрупп металлами аналогичен механизму восстановления карбонильных соединений, но восстанавливающая активность перечисленных металлов ниже щелочных и в передаче электронов участвует атом водорода.
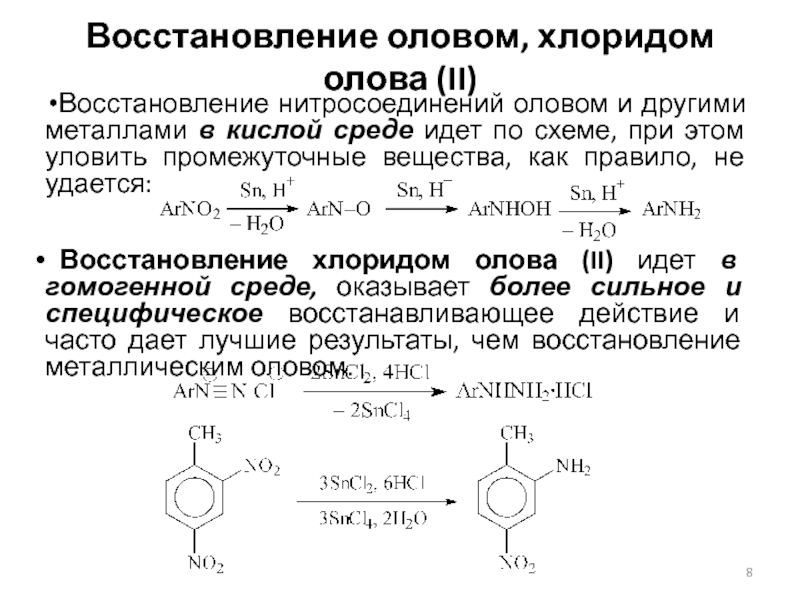
Слайд 8Восстановление оловом, хлоридом олова (II)
Восстановление нитросоединений оловом и другими металлами
в кислой среде идет по схеме, при этом уловить промежуточные
вещества, как правило, не удается:
Восстановление хлоридом олова (II) идет в гомогенной среде, оказывает более сильное и специфическое восстанавливающее действие и часто дает лучшие результаты, чем восстановление металлическим оловом.
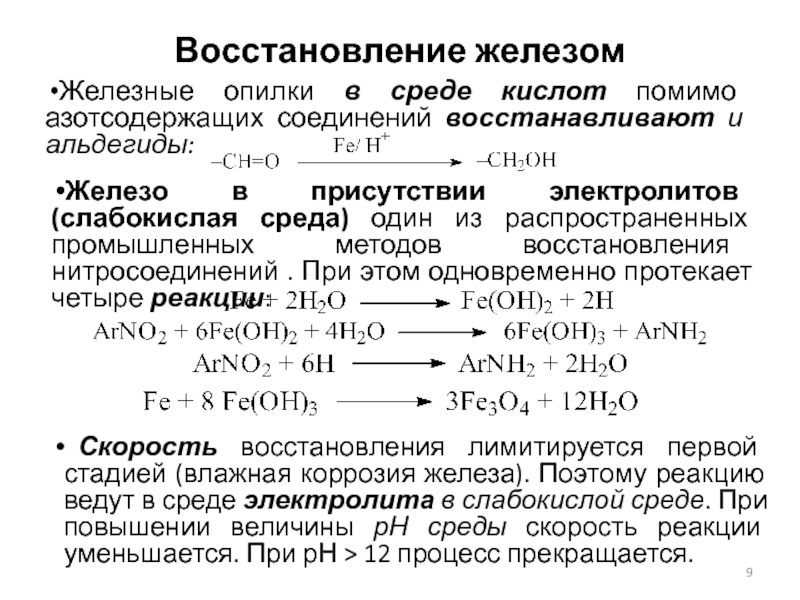
Слайд 9Восстановление железом
Железные опилки в среде кислот помимо азотсодержащих соединений восстанавливают
и альдегиды:
Железо в присутствии электролитов (слабокислая среда) один из распространенных
промышленных методов восстановления нитросоединений . При этом одновременно протекает четыре реакции:
Скорость восстановления лимитируется первой стадией (влажная коррозия железа). Поэтому реакцию ведут в среде электролита в слабокислой среде. При повышении величины рН среды скорость реакции уменьшается. При рН > 12 процесс прекращается.
Слайд 10Технология восстановления железом в электролитах
Электролиты (хлорид аммония, железа (II), и
др.) можно получать в самом реакторе при протравливании чугунной стружки
соляной кислотой.
Лучше использовать стружку серого чугуна, активность которого объясняется возникновением гальванической пары на границе раздела железо–графит. Это приводит к распаду его на мелкие частицы и к ускорению реакции.
Подготовка восстановителя: измельчение, просев, удаления пыли, обезжиривание и протравливание.
Процесс восстановления ведут при температуре кипения реакционной массы. Обогрев чаще всего производят острым паром.
К кипящей суспензии чугунной стружки в растворе электролита загружают нитропродукт. Амин отгоняются с водяным паром, отделяют или экстрагируют из реакционной массы органическими растворителями.
Слайд 11Технология восстановления железом в электролитах
В производстве восстановление проводят в стальных
или чугунных аппаратах (редукторах), футерованных диабазовой плиткой на кислотоупорной замазке
и снабженных мешалкой (лопастной или сошниковой) и барботером для подачи острого пара.
Метод - простотой, технологичный, дешевый, высокий выход. Недостаток метода - фильтрация, транспортировка тяжелого и содержащего абразивные частицы осадка.
Этот метод используют при производстве анестезина, новокаина и ряда других препаратов:
Слайд 12Восстановление цинком
более сильное восстанавливающее действие, чем у Fe
в кислой среде
цинком помимо азотсодержащих групп восстанавливают:
а) карбонильные соединения до спиртов.
б)
аренсульфохлориды до тиофенолов
в) двойную связь в α,β-ненасыщенных карбонильных соединениях до насыщенных карбонильных соединений
Цинк в щелочной среде помимо азотсодержащих групп восстанавливает:
а)карбонильные соединения до спиртов;
б) галогениды до углеводородов.
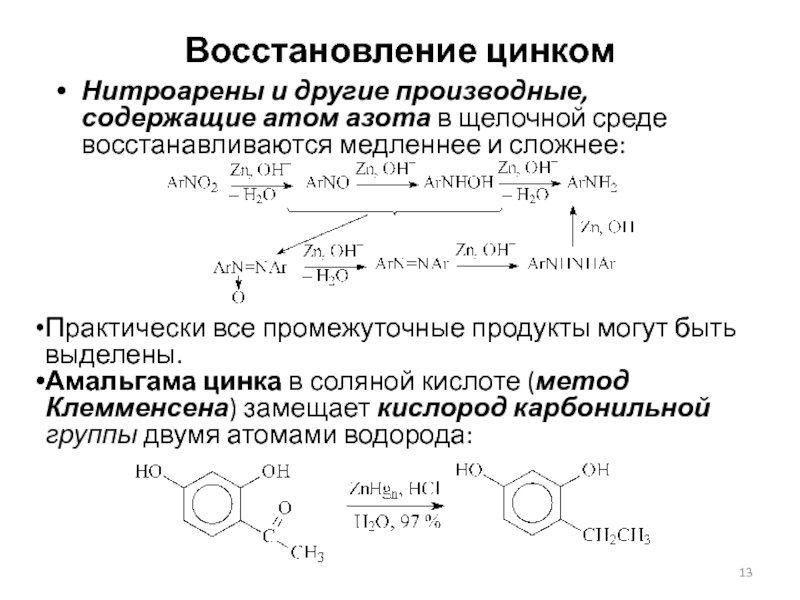
Слайд 13Восстановление цинком
Нитроарены и другие производные, содержащие атом азота в щелочной
среде восстанавливаются медленнее и сложнее:
Практически все промежуточные продукты могут быть
выделены.
Амальгама цинка в соляной кислоте (метод Клемменсена) замещает кислород карбонильной группы двумя атомами водорода:
Слайд 14Восстановление алкоголятами алюминия
Методом Меервейна-Понндорфа-Верлея) восстанавливают карбонильные соединения в спирты,
не затрагивая другие функциональные группы.
Алюминий в молекуле алкоголята образует
комплекс с карбонильной группой, повышает ее электрофильную активность и вызывает сдвиг электронов в исходящих от него связях. Вследствие этого α-водородный атом алкоголята с электронной парой переносится к электронодефицитному карбонильному атому углерода:
Слайд 15Восстановление гидридами металлов
сильные восстановители (LiAlH4 и NaBH4), используются для восстановления
полярных двойных связей углерод–гетероатом, в очень мягких условиях и с
высоким выходом по механизму нуклеофильного присоединения:
сильные восстановители (LiAlH4 и NaBH4), используются для восстановления полярных двойных связей углерод–гетероатом, в очень мягких условиях и с высоким выходом по механизму нуклеофильного присоединения:
Алюмогидрид лития восстанавливает :
не восстанавливает двойные связи углерод–углерод.
Работа с алюмогидридом лития требует особых мер предосторожности. Важно избегать контакта алюмогидрида лития с водой.
Слайд 16Восстановление гидридами металлов
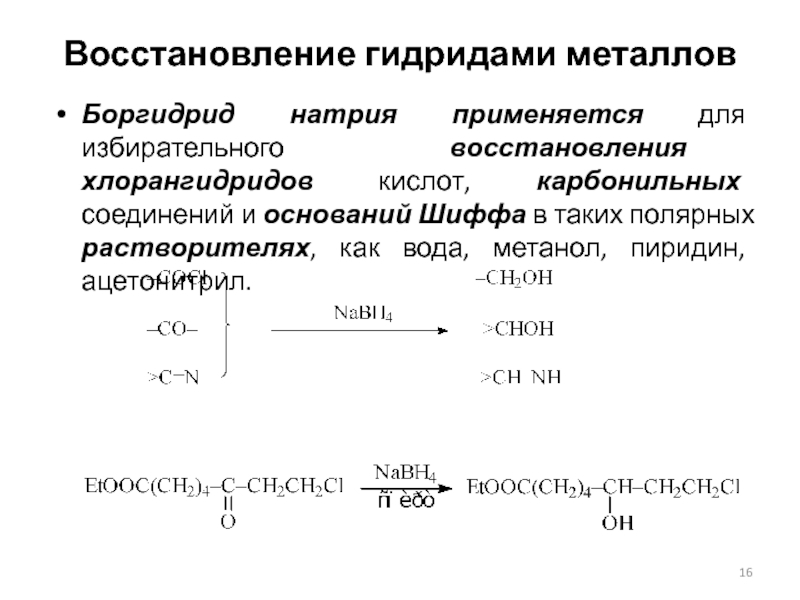
Боргидрид натрия применяется для избирательного восстановления хлорангидридов кислот,
карбонильных соединений и оснований Шиффа в таких полярных растворителях, как
вода, метанол, пиридин, ацетонитрил.
Слайд 17Каталитическое восстановление водородом
Достоинства: универсальность, высокая скорость процесса, чистота получаемых продуктов
и простота их выделения.
Недостатки: дефицитность применяемого электролитического водорода и
катализаторов, большая пожаро- и взрывоопасность процесса и необходимость во многих случаях использования автоклавов.
Скорость восстановления водородом на поверхности катализатора (контактно-каталитического восстановления) зависит от структуры субстрата, пространственных факторов, от его сорбционной активности. Легкость гидрирования отдельных групп, как правило, уменьшается в следующей последовательности:
Слайд 18Катализаторы
В химико-фармацевтической промышленности широко применяют скелетный катализатор никель Ренея при
нагревании в автоклавах, реже платиновые и палладиевые катализаторы, которые, обладая
всеми достоинствами никелевых, значительно активнее их.
Водородом в их присутствии восстанавливают почти все органические соединения, способные к восстановлению, причем часто при атмосферном давлении. Однако платиновые и палладиевые катализаторы дорогие и, из-за большой активности, обычные катализаторы обладают малой селективностью.
Для изменения активности катализаторов и увеличения их селективности используют различные добавки (промоторы и ингибиторы)
Слайд 19Электролитическое восстановление
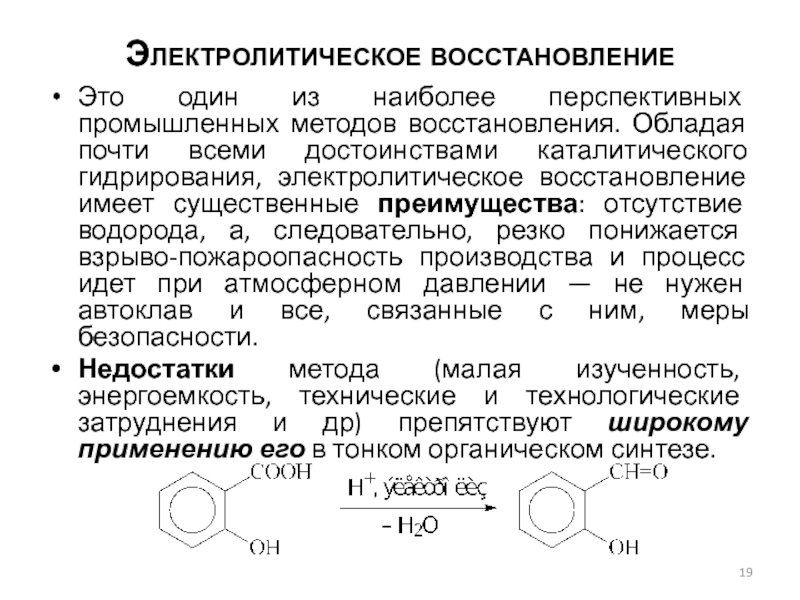
Это один из наиболее перспективных промышленных методов восстановления. Обладая
почти всеми достоинствами каталитического гидрирования, электролитическое восстановление имеет существенные преимущества:
отсутствие водорода, а, следовательно, резко понижается взрыво-пожароопасность производства и процесс идет при атмосферном давлении — не нужен автоклав и все, связанные с ним, меры безопасности.
Недостатки метода (малая изученность, энергоемкость, технические и технологические затруднения и др) препятствуют широкому применению его в тонком органическом синтезе.
Слайд 20Окислительные методы получения органических соединений
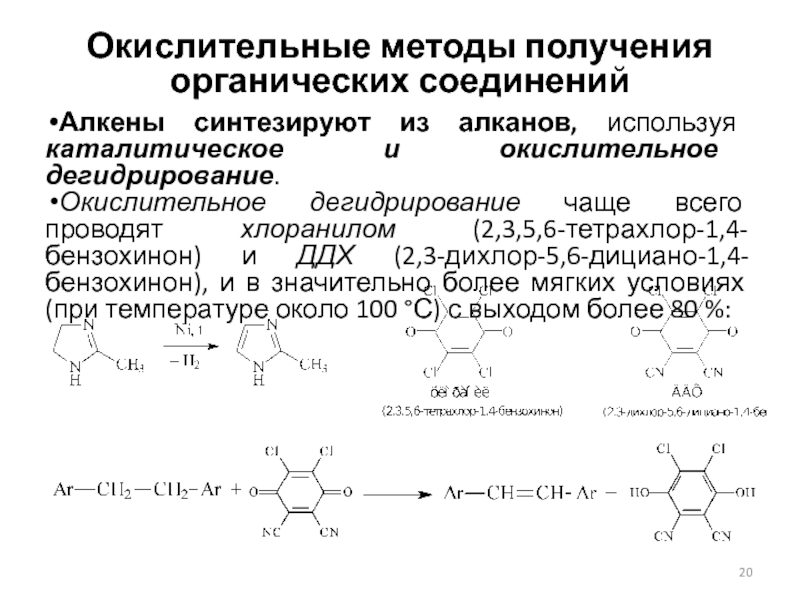
Алкены синтезируют из алканов, используя каталитическое
и окислительное дегидрирование.
Окислительное дегидрирование чаще всего проводят хлоранилом (2,3,5,6-тетрахлор-1,4-бензохинон)
и ДДХ (2,3-дихлор-5,6-дициано-1,4-бензохинон), и в значительно более мягких условиях (при температуре около 100 °С) с выходом более 80 %:
Слайд 21Получение карбонильных соединений
Альдегиды, как правило, окисляются легче, чем субстрат, полимеризуются
и конденсируются, поэтому их лучше всего получать дегидрированием спиртов в
присутствии катализаторов на основе меди. Процесс идет с хорошим выходом, но при более 200 °С.
Кетоны трудно окисляются, что сильно упрощает их синтез окислительными методами из вторичных спиртов бихроматом или оксидом хрома (VI) в кислой среде, и другие методы.
Слайд 22Окисление соединений в альдегиды
Применение высокоселективных окислителей (оксид селена (IV), комплексы
оксида хрома (VI) и ДМСО, периодат натрия, уротропин и др)
Применение кислорода и высокоселективных катализаторов
Слайд 23Окисление соединений в альдегиды
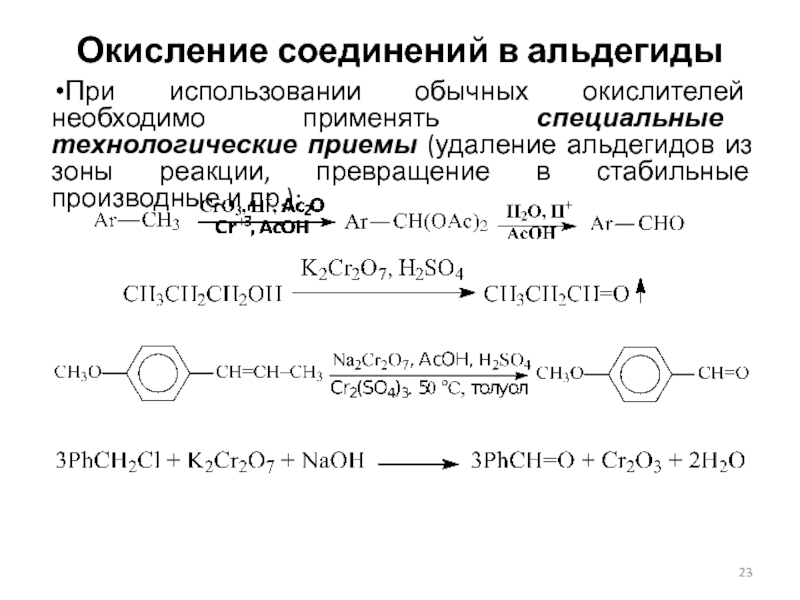
При использовании обычных окислителей необходимо применять специальные
технологические приемы (удаление альдегидов из зоны реакции, превращение в стабильные
производные и др.):
Слайд 24Окисление алканов и активированные группы в карбоновые кислоты
Алканы окисляют кислородом
на катализаторе.
Активированные алкильные группы (связанные с карбонильной группой, ароматическим кольцом
и другими акцепторными группами) - сильными окислителями , как правило, по α-углеродному атому: разбавленной азотной кислотой, бихроматом и хромовым ангидридом в кислой среде, перманганатом калия и др. Используется каталитическое окисление и окислительное амминирование в присутствии катализатора.
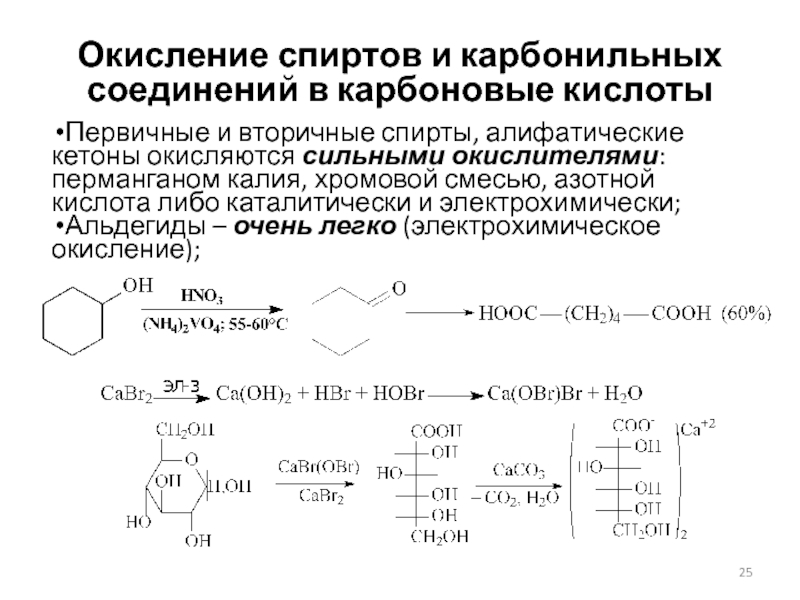
Слайд 25Окисление спиртов и карбонильных соединений в карбоновые кислоты
Первичные и вторичные
спирты, алифатические кетоны окисляются сильными окислителями: перманганом калия, хромовой смесью,
азотной кислота либо каталитически и электрохимически;
Альдегиды – очень легко (электрохимическое окисление);
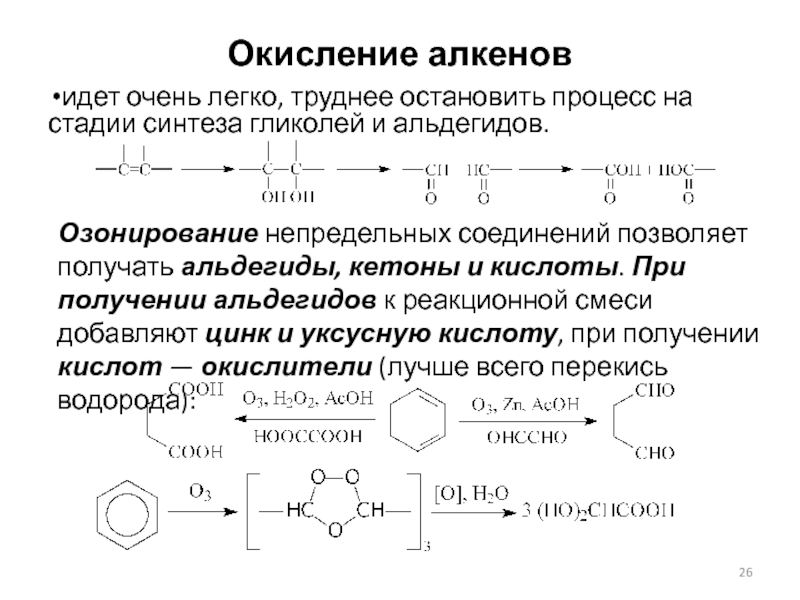
Слайд 26Окисление алкенов
идет очень легко, труднее остановить процесс на стадии
синтеза гликолей и альдегидов.
Озонирование непредельных соединений позволяет получать альдегиды, кетоны
и кислоты. При получении альдегидов к реакционной смеси добавляют цинк и уксусную кислоту, при получении кислот — окислители (лучше всего перекись водорода):
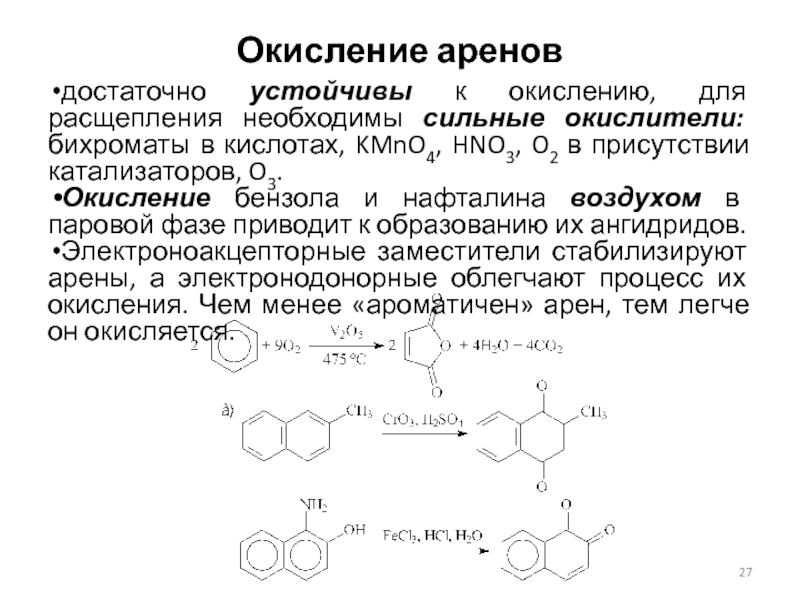
Слайд 27Окисление аренов
достаточно устойчивы к окислению, для расщепления необходимы сильные окислители:
бихроматы в кислотах, KMnO4, HNO3, O2 в присутствии катализаторов, O3.
Окисление бензола и нафталина воздухом в паровой фазе приводит к образованию их ангидридов.
Электроноакцепторные заместители стабилизируют арены, а электронодонорные облегчают процесс их окисления. Чем менее «ароматичен» арен, тем легче он окисляется.