Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Межмолекулярное вза имодействие
Содержание
- 1. Межмолекулярное вза имодействие
- 2. Слабее, чем химическая связьИон–дипольДиполь–дипольДиполь–непо-лярная молекула2 неполярных молекулыИон–неполяр-ная молекулаВодородная связь
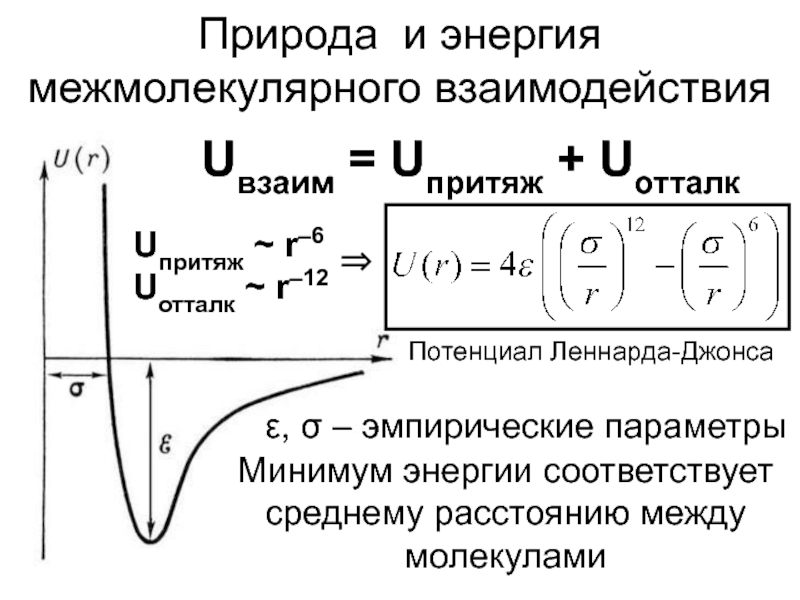
- 3. Природа и энергия межмолекулярного взаимодействияUвзаим = Uпритяж
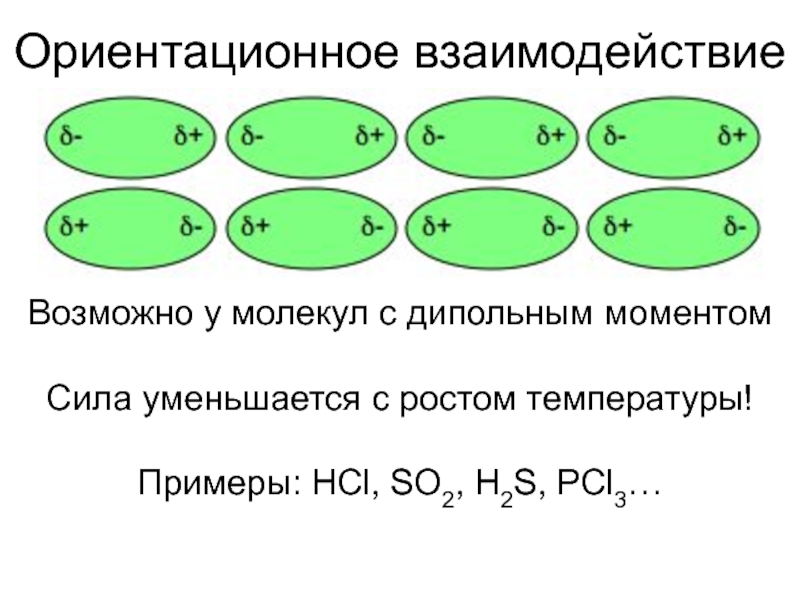
- 4. Ориентационное взаимодействиеВозможно у молекул с дипольным моментомСила уменьшается с ростом температуры!Примеры: HCl, SO2, H2S, PCl3…
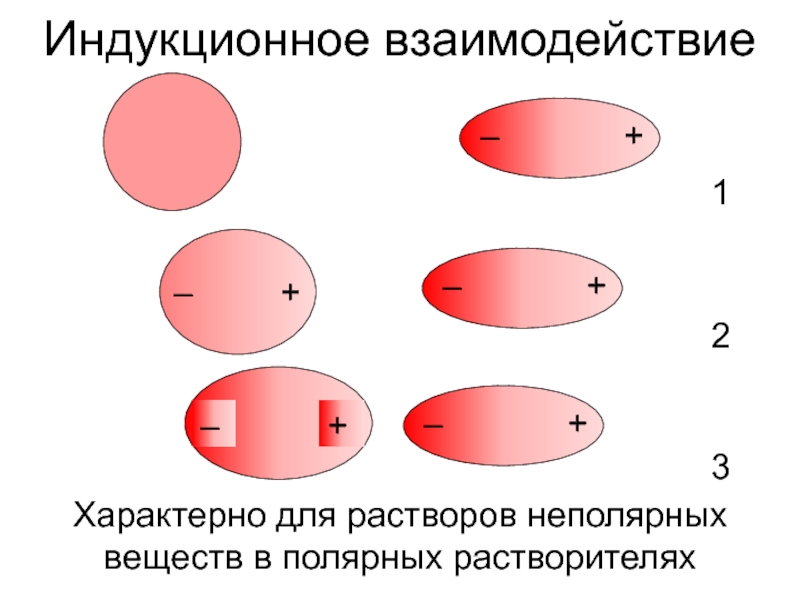
- 5. Индукционное взаимодействиеХарактерно для растворов неполярных веществ в полярных растворителях123
- 6. Дисперсионное взаимодействиеХарактерно для неполярных веществСила пропорциональна поляризуемости123Мгновенные диполи
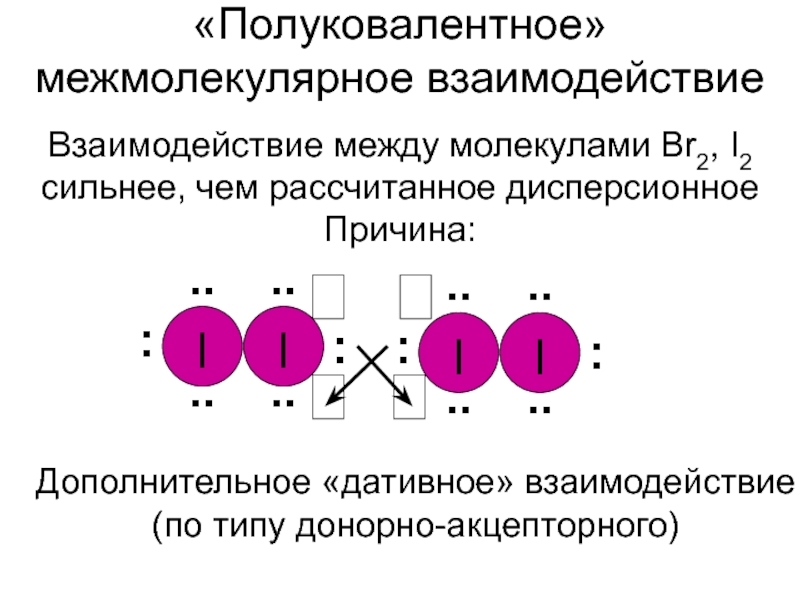
- 7. «Полуковалентное» межмолекулярное взаимодействиеВзаимодействие между молекулами Br2, I2сильнее, чем рассчитанное дисперсионноеПричина:Дополнительное «дативное» взаимодействие (по типу донорно-акцепторного)
- 8. Природа водородной связиРадиусы Н: Орбитальный: 78 пмКовалентный: 30
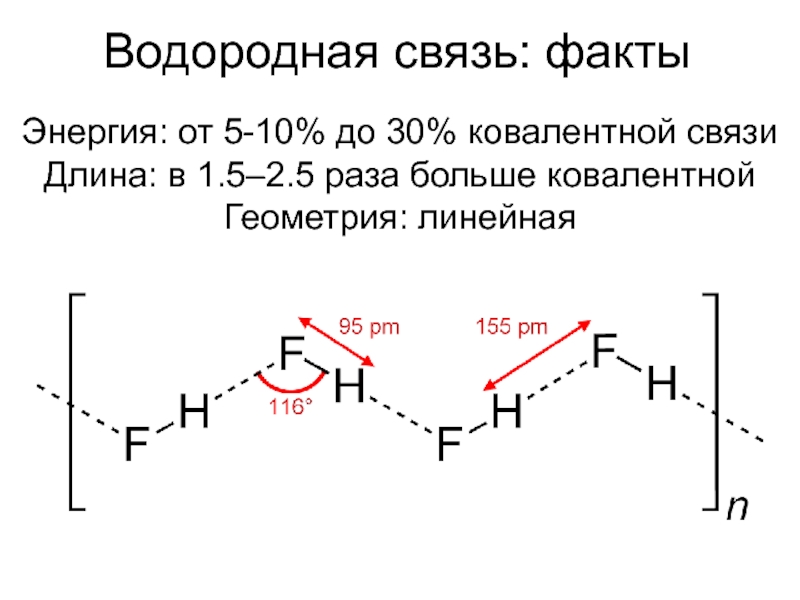
- 9. Водородная связь: фактыЭнергия: от 5-10% до 30% ковалентной связиДлина: в 1.5–2.5 раза больше ковалентнойГеометрия: линейная
- 10. Водородная связь: требования к строению частицX–H…Y
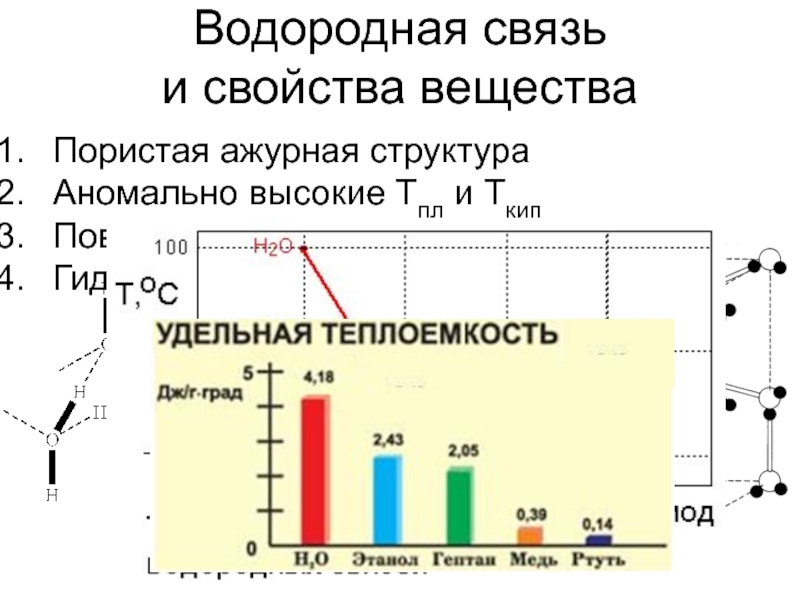
- 11. Водородная связь и свойства веществаПористая ажурная структура Аномально высокие Тпл и ТкипПовышенная теплоемкостьГидрофильность
- 12. Внутримолекулярная водородная связьАцетилсалициловая кислота (действующее начало аспирина)орто-НитрофенолОслабляется ассоциация молекуло-Нитрофенол перегоняется с водяным паромПоследствия?
- 13. Водородные связи в белкахC=O…H–NФиксируют вторичную структуру белка
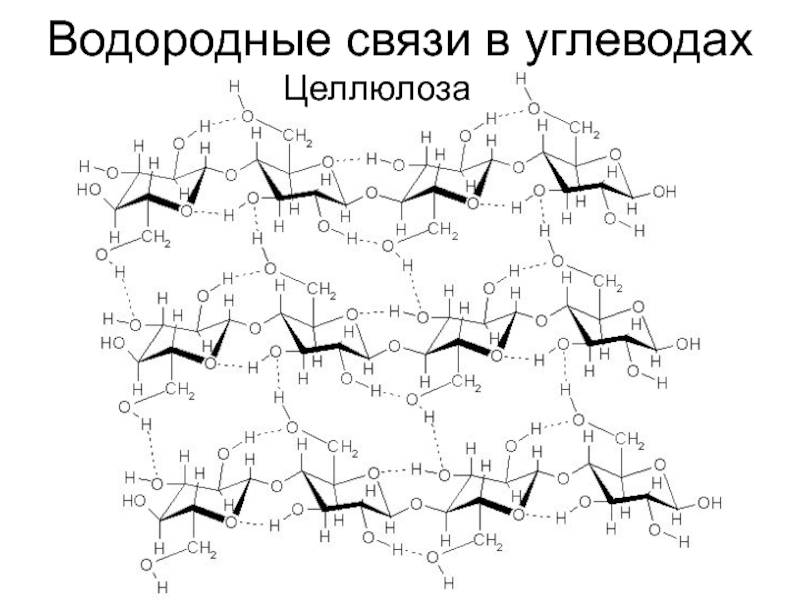
- 14. Водородные связи в углеводахЦеллюлоза
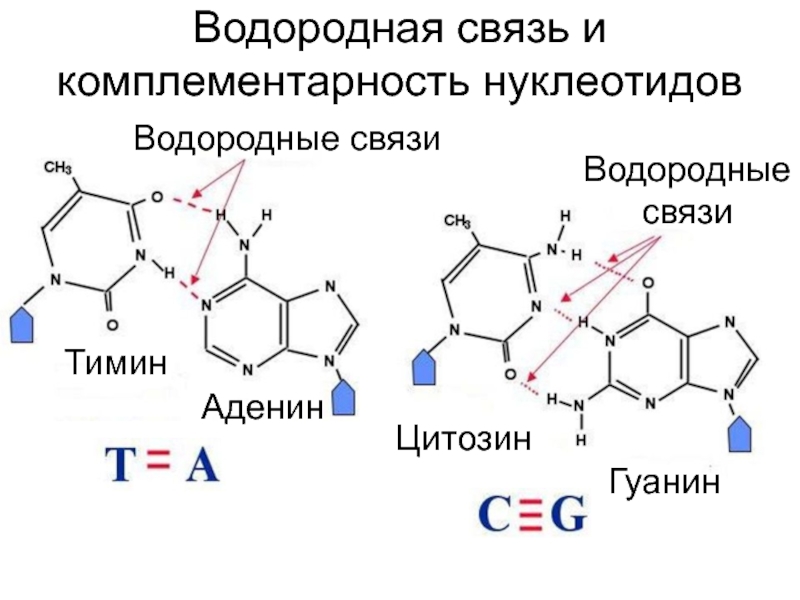
- 15. Водородная связь и комплементарность нуклеотидовВодородные связиВодородные связиТиминАденинЦитозинГуанин
- 16. Скачать презентанцию
Слабее, чем химическая связьИон–дипольДиполь–дипольДиполь–непо-лярная молекула2 неполярных молекулыИон–неполяр-ная молекулаВодородная связь
Слайды и текст этой презентации
Слайд 2Слабее, чем химическая связь
Ион–диполь
Диполь–диполь
Диполь–непо-
лярная молекула
2 неполярных
молекулы
Ион–неполяр-
ная молекула
Водородная связь
Слайд 3Природа и энергия межмолекулярного взаимодействия
Uвзаим = Uпритяж + Uотталк
Потенциал Леннарда-Джонса
Uпритяж
r–6
среднему расстоянию между молекуламиСлайд 4Ориентационное взаимодействие
Возможно у молекул с дипольным моментом
Сила уменьшается с ростом
температуры!
Примеры: HCl, SO2, H2S, PCl3…
Слайд 5Индукционное взаимодействие
Характерно для растворов неполярных веществ в полярных растворителях
1
2
3
Слайд 6Дисперсионное взаимодействие
Характерно для неполярных веществ
Сила пропорциональна поляризуемости
1
2
3
Мгновенные
диполи
Слайд 7«Полуковалентное» межмолекулярное взаимодействие
Взаимодействие между молекулами Br2, I2
сильнее, чем рассчитанное дисперсионное
Причина:
Дополнительное
«дативное» взаимодействие (по типу донорно-акцепторного)
Слайд 8Природа водородной связи
Радиусы Н:
Орбитальный: 78 пм
Ковалентный: 30 пм
Вандерваальсов: 120 пм
Катион
H+: 10–5 пм
Катион – ядро без электронной оболочки!
В соединениях
с электроотрицательными элементами атом Н – “почти катион”Проникает в чужую электронную оболочку
Причина?