Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
№ 4 лекция. Натрий алкилсульфонаттарын алу Натрий алкилсульфаттарын алу
Содержание
- 1. № 4 лекция. Натрий алкилсульфонаттарын алу Натрий алкилсульфаттарын алу
- 2. Натрий алкилсульфонаттарын алу. Алкилсульфонаттардың өндірісінде шикізат ретінде
- 3. Өндірісте алкилсульфонатар сульфохлорлау әдісімен алынады. Сульфохлорлау реакциясында
- 4. Радиациялық- химиялық сульфохлорлау перспективті бағыт болып табылады.
- 5. Өндірістік көлемде сульфохлорлау реакциясының 3 өнімі алынды,
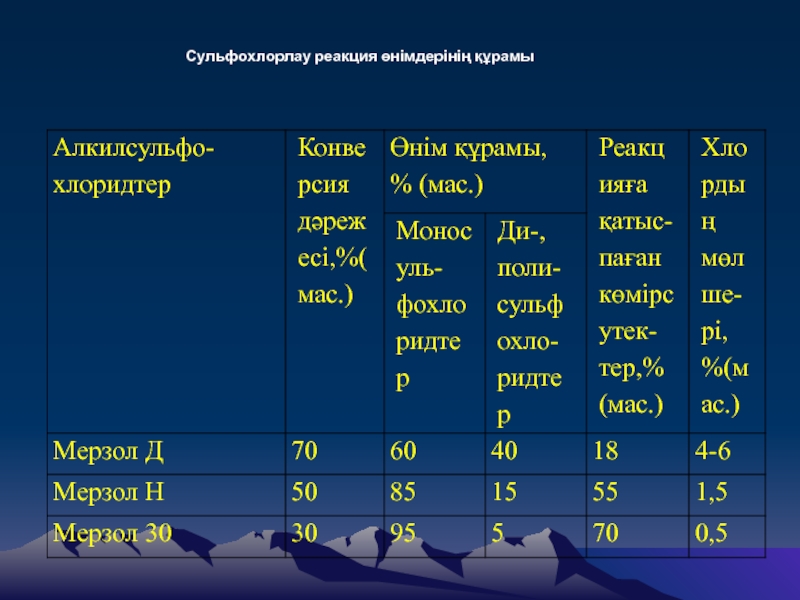
- 6. Сульфохлорлау реакция өнімдерінің құрамы
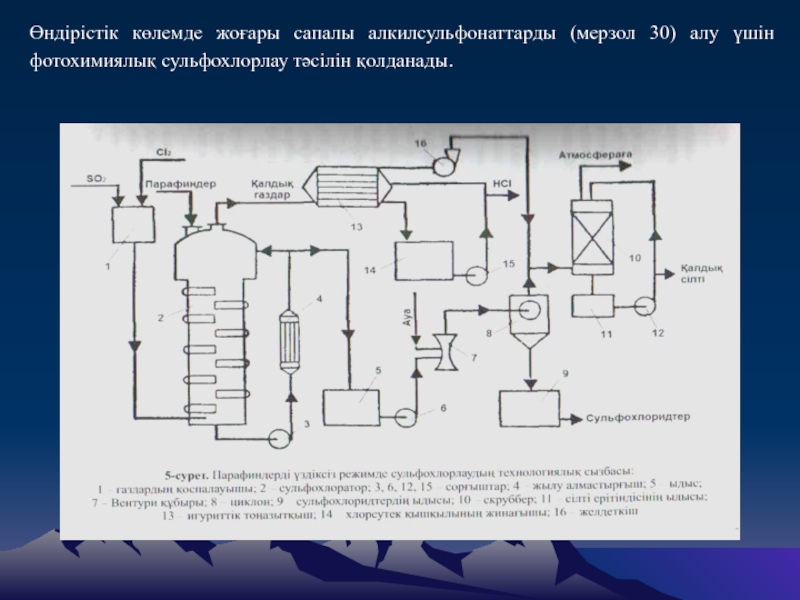
- 7. Өндірістік көлемде жоғары сапалы алкилсульфонаттарды (мерзол 30) алу үшін фотохимиялық сульфохлорлау тәсілін қолданады.
- 8. Сульфохлоратор – ішкі жағы қорғасындалған немесе поливинилхлоридтік
- 9. Слайд 9
- 10. Бұл технология сульфонаттардың 2 сұрпын- А сульфонаты
- 11. Сульфохлорлау тәсілінің кемшілігі- газ тәрізді хлорды пайдалану,
- 12. Бұл процесте инициатор ретінде ультракүлгін жарық пен
- 13. Н- парафиндерді сульфототықтыру процесі:
- 14. Натрий алкилсульфаттарын алу. Алкилсульфаттарды өндіру үшін молекулалық
- 15. Негізгі өнім – қышқыл алкилсульфаттардың максимал шығымын
- 16. Күкірт қышқылы және олеум көмегімен сульфаттаудың бірқатар
- 17. Хлорсульфон қышқылымен сульфаттау үлкен тереңдігімен, артық шамадағы
- 18. Әлемдік тәжірибеде газ тәрізді күкірттің триоксидімен сульфаттау
- 19. Сульфаттау реакциясына температура айтарлықтай әсер етеді; оның
- 20. Мысалы, олеин спиртін күкірт қышқылымен немесе олеуммен
- 21. Күкірт триоксидімен сульфаттаған жағдайда қосымша реакциялардың нәтижесінде
- 22. Күкірт қышқылымен сульфаттағанда конверсия дәрежесі 80%, хлорсульфон
- 23. Екіншілік алкендер үшін ең жақсы сульфаттаушы
- 24. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Натрий алкилсульфонаттарын алу. Алкилсульфонаттардың өндірісінде шикізат ретінде тізбектегі көміртек атомдарының
Слайд 3Өндірісте алкилсульфонатар сульфохлорлау әдісімен алынады. Сульфохлорлау реакциясында н-парафиндер күкірт диоксиді
және хлормен бір уақытта әрекеттеседі:
R-H + SO2+Cl2→ R-SO2Cl + HCl
Сульфохлоридтер
қышқылдық гидролизге тұрақты болып келеді және тек сумен ұзақ уақыт қайнатқанда ғана сульфон қышқылдарына айналады:R- SO2Cl+Н2О→R- SO3Н + HCl
Сілтімен бейтараптағанда сульфохлоридтер сульфон қышқылдарының тұздарын түзеді:
R- SO2Cl+2NaOH→R- SO2ONa + NaCl + H2O
Слайд 4Радиациялық- химиялық сульфохлорлау перспективті бағыт болып табылады. Инициатор ретінде радиоактивті
кобальттың γ-сәулелері қолданылады. Ультракүлгін жарыққа қарағанда γ-сәулелері тиімді болып табылады,
себебі фотохимиялық технологиядағы УК жарық шырақтарының қысқа мерзімді қызметіне байланысты қиындықтары жойылады.Хлор молекуласына иондағыш сәулелеу арқылы әсер еткенде хлордың бос радикалдары түзіліп, тізбекті сульфохлорлау реакциясын бастайды. Бұл кезде ди-, және полисульфохлоридтердің түзілуімен жүретін қосымша реакциялар да орын алады:
R-CH(SO2Cl)-(CH2)n-CH2-R+ SO2+Cl2→
→ R-CH(SO2Cl)-(CH2)n-CH(SO2Cl)-R
Слайд 5Өндірістік көлемде сульфохлорлау реакциясының 3 өнімі алынды, олардың н- парафиндердің
конверсия дәрежесіне қарай техникалық аталуы – мерзол Д, мерзол Н
және мерзол 30( сәйкесінше конверсия дәрежелері – 70,50 және 30%). Бұл өнімдердің құрамы кестеде келтірілген.Конверсия дәрежесі артуымен қоспадағы ди- және полисульфидтердің мөлшері де арта түседі. Қосымша реакцияларды болдырмау үшін көмірсутектердің айналу дәрежесі 30% -дан сапағаны жөн. Онда SO2 артық мөлшерін пайдаланып, процесті 20-300С температурада жүреді.Слайд 7Өндірістік көлемде жоғары сапалы алкилсульфонаттарды (мерзол 30) алу үшін фотохимиялық
сульфохлорлау тәсілін қолданады.
Слайд 8Сульфохлоратор – ішкі жағы қорғасындалған немесе поливинилхлоридтік шайыр немесе бакелиттік
лакпен жабылған мұнара. Сульфохлораторға 14 дана есебінен сынап- кварцтық шырақтар
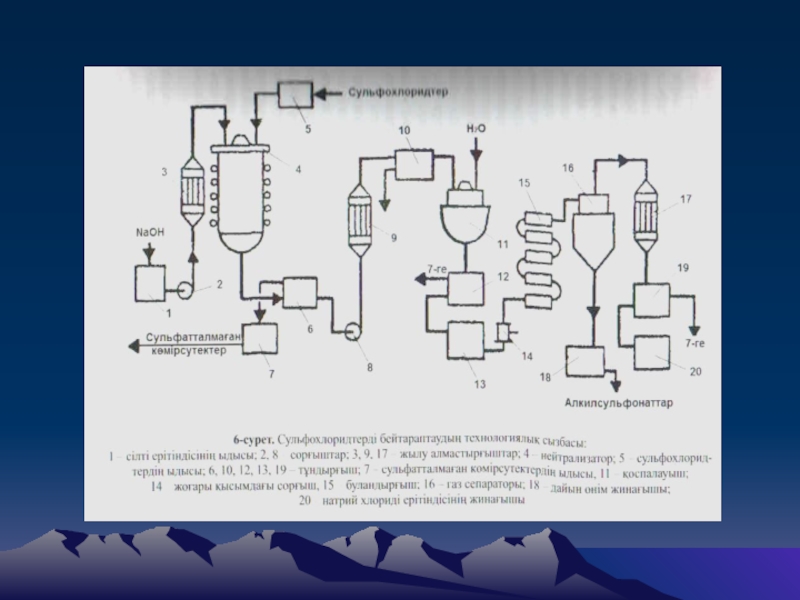
да қолданылады. Сульфохлоридтің 1 моліне шаққанда 0,015 кВт сағ шамасын құрайды. Үздіксіз режимде сульфохлорлаудың технологиялық сызбасы (5-сурет) бойынша газ тәрізді SO2менCl2 (1,05-1,1) :1,0 қатынасында жүзеге асады. Сульфохлоратордан шыққан сульфохлоридтер әрі қарай бейтараптауға жіберіледі(6-сурет).Слайд 10Бұл технология сульфонаттардың 2 сұрпын- А сульфонаты мен Б сульфонатын
алуға мүмкіндік береді.
А сульфонатының құрамына кемінде 90%(мас.) натрий алкилсульфонаттары, 7%-дан
(мас.) аспайтын натрий хлориді, 2%-дан (мас.) аспайтын көмірсутектер және 0,01%-дай (мас.) темір кіреді. Кемінде 92%-дан (мас.) моноалкилсульфонаттардан тұратын өнім арнайы эмульгаторларлар алуда қолданылады.Б сульфонаты- ұнтақ тәрізді өнім, 50-60% (мас.) алкилсульфонаттар, қалғанын натрий хлориді құрайды. Олар жақсы жұқтырғыш және көбік түзгіш болып табылады. Техникалық жуғыш зат ретінде пайдаланылады.
А сульфонатының 1 т алу үшін 1,43 т парафиндер, 0,57 т хлор, 0,6 т күкірт диоксиді, 0,6 т натрий гидроксиді жұмсалады.
Слайд 11Сульфохлорлау тәсілінің кемшілігі- газ тәрізді хлорды пайдалану, себебі реакциялық ортадан
шыққаннан кейін ол жоғалады.
Сондықтан, алкилсульфонаттарды газ тәрізді парафиндерді күкірт диоксиді
және ауа оттегімен парафиндерді сульфототықтыру әдісі арқылы алу қызуғышылық туғызады.Сульфототықтыру әдісімен алкилсульфонаттарды алу реакциясының теңдеуін
R-H + SO2 +0.5O2→ R- SO3H
түрінде жазуға болады.
Слайд 12Бұл процесте инициатор ретінде ультракүлгін жарық пен радиоактивті кобальттің γ-
сәулелерін, пероксидтік қосылыстарды пайдаланады.
С10-С18 фракциясындағы парафиндерді сульфототықтыру әдісімен алкилсульфонаттарды
алу прцесі келесі сатылардан тұрады:Сульфоқышқылды алу;
Сульфоқышқылдар экстрактін сутек пероксидімен ағарту;
Сульфоқышқылдарды бейтараптау;
қысым арқылы реакцияға түспеген көмірсутектерді бөліп алу;
изопропанолмен алкилсульфаттарды натрий сульфатынан тазарту;
сульфонаттың сулы-спирттікерітіндісін буландыру;
изопропанолды регенерациялау.
Слайд 13Н- парафиндерді сульфототықтыру процесі:
hv
R=H+ 2SO2 +
O2→ R-SO3H + H2SO4тізбекті механизмі бойынша жүзеге асады.
Түзілген сульфоқышқылдарды сумен экстракциялап, реакция зонасынан шығарып отырады. Бидистиллят күйіндегі суды тікелей реакторға береді. Бейтараптаудың алдында сульфоқышқылды сутек асқын тотығының 30%-дық ерітіндісімен өңдейді.
Ағартылған және бейтарапталған қоспаны 1600С температурасы мен 6 атм. қысымда тұндырып, реакцияға түспеген көмірсутектердің қабатын бөліп алады.натрий сульфатынан бөліп алу үшін алкилсульфонаттардың сулы ерітіндісін изопропил спиртімен араластырып суытады, нәтижесінде 5-100С-де натрий сульфаты кристал түрінде тұнбаға түседі. Әрі қарай алкилсульфонаттардың сулы- спиртті ерітіндісін сүзеді, сусыздандырады және айдайды.
Слайд 14Натрий алкилсульфаттарын алу. Алкилсульфаттарды өндіру үшін молекулалық массасы 190-280 (көміртек
атомдарының саны 10-18) болатын алифатикалық (қаныққан) спирттер қолданылады. Күкірт қышқылы
мен олеум көмегімен сульфаттаған жағдайда оларды артық шамада алады, ал хлорсульфон қышқылын пайдаланғанда артық шикізаттың мөлшері қажет емес.Алкилсульфоэфирлерді алудың:
R-OH + H2SO4 R-OSO2OH + H2O
R-CH2OH + ClSO3H R-CH2OSO3H + HCl
негізгі реакцияларымен қатар қосымша реакциялары да жүруі мүмкін. Бұл қолданыстағы сульфирлегіш агенттердің күшті тотықтырғыш қасиеттеріне байланысты.
Слайд 15Негізгі өнім – қышқыл алкилсульфаттардың максимал шығымын қамтамасыз ету үшін
процесті оңтайлы, яғни қосымша реакциялардың ықтималдығы төмен болатын жағдайда жүргізу
керек.Хлорсульфон қышқылымен сульфаттағанда сутек хлориді түзілгендіктен, процесті вакуумда өткізеді. Қосымша реакцияларды болдырмау үшін температура неғұрлым төмен деңгейде ұстауға тырысады, бірақ температураның төмендеуі негізгі реакцияны баяулататынын ескеру керек. Сульфаттаудың оңтайлы температурасы біріншілікті спирттер үшін 35-40°С құраса, екіншілік спирттер үшін 20°С-ден аспау керек. Осы шарттар орындалған жағдайда сульфаттау тереңдігі аз болатын себебі дегидротация, тотығу, конденсация, полимерлену және т.б. қосымша реакциялардың жүруіне байланысты. Біріншілікті спирттерді хлорсульфон қышқылымен сульфаттаудың тереңдігі, әдетте 90%-дан асады.
Слайд 16Күкірт қышқылы және олеум көмегімен сульфаттаудың бірқатар кемшіліктері бар:
Сульфаттаудың аз
тереңдігінің нәтижесінде шикізаттың үлкен шығыны;
Реакцияға түспеген спирттерді бөлінетін газдардан тазалау
қажеттілігі;Сульфаттаушы агенттің артық мөлшерінің қажеттілігі;
Сульфоэфирлерді бейтараптаудан кейін натрий сульфатының қосымша өнім ретінде бөлінуі.
Күкірт қышқылы немесе олеуммен сульфаттаудың технологиялық сызбасы мен аппараттық жабдықталуының қарапайымдылығы осы процестің артықшылығы болып табылады.
Слайд 17Хлорсульфон қышқылымен сульфаттау үлкен тереңдігімен, артық шамадағы сульфаттаушы агенттің аз
болуымен және натрий сульфатының қалдығымен сипатталады. Реакциялық массаның тығыздығын азайтып
жылу алмастыруды нашарлататын газ тәрізді хлорсутектің бөлінуі процестің кемшілігі болып табылады. Сонымен қатар, хлорсульфон және хлорсутек қышқылдары буларының улылығына байланысты техникалық қауіпсіздік шаралары күрделіленіп, химиялық тұрақты материалдан жасалған қондырғыларды қолдану қажеттілігі туындайды. Осындай қиыншылықтар хлорсульфон қышқылын сульфаттағыш агент ретінде қолдануын шектейді.Слайд 18Әлемдік тәжірибеде газ тәрізді күкірттің триоксидімен сульфаттау кеңінен таралған:
R-CH2OH +
SO3 R-CH2OSO3H
Күкірттің триоксидімен этерификациялау реакциясының жылдамдығы басқа сульфаттағыш агенттерге қарағанда
неғұрлым жоғары, бірақ қосымша реакциялар мұнда да орын алады. Этерификация реакциясының жылдамдығы өте үлкен екені анықталған және бұл реакция жоғары температурада да жүреді. Газ тәрізді күкірт триоксидімен сульфаттаудың лимиттеуші сатысы – триоксидті газ фазасынан сұйық фазаға ауыстыруы. Мұндай масса ауыстыру процесінің жылдамдық теңдеуі
υ= KΔcF
түрінде жазылады.
Мұндағы, К – масса тасымалдау коэффициенті; Δc – процестің қозғалтқыш күші; F – фазалардың жанасу ауданы.
Слайд 19Сульфаттау реакциясына температура айтарлықтай әсер етеді; оның артуымен көп мөлшерде
қанықпаған қосылыстар (алкендер және т.б.) түзіліп полимерленеді, нәтижесінде сульфо масса
қара қоңыр түске ие болады. Температура төмен болған жағдайда реакциялық массаның тұтқырлығы артып, әр жерде локальды қызу пайда болады да өнім қараяды. Біріншілікті спирттерді газ тәрізді SO3-пен сульфаттаудың оңтайлы температурасы 40-45°С шамасын құрайды.Сульфаттау тереңдігі мен реакциялық массаның түсіне процестің ұзақтығы әсер етеді: ол 1 минуттың бірнеше бөлігінен аспау керек.
Сульфаттау реакциясын реагенттердің стехиометриялық қатынасында жүргізіп, күкірт триоксидінің жоғары реакциялық қабілеттілігін азайту үшін оны ауамен қосып, 4-8% (көлем.) концентрациясында береді.
Процесті осы оңтайлы жағдайларда жүргізсе, сульфаттау тереңдігі 94-98 % құрап, реакциялық массаны бейтараптағаннан кейін соңғы өнімде аз мөлшерде натрий сульфаты болады.
Қанықпаған спирттерді күкірт не,месе хлорсульфон қышқылмен сульфаттауы қосымша реакциямен – сульфатты топтың қос байланысқа қосылуымен қатар жүреді.
Слайд 20Мысалы, олеин спиртін күкірт қышқылымен немесе олеуммен сульфаттағанда, екі сульфаттық
тобы бар алкилсульфаттар түзіледі:
CH3(CH2)7CH=CH(CH2)7CH2OH + H2SO4
CH3(CH2)7CH2CH(OSO3H)(CH2)7CH2OSO3H
Хлорсульфон қышқылымен сульфаттағанда реация
75-80 % өтеді:CH3(CH2)7CH=CH(CH2)7CH2OH + 2ClSO3H
CH3(CH2)7CH(Cl)CH(OSO3H)(CH2)7CH2OSO3H
Қанықпаған спирттер үшін де қаныққан біріншілікті спирттердегідей қосымша реакциялар жүреді.
Слайд 21Күкірт триоксидімен сульфаттаған жағдайда қосымша реакциялардың нәтижесінде
қанықпаған сульфоқышқылдар және
сульфондар түзіледі:
R-CH2-CH=CH-CH2-CH2OH + 2SO3→R-CH=CH-CH(SO3H)-CH2-CH2OSO3H;
R - CH2– CH = CH -
CH2- CH2OH + 2SO3→ R - CH2– CH –CH – CH2 – CH2OSO3H
O – SO2
Реакциялық массаны сілтінің көмегімен нейтрализациялайды:
R-CH2OSO3H +NaOH→ R-CH2OSO3Na + H2O.
Нейтрализацияны сілтінің артық мөлшерінде жүргізеді (ерітіндінің рН = 7.5-8). Реакция кезінде үлкен мөлшерде жылу бөлінеді. Сілті концентрациясы сульфаттағыш агенттің түріне байланысты: күкірт қышқылы немесе олеуммен сульфаттағанда сілтінің 20%-дық ерітіндісі; хлорсульфон қышқылы немесе күкірт триоксидімен сульфаттағанда – 8-10%-дық ерітінді қолданылады. Нейтрализация температурасы – 45-500С.
Слайд 22Күкірт қышқылымен сульфаттағанда конверсия дәрежесі 80%, хлорсульфон қышқылымен 90%, күкірт
триоксидімен 94% шамаларын құрайды.
Екіншілік алкилсульфаттарды алу үшін көміртек атом
саны 14-18 болатын алкендер фракциясын қолданады, фракция құрамына 70-80% алкендер мен 20-30% қаныққан көмірсутектер кіреді.Екіншілік алкилсульфаттарды алу үшін алкендерге күкірт қышқылын қосу әдісін қолданады. Реакция нәтижесінде түзілген сульфоэфирлер әрі қарай сілті ерітіндісімен нейтралданады:R-CH=CH2 + H2SO4 → R-C(OSO3H)HCH3;
R-C(OSO3H)HCH3+ NaOH→ R-C(OSO3Na)HCH3 + H2O.