Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Н Е М Е Т А Л Л Ы
Содержание
- 1. Н Е М Е Т А Л Л Ы
- 2. НЕМЕТАЛЛЫ - это химические элементы, для
- 3. Положение неметаллов в периодической системе химических элементов
- 4. Кроме того, к неметаллам относят также водород
- 5. Слайд 5
- 6. НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В
- 7. Слайд 7
- 8. Чаще неметаллы находятся в химически связанном виде:
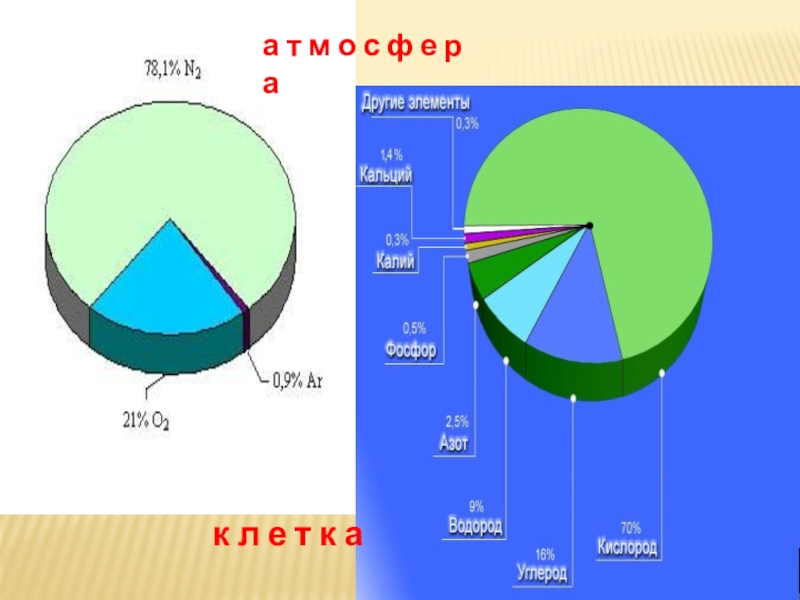
- 9. а т м о с ф е р ак л е т к а
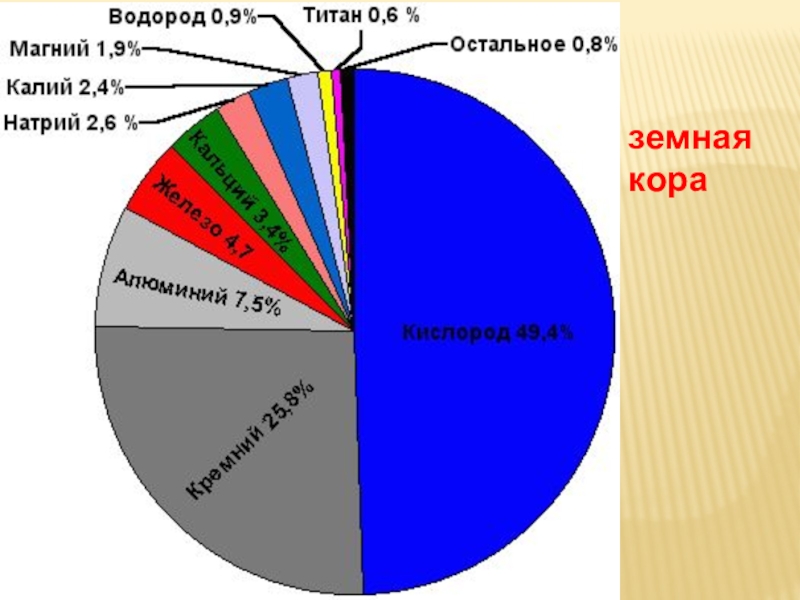
- 10. земная кора
- 11. ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВПРОСТЫЕ ВЕЩЕСТВА – атомы в
- 12. С Е Р АКРАСНЫЙ ФОСФОРБЕЛЫЙ ФОСФОР
- 13. КРЕМНИЙСЕЛЕН
- 14. У некоторых неметаллов наблюдается проявление аллотропии: -
- 15. ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВОкислительные свойства простых веществ:Реагируют с
- 16. Восстановительные свойства неметаллов (
- 17. ПОЛУЧЕНИЕ НЕМЕТАЛЛОВв промышленности
- 18. Молекулярный азот в промышленности получают фракционной перегонкой
- 19. Фосфор получают из апатитов или фосфоритов в
- 20. Хлор в промышленных масштабах получают вместе с
- 21. 1. Неметаллы, расположенные в порядке усиления их
- 22. 5. Верны ли следующие суждения о неметаллах
- 23. 9. Схеме превращения P⁻³→ P⁺⁵
- 24. ЗАДАНИЕ:Напишите электронные формулы - серы, фтора,
- 25. ЗАДАНИЕ:Напишите уравнения реакций и укажите окислитель: Na
- 26. ЗАДАНИЕСоставьте уравнения реакций и определите восстановитель:Si +
- 27. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2НЕМЕТАЛЛЫ - это химические элементы, для
атомов
которых характерна способностьпринимать электроны до завершения
внешнего уровня.
В главной подгруппе:
число электронов на внешнем слое не изменяется
радиус атома увеличивается
электроотрицательность
уменьшается
окислительные свойства
уменьшаются
-НЕМЕТАЛЛИЧЕСКИЕ свойства УМЕНЬШАЮТСЯ
В периоде:
радиусы атомов уменьш.
- число электронов на
внешнем слое уменьш.
- электроотрицательность
увеличивается
окислительные свойства
увеличиваются
- НЕМЕТАЛЛИЧЕСКИЕ
свойства
УВЕЛИЧИВАЮТСЯ
Слайд 3Положение неметаллов в периодической системе химических элементов
Немета́ллы — химические элементы
с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической
системы.
Расположение их в главных подгруппах соответствующих периодов: .
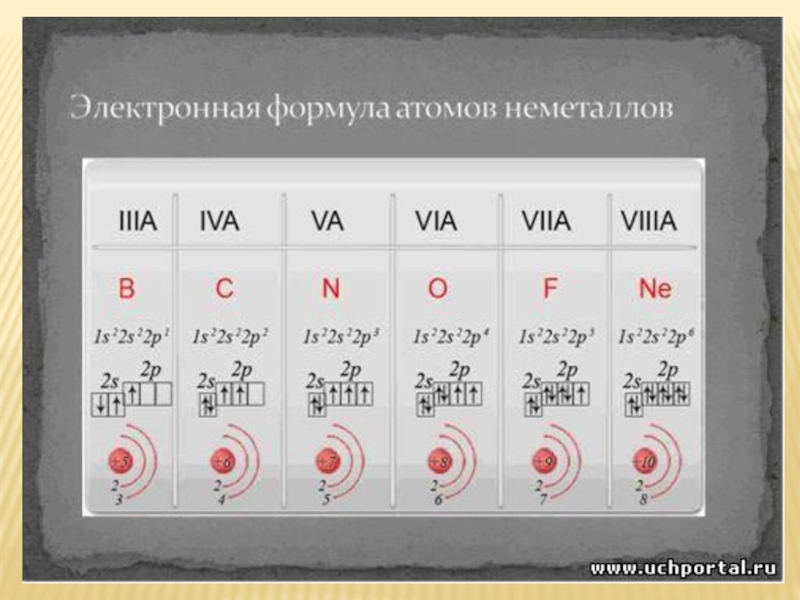
Слайд 4Кроме того, к неметаллам относят также водород и
гелий.
Характерной особенностью
неметаллов является большее (по сравнению с металлами) число электронов на
внешнем энергетическом уровне их атомов:O 1ѕ²2ѕ²2p⁴ Cl 1ѕ²2s²2p⁶3s²3p⁵
Это определяет их большую способность к присоединению дополнительных электронов,
и проявлению более высокой окислительной активности, чем у металлов.
Слайд 6НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В ПРИРОДЕ
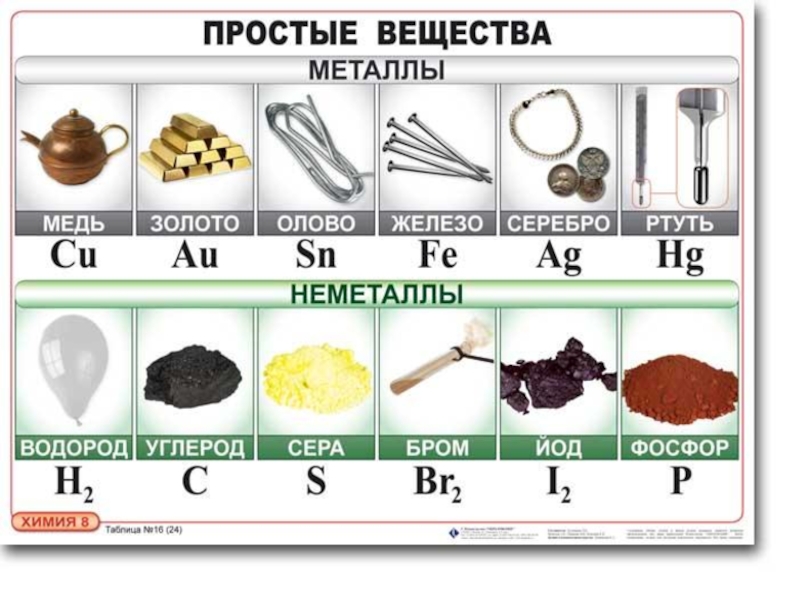
В свободном виде
могут быть газообразные неметаллические простые вещества —
фтор, хлор, кислород,
азот, водород, инертные газы,
твёрдые — иод, астат, сера, селен, теллур,
фосфор, мышьяк, углерод, кремний, бор,
при комнатной температуре в жидком состоянии существует
бром.
Распространёнными являются
кислород, кремний, водород;
редкими — мышьяк, селен, иод.
Слайд 8Чаще неметаллы находятся в химически связанном виде:
вода, минералы, горные породы,
различные силикаты, фосфаты, сульфиды.
силикат натрия
сульфид свинца
Слайд 11ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ
ПРОСТЫЕ ВЕЩЕСТВА – атомы в молекуле связаны
ковалентной неполярной связью.
СТРОЕНИЕ:
Молекулярное - а) газы - O₂ , Cl₂ , N₂ , H₂ , F₂ , O₃
(летучие) б) твердые - I₂ , P₄ , S₈
в) жидкие - Br₂
Атомное - твердые - C , B , Si , Se , Te
( длинные цепи атомов)
- высокие: твердость, температура плавления и
кипения
ОБЩИЕ ЧЕРТЫ: почти все – диэлектрики, кристаллы
непластичны, легко разрушаются
Слайд 14У некоторых неметаллов наблюдается проявление
аллотропии:
- для газообразного кислорода
характерны
две аллотропных модификации — кислород (O2)
и озон (O3),
- для твёрдого углерода множество форм — алмаз, астралены, графен, графан, графит, карбин,
фуллерены, стеклоуглерод
ФИЗИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ
АЛМАЗ
ГРАФИТ
Слайд 15ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВ
Окислительные свойства простых веществ:
Реагируют с металлами
2K + S⁰ = K₂S⁻²
3Ca + N₂⁰ = Ca₃N₂⁻³2Fe + 3 Cl₂⁰ = 2 FeCl⁻₃
Реагируют с водородом
H₂ + S⁰ = H₂S⁻² 3N₂⁰ + H₂ = 2N⁻³H₃
Реагируют с неметаллами с более низким
значением электроотрицательности
2P⁰ + 5S⁰ = P₂⁺⁵S₅⁻² S⁰ + 3 F₂⁰ = S⁺⁶F₆⁻
Реагируют с некоторыми сложными веществами
C⁻⁴H⁺₄ + 2 O⁰₂ = C⁺⁴O₂⁻² + 2 H₂⁺O⁻²
2 KI⁻ + Cl₂⁰ = 2 KCl⁻ + I₂⁰
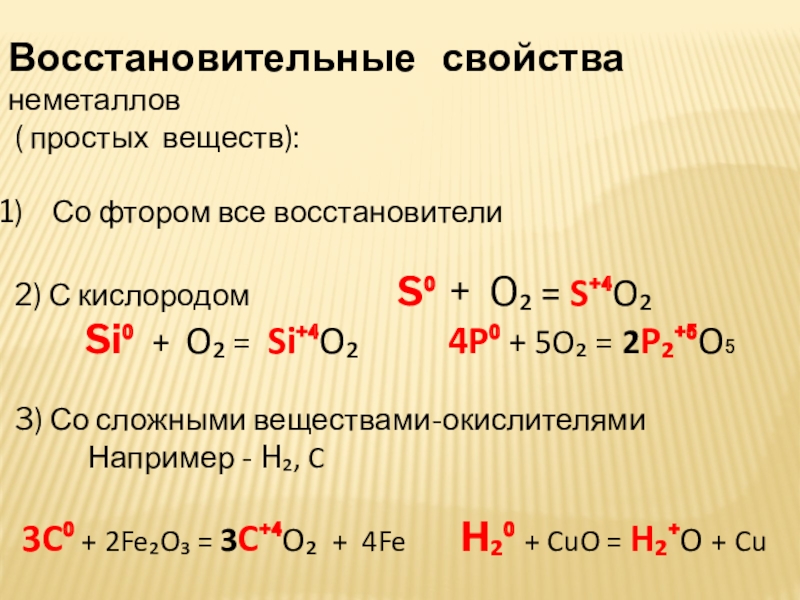
Слайд 16Восстановительные свойства неметаллов
( простых веществ):
Со фтором
все восстановители
2) С кислородом
S⁰ + O₂ = S⁺⁴O₂Si⁰ + O₂ = Si⁺⁴O₂ 4P⁰ + 5O₂ = 2P₂⁺⁵O₅
3) Со сложными веществами-окислителями
Например - H₂, C
3C⁰ + 2Fe₂O₃ = 3C⁺⁴O₂ + 4Fe H₂⁰ + CuO = H₂⁺O + Cu
Слайд 18Молекулярный азот в промышленности получают фракционной перегонкой жидкого воздуха. Этим
методом можно получить и «атмосферный азот:
В промышленности кремний технической чистоты
получают, восстанавливая расплав SiO2 коксом при температуре около 1800 °C в руднотермических печах шахтного типа. Чистота полученного таким образом кремния может достигать 99,9 % Слайд 19Фосфор получают из апатитов или фосфоритов в
результате взаимодействия с
коксом и
кремнезёмом при температуре 1600 °С:
Образующиеся пары белого фосфора конденсируются
2Ca₃(PO₄)₂↓+10C+6SiO₂↓=P₄+10CO↑+6CaSiO₃↓
в приёмнике
под водой.
Слайд 20Хлор в промышленных масштабах получают вместе
с гидроксидом натрия
и водородом путём
электролиза раствора поваренной
соли: 2NaCl + 2H2О ±2е- → H2↑ + Cl2↑ + 2NaOH
Слайд 211. Неметаллы, расположенные в порядке усиления их неметалличности, -
это
1) азот, углерод, бор
3) фтор, кислород, хлор 2) сера, хлор, фтор 4) бор, кремний, водород
2. Неметаллические свойства элементов в ряду углерод- азот- кислород-фтор:
1) не изменяются 2) усиливаются 3) ослабевают 4) изменяются периодически
Т Е С Т
3.Завершенный внешний энергетический имеет частица:
1) P⁺³ 2) S⁺⁴ 3) Cl⁺⁵ 4) C⁻⁴
4. Частице Si⁻⁴ соответствует электронная конфигурация:
1) 1s²2s²2p⁶3s² 2) 1s²2s²2p⁶3s²3p⁴ 3) 1s²2s²2p⁶3s²3p⁶4s²
Слайд 225. Верны ли следующие суждения о неметаллах и их
соединениях:
А. Низшая степень окисления азота и фосфора равна
-5.Б. Высший оксид кремния проявляет кислотные
свойства.
1 ) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения неверны
6. Ковалентная полярная связь образуется в соединении:
1) NaCl 2) NH₃ 3) P₄ 4) BaCl₂
7. Атомную кристаллическую решетку имеет:
1) I₂ 2) CO₂ 3) KCl 4) Si
8. Молекулярное строение имеет:
1) Кремний 2) Сера 3) Бор 4) Цинк
Слайд 239. Схеме превращения P⁻³→ P⁺⁵ соответствует
уравнение:
1) 4P + 5O₂ = 2P₂O₅
2) P₂O₅ + 3H₂O = 2H₃PO₄3)2PH₃ + 4O₂ = P₂O₅ + 3H₂O
4) P₂O₅ + 6NaOH = 2Na₃PO₄ + 3H₂O
10. Простое вещество сера взаимодействует с каждым из
веществ ряда:
1) HCl, Na, O₂ 2) Mg, O₂, H₂
3) K, Zn, Na₂SO₄ 4) Al, H₂O, O₂
11. Расставьте коэффициенты в схеме реакции:
P + H₂SO₄ → H₃PO₄+ SO₂ + H₂O
Слайд 24ЗАДАНИЕ:
Напишите электронные формулы - серы, фтора,
мышьяка, брома
S 1s²2s²2p⁶3s²3p⁴
F 1s²2s²2p⁵As 1s²2s²2p⁶3s²3p⁶4s²4p³ Br 1s²2s²2p⁶3s²3p⁶4s²4p⁵
У какого из элементов ярче выражены
неметаллические свойства и почему:
а) As - N б) Cl - S
а) N – меньше радиус атома (больше значение
электроотрицательности)
б) Cl - меньше радиус атома, больше валентных
электронов ( больше значение ЭО)
Слайд 25ЗАДАНИЕ:
Напишите уравнения реакций и укажите окислитель:
Na + Br₂
→ ? Mg + P
→ ? Na + Si → ?Ответ: 2Na + Br₂⁰ = 2 NaBr⁻ 3Mg + 2P⁰ = Mg₃P₂⁻³
4Na + Si⁰ = Na₄Si⁻⁴
H₂ + Cl ₂ → ? P + Cl₂ → ? CH₄ + Cl₂ → ?
Ответ: H₂ + Cl₂⁰ = 2HCl⁻ 2P + 5Cl₂⁰ = 2PCl₅⁻
CH₄ + Cl₂⁰ = CH₃Cl⁻ + HCl⁻
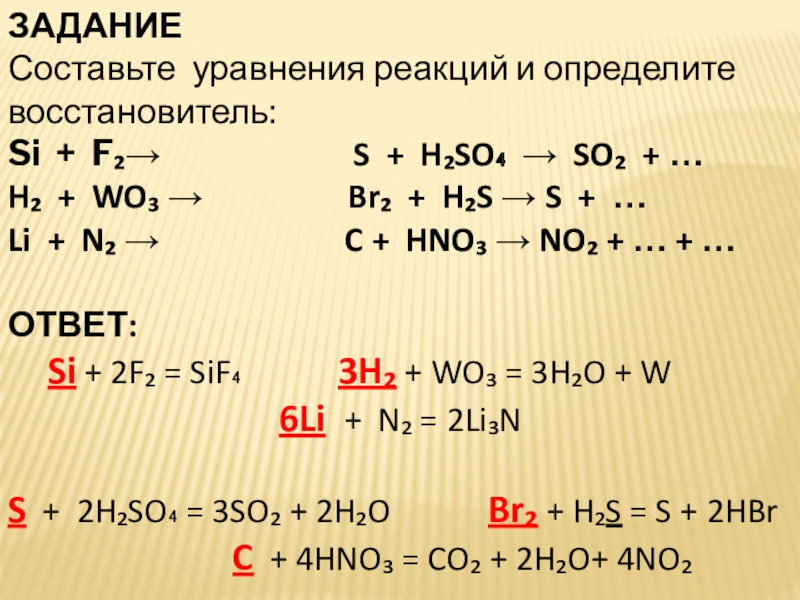
Слайд 26ЗАДАНИЕ
Составьте уравнения реакций и определите восстановитель:
Si + F₂→
S
+ H₂SO₄ → SO₂ + …H₂ + WO₃ → Br₂ + H₂S → S + …
Li + N₂ → C + HNO₃ → NO₂ + … + …
ОТВЕТ:
Si + 2F₂ = SiF₄ 3H₂ + WO₃ = 3H₂O + W
6Li + N₂ = 2Li₃N
S + 2H₂SO₄ = 3SO₂ + 2H₂O Br₂ + H₂S = S + 2HBr
C + 4HNO₃ = CO₂ + 2H₂O+ 4NO₂