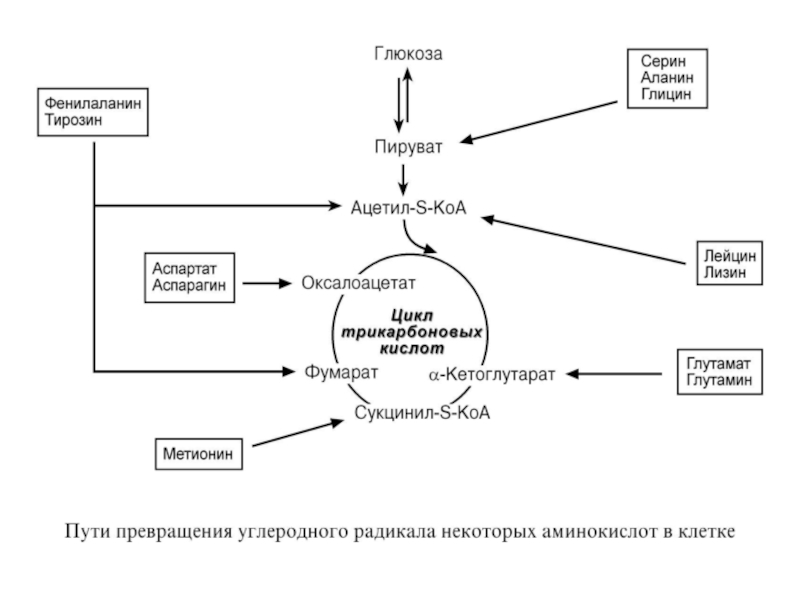
Слайд 1Обмен белка и аминокислот
Катаболизм:
1.гидролиз белка до аминокислот (внешний этап
в полости ЖКТ), в лизосомах, протеасомах клеток.
2. дезаминирование, декарбоксилирование, окисление
углеродного скелета и специфические превращения аминокислот по радикалу.
Анаболизм:
1.биосинтез аминокислот
2. биосинтез белков
Слайд 2Потребность в белках и нормы белкового питания
Белки – незаменимый компонент
пищи, практически единственный источник азота для синтеза аминокислот и азотистых
оснований.
В норме у здоровых взрослых людей количество потребляемого азота и выводимого азота примерно одинаково ( N2 – баланс равен нулю (азотистое равновесие).
Отрицательный азотистый баланс характерен для пожилого возраста, голодания, раковой кахексии, ожоговой болезни, длительной инфекции.
Положительный – для беременных женщин и младенцев, при выздоровлении.
Слайд 3Потребности в белковой пище
Коэффициент Рубнера (коэффициент изнашивания) = 53 мг
N2 /кг массы тела.
23 г белка распадается ежесуточно.
Т50 для белков
всего тела = 80 суткам.
Медленнее всего обновляются белки соединительной и мышечной ткани
(до полугода),
Быстрее всего – белки крови (10-14 дней), ферменты, гормоны, рецепторы
Слайд 4Потребность в белках
Физиологический минимум = 35 -50 г в сутки.
Оптимум
– 85 -100 г в сутки
Качество поступающего белка (биологическая ценность)
определяется его аминокислотным составом и биологической доступностью (животный или растительный белок) и растворимостью (способностью гидролизоваться). Наибольшей биологической ценностью обладают яичный альбумин и казеиноген молока.
400 – 500 г белка ежесуточно синтезируется в организме (до 300 г экзогенных и эндогенных аминокислот подвергается реутилизации). Аминоацидурия ограничена в норме (реабсорбция!) и касается в основном заменимых аминокислот.
Слайд 5Внешний обмен белка (переваривание, гидролиз)
Поэтапный протеолиз белков до аминокислот,
лишение
их видоспецифичности и антигенности.
Главными компонентами желудочного сока являются:
НСL (выделяется обкладочными
клетками).
Муцин – гликопротеин образующий защитную слизь (выделяется добавочными клетками).
Пепсиноген – предшественник пепсина (выделяется главными клетками слизистой оболочки желудка).
Химозин (реннин) у грудных детей.
Слайд 7Роль соляной кислоты
1. Создает кислую среду в полости желудка (рН
1,5 -2), условия для самоактивации (автокатализа) пепсина.
2. Денатурирует пищевые белки,
улучшая их протеолиз.
Оказывает бактерицидное действие.
Регулирует поступление пищи из желудка в 12 –перстную кишку.
Слайд 8Регуляция синтеза соляной кислоты
Гистидин гистамин – активация аденилатциклазы –
активация фосфопротеинкиназы с участием цАМФ – фосфорилирование карбангидразы (активация) ключевого
фермента в синтезе соляной кислоты в эпителиальных клетках желудка.
Слайд 9ПЕПСИНОГЕН → ПЕПСИН
Пепсин – простой одноцепочечный белок, карбоксильная (в активном
центре асп-асп) эндопротеиназа..
Активируется при отщеплении N-концевого пептида из 40
аминокислот (в основном катионных), блокирующего активный центр фермента:
1) в кислой среде (кислотный гидролиз с участием
НСl, медленно),
2) автокатализ (очень быстро).
Сайт-специфичность в отношении гидролиза пептидной связи, образованной:
1) -NH2 группой лей, фен,тир или
2) -СООН группой глу или глн.
Слайд 10Панкреатические протеиназы
Сериновые эндогенные сайтспецифичные протеиназы.
Оптимум рН: в
слабощелочной среде обеспечивают бикарбонаты сока поджелудочной железы.
Синтез: в виде
проферментов
Активация: в просвете 12 – перстной кишки путём лимитированного протеолиза.
Инициирует активацию энтерокиназа, фиксированная на поверхности энтероцитов. Она отщепляет от трипсиногена N-концевой пептид, при этом формируется активный центр фермента трипсина. Далее – автокатализ.
Слайд 11Панкреатические протеиназы
Трипсин обеспечивает активацию химотрипсиногена, проэластазы, прокарбоксипептидазы,
отщепляя N–концевые пептиды.
Каскад
протеолитических эндо- и экзо- протеиназ, дипептидаз ЖКТ обеспечивает гидролиз белков
пищи до свободных аминокислот.
Слайд 12Протеазы кишечника
Карбоксипептидазы – со стороны свободной карбоксигруппы
1) карбоксипептидаза
А
специфичность – незаряженные АК
2) карбоксипептидаза В
специфичность – лиз и арг
Аминопептидазы – , делают то же самое со стороны свободной аминогруппы.
ПРОДУКТЫ: три- и дипептиды,
Три- и дипептидазы с разной субстратной специфичностью
ПРОДУКТЫ: свободные аминокислоты
Слайд 13 Переваривание сложных белков
Пепсин и HCl желудка: от белков отделяют
простетические группы, далее эти группы превращаются в соответствии с их
химической природой.
Гем хромопротеинов окисляется в гематин, он почти не всасывается, выход с калом.
Нуклеиновые кислоты под действием рибонуклеаз и дезоксирибонуклеаз панкреатического сока расщепляются до мононуклеотидов.
Стенка кишечника выделяет полинуклеотидазы, фосфодиэстеразы и фосфатазы. Они расщепляют нуклеиновые кислоты до мононуклеотидов и далее.
Механизм действия: эндо- и экзонуклеазы, нуклеотидазы, фосфатазы.
1) эндонуклеазы: нуклеиновые кислоты → олигонуклеотиды.
2) экзонуклеазы: от нуклеиновых кислот, олигонуклеотидов → концевые мононуклеотиды,
3) нуклеотидазы, фосфатазы: мононуклеотиды → фосфорная кислота и нуклеозиды → до свободных азотистых оснований и пентоз.
Всасывание. Мононуклеотиды в стенку кишечника почти не поступают. В кровь → нуклеозиды, продукты полного расщепления нуклеотидов и пуриновых оснований.
Микрофлора кишечника: часть пуриновых нуклеотидов → в гипоксантин, ксантин, мочевую кислоту, которые всасываются.
Человек большую часть поступивших в кровь нуклеозидов, пуринов и пиримидинов не использует, всё деградирует до конечных продуктов обмена и выводится.
Экзогенные нуклеиновые кислоты практически не бывают предшественниками нуклеотидов. Потребности в нуклеотидах полностью покрываются за счет эндогенного синтеза “de novo“ при необходимом количестве исходных веществ.

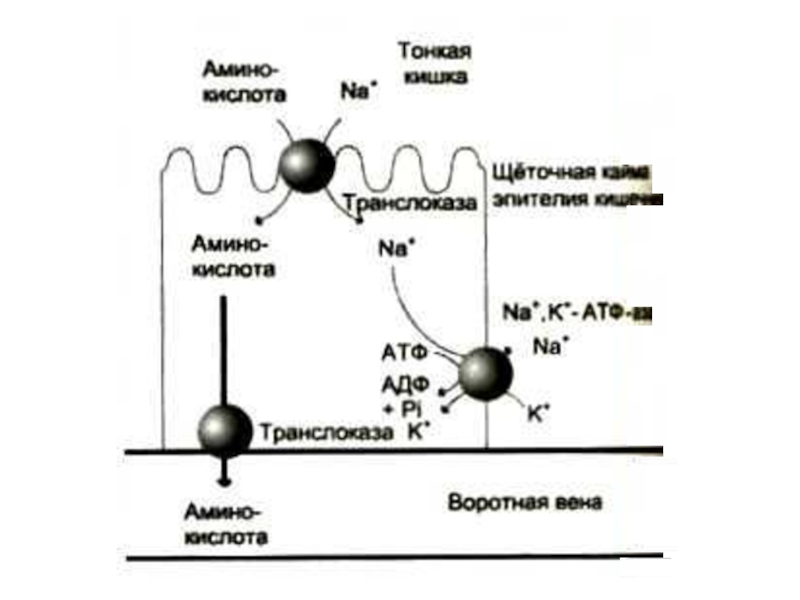
Слайд 14Всасывание аминокислот в кишечнике
в кровь (95%) и в лимфу
1)
В мембранах энтероцитов кишечных ворсинок – несколько систем активного транспорта
(Na+-зависимый симпорт), для аминокислот с различными радикалами.
2) g-глютамилтранспептидаза –
фермент, способный осуществлять трансмембранный перенос аминокислот и пептидов.
Слайд 15Транспортёры аминокислот
5 групп транспортёров для разных аминокислот:
нейтральных (глицин,
аланин);
нейтральных с длинной разветвлённой
цепью (лейцин, изолейцин);
с катионным радикалом (лизин);
с анионным радикалом (аспарагиновая,
глутаминовая кислоты);
иминокислот (аргинин).
Слайд 18целиакия
наследственное прогрессирующее заболевание, приводящее к изменениям в тощей кишке: воспалению
и сглаживанию слизистой оболочки, исчезновению ворсинок, атрофии щеточной каемки
и
появлению кубовидных энтероцитов.
ПричинА: врожденная непереносимость глютена белка клейковины злаков (растворимой фракции – глиадина).
Проявляется после введения в рацион младенца глиадинсодержащих продуктов (манной каши…)
Патогенез до конца не выяснен. Гипотезы:
1) прямое токсическое воздействие белка на стенку кишечника и
2) иммунный ответ на белок в стенке кишки
Слайд 19Гниение белков в кишечнике
Реакции дезаминирования и декарбоксилирования аминокислот с участием
бактериальных ферментов.
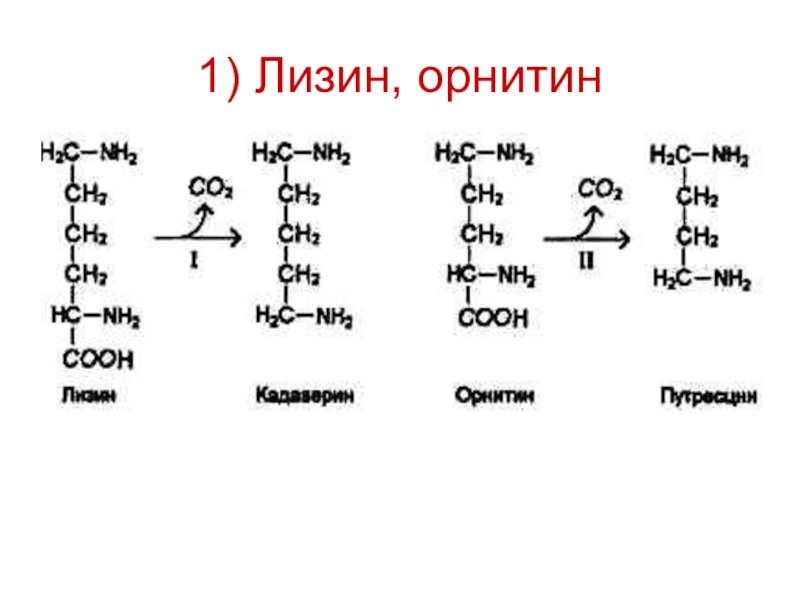
В кишечнике накапливаются токсичные, биологически активные вещества:
Путресцин и
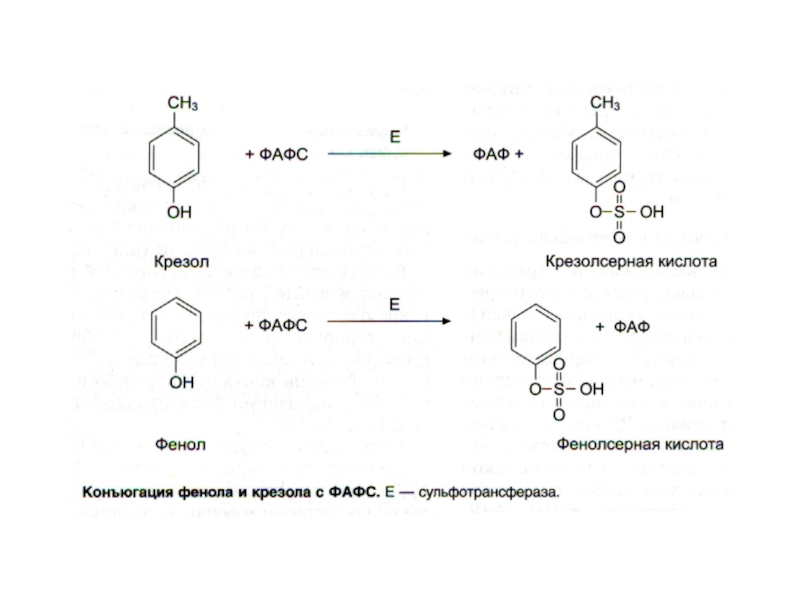
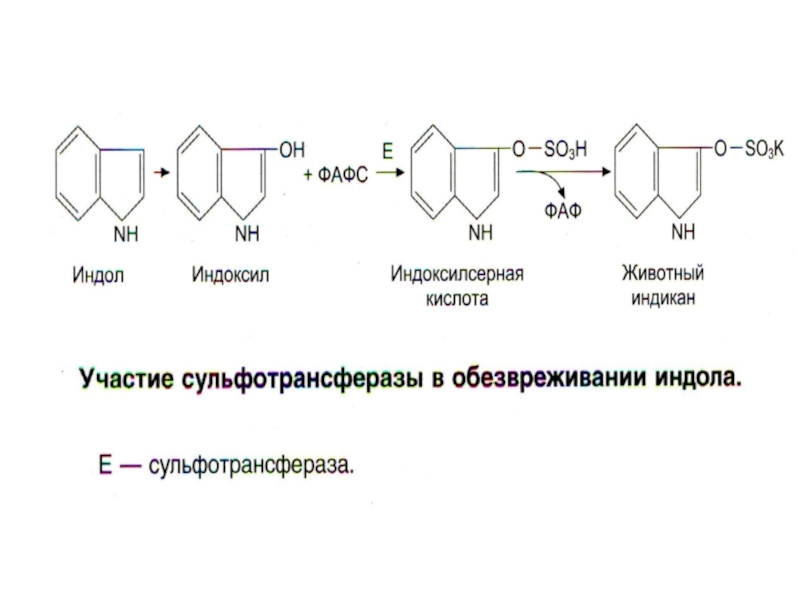
кадаверин (трупные яды), крезол, фенол, индол, скатол, аммиак, сероводород.
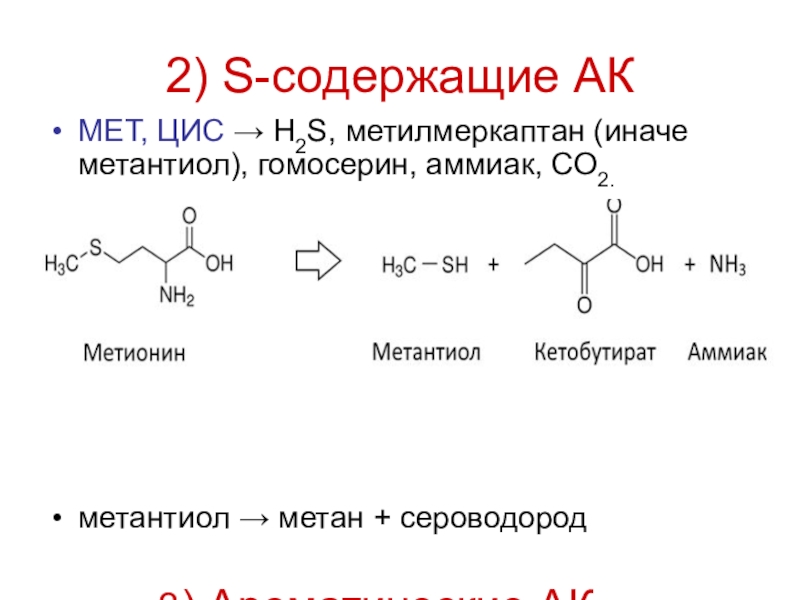
Слайд 212) S-содержащие АК
МЕТ, ЦИС → H2S, метилмеркаптан (иначе метантиол), гомосерин,
аммиак, СО2.
метантиол → метан + сероводород
3) Ароматические АК
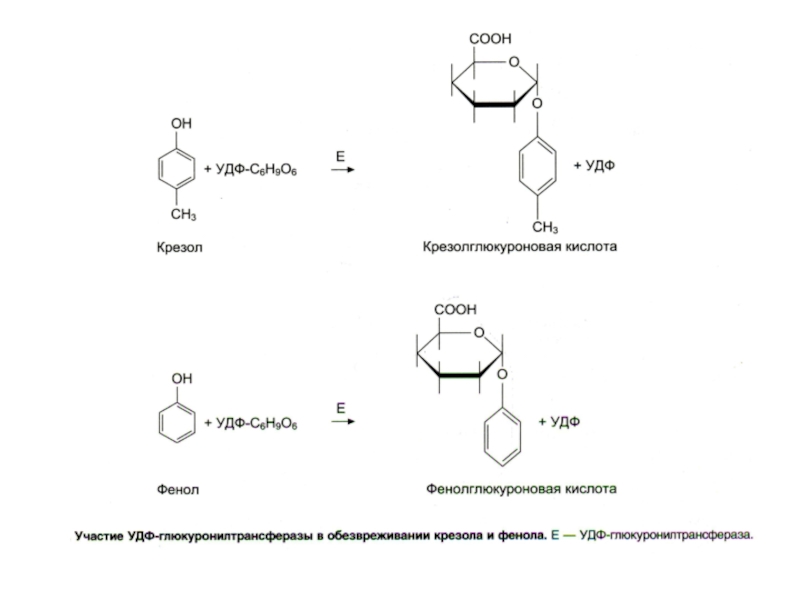
Слайд 29Обезвреживание продуктов гниения в печени
Биотрансформация: 1) стадия - химическая модификация
+ 2) стадия - конъюгация
Во 2-й стадии участвуют неспецифические, индуцибельные
ферменты микросом печени:
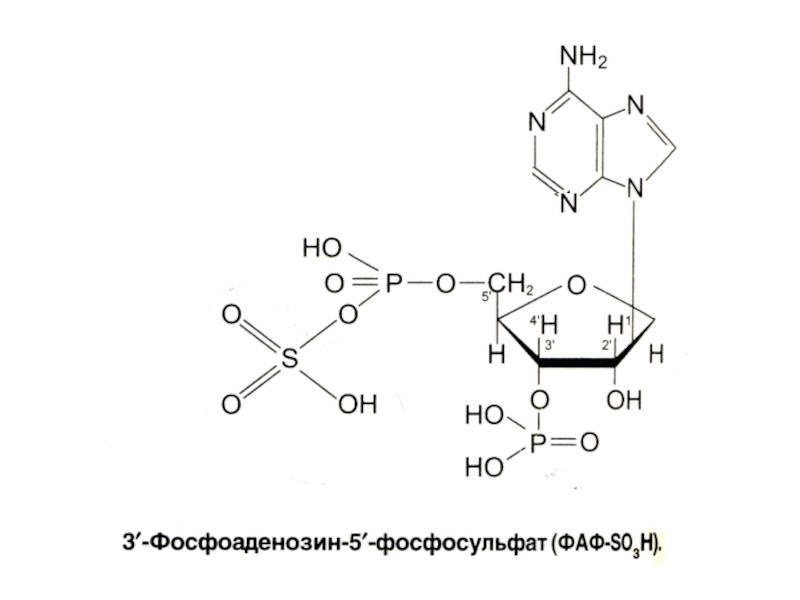
ФАФС-трансфераза, УДФ-трансфераза;
они образуют парные, нетоксичные, растворимые соединения с различными субстратами (эндогенными и экзогенными) – глюкурониды или сульфаты.
Глутатионтрансфераза – фермент образует конъюгаты с глутатионом (GSH)
Слайд 30Внутриклеточный протеолиз
Олиго- и дипептиды могут быть гидролизованы в цитоплазме пептидазами.
Лизосомы.
Кислые гидролазы: тиоловые и аспартатные протеиназы (катепсины В, L, H,
D), гидролизующие белки.
Высокоизбирательные протеасомные гидролитические комплексы в цитоплазме для удаления дефектных, поврежденных или регуляторных, короткоживущих белков.
Для этого существует регуляторный, распознающий комплекс, «помечающий» белки, подлежащие деградации (убиквитин).
Слайд 31Защита от протеолиза
Как в клетках, так и во внеклеточном пространстве,
в крови работают и системы протеолиза и антипротеолитической защиты.
Механизмы защиты:
Пространственные
ограничения (мембрана лизосом, регуляторные комплексы протеасом)
Существование протеиназ в виде неактивных предшественников.
Гликозилирование белков
Эндогенные ингибиторы протеиназ:
a1–антитрипсин, a2-макроглобулин плазмы, тканевые кислотостабильные ингибиторы.
Слайд 32Промежуточный обмен аминокислот
Общие пути катаболизма аминокислот (дезаминирование, трансаминирование, декарбоксилирование)
Частные
реакции превращений аминокислот.
Пути синтеза заменимых аминокислот.
Слайд 33Метаболические функции аминокислот
Кроме участия в синтезе пептидов и белков, участия
в получении энергии (окисление до СО2, Н2О даёт ≈ 15%
энергии), у большинства аминокислот активная метаболическая «судьба»:
18 аминокислот являются гликогенными (кроме лей и лиз)
Мет, сер – б/с фосфолипидов
Мет – б/с всех белков, стартовая АК
Гли – б/с порфиринов, гли - нейромедиатор
Асп, гли, глн, мет – б/с азотистых оснований
Тир – б/с катехоламинов и тиреоидов, меланина
Глу, три – б/с нейромедиаторов
Глу, гли, цис, арг – б/c глутатиона, креатина
Слайд 34СИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ
Источник углеродных скелетов – глюкоза,
источник азота –
NH2-группы АК, NH3.
Реакции трансаминирования
Восстановительного аминирования
Арг – в реакциях синтеза мочевины
Тир
– из фен
Цис – из мет
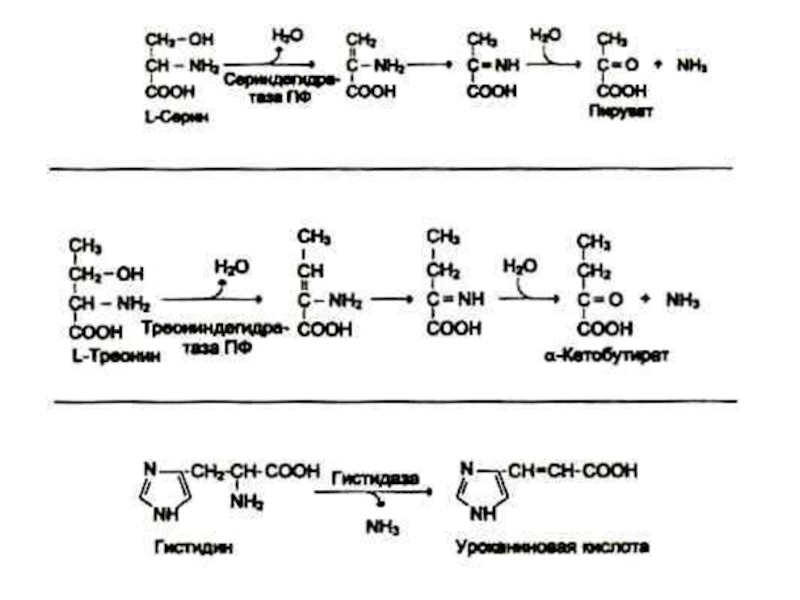
Слайд 35Дезаминирование аминокислот
Механизмы: восстановительный; гидролитический; внутримолекулярный, окислительный. Все они используются микрофлорой
полости рта
В клетках млекопитающих:
Гис подвергается внутримолекулярному дезаминированию,
Сер и тре –
гидролитическому.
Глу – прямому окислительному дезаминированию. Важно в обмене веществ!
На основе этого:
все другие АК – непрямому дезаминированию (через переаминирование с a-кетоглутаратом)
все другие АК подвержены окислительному дезаминированию весьма условно: почему? → см. далее
Слайд 37Окислительное дезаминирование АК
Для каждой аминокислоты есть специфическая оксидаза
(печень, почки):
FMN-зависимые оксидазы L-аминокислот имеют оптимум рН в щелочной среде
рН=10 (активность очень и очень низка и реакции протекают слишком медленно).
FAD-зависимые оксидазы D-аминокислот
(эти АК не характерны для живого организма!) высокоактивны в нейтральной среде, окисле-ние идёт до кетокислот, которые становятся субстратами для ресинтеза L-аминокислот (в реакциях переаминирования)
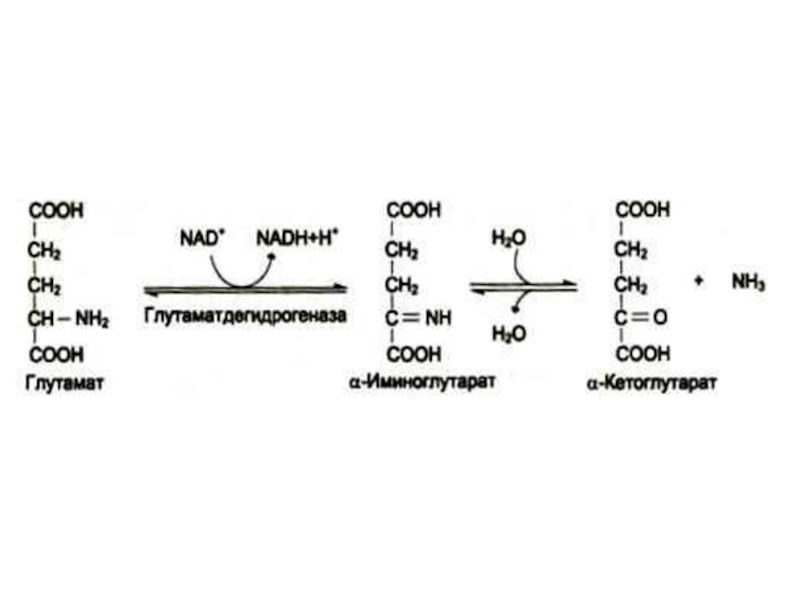
Слайд 38Окислительное дезаминирование
Наиболее активной дезаминазой является глутаматдегидрогеназа (NAD- зависимая)
Реакция идет в
две стадии: ферментативное окисление и спонтанное освобождение аммиака с участием
воды. Реакция обратима во всех тканях, кроме мышечной.
Фермент олигомерный, аллостерический, отрицательные эффекторы: ATF, NADH, положительные: ADF, NAD.
Синтез фермента индуцируется кортикостероидами.
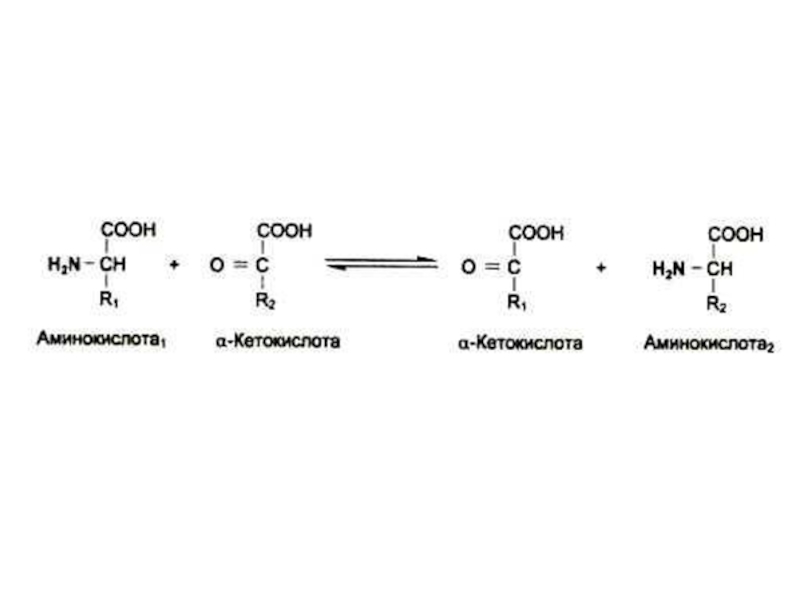
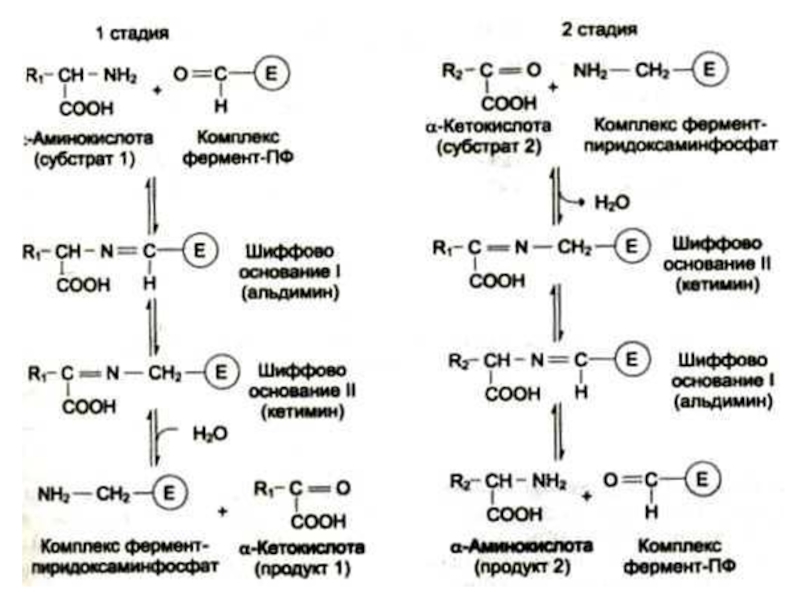
Слайд 40Трансаминирование
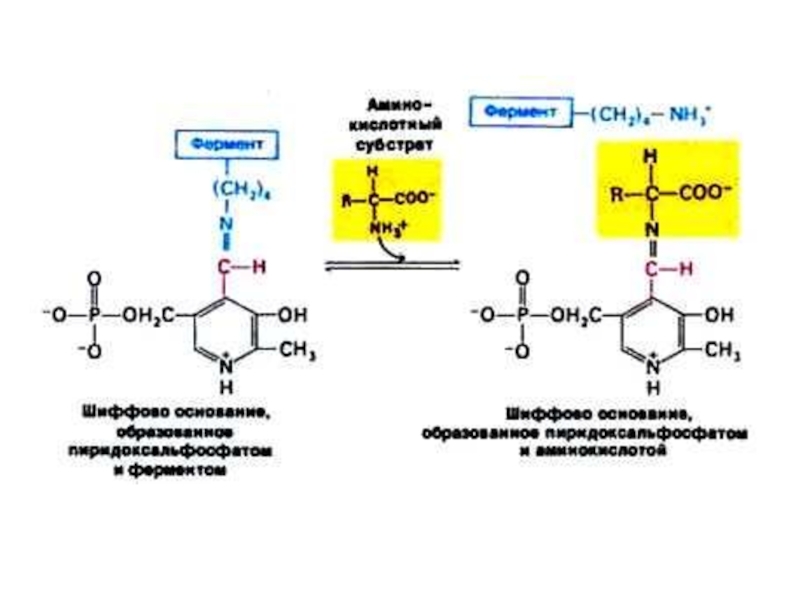
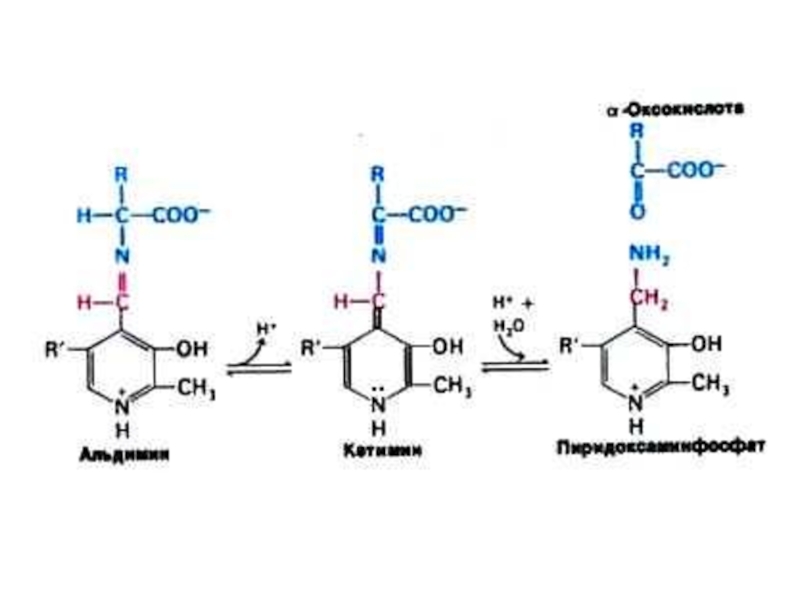
Обратимая реакция между кетокислотами и аминокислотами (аминогруппу переносит кофактор
– пиридоксальфосфат).
На основе кетокислот возникают новые аминокислоты.
Не освобождается аммиак!
Путь к
непрямому дезаминированию аминокислот, когда при переаминировании АК с кетоглутаратом образуется глутамат. ГЛУ – это единственная аминокислота, подвергающаяся уже прямому окислительному дезаминированию
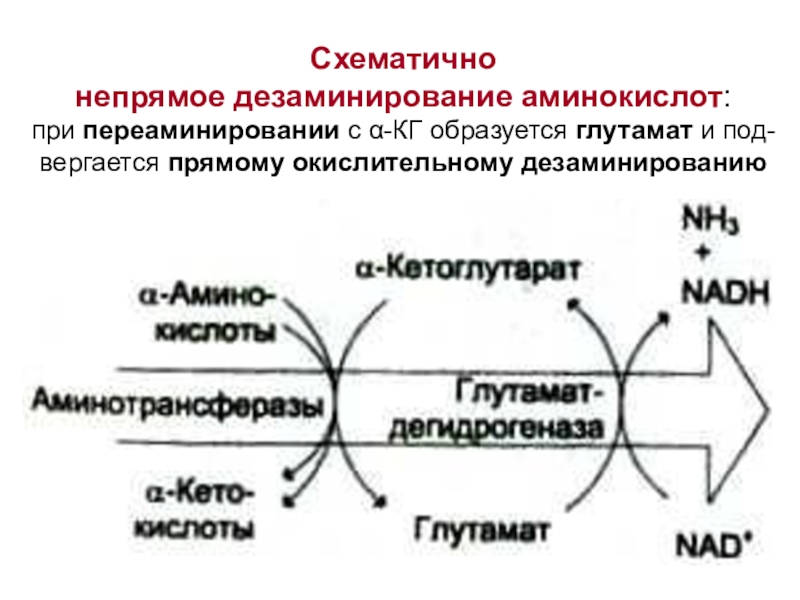
Слайд 45Схематично
непрямое дезаминирование аминокислот:
при переаминировании с α-КГ образуется глутамат
и под-
вергается прямому окислительному дезаминированию
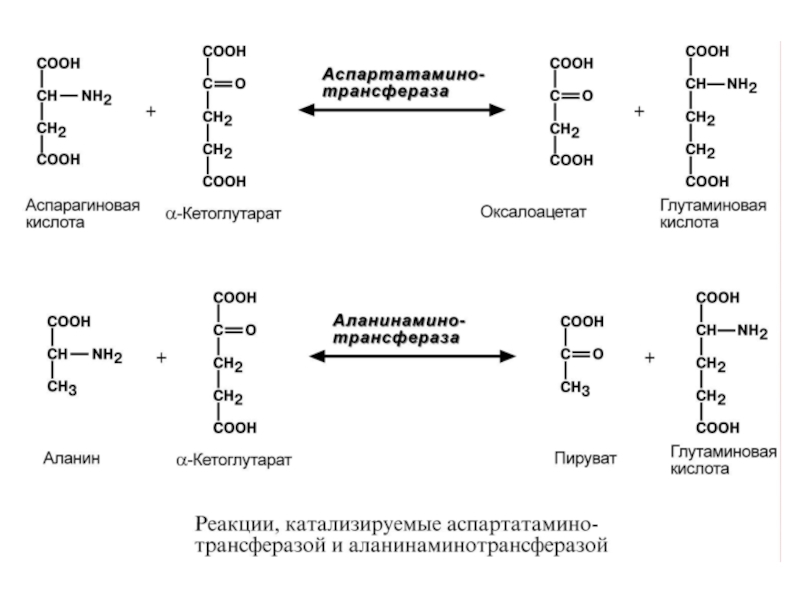
Слайд 46Аминотрансферазы
Локализованы внутриклеточно, но при нарушениях, сопровождающихся деструкцией тканей (острые и
хронические заболевания), ферменты из разрушенных клеток выходят в кровь (индикаторные
ферменты).
АсАТ – сердце (МХ), АлАТ – печень (цитопл.)
В норме какое-то количество клеток в орга-низме всегда разрушается, фон отношения активности АсАТ к активности АлАТ (коэффициент де Ритиса) равен 1,33 (≈20/15)
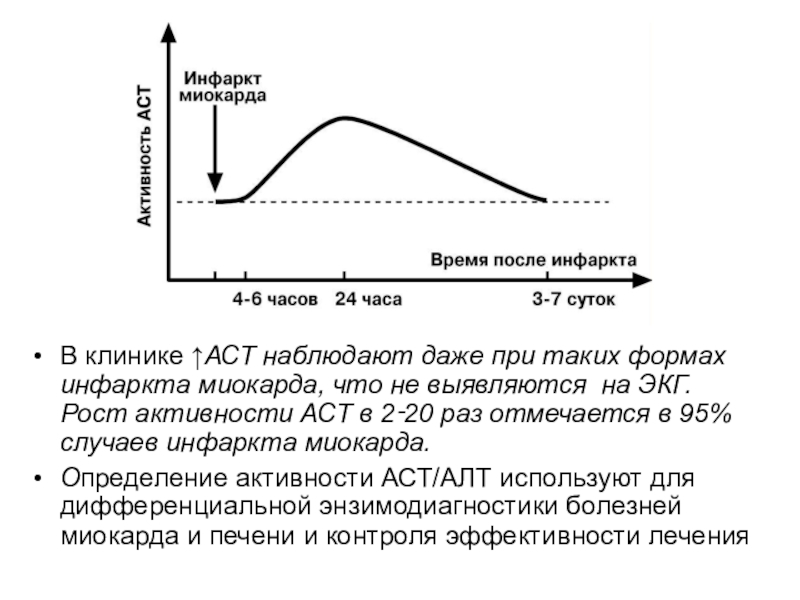
Слайд 47В клинике ↑АСТ наблюдают даже при таких формах инфаркта миокарда,
что не выявляются на ЭКГ. Рост активности АСТ в 2‑20
раз отмечается в 95% случаев инфаркта миокарда.
Определение активности АСТ/АЛТ используют для дифференциальной энзимодиагностики болезней миокарда и печени и контроля эффективности лечения
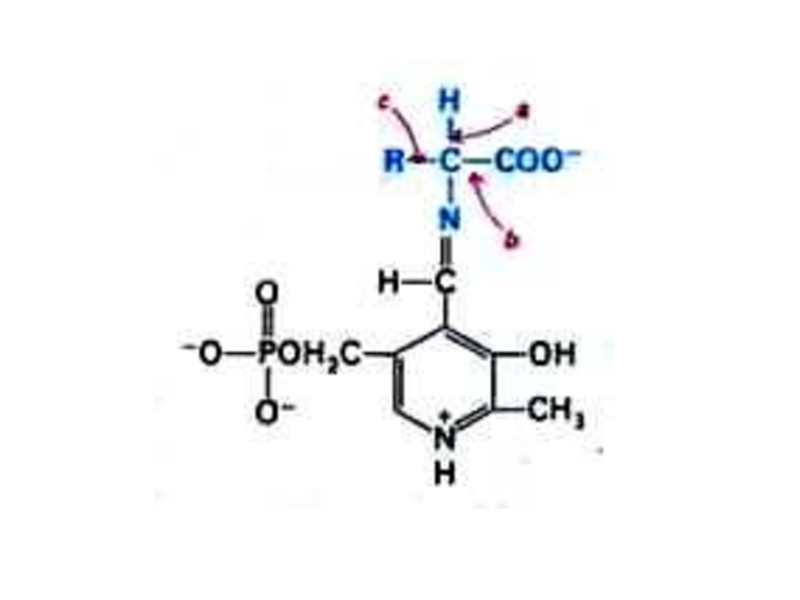
Слайд 49Декарбоксилирование аминокислот
При участии пиридоксальзависимых декарбоксилаз образуются биогенные амины.
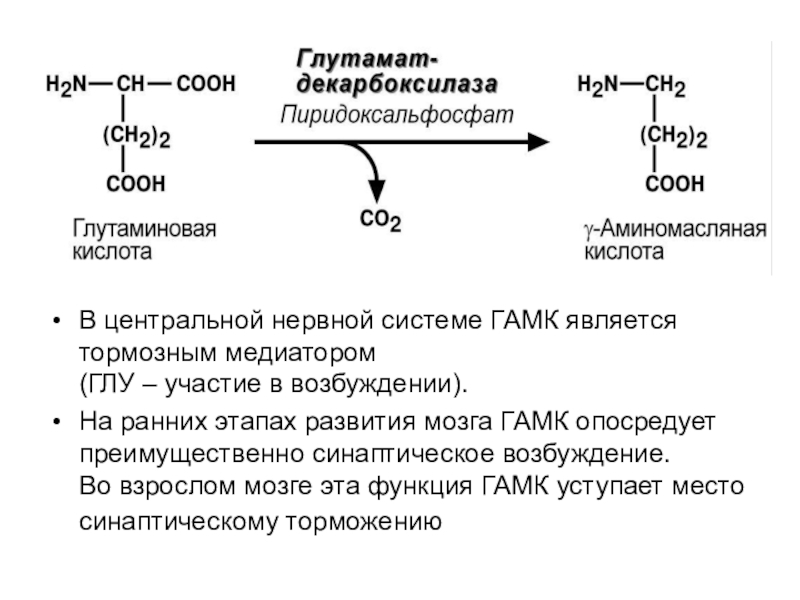
Глу
g - аминомасляная кислота
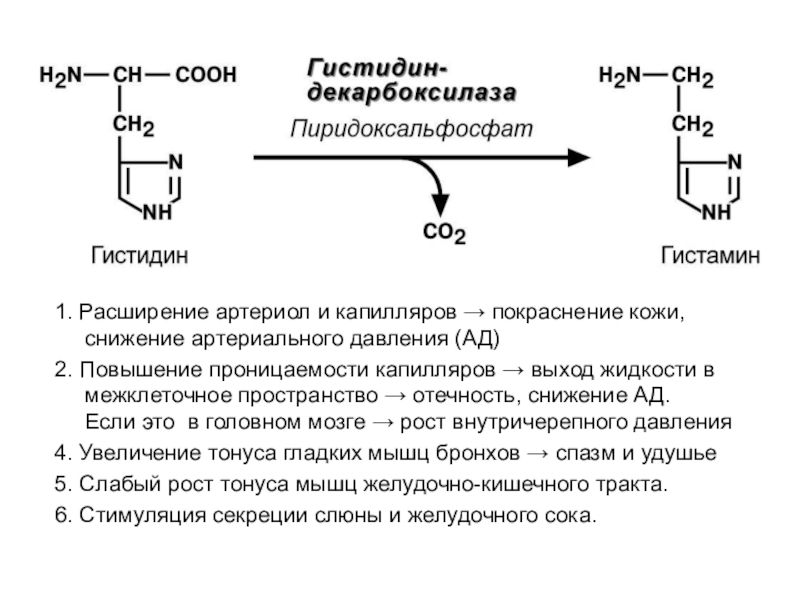
Гис гистамин
Три серотонин
Тир
дофамин
Амины быстро утилизируются оксидазами микросом.
Слайд 51В центральной нервной системе ГАМК является тормозным медиатором
(ГЛУ –
участие в возбуждении).
На ранних этапах развития мозга ГАМК опосредует преимущественно
синаптическое возбуждение.
Во взрослом мозге эта функция ГАМК уступает место синаптическому торможению
Слайд 521. Расширение артериол и капилляров → покраснение кожи, снижение артериального
давления (АД)
2. Повышение проницаемости капилляров → выход жидкости в межклеточное
пространство → отечность, снижение АД.
Если это в головном мозге → рост внутричерепного давления
4. Увеличение тонуса гладких мышц бронхов → спазм и удушье
5. Слабый рост тонуса мышц желудочно-кишечного тракта.
6. Стимуляция секреции слюны и желудочного сока.
Слайд 531. Стимулирует сокращение гладких мышц ЖКТ → повышение
перистальтики ЖКТ
2. Стимулирует сокращение гладких мышц сосудов, кроме
сосудов миокарда и скелетных мышц → повышение
артериального давления
3. Слабо увеличивает тонус гладких мышц бронхов
4. В ЦНС является тормозным медиатором
5. В периферических нервных окончаниях ведёт к возникновению
боли и зуда (например, при укусе насекомых).
Слайд 54Медиатор дофаминовых рецепторов в подкорковых образованиях ЦНС
В больших дозах:
расширяет сосуды сердца, стимулирует частоту и силу сердечных сокращений
расширяет
сосуды почек, увеличивая диурез
Слайд 55инактивация биогенных аминов
дезаминирование
наиболее активна МАО в
печени, желудке,
почках, кишечнике, нервной ткани
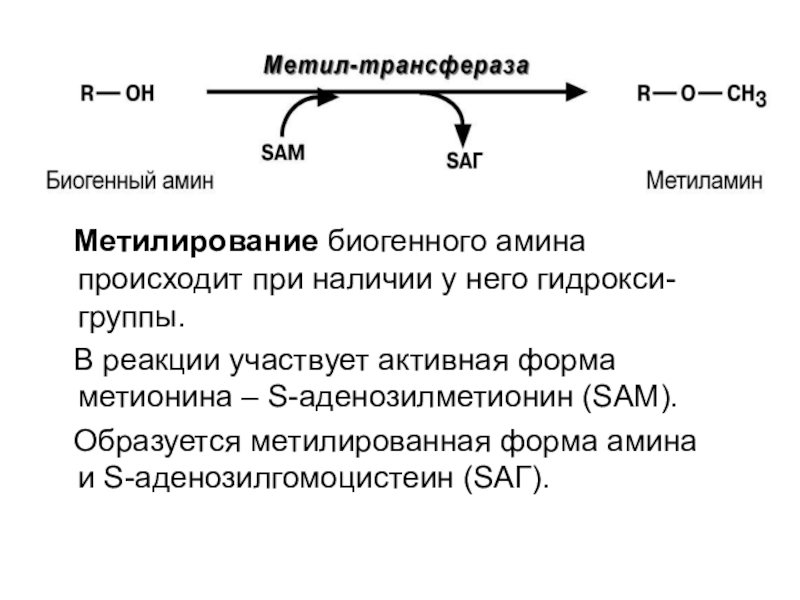
2) метилирование
Слайд 56 Метилирование биогенного амина происходит при наличии у него
гидрокси- группы.
В реакции участвует активная форма метионина
– S-аденозилметионин (SAM).
Образуется метилированная форма амина
и S-аденозилгомоцистеин (SАГ).
Слайд 59Конечные продукты белкового обмена
Аммиак образуется как результат:
дезаминирования аминокислот
окисления биогенных
аминов
утилизации азотистых оснований
Локализация образования аммиака :
- как в клетках
организма,
- так и в кишечнике с участием бактериальных ферментов.
Слайд 60АММИАК
В сутки в норме образуется до 20 г аммиака (это
4 г/л), тем не менее концентрация его
в крови всего
0,2-1,32 мг/л (12-78 мкмоль/л);
в моче 30-60 ммоль/сут.
Несколько мощных систем обезвреживания в 1000 раз снижают концентрацию аммиака!
Увеличение в крови концентрации аммиака до 0,6 ммоль/л – судороги и далее коматозное состояние.
Слайд 61Механизмы токсичности аммиака
NH3 проникает через мембраны (клеточную и митохондриальные).
Увеличение скорости
восстановительного аминирования a–кетоглутарата
снижает его участие в переаминировании и синтезе
ацетилхолина, дофамина;
снижает образование ГАМК,
снижает скорость ЦТК, угнетает цитохромоксидазу (IVкомплекс ДЦ МХ) → гипоэнергетическое состояние
Аминирование глу до глн повышает осмотическое давление глии и вызывает отёк мозга.
Увеличение содержания NН3 в крови вызывает алкалоз, повышает сродство Hb к О2……….
NH4 + нарушает трансмембранный перенос Na+ и K+ как конкурент.
Слайд 62Пути обезвреживания аммиака
1) На выведение (печень и почки):
Синтез мочевины
Аммониогенез
2)
Для транспорта и использования организмом
Образование амидов
Восстановительное аминирование
Синтез азотистых оснований (пиримидинов)
«Косвенные»
пути, реакции утилизации аминокислот без освобождения аммиака (реакции переаминирования, синтез креатина, глютатиона и др.)
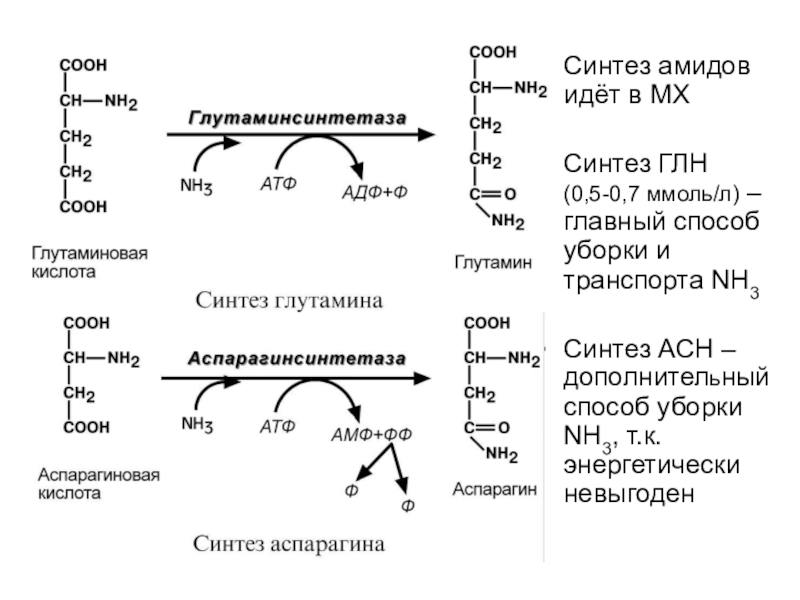
Слайд 63Образование амидов дикарбоновых кислот
Глутамин- и аспарагин-синтетазы включают аммиак в состав
амидов, образуя его временную, транспортную нетоксичную форму, более проницаемую для
мембран клеток.
Амиды вновь гидролизуются
с освобождением аммиака
в почках и печени, где происходит
его окончательное обезвреживание
Или поставляют аммиак для синтезов (например, для пиримидинов).
Слайд 64
Синтез амидов идёт в МХ
Синтез ГЛН
(0,5-0,7 ммоль/л) –
главный способ уборки и транспорта NH3
Синтез АСН – дополнительный способ
уборки NH3, т.к. энергетически невыгоден
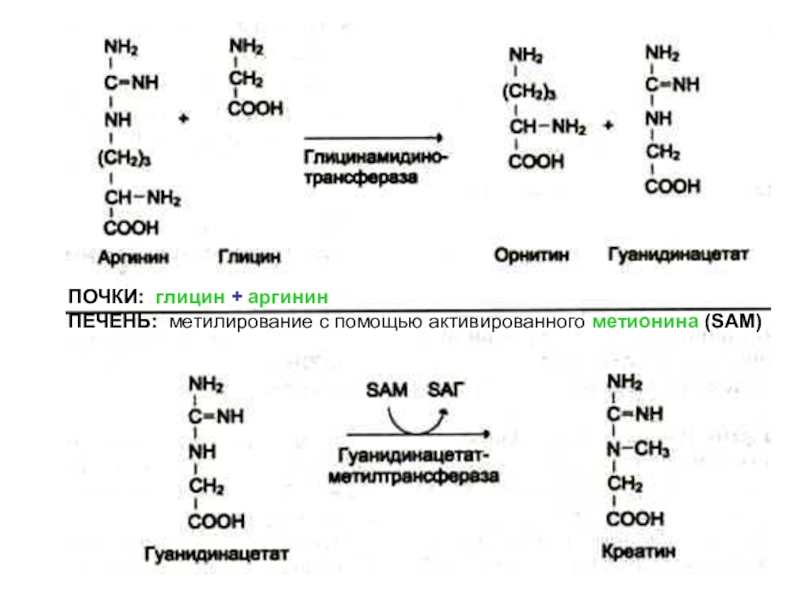
Слайд 65Синтез креатинина
Осуществляется при участии ферментов (1)почек и (2)печени
из глицина,
аргинина и метионина.
Креатин фосфорилируется до креатин~ фосфата (макроэрг!) в (3)мышцах
и мозге
Креатинфосфат гидролизуется и креатинин выводится с мочой.
Слайд 66ПОЧКИ: глицин + аргинин
ПЕЧЕНЬ: метилирование c помощью активированного метионина
(SAM)
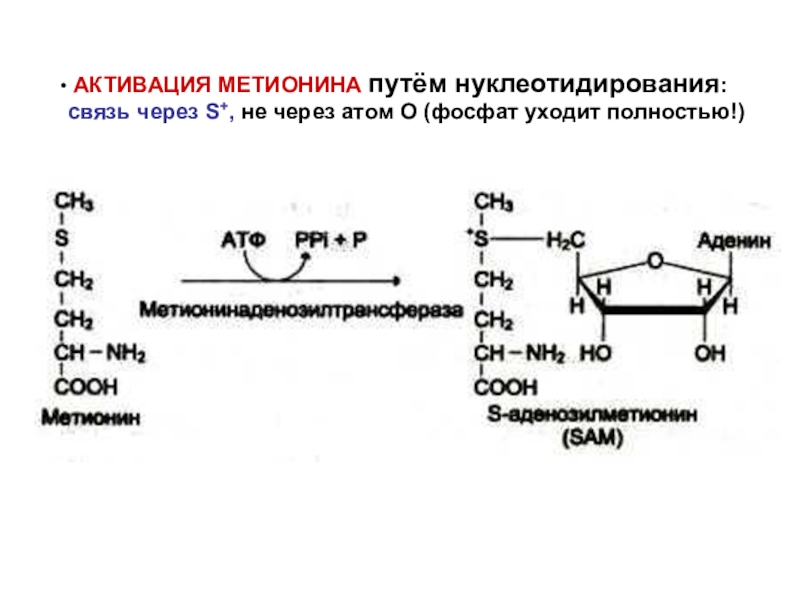
Слайд 67 АКТИВАЦИЯ МЕТИОНИНА путём нуклеотидирования:
связь через S+, не через атом
О (фосфат уходит полностью!)
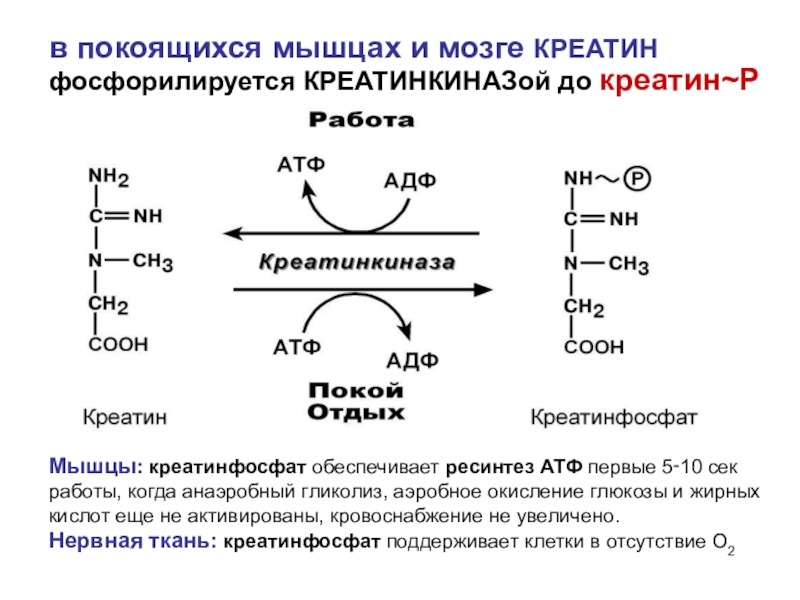
Слайд 68в покоящихся мышцах и мозге КРЕАТИН
фосфорилируется КРЕАТИНКИНАЗой до креатин~Р
Мышцы:
креатинфосфат обеспечивает ресинтез АТФ первые 5‑10 сек работы, когда анаэробный
гликолиз, аэробное окисление глюкозы и жирных кислот еще не активированы, кровоснабжение не увеличено.
Нервная ткань: креатинфосфат поддерживает клетки в отсутствие О2
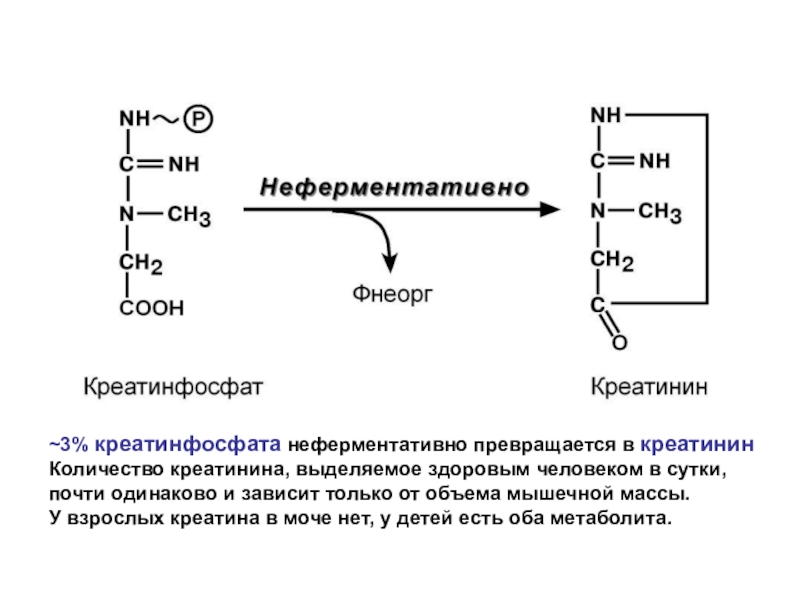
Слайд 69~3% креатинфосфата неферментативно превращается в креатинин
Количество креатинина, выделяемое здоровым человеком
в сутки,
почти одинаково и зависит только от объема мышечной
массы.
У взрослых креатина в моче нет, у детей есть оба метаболита.
Слайд 70Восстановительное аминирование кетокислот
NADFН-зависимая редуктаза восстанавливает кетокислоты (напри-мер, ОА и α-КГ
из ЦТК) до аминокислот.
Это путь образования заменимых АК
и реакция
обезвреживания аммиака
Это и механизм токсичности высоких концентраций аммиака, т.к. из ЦТК
на его детоксикацию уходят ОА и α-КГ,
и образование энергии в МХ снижается
Слайд 71Синтез азотистых оснований (пиримидинов)
Синтез пиримидинов начинается с карбамоилсинтетазной реакции:
NH3+ CO2+ ATP NH2COPO32-.
Аммиак поставляется глутамином
Синтез пуринов идёт с
участием глутамина
Слайд 72Конечные продукты азотистого обмена
У организмов разных видов с мочой выделяются
разные продукты:
Аммонийтелический тип (NH3) – рыбы;
Урикотелический тип (мочевая кислота) –
птицы, рептилии;
Уротелический тип (мочевина) – млекопитающие, амфибии.
Слайд 73Аммониогенез в почках
Глутамин в почках вновь освобождает аммиак (гидролиз глутаминазой)
Образовавшася
с помощью карбангидразы Н2СО3 диссоциирует на Н+ и НСО3-, который
идёт в кровь и с Na+ образует компонент буферной системы крови
NH3 захватывая Н+, выводится в мочу в виде аммонийной соли (чаще хлорида), так почки участвуют в поддержании кислотно-основного состояния крови.
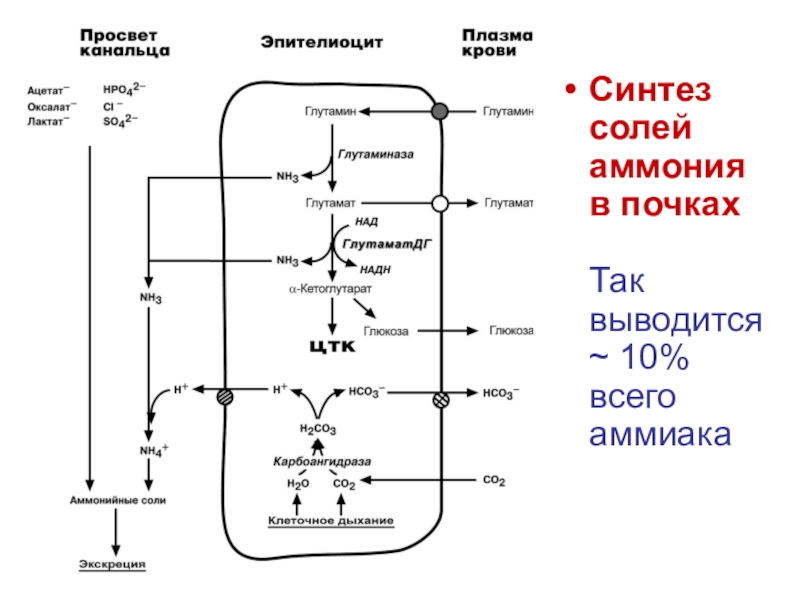
Слайд 74Синтез
солей
аммония
в почках
Так выводится ~ 10% всего аммиака
Слайд 75Орнитиновый цикл
синтеза мочевины
(цикл Кребса, Ханзеляйта)
Гепатоциты: митохондрии, аэробные условия.
АТР,
аммиак, СО2, орнитин, цитруллин, аспартат, аргинин.
Орнитиновый цикл сопряжён с реакциями
переаминирования аминокислот и циклом трикарбоновых кислот.
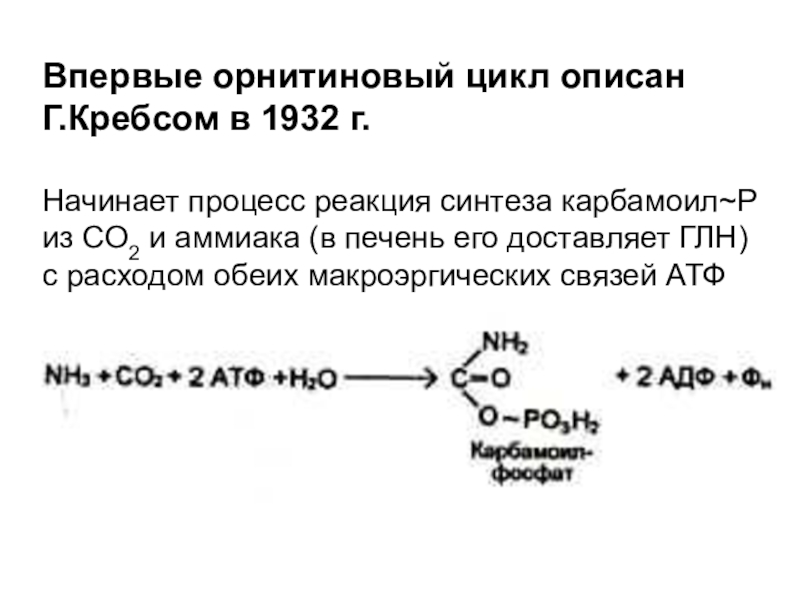
Слайд 76Впервые орнитиновый цикл описан
Г.Кребсом в 1932 г.
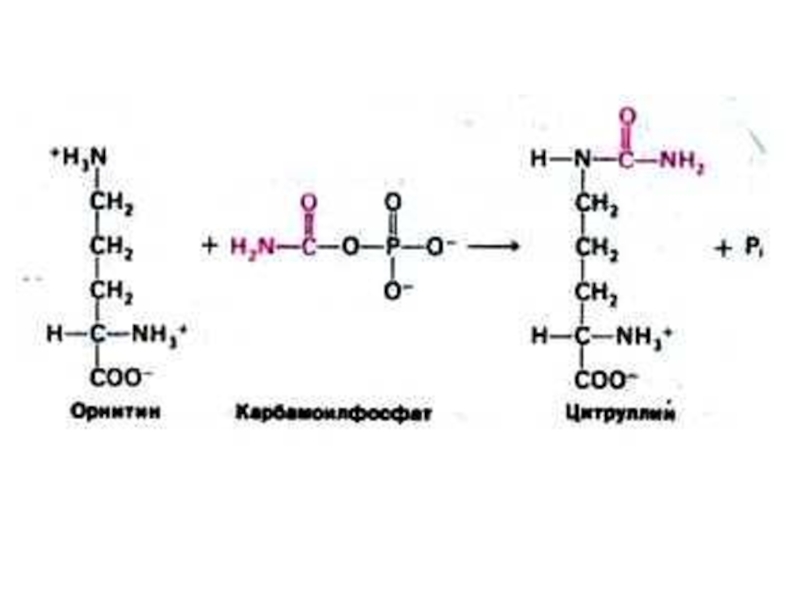
Начинает процесс
реакция синтеза карбамоил~Р
из СО2 и аммиака (в печень его доставляет
ГЛН)
с расходом обеих макроэргических связей АТФ
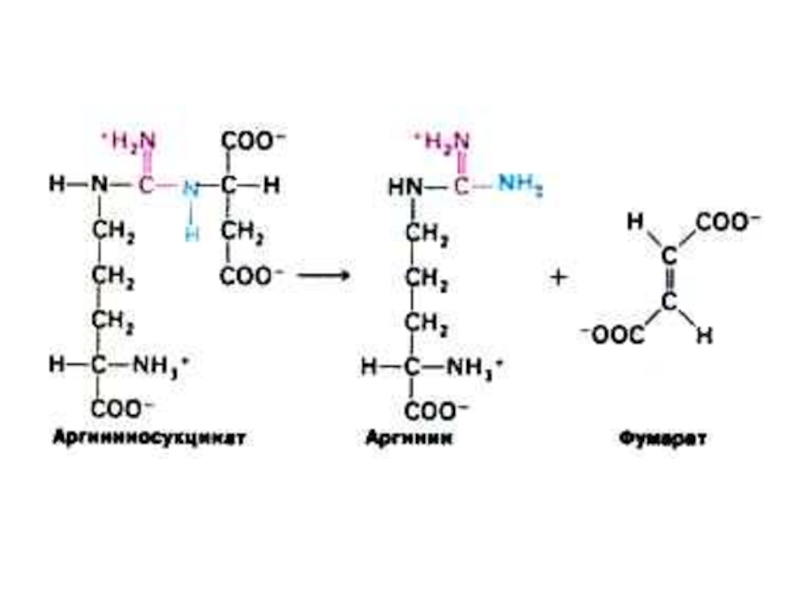
Слайд 81Источники атомов в молекуле мочевины:
N и Н – аммиак
и аспартат; С и О – углекислый газ
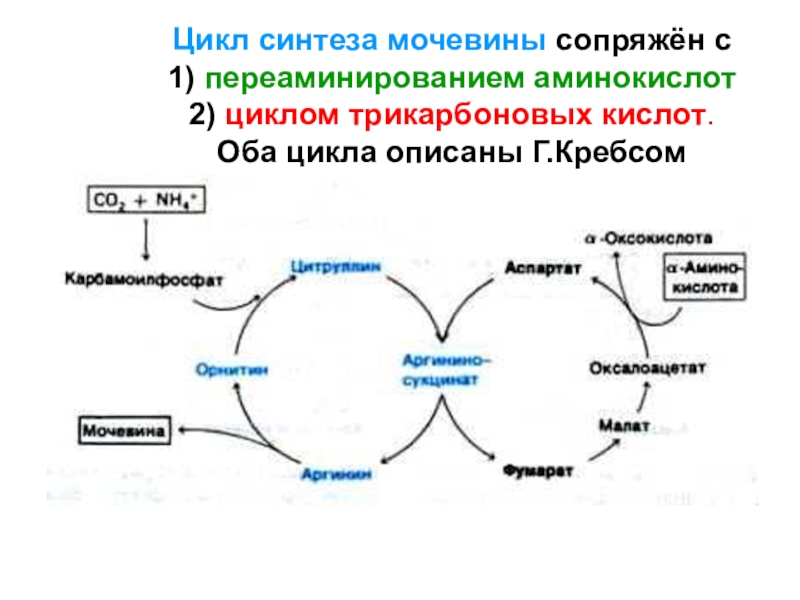
Слайд 82Цикл синтеза мочевины сопряжён с
1) переаминированием аминокислот
2) циклом трикарбоновых
кислот.
Оба цикла описаны Г.Кребсом
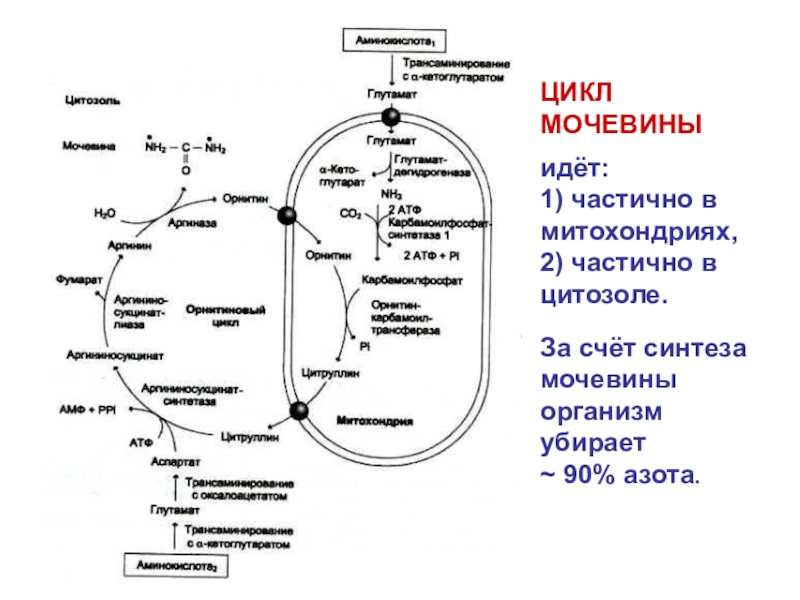
Слайд 83ЦИКЛ МОЧЕВИНЫ
идёт:
1) частично в митохондриях,
2) частично в
цитозоле.
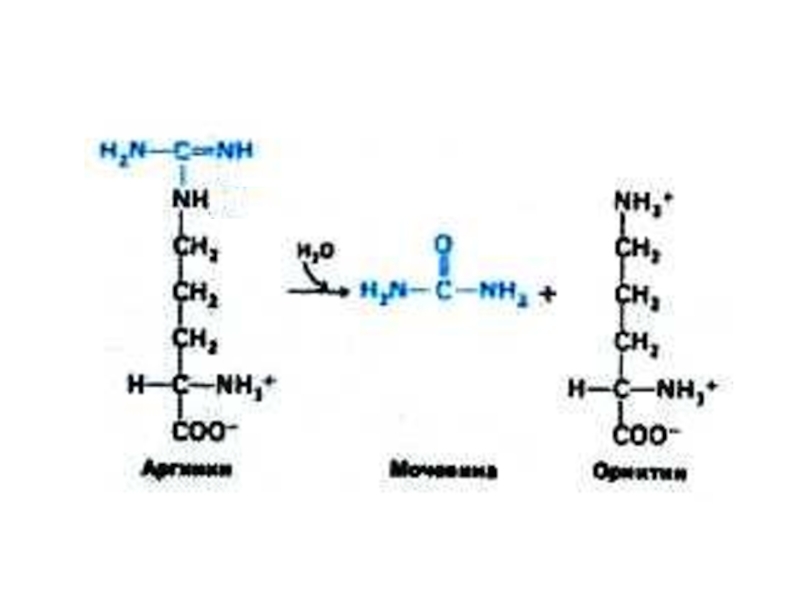
За счёт синтеза
мочевины организм
убирает
~ 90% азота.
Слайд 84Конечные продукты азотистого обмена
Фракции «остаточного» азота в крови:
Мочевина 50%
Аминокислоты
25%
Креатинин, креатин 7,5%
Пептиды, нуклеотиды, азотистые основания 5%
Мочевая кислота 4%
Аммиак и
индикан 0,5%
и другие (билирубин, холин …).
Совокупность низкомолекулярных N-содержащих веществ,
оставшихся в сыворотке крови после осаждения белков