Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОБМЕН ВЕЩЕСТВ (МЕТАБОЛИЗМ) У МИКРООРГАНИЗМОВ ТЕМА № 2 Лекция для студентов
Содержание
- 1. ОБМЕН ВЕЩЕСТВ (МЕТАБОЛИЗМ) У МИКРООРГАНИЗМОВ ТЕМА № 2 Лекция для студентов
- 2. ПЛАН ЛЕКЦИИ:Энергетические процессы у микроорганизмов.Формы энергии в
- 3. МЕТАБОЛИЗМкатаболизм –совокупность реакций, приводящих к расщеплению и
- 4. ФОРМЫ ЭНЕРГИИ В КЛЕТКЕАТФ (аденозинтрифосфат) – высокоэнергетическая
- 5. РЕАКЦИИ СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ1,3-диФГК + ADP → 3-ФГК
- 6. Брожение – окислительно-восстановительный процесс, приводящий к образованию
- 7. КДФГ-путь(2-кето-3-дезокси-6-фосфоглюконатный), путь Энтнера-Дудорова.Встречается только у микроорганизмов (в
- 8. ПУТЬ ЭМБДЕНА-МЕЙЕРГОФА-ПАРНАСАГликолиз (фруктозо-1,6-бифосфатный путь)Гексокиназа.Глюкозофосфат-изомераза.Фосфофруктокиназа.Фруктозобисфосфат-альдолаза.Триозофосфат-изомераза.глюкозаглюкозо-6-фосфатфруктозо-6-фосфатфруктозо-1,6-дифосфат3-фосфоглицериновый альдегид(ФГА)диоксиацетонфосфат(ДОАФ)
- 9. Необратимые реакции: Гексокиназная.6-фосфофруктокиназная.Пируваткиназная.Глицеральдегид-3-фосфатдегидрогеназ.Фосфоглицераткиназа.Фосфоглицеромутаза.Енолаза.Пируваткиназа.1,3-дифосфоглицерат (1,3-диФГК)3-фосфоглицерат (3-ФГК)2-фосфоглицерат (2-ФГК)фосфоенолпируват (ФЕП)пируват (ПВК)ПУТЬ ЭМБДЕНА-МЕЙЕРГОФА-ПАРНАСА
- 10. ПУТЬ ВАРБУРГА-ДИККЕНСА-ХОРЕККЕРАПентозофосфатный путьглюкозаглюкозо-6-фосфат6-фосфоглюконовая кислота6-фосфоглюконолактон2 рибулозо-5-фосфатГексокиназа.Глюкозо-6-фосфат дегидрогеназа.Глюконолактоназа.6-фосфоглюконат дегидрогеназа.
- 11. Фосфопентоза изомераза.Фосфопентоза эпимераза.ПУТЬ ВАРБУРГА-ДИККЕНСА-ХОРЕКЕРАрибозо-5-фосфатксилозо-5-фосфатглицеральдегид-3-фосфат(ФГА)седогептулозо-7-фосфатэритрозо-4-фосфатфруктозо-6-фосфатглицеральдегид-3-фосфат(ФГА)фруктозо-1,6-дифосфат
- 12. ПУТЬ ЭНТНЕРА-ДУДОРОВАКДФГ-путьглюкозаглюкозо-6-фосфат2-кето-3-дезокси-6-фосфоглюконат6-фосфоглюконатпируват (ПВК)3-фосфоглицериновыйальдегид (3-ФГА)Фосфоглюконат дегидратаза.Альдолаза.
- 13. глюкоза2 пируват (ПВК)КДФГБИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ПУТЕЙ РАСПАДА ГЛЮКОЗЫдля реакций биосинтеза
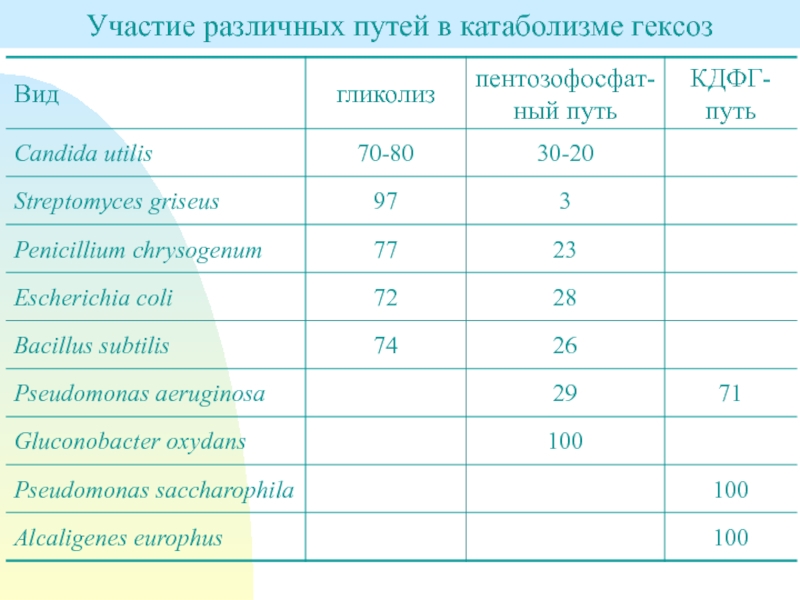
- 14. Участие различных путей в катаболизме гексоз
- 15. (1) пируват + СоА + NAD+
- 16. СПИРТОВОЕ БРОЖЕНИЕдрожжи Saccharomyces, Schizosacchsromycesбактерии рода Sarcina, Zymomonas
- 17. МОЛОЧНОКИСЛОЕ БРОЖЕНИЕмолочнокислые бактерии:порядков Lactobacillales, Bacillales класса Bacilli
- 18. ПРОПИОНОВОКИСЛОЕ БРОЖЕНИЕкласс Actinobacteria подпорядок Propionibacterineaeв основном путь Эмбдена-Мейергофа-Парнаса (гликолиз)3С6Н12О6 = 4СН3СН2COОН + 2СН3СООН+ 2СО2 + 2Н2О
- 19. БРОЖЕНИЕ, ВЫЗЫВАЕМОЕ БАКТЕРИЯМИ РОДА CLOSTRIDIUMМАСЛЯНОКИСЛОЕ И АЦЕТОНОБУТИЛОВОЕ
- 20. СМЕШАННОЕ (МУРАВЬИНОКИСЛОЕ) БРОЖЕНИЯпорядок Enterobacterialesпуть Эмбдена-Мейергофа-Парнаса (гликолиз)С6Н12О6 = СН3СН2ОН + СО2 + Н2О + ОРГ.КИСЛОТЫ:АЦЕТАТЛАКТАТСУКЦИНАТФОРМИАТ
- 21. ОБЩАЯ ХАРАКТЕРИСТИКА ДЫХАНИЯДыхание – окислительно-восстановительный процесс, идущий
- 22. ФАЗЫ АЭРОБНОГО ДЫХАНИЯПервая фаза включает серию реакций,
- 23. ЦИКЛ КРЕБСА (ЦТК)1. Пируватдегидрогеназа.
- 24. ЦИКЛ КРЕБСА (ЦТК)2. Цитратлиаза.
- 25. ЦИКЛ КРЕБСА (ЦТК)3,4. Аконитатгидратаза.
- 26. ЦИКЛ КРЕБСА (ЦТК)5. Изоцитратдегидрогеназа.6. Декарбоксилаза.56
- 27. ЦИКЛ КРЕБСА (ЦТК)7,8. α-кетоглутаратдегидрогеназа.
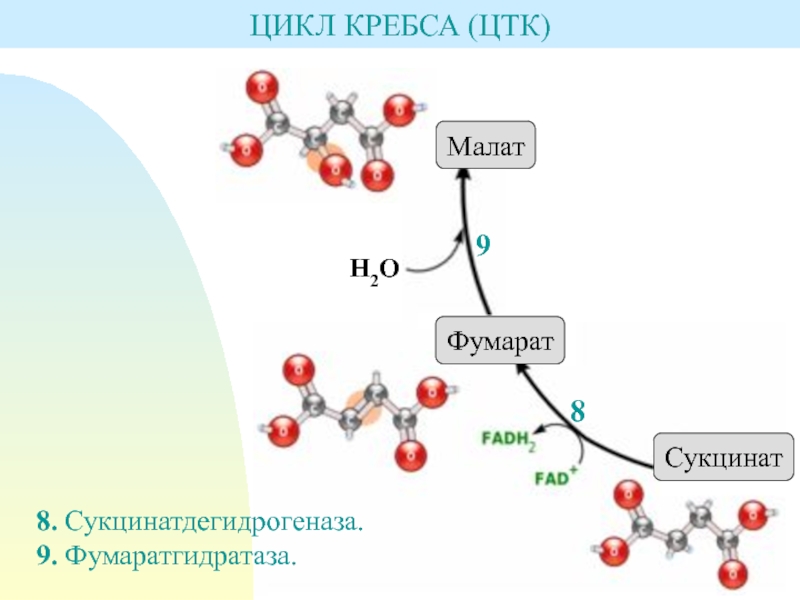
- 28. ЦИКЛ КРЕБСА (ЦТК)8. Сукцинатдегидрогеназа.9. Фумаратгидратаза.
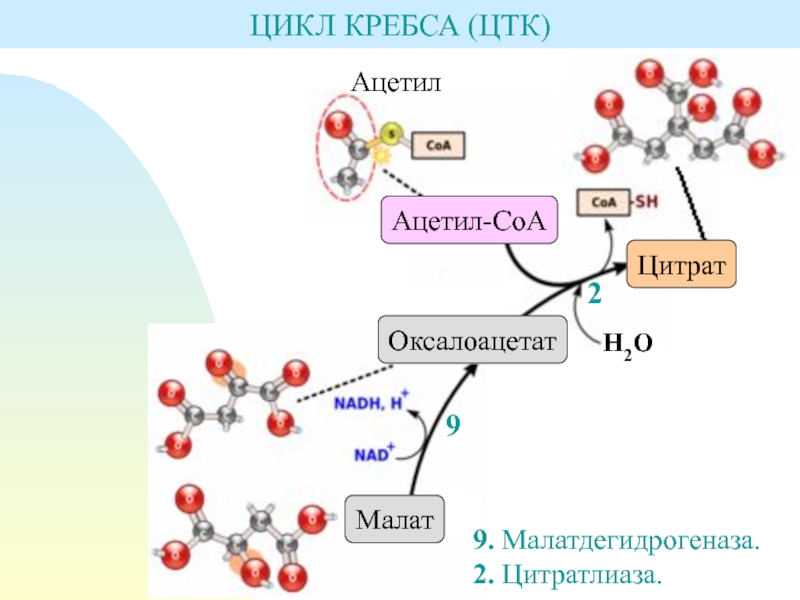
- 29. ЦИКЛ КРЕБСА (ЦТК)9. Малатдегидрогеназа.2. Цитратлиаза.92
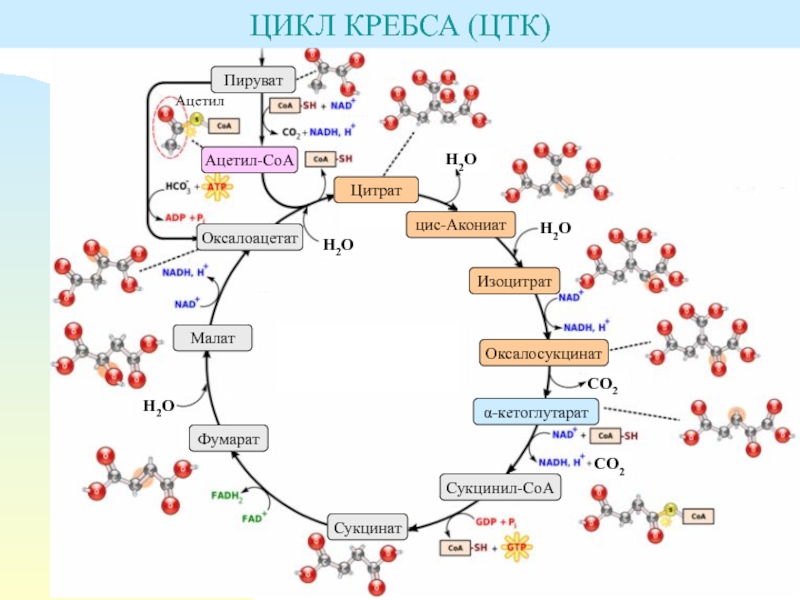
- 30. ЦИКЛ КРЕБСА (ЦТК)
- 31. ДЫХАТЕЛЬНАЯ ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВСистему транспорта электронов и
- 32. Флавопротеиды передают атомы водорода от восстановленных пиримидиновых
- 33. ДЫХАТЕЛЬНАЯ ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ
- 34. ДЫХАТЕЛЬНАЯ ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ
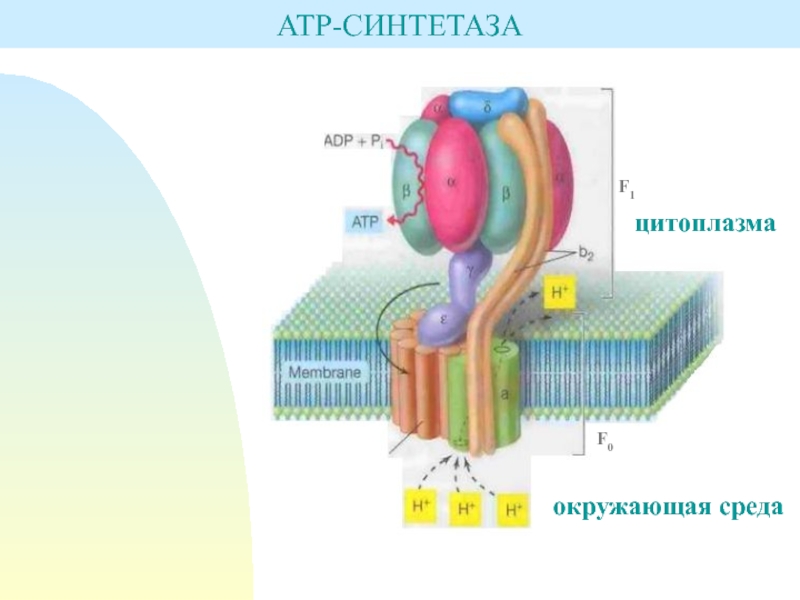
- 35. ATP-СИНТЕТАЗА
- 36. АНАЭРОБНОЕ ДЫХАНИЕ
- 37. АНАЭРОБНОЕ ДЫХАНИЕна примере денитрификации NO3-→NO2- →NO →N2O
- 38. ФОТОСИНТЕЗФотосинтез – метаболический процесс, при котором происходит
- 39. ФОТОСИНТЕТИЧЕСКИЙ АППАРАТСветособирающие пигменты, поглощающие энергию света и
- 40. ФОТОСИНТЕТИЧЕСКИЕ ПИГМЕНТЫ ЭУБАКТЕРИЙОтносятся к двум химическим классам
- 41. МЕМБРАННЫЕ СТРУКТУРЫ ФОТОСИНТЕТИЧЕСКОГО АППАРАТАСтержни из светособирающих пигментовБазальная пластинкаРеакционный центрЦПММембрана тилакоидааллофикоцианинфикоцианинфикоэритринЗЕЛЕНЫЕ БАКТЕРИИЦИАНОБАКТЕРИИ
- 42. РЕАКЦИОННЫЕ ЦЕНТРЫ.................. Циклический поток электронов— —
- 43. ФОТОСИСТЕМА IВ состав фотосистемы I входят переносчики
- 44. ФОТОСИСТЕМА IP700 – первичный донор РЦ ФС
- 45. ФОТОСИСТЕМА IIКаркас ФС II, образованном белками D1(PsbA
- 46. ФОТОСИСТЕМА I и II
- 47. РЕАКЦИОННЫЕ ЦЕНТРЫРеакционные центры I типа присутствуют у
- 48. Реакционные центры IПервичным донором электронов у зеленых
- 49. ФОТОСИНТЕТИЧЕСКАЯ РЕАКЦИЯ ФОТОТРОФОВ
- 50. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ОБМЕН ВЕЩЕСТВ (МЕТАБОЛИЗМ) У МИКРООРГАНИЗМОВ
ТЕМА № 2
Лекция для студентов специальности
020209.65 Микробиология
Слайд 2ПЛАН ЛЕКЦИИ:
Энергетические процессы у микроорганизмов.
Формы энергии в клетке.
Общая характеристика брожения.
Стадии
брожения.
Пути окисления глюкозы в пируват.
Пути окисления пирувата.
Виды брожения.
Дыхание, понятие, виды.
Аэробное
дыхание.Дыхательная цепь переноса электронов.
Анаэробное дыхание.
Фотосинтез.
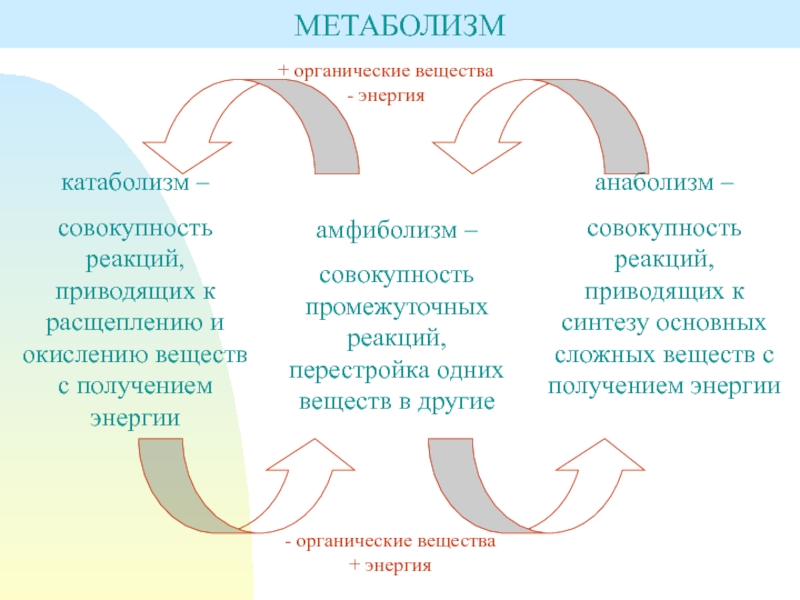
Слайд 3МЕТАБОЛИЗМ
катаболизм –
совокупность реакций, приводящих к расщеплению и окислению веществ с
получением энергии
анаболизм –
совокупность реакций, приводящих к синтезу основных сложных веществ
с получением энергииамфиболизм –
совокупность промежуточных реакций, перестройка одних веществ в другие
+ органические вещества
- энергия
- органические вещества
+ энергия
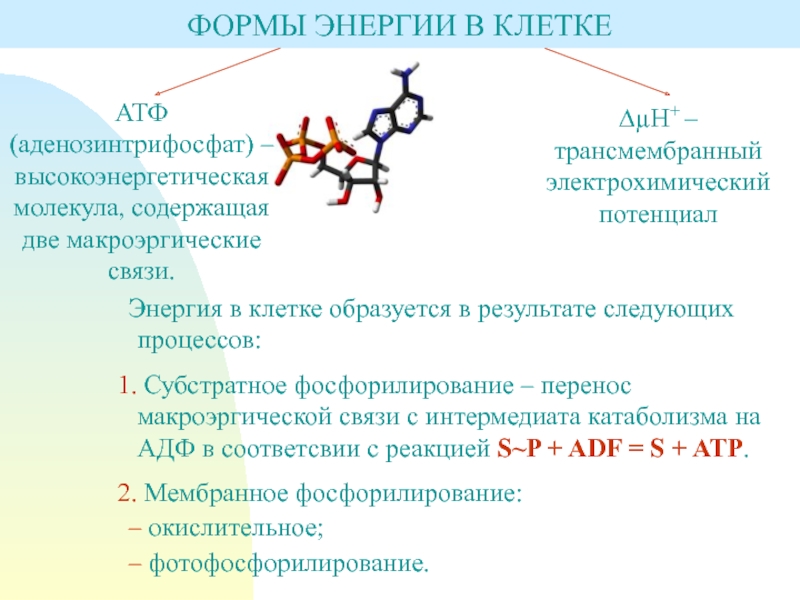
Слайд 4ФОРМЫ ЭНЕРГИИ В КЛЕТКЕ
АТФ (аденозинтрифосфат) – высокоэнергетическая молекула, содержащая две
макроэргические связи.
∆µН+ – трансмембранный электрохимический потенциал
Энергия в клетке образуется в
результате следующих процессов:Субстратное фосфорилирование – перенос макроэргической связи с интермедиата катаболизма на АДФ в соответсвии с реакцией S~P + ADF = S + ATP.
Мембранное фосфорилирование:
– окислительное;
– фотофосфорилирование.
Слайд 5РЕАКЦИИ СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ
1,3-диФГК + ADP → 3-ФГК + ATP
ФЕП +
ADP → ПВК + ATP
Ацетил~Р + АDP → ацетат +
ATPСлайд 6Брожение – окислительно-восстановительный процесс, приводящий к образованию АТФ, в котором
окислителем и восстановителем служат органические соединения, образующиеся в ходе самого
брожения.Стадии брожения:
Окислительная: разрыв углеродной цепи глюкозы и отщепление двух пар атомов водорода с образованием пирувата.
Восстановительная: восстановление пирувата до конечных продуктов, характерных для каждого вида брожения.
ОБЩАЯ ХАРАКТЕРИСТИКА БРОЖЕНИЯ
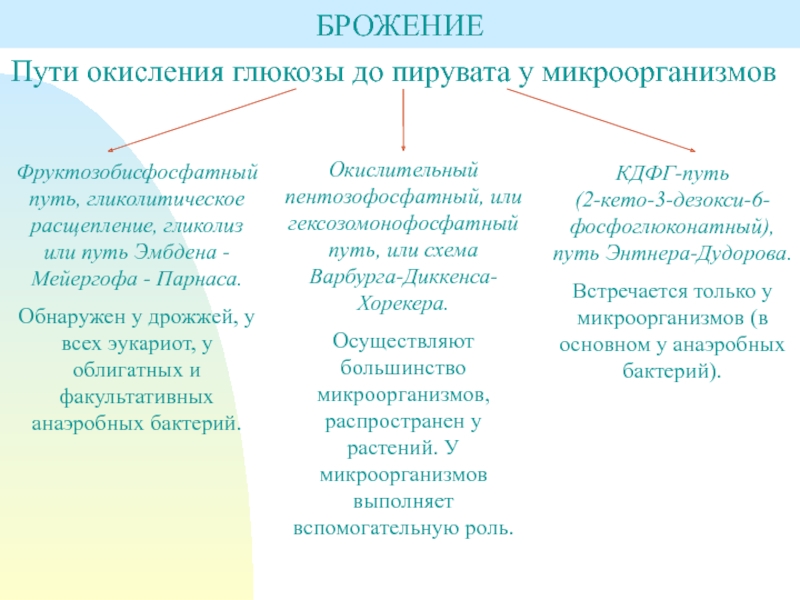
Слайд 7КДФГ-путь
(2-кето-3-дезокси-6-фосфоглюконатный), путь Энтнера-Дудорова.
Встречается только у микроорганизмов (в основном у
анаэробных бактерий).
БРОЖЕНИЕ
Пути окисления глюкозы до пирувата у микроорганизмов
Фруктозобисфосфатный путь, гликолитическое
расщепление, гликолиз или путь Эмбдена - Мейергофа - Парнаса.Обнаружен у дрожжей, у всех эукариот, у облигатных и факультативных анаэробных бактерий.
Окислительный пентозофосфатный, или гексозомонофосфатный путь, или схема Варбурга-Диккенса-Хорекера.
Осуществляют большинство микроорганизмов, распространен у растений. У микроорганизмов выполняет вспомогательную роль.
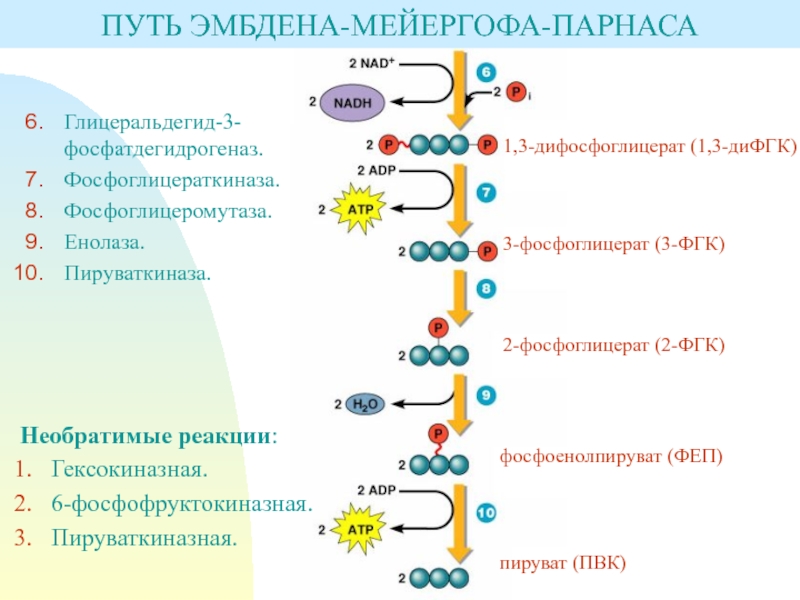
Слайд 8ПУТЬ ЭМБДЕНА-МЕЙЕРГОФА-ПАРНАСА
Гликолиз (фруктозо-1,6-бифосфатный путь)
Гексокиназа.
Глюкозофосфат-изомераза.
Фосфофруктокиназа.
Фруктозобисфосфат-альдолаза.
Триозофосфат-изомераза.
глюкоза
глюкозо-6-фосфат
фруктозо-6-фосфат
фруктозо-1,6-дифосфат
3-фосфоглицериновый альдегид
(ФГА)
диоксиацетонфосфат
(ДОАФ)
Слайд 9Необратимые реакции:
Гексокиназная.
6-фосфофруктокиназная.
Пируваткиназная.
Глицеральдегид-3-фосфатдегидрогеназ.
Фосфоглицераткиназа.
Фосфоглицеромутаза.
Енолаза.
Пируваткиназа.
1,3-дифосфоглицерат (1,3-диФГК)
3-фосфоглицерат (3-ФГК)
2-фосфоглицерат (2-ФГК)
фосфоенолпируват (ФЕП)
пируват (ПВК)
ПУТЬ ЭМБДЕНА-МЕЙЕРГОФА-ПАРНАСА
Слайд 10ПУТЬ ВАРБУРГА-ДИККЕНСА-ХОРЕККЕРА
Пентозофосфатный путь
глюкоза
глюкозо-6-фосфат
6-фосфоглюконовая кислота
6-фосфоглюконолактон
2 рибулозо-5-фосфат
Гексокиназа.
Глюкозо-6-фосфат дегидрогеназа.
Глюконолактоназа.
6-фосфоглюконат дегидрогеназа.
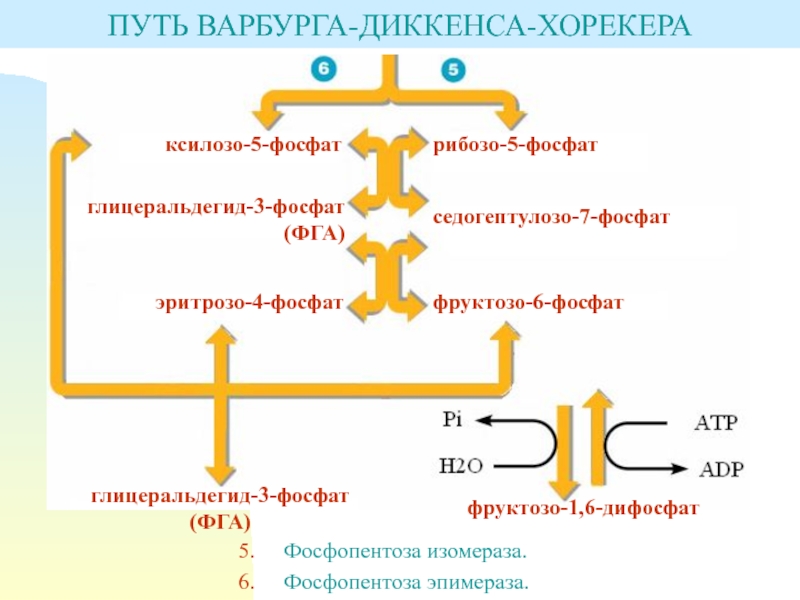
Слайд 11Фосфопентоза изомераза.
Фосфопентоза эпимераза.
ПУТЬ ВАРБУРГА-ДИККЕНСА-ХОРЕКЕРА
рибозо-5-фосфат
ксилозо-5-фосфат
глицеральдегид-3-фосфат
(ФГА)
седогептулозо-7-фосфат
эритрозо-4-фосфат
фруктозо-6-фосфат
глицеральдегид-3-фосфат
(ФГА)
фруктозо-1,6-дифосфат
Слайд 12ПУТЬ ЭНТНЕРА-ДУДОРОВА
КДФГ-путь
глюкоза
глюкозо-6-фосфат
2-кето-3-дезокси-6-фосфоглюконат
6-фосфоглюконат
пируват (ПВК)
3-фосфоглицериновый
альдегид (3-ФГА)
Фосфоглюконат дегидратаза.
Альдолаза.
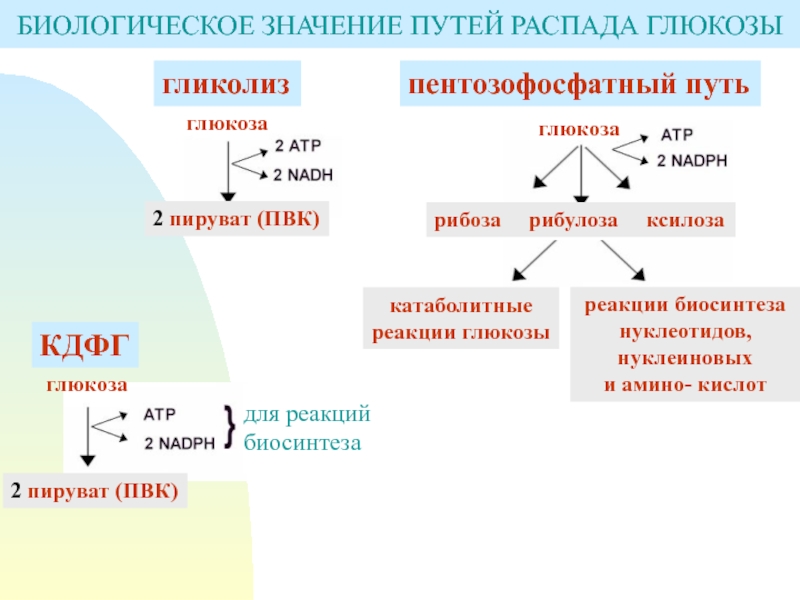
Слайд 13глюкоза
2 пируват (ПВК)
КДФГ
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ПУТЕЙ РАСПАДА ГЛЮКОЗЫ
для реакций биосинтеза
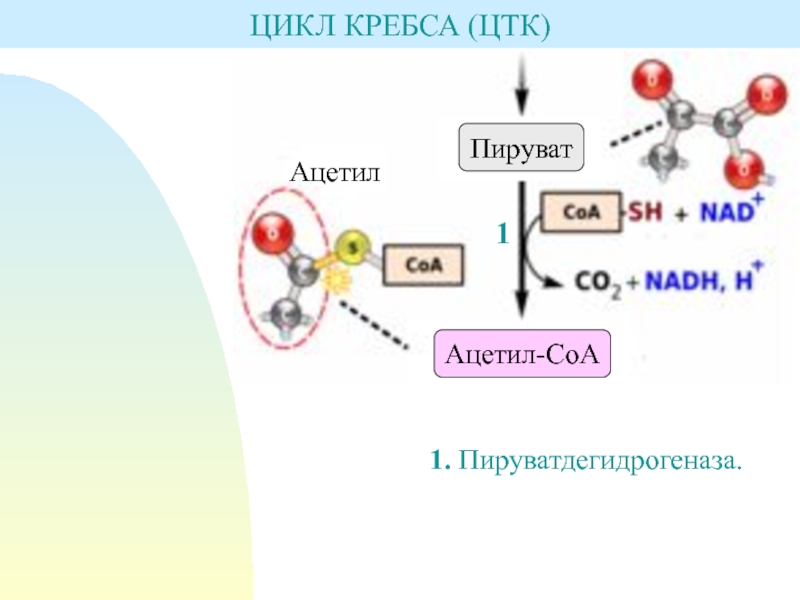
Слайд 15(1) пируват + СоА + NAD+
ацетил-СоА + NADH + СО2 + Н+
ФЕРМЕНТ: пируватдегидрогеназа
(кофермент витамин В1)характерен для аэробных микроорганизмов
(2) пируват + СоА + Fd ацетил-СоА + FdH2 + СО2
ФЕРМЕНТ: пируват:ферредоксин-оксидоредуктаза
характерен для анаэробных микроорганизмов (напр., для Clostridium)
(3) пируват + СоА ацетил-СоА + формиат
ФЕРМЕНТ: пируват:формиатлиаза
характерен для Enterobacteriaceae, фотобактерий, некоторых фототрофов
(4) пируват ацетальдегид + СО2
ФЕРМЕНТ: пируватдекарбоксилаза
характерен для дрожжей
ОКИСЛЕНИЕ ПИРУВАТА
Слайд 16СПИРТОВОЕ БРОЖЕНИЕ
дрожжи Saccharomyces, Schizosacchsromyces
бактерии рода Sarcina, Zymomonas mobilis, Zymomonas anaerobica,
Leuconostos mesenteroides, некоторые энтеробактерии и клостридии
грибы Aspergillus, Mucor, Fusarium
эффект Пастера;
часто этиловый спирт как побочный продуктв основном путь Эмбдена-Мейергофа-Парнаса (гликолиз)
С6Н12О6 = 2СН3СН2ОН + 2СО2
Слайд 17МОЛОЧНОКИСЛОЕ БРОЖЕНИЕ
молочнокислые бактерии:
порядков Lactobacillales, Bacillales класса Bacilli и класса Actinobacteria
семейства Bifidobacteriaceae
энергию получают только в процессе брожения
в основном путь Эмбдена-Мейергофа-Парнаса
(гликолиз)Гомоферментативное (молочная кислота)
С6Н12О6 = 2СН3СНОНСООН
Гетероферментативное (молочная кислота, этанол и углекислый газ)
С6Н12О6 = СН3СНОНСООН + СН3СН2ОН + 2СО2
Бифидоброжение (уксусная и молочная кислота)
2С6Н12О6 = 3СН3СООН + 2СН3СНОНСООН
Слайд 18ПРОПИОНОВОКИСЛОЕ БРОЖЕНИЕ
класс Actinobacteria подпорядок Propionibacterineae
в основном путь Эмбдена-Мейергофа-Парнаса (гликолиз)
3С6Н12О6 =
4СН3СН2COОН + 2СН3СООН+ 2СО2 + 2Н2О
Слайд 19БРОЖЕНИЕ, ВЫЗЫВАЕМОЕ БАКТЕРИЯМИ РОДА CLOSTRIDIUM
МАСЛЯНОКИСЛОЕ И АЦЕТОНОБУТИЛОВОЕ БРОЖЕНИЕ
путь Эмбдена-Мейергофа-Парнаса (гликолиз)
сахаролитические
клостридии
4С6Н12О6 = 3СН3СН2СН2СООН + 2СН3СООН + 8СО2 + 8Н2
протеолитические клостридии
АМИКИСЛОТЫ;
С6Н12О6 = nNH3 + mCO2 + zЖКнапр., АЛА + 2ГЛИ = 3СН3СООН + 3NH3 + CO2
пуринолитичиские клостридии
ПУРИНЫ; ПИРИМИДИНЫ = nNH3 + mСН3СООН + zCO2
сукцинат-этанольные клостридии
СН2СН2(СООН)2 + СН3СН2ОН = 3СН3СООН
Слайд 20СМЕШАННОЕ (МУРАВЬИНОКИСЛОЕ) БРОЖЕНИЯ
порядок Enterobacteriales
путь Эмбдена-Мейергофа-Парнаса (гликолиз)
С6Н12О6 = СН3СН2ОН + СО2
+ Н2О + ОРГ.КИСЛОТЫ:
АЦЕТАТ
ЛАКТАТ
СУКЦИНАТ
ФОРМИАТ
Слайд 21ОБЩАЯ ХАРАКТЕРИСТИКА ДЫХАНИЯ
Дыхание – окислительно-восстановительный процесс, идущий с образованием АТФ;
роль доноров водорода (электронов) в нем играют органические или неорганические
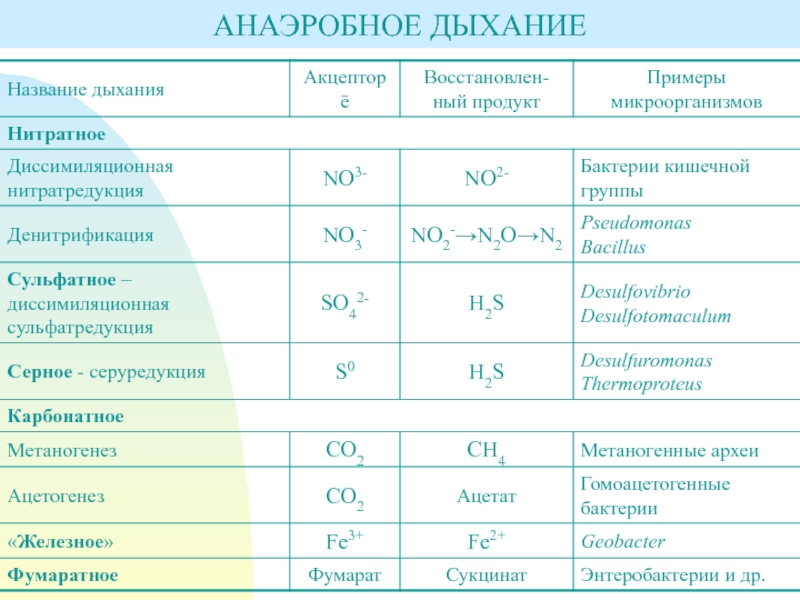
соединения, акцепторами водорода (электронов) в большинстве случаев служат неорганические соединения.Анаэробное дыхание – дыхательный процесс, при котором конечным акцептором электронов служит не молекулярный кислород, а иные соединения, такие, как нитраты, сульфаты и карбонаты.
Аэробное дыхание – дыхательный процесс, при котором конечный акцептор электронов – молекулярный кислород.
Слайд 22ФАЗЫ АЭРОБНОГО ДЫХАНИЯ
Первая фаза включает серию реакций, благодаря которым органический
субстрат окисляется до СО2, а освобождающиеся атомы водорода перемещаются к
акцепторам.Данная фаза состоит из цикла реакций гликолиза, приводящих к образованию пирувата (ПВК), и цикла реакций, известного под названием цикла Кребса, или цикла трикарбоновых кислот (ЦТК).
Вторая фаза представляет окисление освобождающихся атомов водорода кислородом с образованием АТФ и получила название окислительное фосфорилирование.
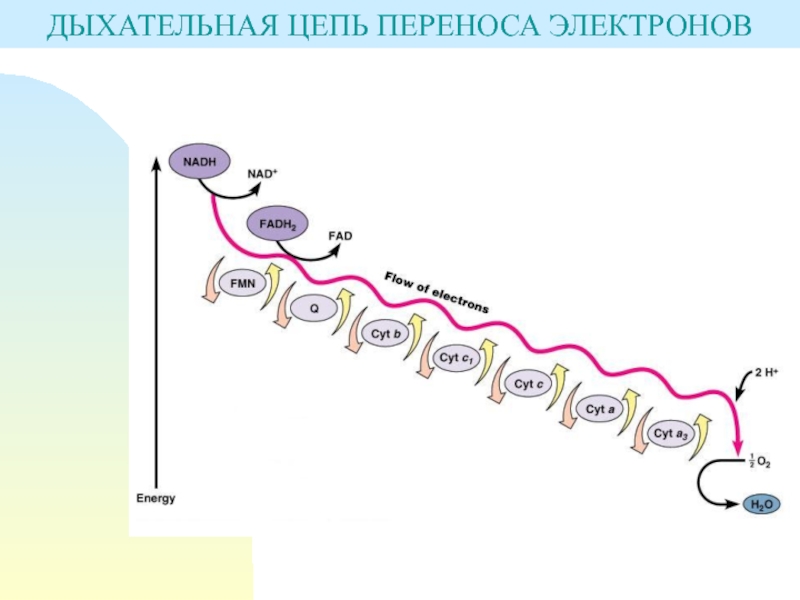
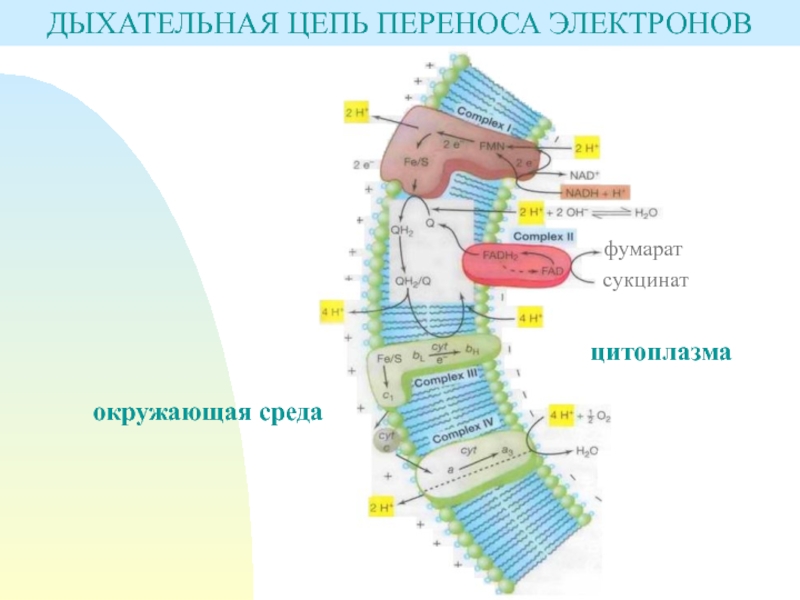
Слайд 31ДЫХАТЕЛЬНАЯ ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ
Систему транспорта электронов и протонов, отщепляющихся при
участии специфических дегидрогеназ в цикле Кребса, а затем переносящихся по
цепи переносчиков называют – дыхательная или электронтранспортная цепь.Переносчики электронов и протонов – молекулы различных групп, представляющие собой окислительно-восстановительные ферменты – флавопротеиды, хиноны и цитохромы.
Слайд 32Флавопротеиды передают атомы водорода от восстановленных пиримидиновых нуклеотидов к последующим
переносчикам дыхательной цепи.
Хиноны (убихинон или кофермент Q) представляют собой небелковые
переносчики небольшой молекулярной массы; они способны переносить водород или электроны и представляют собой промежуточные компоненты между флавопротеидами и цитохромами.Цитохромы. Данные ферменты переносят электроны. Известны цитохромы а, а3, b, с, с1 и ряд других.
ДЫХАТЕЛЬНАЯ ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ
Слайд 37АНАЭРОБНОЕ ДЫХАНИЕ
на примере денитрификации
NO3-→NO2- →NO →N2O →N2
NO3- + 2ē
+ 2Н+ → NO2- + Н2О Е: нитратредуктаза
NO2-
+ ē + Н+ → NO- + ОН- Е: NO-образующая нитратредуктаза2NO- + 2ē + 2Н+ → N2O + H2O Е: редуктаза окиси азота
N2O + 2ē + 2Н+ → N2 + H2O Е: редуктаза закиси азота
Энергию, необходимую для восстановления нитратов, микроорганизмы получают в результате окисления органических веществ.
5С6Н12О6 + 24КNO3 → 24KHCO3 + 6CO2 + 12N2 + 18H2O
Слайд 38ФОТОСИНТЕЗ
Фотосинтез – метаболический процесс, при котором происходит не только преобразование
солнечной энергии в биохимически доступную, но и синтез клеточных компонентов.
цианобактерии,
прохлорофиты,
зеленые
серные и несерные бактерии,пурпурные серные и несерные бактерии,
гелиобактерии,
глоархеи.
Слайд 39ФОТОСИНТЕТИЧЕСКИЙ АППАРАТ
Светособирающие пигменты, поглощающие энергию света и передающие ее в
реакционные центры.
Фотохимические реакционные центры, трансформирующие электромагнитную форму энергии в химическую.
Фотохимические
электронотранспортные системы, обеспечивающие перенос электронов, сопряженный с запасанием энергии в молекулах АТФ.Слайд 40ФОТОСИНТЕТИЧЕСКИЕ ПИГМЕНТЫ ЭУБАКТЕРИЙ
Относятся к двум химическим классам соединений:
Пигменты, в основе
которых лежит тетрапиррольная структура.
Основные: хлорофиллы: Chl a, Chl b (эубактерии,
цианобактерии). Вспомогательные: фикобиллипротеины: фикоэритрин (коасный пигмент) и фикоцианин (синий пигмент) (красные водоросли, цианобактерии).
Пигменты, основу которых составляют длинные полиизопреноидные цепи.
Вспомогательные: каротиноиды: β-каротин (прохлорофиты, большинство водорослей) и фукоксантин (динофлагеллят, диатомовые и бурые водоросли).
Вспомогательные пигменты: помимо участия в фотосинтезе, предохраняют хлорофилл от фотоокисления.
Слайд 41МЕМБРАННЫЕ СТРУКТУРЫ ФОТОСИНТЕТИЧЕСКОГО АППАРАТА
Стержни из светособирающих пигментов
Базальная пластинка
Реакционный центр
ЦПМ
Мембрана тилакоида
аллофикоцианин
фикоцианин
фикоэритрин
ЗЕЛЕНЫЕ
БАКТЕРИИ
ЦИАНОБАКТЕРИИ
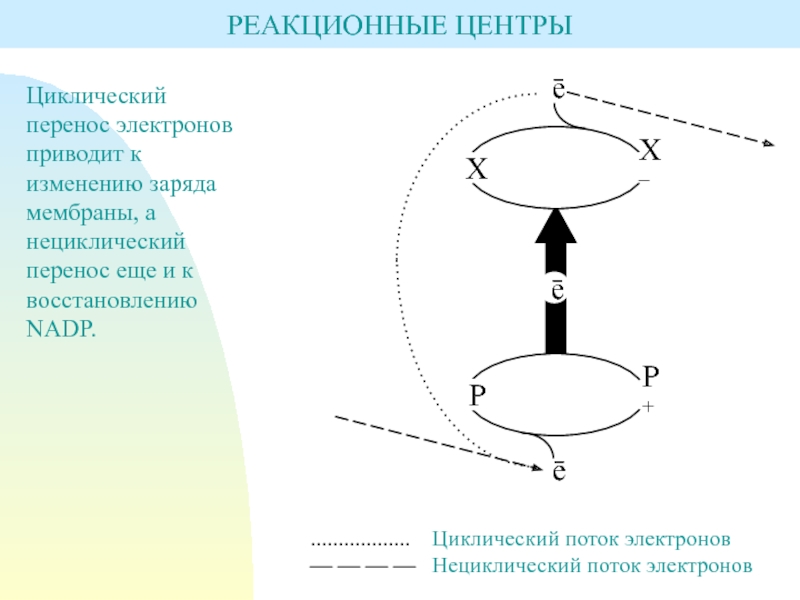
Слайд 42РЕАКЦИОННЫЕ ЦЕНТРЫ
.................. Циклический поток электронов
— — — —
Нециклический поток электронов
Циклический перенос электронов приводит к изменению заряда мембраны,
а нециклический перенос еще и к восстановлению NADP.Слайд 43ФОТОСИСТЕМА I
В состав фотосистемы I входят переносчики электронов:
- первичный донор
P700 (от англ. pigment), «димер» из двух близкорасположенных молекул Chl
a или Chl d;- первичный акцептор А0 , «мономерная» молекула Chl a;
- промежуточный акцептор А1, молекула филлохинона;
- вторичные акцепторы FX, FA, FB (ferredoxin), [FeS]-кластеры.
Слайд 44ФОТОСИСТЕМА I
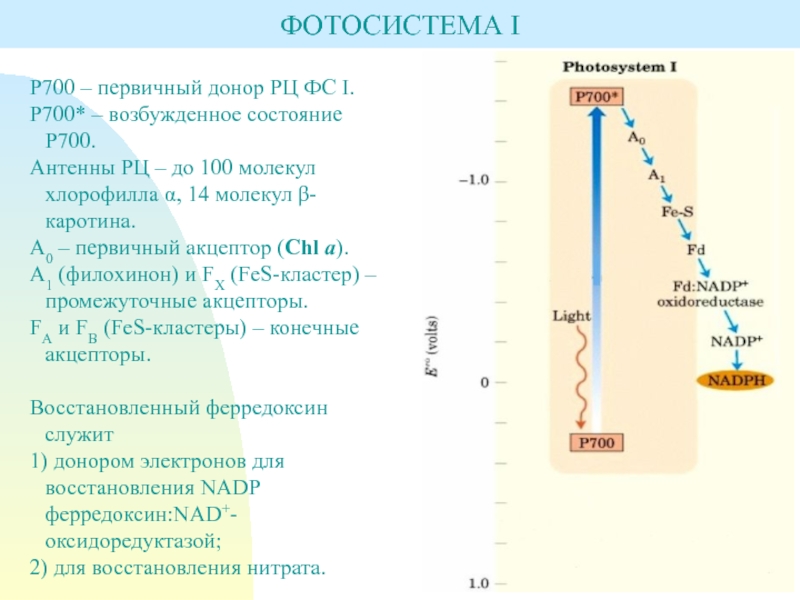
P700 – первичный донор РЦ ФС I.
Р700* –
возбужденное состояние Р700.
Антенны РЦ – до 100 молекул хлорофилла α,
14 молекул β-каротина. А0 – первичный акцептор (Chl a).
A1 (филохинон) и FХ (FeS-кластер) – промежуточные акцепторы.
FA и FB (FeS-кластеры) – конечные акцепторы.
Восстановленный ферредоксин служит
1) донором электронов для восстановления NADP ферредоксин:NАD+-оксидоредуктазой;
2) для восстановления нитрата.
Слайд 45ФОТОСИСТЕМА II
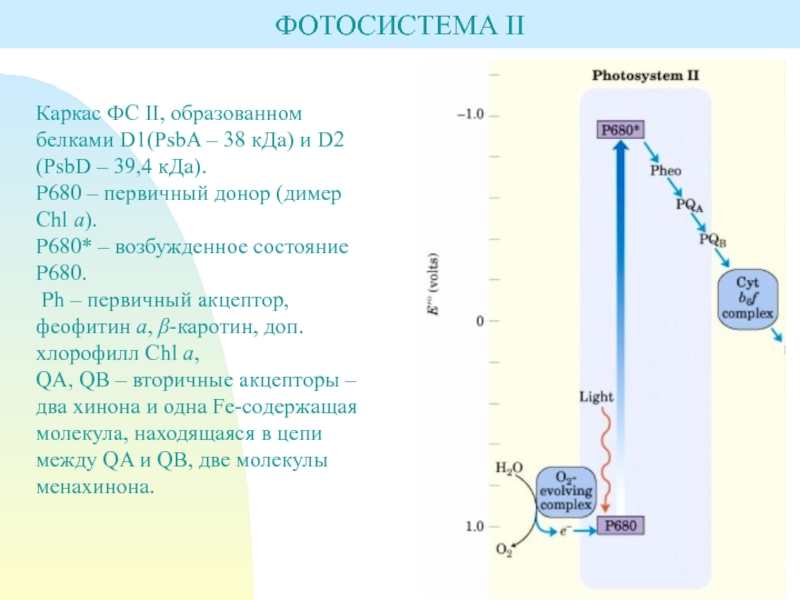
Каркас ФС II, образованном белками D1(PsbA – 38 кДа)
и D2 (PsbD – 39,4 кДа).
Р680 – первичный донор
(димер Chl а).Р680* – возбужденное состояние Р680.
Ph – первичный акцептор, феофитин а, β-каротин, доп. хлорофилл Chl а,
QA, QB – вторичные акцепторы – два хинона и одна Fe-coдержащая молекула, находящаяся в цепи между QA и QB, две молекулы менахинона.
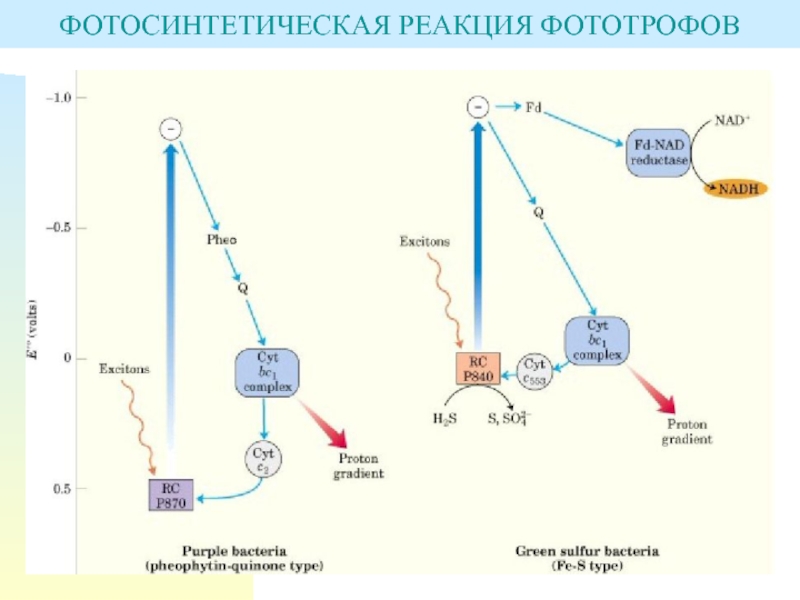
Слайд 47РЕАКЦИОННЫЕ ЦЕНТРЫ
Реакционные центры I типа присутствуют у следующих микроорганизмов:
зеленых серных
бактерий (Chlorobium limicola);
грамположительных бактерий (Неliobacillus mobilis);
цианобактерий (Аnаcystis nidulans);
водорослей;
высших растений (у
цианобактерий и фототрофов-эукариот они представляют фотосистему I). Реакционные центры II типа присутствуют у следующих микроорганизмов :
серных и несерных пурпурных бактерий (Rhodopseudomonas viridis, Chromatium vinosum);
зеленых несерных бактерий Chloroflexus;
цианобактерий;
фототрофных эукариот.
Слайд 48Реакционные центры I
Первичным донором электронов у зеленых серных бактерий служит
Р840 – димер бактериохлорофилла а, у гелиобактерий – Р798, димер
бактериохлорофилла g.Первичным акцептором (Ао) служит мономерный бактериохлорофилл В663.
Реакционные центры II
Первичным донором электронов в РЦ II у пурпурных бактерий служит специальная пара молекул, бактериохлорофилл α или бактериохлорофилл b.
Первичным акцептором электронов служит вспомогательный бактериохлорофилл α .
РЕАКЦИОННЫЕ ЦЕНТРЫ