Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Общая и неорганическая химия. Лекция 11
Содержание
- 1. Общая и неорганическая химия. Лекция 11
- 2. Магнитные свойстваАтомы или ионы, имеющие только спаренные
- 3. Магнитные свойстваАтомы или ионы, имеющие один или
- 4. Энергия ионизации Энергия (потенциал) ионизации атома Ei -
- 5. Сродство к электронуСродство атома к электрону Ee
- 6. Электроотрицательность(абсолютная электроотрицательность)Относительная электроотрицательность: F = 4Лайнус-Карл ПОЛИНГ
- 7. Слайд 7
- 8. Ряды Рихтера и триады Дёберейнера Немецкий химик
- 9. Группы элементов ГессаВ изданном в 1849 г.
- 10. Спираль Шанкуртуа или «теллурический винт»В 1862 году
- 11. Закон октавВ 1865 г. американский химик Дж.
- 12. Таблица Лотара МейераВ 1864 г. немецкий химик
- 13. Периодический закон и периодическая система химических элементов Д.И. Менделеев, 1869 г. Создание учебника «Основы химии»
- 14. Периодический закон"Свойства простых тел, а также формы
- 15. Периодическая система химических элементов Д.И. Менделеева (1873 г.)
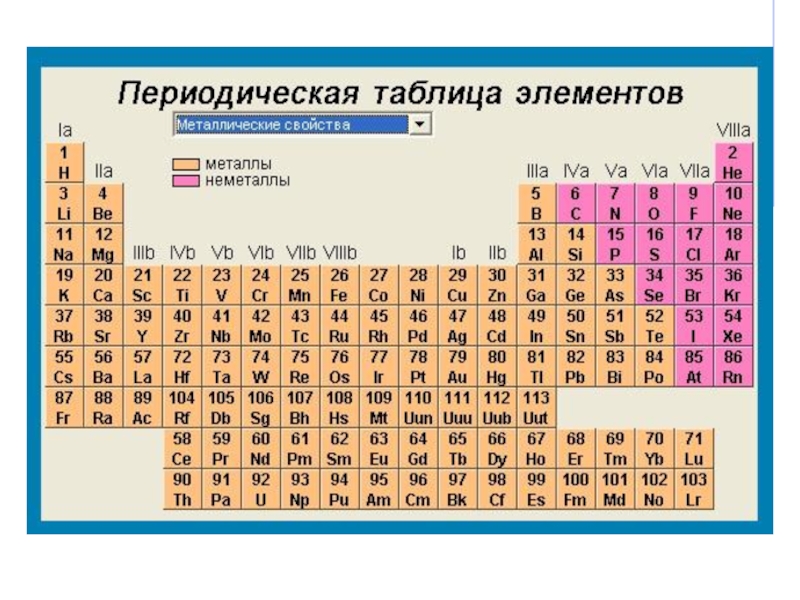
- 16. Периодическая таблица химических элементов, 2005 г.
- 17. Атомные массы и периодическая система химических элементов
- 18. Предсказание химических элементовМенделеев оставил в таблице пустые
- 19. Физический смысл порядкового номера элементаА.И. Ван ден
- 20. Периодический закон сегодня:"Свойства химических элементов, а также
- 21. Структура периодической системы элементовПериодическая система химических элементов
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Период и группаПериод – горизонтальная последовательность элементов,
- 26. Правило Клечковского (правило n + l )Заселение
- 27. Слайд 27
- 28. Слайд 28
- 29. ПериодичностьПериодичность – это повторяемость свойств химических и
- 30. Вертикальная периодичностьПовторяемость свойств химических элементов в вертикальных
- 31. Горизонтальная периодичностьГоризонтальная периодичность заключается в появлении максимальных
- 32. Горизонтальная периодичность
- 33. Диагональная периодичностьПовторяемость свойств простых веществ и соединений
- 34. Звездная периодичностьПример: свойства германия напоминают свойства его
- 35. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Общая и неорганическая химия. Лекция 11
Периодический закон и периодическая система
химических элементов.
Слайд 2Магнитные свойства
Атомы или ионы, имеющие только спаренные электроны, выталкиваются из
магнитного поля (они диамагнитны).
Примеры: He – 1s2
Be – 1s22s2
F–
– 1s22s22p6Al3+ – 1s22s22p63s03p0
Слайд 3Магнитные свойства
Атомы или ионы, имеющие один или несколько неспаренных электронов,
втягиваются в магнитное поле (они парамагнитны).
Примеры: 1H – 1s1
3Li
– 1s22s17N – 1s22s22p3
24Cr – [Ar]4s13d 5
Слайд 4Энергия ионизации
Энергия (потенциал) ионизации атома Ei - минимальная энергия, необходимая
для удаления электрона из атома:
Х = Х+ + е−;
Ei Значения Ei (кДж/моль):
H 1312,1
K 418,7 F 1680,8 He 2372
Rb 403,0 Cl 1255,5 Ne 2080
Cs 375,7 Br 1142,6 Ar 1520
Слайд 5Сродство к электрону
Сродство атома к электрону Ee – способность атомов
присоединять добавочный электрон и превращаться в отрицательный ион.
Мерой сродства
к электрону служит энергия, выделяющая или поглощающаяся при этом: Х + е− = Х− ; Ee Значения Ee (кДж/моль)
F −345,7
Cl −366,7
Br −341,6
Слайд 6Электроотрицательность
(абсолютная электроотрицательность)
Относительная электроотрицательность: F = 4
Лайнус-Карл ПОЛИНГ
(28.02.1901 – 19.08.1994)
Одна
из самых распространенных – шкала электроотрицательности Оллреда – Рохова
Слайд 8Ряды Рихтера и триады Дёберейнера
Немецкий химик И.В. Рихтер в
1793 г. расположил металлы, обладающие близкими свойствами (натрий и калий;
магний, кальций, стронций и барий) в ряд по возрастанию их атомных масс.В 1817 году немецкий химик И.В. Дёберейнер обнаружил, триады сходных по свойствам элементов: кальций – стронций – барий, литий - натрий - калий; сера - селен - теллур и хлор - бром - иод.
Слайд 9Группы элементов Гесса
В изданном в 1849 г. учебнике "Основания чистой
химии", российский химик Г.И. Гесс рассмотрел группы элементов-неметаллов: углерод −
бор − кремний; азот − фосфор − мышьяк; сера − селен − теллур и хлор − бром − иод.Считается, что именно Гесс впервые ввел в употребление понятие "группа элементов".
Герман Иванович ГЕСС (7.08.1802 - 12.12.1850)
Слайд 10Спираль Шанкуртуа или «теллурический винт»
В 1862 году французский ученый А.
Бегье де Шанкуртуа сгруппировал элементы по спирали вокруг цилиндра в
порядке возрастания атомных масс.В спирали Шанкуртуа сходные по химическим свойствам элементы расположены на образующей цилиндра, на который навертывается «спираль».
БЕГЬЕ ДЕ ШАНКУРТУА Александр-Эмиль (1819-1886)
Слайд 11Закон октав
В 1865 г. американский химик Дж. Ньюлендс предложил "закон
октав".
В таблице Ньюлендса близкие по свойствам элементы повторялись через
семь номеров.Дж. Ньюлендс впервые употребил термин «порядковый номер элемента».
Джон-Александер-Рейна НЬЮЛЕНДС (26.09.1837-29.07.1898)
1.H 8.F 15.Cl 22.Co,Ni
2.Li 9.Na 16.K 23.Rb,Cs
3.Be 10.Mg 17.Ca 24.Zn
4.B 11.Al 18.Cr 25.Y
5.C 12.Si 19.Ti 26.In
6.N 13.P 20.Mn 27.As
7.O 14.S 21.Fe 28.Se
Слайд 12Таблица Лотара Мейера
В 1864 г. немецкий химик Л.Ю. Мейер в
книге "Современные теории химии и их значения для химической статики"
опубликовал таблицу, где химические элементы были расположены в порядке увеличения их атомных масс.В эту таблицу Мейер поместил 27 элементов.
Лотар-Юлиус МЕЙЕР (19.08.1830 - 11.04.1895)
Слайд 13Периодический закон и периодическая система химических элементов
Д.И. Менделеев, 1869
г. Создание учебника «Основы химии»
Слайд 14Периодический закон
"Свойства простых тел, а также формы и свойства соединений
элементов находятся в периодической зависимости (или, выражаясь алгебраически, образуют периодическую
функцию) от величины атомных весов элементов».МЕНДЕЛЕЕВ Дмитрий Иванович (8.02.1834 - 2.02.1907)
Слайд 17Атомные массы и периодическая система химических элементов
Менделеев учитывал, что
для некоторых элементов атомные массы могли быть определены неточно (пример
– бериллий).Исключения в порядке возрастания масс атомов с ростом атомного номера (особенности изотопного состава элементов):
Cl − 35,5 Ar − 39,9 K − 39,1
Fe − 55,8 Co − 58,9 Ni − 58,7
Sb − 121,8 Te − 127,6 I − 126,9
Слайд 18Предсказание химических элементов
Менделеев оставил в таблице пустые места для не
открытых элементов (экабор, экаалюминий, экасилиций, экамарганец и двимарганец), которые были
заполнены в последующие десятилетия (элементы скандий, галлий, германий и др.)Слайд 19Физический смысл порядкового номера элемента
А.И. Ван ден Брук (1870-1926) предположил,
что "каждому элементу должен соответствовать внутренний заряд, соответствующий его порядковому
номеру".В 1913 г. это подтвердил Г. Мозли (1887-1915) своими рентгеноспектральными исследованиями.
В 1920 г. Дж. Чедвик (1891-1974) экспериментально определил заряды ядер атомов меди, серебра и платины. Было установлено, что порядковый номер элемента совпадает с зарядом его ядра.
Слайд 20Периодический закон сегодня:
"Свойства химических элементов, а также образуемых ими простых
и сложных веществ находятся в периодической зависимости от заряда ядра".
Заряд ядра атома определяет число электронов.
Электроны заселяют атомные орбитали таким образом, что строение внешней электронной оболочки периодически повторяется.
Это выражается в периодическом изменении химических свойств элементов и их соединений.
Слайд 21Структура периодической системы элементов
Периодическая система химических элементов - естественная классификация
химических элементов, являющаяся табличным выражением периодического закона Д.И. Менделеева.
Прообразом
Периодической системы химических элементов послужила таблица, составленная Д.И. Менделеевым 1 марта 1869 г.В 1870 г. Менделеев назвал систему естественной, а в 1871 г. - периодической.
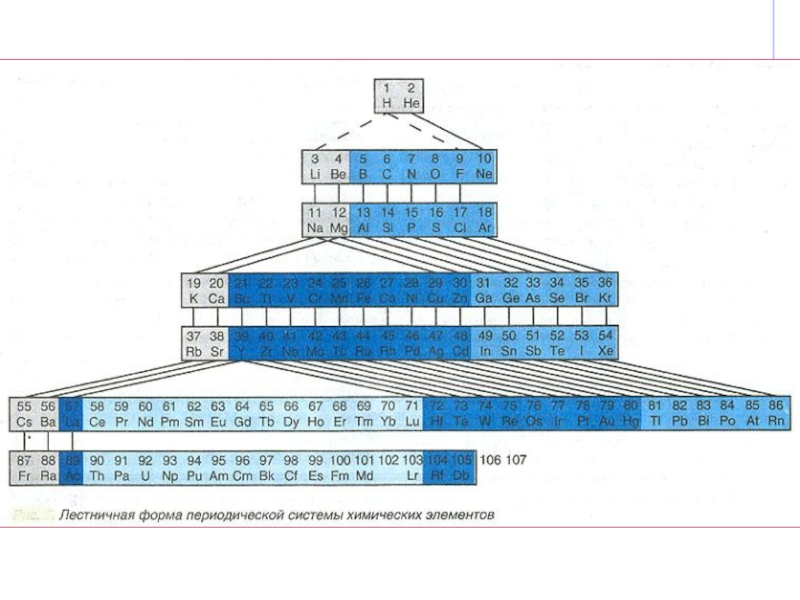
Формы периодической таблицы: короткопериодная, длиннопериодная, лестничная
Слайд 25Период и группа
Период – горизонтальная последовательность элементов, начинающаяся со щелочного
металла и заканчивающаяся благородным газом; главное квантовое число n, равное
номеру периода и характеризующее внешний энергетический уровень, у всех элементов периода одинаково.Группа элементов (в длиннопериодном варианте П.С.) – вертикальная совокупность элементов, обладающих однотипной электронной конфигурацией и определенным химическим сходством.
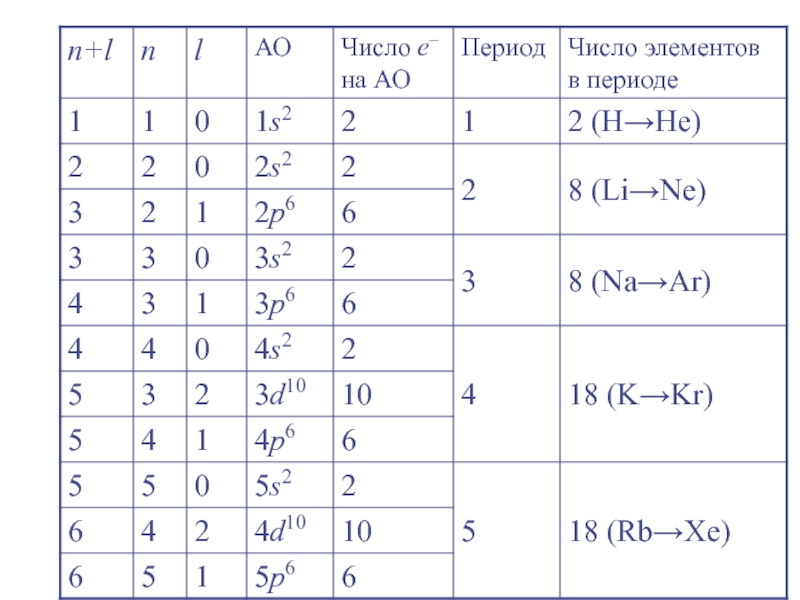
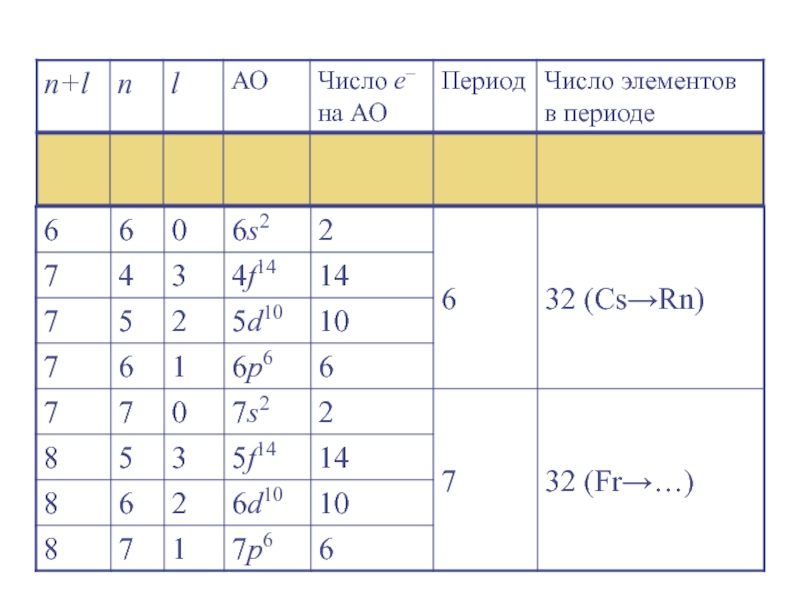
Слайд 26Правило Клечковского (правило n + l )
Заселение электронами энергетических уровней
и подуровней в нейтральных атомах в основном состоянии происходит с
увеличением порядкового номера элемента в порядке увеличения суммы главного и орбитального квантовых чисел (n + l), а при одинаковом значении (n + l) − в порядке увеличения главного квантового числа n.Слайд 29Периодичность
Периодичность – это повторяемость свойств химических и физических свойств элементов
и их соединений по определенному направлению П.С. при скачкообразном изменении
порядкового номера элементов.Виды периодичности: вертикальная, горизонтальная, диагональная, звездная.
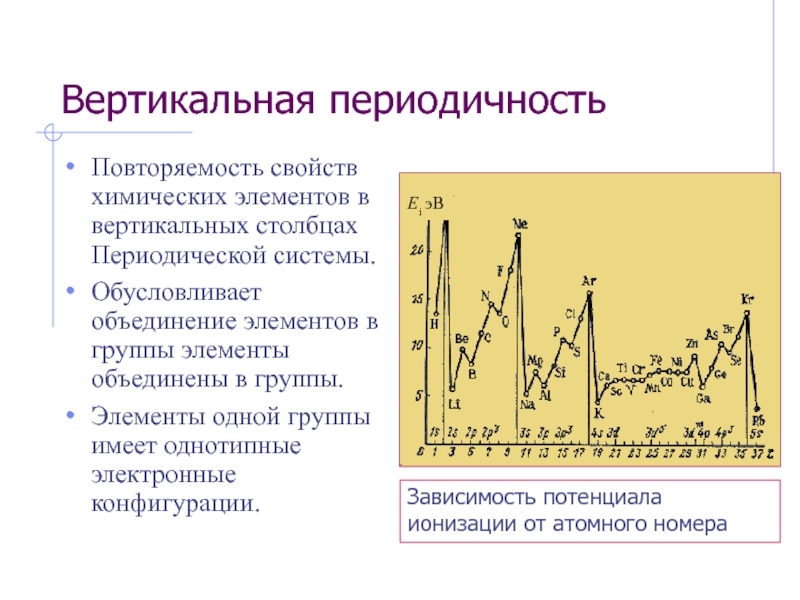
Слайд 30Вертикальная периодичность
Повторяемость свойств химических элементов в вертикальных столбцах Периодической системы.
Обусловливает
объединение элементов в группы элементы объединены в группы.
Элементы одной группы
имеет однотипные электронные конфигурации. Зависимость потенциала ионизации от атомного номера
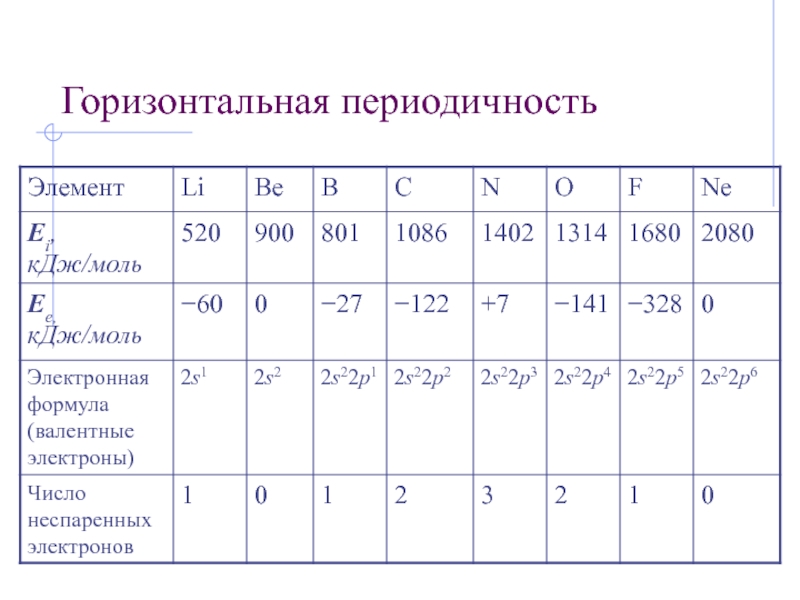
Слайд 31Горизонтальная периодичность
Горизонтальная периодичность заключается в появлении максимальных и минимальных значений
свойств простых веществ и соединений в пределах каждого периода.
Слайд 33Диагональная периодичность
Повторяемость свойств простых веществ и соединений по диагоналям Периодической
системы; связана с возрастанием неметаллических свойств в периодах слева направо
и в группах снизу вверх.Примеры: литий похож по свойствам на магний, бериллий на алюминий, бор на кремний, углерод на фосфор.
Так, литий и магний образуют много алкильных и арильных соединений, которые часто используют в органической химии.
Бериллий и алюминий имеют сходные значения окислительно-восстановительных потенциалов. Бор и кремний образуют летучие, реакционноспособные молекулярные гидриды.