Слайд 2Важнейшие функции печени
Синтез многочисленных белков и липопротеидов плазмы крови
Конъюгация билирубина
и образование желчи
Детоксикационная (защитная, барьерная) функция
Промежуточный обмен углеводов, белков, липидов,
аминокислот
Депонирование железа, В12, фолиевой кислоты и др.
Слайд 3Печеночная недостаточность –
это нарушения какой-либо из известных ее функций
В настоящее время данный термин применяется для обозначения:
как легких
изменений, улавливаемых с помощью высокочувствительных тестов (клиника отсутствует)
так и тяжелых нарушений – печеночной энцефалопатии, печеночной комой
Слайд 4ЭТИОЛОГИЯ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ
I. «ПЕЧЕНОЧНАЯ ГРУППА»
1. Гепатиты – вирусные, бактериальные, сывороточные,
вызванные простейшими и др.
2. Интоксикация гепатотропными ядами и лекарственными препаратами:
неорганические
вещества (мышьяк, фосфор, золото, селен и др.);
органические соединения (хлороформ, четыреххлористый углерод, бензол, тринитротолоул);
лекарственные препараты (антибиотики, сульфаниламиды, цитостатики, наркотики);
растительные яды (яды грибов и растений, фаллоидин).
3. Холестаз, региональные нарушения кровоснабжения печени.
4. Циррозы и дистрофии печени.
5. Злокачественные новообразования печени.
Слайд 5II. «ВНЕПЕЧЕНОЧНАЯ ГРУППА»
1. Гипоксия, различные виды шока, острая недостаточность правого
сердца.
2. Септические состояния, сопровождающиеся массивной бактериальной инвазией и гемолизом.
3. Метаболические
факторы:
гипо-, авитаминозы, дисвитаминозы;
белковая и жировая недостаточность (недостаток серосодержащих аминокислот, холина).
4. Эндокринопатология (патология паращитовидных желез, гипокортицизм).
5. Хроническая почечная недостаточность.
Слайд 6ПАТОГЕНЕЗ
В основе патогенеза развития печеночной
недостаточности лежат структурно-функциональные нарушения гепатоцитов вплоть до их цитолиза и
некроза.
В зависимости от характера этиологического фактора, различают несколько инициирующих механизмов данных нарушений:
при острых гипоксических состояниях – АТФ↓, повреждение мембраны клетки и органоидов гепатоцита (митохондрий, лизосом), вакуолизация и фрагментация эндоплазматического ретикулума, выход гидролаз лизосом → кариолизис;
ряд химических соединений обезвреживается в гладком эндоплазматическом ретикулуме оксидазой, что приводит к образованию активных кислородных радикалов (АКР) → ПОЛ → повреждение мембран эндоплазматического ретикулума → диссоциация полирибосом → нарушение биосинтеза белка.
Слайд 7ПАТОГЕНЕЗ
Для вирусной и бактериальной этиологических групп характерно:
непосредственное, прямое действие на
гепатоцит;
цитотоксическое действие сенсибилизированных лимфоцитов, аутоантител, макрофагов (аутоиммунные механизмы повреждения).
В патогенезе
печеночной недостаточности, обусловленной большой группой причинных факторов, особо подчеркивается роль активации перекисного окисления мембранных липидов. Данный механизм может быть инициирующим, а так же служить дальнейшей основой развития печеночной недостаточности.
Слайд 8
Учитывая медико-социальное значение роли вирусной патологии в развитии печеночной недостаточности,
серьезную оценку заслуживают аутоиммунные механизмы патогенеза (синтез аутоантител к различным
компонентам гепатоцитов, формирование клонов сенсибилизированных лимфоцитов).
Данные механизмы могут:
быть инициальными и основными звеньями в патогенезе;
по механизму «порочного круга» поддерживать и усиливать друг друга.
Слайд 9Основу патогенеза печеночной недостаточности составляют:
активация перекисного окисления (АКР, ПОЛ);
аутоиммунные механизмы;
гипоксические
повреждения;
непосредственное повреждение гепатоцита.
Слайд 10ВИДЫ (ТИПЫ, ФОРМЫ)
ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ
ПЕЧЕНОЧНО-КЛЕТОЧНАЯ ФОРМА недостаточности печени – наиболее
важный и часто встречающийся вид недостаточности. Клинически проявляется от снижения
тургора и пигментации кожи, гинекомастии, желтухи до печеночной энцефалопатии и комы.
ЭКСКРЕТОРНЫЙ ТИП (холестатическая форма) – характеризуется симптомами внутрипеченочного и/или внепеченочного холестаза – желтуха, брадикардия, стеаторея, дисбактериоз.
ВАСКУЛЯРНАЯ ФОРМА – выраженные нарушения кровообращения печени способствуют развитию синдрома портальной гипертензии с характерными клиническими проявлениями – коллатеральное кровообращение («голова медузы»), кровотечение из варикозно измененных венозных сплетений, асцит, спленомегалия.
Слайд 11ЭНЗИМОДИАГНОСТИКА ПАТОЛОГИИ ПЕЧЕНИ.
БИОХИМИЧЕСКИЕ (лабораторные) СИНДРОМЫ
В каждой печеночной клетке содержится несколько
тысяч ферментов. При патологии печени их уровень в крови (концентрация,
активность) может либо увеличиваться, либо уменьшаться. И вот этот, так называемый «ферментный спектр», позволяет судить о виде и степени поражения данного органа.
В клинической практике различают следующие группы ферментов печени:
I. СЕКРЕТОРНЫЕ ФЕРМЕНТЫ – секретируются гепатоцитами и в физиологических условиях выделяются в кровь, к ним относят: холинэстеразу, церуллоплазмин, про- и частично антикоагуляты. При патологии их концентрация в крови снижается.
Слайд 12ЭНЗИМОДИАГНОСТИКА ПАТОЛОГИИ ПЕЧЕНИ.
БИОХИМИЧЕСКИЕ (лабораторные) СИНДРОМЫ (продолжение)
II. ИНДИКАТОРНЫЕ ФЕРМЕНТЫ – выполняют
внутриклеточные функции. Некоторые из них (ЛДГ, АлАТ, АсАТ, альдолаза) и
в норме, в небольших количествах, обнаруживается в крови, другие же, появляются в ней только при патологии печени. Индикаторные ферменты, в зависимости от расположения в клетке разделяются на цитоплазматические (ЛДГ, АлТ), и ферменты находящиеся в различных органоидах клетки – АсАТ, малатдегидрогеназа, сорбитдегидрогеназа и др.
III. ЭКСКРЕТОРНЫЕ ФЕРМЕНТЫ – в физиологических условиях, синтезируются печенью и выделяются с желчью: щелочная фосфатаза, 5-нуклеотидаза и др.
В связи с этим, по патофизиологическому принципу, выделяют несколько биохимических (лабораторных) синдромов:
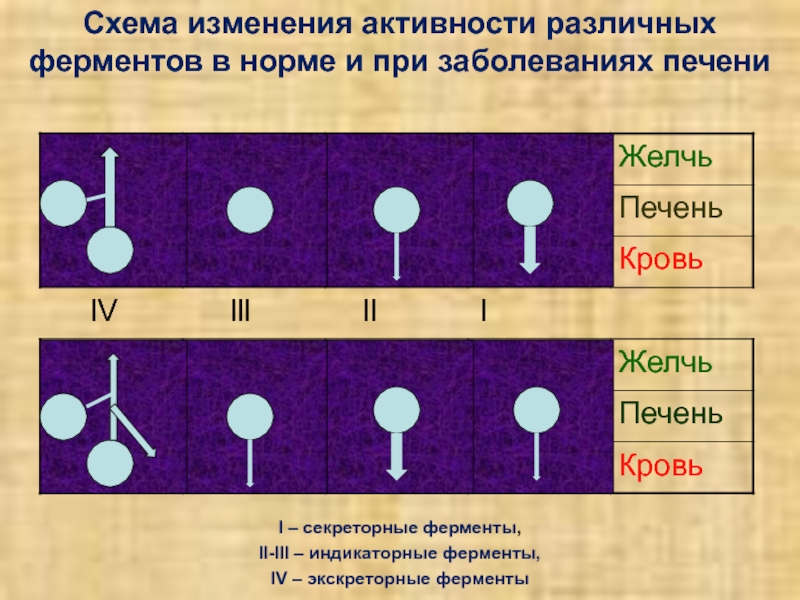
Слайд 13Схема изменения активности различных ферментов в норме и при заболеваниях
печени
l – секреторные ферменты,
ll-lll – индикаторные ферменты,
lV –
экскреторные ферменты
Слайд 14
I. СИНДРОМ ЦИТОЛИЗА (цитолитический синдром). Различают несколько видов цитолиза по
этиологическому принципу:
цитотоксический
иммуноцитолиз
гидростатический
гипоксический
опухолевый
нутриитивный
Индикаторные тесты синдрома:
выявление «ферментов повреждения» – АлТ, АсТ
, глютаматдегидрогеназы (ГлДг) и др.;
биохимические тесты – гипербилирубинемия (с преимущественным увеличением прямого билирубина), повышение концентрации в сыворотке крови вит. В12, железа.
Синдром цитолиза развивается при вирусных и других гепатитах , чаще острых, повреждениях печени (лекарственных, токсических), циррозах, быстро развивающихся и длительных надпеченочных желтухах.
Слайд 15
II. СИНДРОМ ХОЛЕСТАЗА. Его развитие обусловлено нарушением желчевыделительной функции печеночных
клеток с нарушением образования желчных мицелл и поражением мельчайших желчных
ходов.
Индикаторные тесты синдрома:
ферментные – повышение активности в крови щелочной фосфатазы, 5-нуклеотидазы;
биохимические – гиперхолестеринемия, гиперфосфолипидемия, холемия, гипербилирубинемия.
Слайд 16
III. ИММУНОВОСПАЛИТЕЛЬНЫЙ СИНДРОМ. Обусловлен сенсибилизацией клеток иммунной системы.
Индикаторные тесты синдром:
иммунологические
– повышение уровня IgG, IgМ, IgА, появление неспецифических АТ к
ДНК, митохондриям и др. компонентам клеток, изменение реакции БТЛ, изменения количества и соотношения хелперов (СД4+) и цитотоксических (СД8+) лимфоцитов;
биохимические – повышение уровня глобулинов в сыворотке крови, положительные белково-осадочные пробы (тимоловая, сулемовая).
Слайд 17
lV. СИНДРОМ ПЕЧЕНОЧНО-КЛЕТОЧНОЙ НЕДОСТАТОЧНОСТИ. Отражает изменение основных функциональных проб печени,
оценивающих поглотительную, экскреторную, метаболическую и синтетическую функции печени.
Индикаторные тесты
синдрома:
синтетическая функция – уменьшение содержания в сыворотке крови общего белка и особенно альбумина, II, V, VII факторов свертывания крови, протромбина, холестерина;
выделительная – бромсульфаленовая проба;
обезвреживающая – антипириновая и кофеиновая пробы;
метаболическая – показатели углеводного и липидного обменов.
Различают:
гепатодепрессивный синдром (малая печеночная недостаточность) – любые нарушения печени без энцефалопатии;
гепаторгию – большая печеночная недостаточность – функциональная недостаточность печени с энцефалопатией.
Слайд 18
V. ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ (синдром портального шунтирования)
Виды:
подпеченочный блок (нарушение кровотока в
системе воротной вены);
внутрипеченочный блок (диффузные заболевания печени);
надпеченочный блок (нарушение кровотока
в печеночных венах).
Индикаторные тесты синдрома:
увеличение содержание аммиака, фенолов и концентрации аминокислот в периферической крови.
VI. СИНДРОМ ПАТОЛОГИЧЕСКОЙ РЕГЕНЕРАЦИИ И ОПУХОЛЕВОГО РОСТА ПЕЧЕНИ.
Индикаторные тесты синдрома:
α-фетопротеин, щелочная фосфатаза.
Слайд 19КЛИНИЧЕСКИЕ СИНДРОМЫ НЕДОСТАТОЧНОСТИ ПЕЧЕНИ
СИНДРОМ «ПЛОХОГО», НАРУШЕННОГО ПИТАНИЯ:
ухудшение аппетита, тошнота,
непереносимость
жирной и белковой пищи,
диспепсия, боли в животе и его
вздутие, неустойчивый стул,
слабость, сухость, истончение и складчатость кожи (снижение тургора). В основе развития синдрома лежат нарушения обменных процессов.
Клинические примеры этого нарушения – печеночный запах (factor heparicus), «малиновый» язык.
Слайд 20
2. АСТЕНО-ВЕГЕТАТИВНЫЙ СИНДРОМ:
слабость, подавленное настроение, головная боль,
раздражительность, бессонница,
снижение работоспособности, кардиалгия.
3. СИНДРОМ ПСИХО-НЕВРОЛОГИЧЕСКИХ НАРУШЕНИЙ:
снижение памяти, сонливость,
неадекватное
поведение,
периодическая дезориентация во времени и пространстве.
В основе 2,3 синдромов лежит печеночная недостаточность (снижение ее обезвреживающей и барьерной функции).
Слайд 21
4. СИНДРОМ ГОРМОНАЛЬНЫХ (эндокринных) НАРУШЕНИЙ:
рано возникает снижение либидо, атрофия яичек,
бесплодие, гинекомастия,
выпадение волос, атрофия молочных желез и матки, нарушение
менструального цикла,
кожные проявления данного синдрома – образование сосудистых звездочек (телеангиоэктазии, звездчатые ангиомы) на шее, лице, плечах, груди, спине, слизистой оболочке верхнего нёба, рта, глотки.
Слайд 22
5. СИНДРОМ НАРУШЕННОЙ ГЕМОДИНАМИКИ (васкулярный синдром):
накопление вазоактивных веществ (гистаминоподобных и
др.), приводит к обширной вазодилятации, и как компенсация, к увеличению
сердечного выброса;
развитие синдрома портальной гипертензии (отечно-асцитический синдром) – его становление связано:
- со снижением синтеза альбумина,
- падением онкотического давления в крови,
- развитием вторичного гиперальдостеронизма,
- цирроза печени.
Все это приводит к асциту и развитию коллатерального кровообращения («голова медузы»).
Слайд 23
6. СИНДРОМ ГЕМОРРАГИЧЕСКОГО ДИАТЕЗА.
7. ГЕМАТОЛОГИЧЕСКИЙ СИНДРОМ – анемия (желудочно-кишечные кровотечения,
уменьшение запасов железа, Вит В12, фолатов, нарушение свертывания крови).
8.
СИНДРОМ ЖЕЛТУХИ
9. ПЕЧЕНОЧНАЯ ЭНЦЕФАЛОПАТИЯ
10.ПЕЧЕНОЧНАЯ КОМА.
Слайд 24
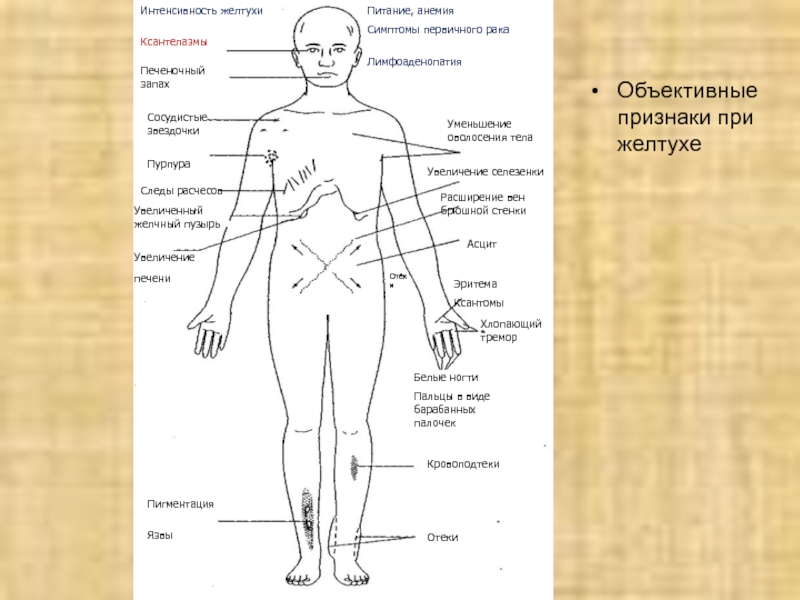
Объективные признаки при желтухе
Отеки
Кровоподтеки
Пигментация
Язвы
Белые ногти
Пальцы в
виде барабанных палочек
Питание, анемия
Симптомы первичного рака
Лимфоаденопатия
Уменьшение оволосения тела
Увеличение
селезенки
Расширение вен брюшной стенки
Асцит
Эритема
Ксантомы
Хлопающий тремор
Увеличение печени
Интенсивность желтухи
Ксантелазмы
Печеночный запах
Сосудистые звездочки
Пурпура
Следы расчесов
Увеличенный желчный пузырь
Слайд 25
Желтуха – клинико-лабораторный синдром, развивающийся вследствие появление в крови избыточного
количества билирубина и проявляющийся желтушным окрашиванием кожи, слизистых оболочек и
склер (билирубин 40 > ммоль/л)
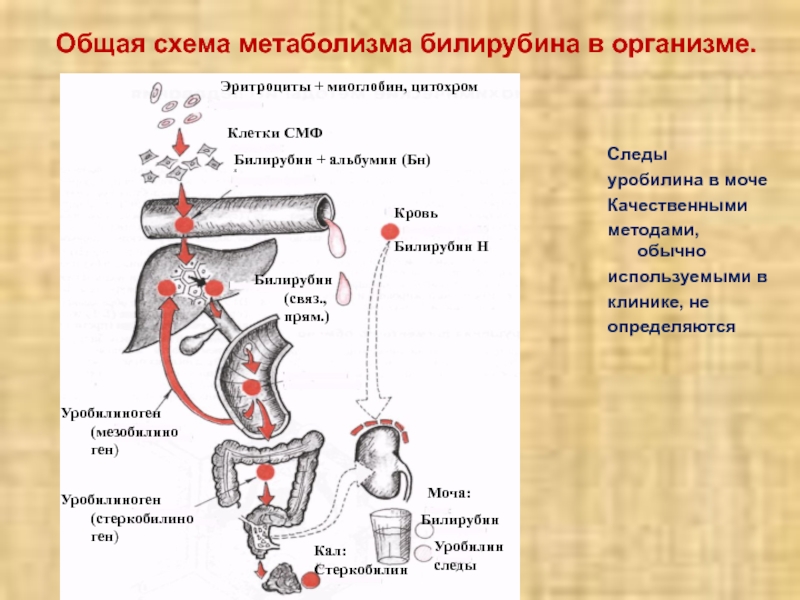
Слайд 26Общая схема метаболизма билирубина в организме.
Следы
уробилина в моче
Качественными
методами, обычно
используемыми в
клинике, не
определяются
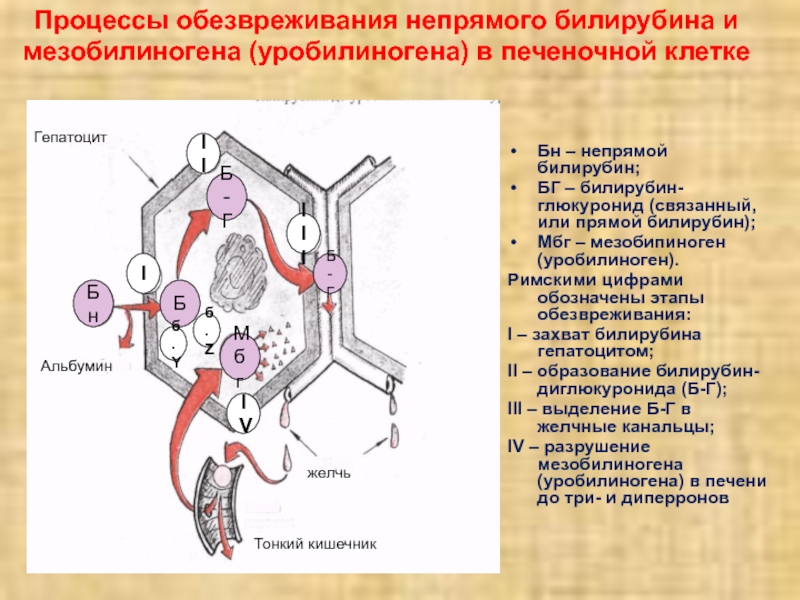
Слайд 27Процессы обезвреживания непрямого билирубина и мезобилиногена (уробилиногена) в печеночной клетке
Бн
– непрямой билирубин;
БГ – билирубин-глюкуронид (связанный, или прямой билирубин);
Мбг – мезобипиноген (уробилиноген).
Римскими цифрами обозначены этапы обезвреживания:
I – захват билирубина гепатоцитом;
II – образование билирубин-диглюкуронида (Б-Г);
III – выделение Б-Г в желчные канальцы;
IV – разрушение мезобилиногена (уробилиногена) в печени до три- и диперронов
Тонкий кишечник
желчь
Альбумин
Гепатоцит
ll
Б-Г
lll
Б-Г
Бн
l
lV
Б
МБГ
Бн
Б
Б-Г
Мбг
Б-Г
I
II
III
IV
б.Z
б.Y
Слайд 28ВИДЫ (ФОРМЫ) БИЛИРУБИНА,
ПРИСУТСТВУЮЩИЕ В ПЕРИФЕРИЧЕСКОЙ КРОВИ
1. Билирубин не конъюгированный (непрямой,
не связанный с глюкуроновой кислотой), поступает в кровь из разрушенных
эритроцитов и не эритроидных источников (миоглобин, цитохромы), связан с белком – альбумином плазмы крови (транспорт, детоксикация), не токсичен, не проходит почечный барьер.
2. Билирубин конъюгированный (прямой, связан с глюкуроновой кислотой) – не токсичен, в крови – незначительное количество, выводится почками.
3. Билирубин свободный – не связан ни с глюкуроновой кислотой, ни с альбумином плазмы: токсическая фракция, способствующая развитию билирубиновой интоксикации – билирубиновой энцефалопатии («ядерная» желтуха).
4. Мезобилиноген (уробилиноген) – всасывается из просвета тонкого кишечника в систему воротной вены и в печени метаболизируется до три- и дипирролов. В норме в крови не присутствует.
5. Стеркобилиноген – всасывается из толстого кишечника (геморроидальные вены) в систему нижней полой вены, выводится почками (уробилин).
Слайд 29
Ж
Е
Л
Т
У
Х
А
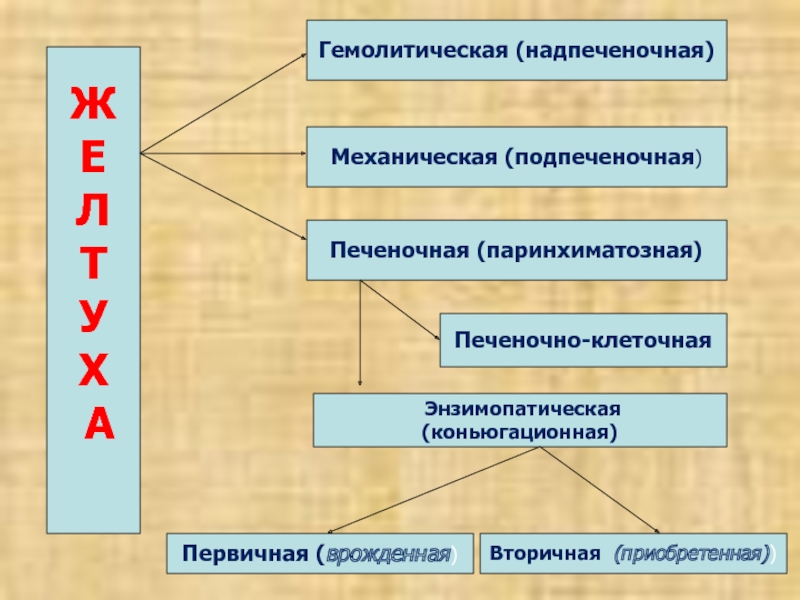
Гемолитическая (надпеченочная)
Механическая (подпеченочная)
Печеночная (паринхиматозная)
Печеночно-клеточная
Энзимопатическая (коньюгационная)
Первичная (врожденная)
Вторичная
(приобретенная))
Слайд 30
ПЕЧЕНОЧНАЯ ЭНЦЕФАЛОПАТИЯ – это комплекс потенциально-обратимых, нервно-психических изменений (с нарушением
интеллекта, неврологических рефлексов и сознания) возникающих в результате острых или
хронических заболеваний печени и/или порто-ковального шунтирования крови.
Слайд 31
І. ЭНДОГЕННЫЕ НЕЙРОТОКСИНЫ:
1) аммиак (гипераммониемия связана со снижением синтеза в
печени из нее мочевины и глютамина):
2) меркаптаны (индол, скатол и
др.) – продукты бактериального гидролиза серосодержащих аминокислот (метионин, цистеин). В норме обезвреживаются печенью
Слайд 32
3) коротко- и среднецепочные жирные кислоты, образуются из пищевых жиров
под действием кишечной флоры и при клеточно-печеночной недостаточности в результате
неполного распада жирных кислот:
4) фенолы – это группа дериватов тирозина и фенилаланина, самостоятельного значения у человека не имеет
Слайд 33
ІІ. АМИНОКИСЛОТНЫЙ ДИСБАЛАНС – характеризуется увеличением уровня ароматических аминокислот (фенилаланина,
тирозина, триптофана) и сниженем концентрации аминокислот с разветвленной боковой цепью
(валина, лейцина, изолейцина).
Слайд 34
Увеличение концентрации ароматических аминокислот в периферической крови → увеличивает их
поступление в головной мозг – его ферментные системы не могут
обеспечить их обычный метаболизм. Кроме того, фенилаланин в высоких концентрациях тормозит синтез допамина.
Все это приводит к синтезу в ЦНС, так называемых «ложных» нейротрансмиттеров, структурно-подобных, но существенно менее активных веществ, чем норадреналин и допамин – октопамин, β-фенилэтиламин. Отсюда – вытеснение истинных нейротрансмиттеров – нарушение (блок) постсинаптической передачи.
Слайд 35
ІІІ. Известна и роль тормозного нейротрансмиттера – γ - аминомаслянной
кислоты (ГАМК). Ее концентрация в головном мозге повышается вследствие:
нарушения обезвреживающей
функции печени (↓ГАМК - трансаминаза печени);
проникновение через гематоэнцефалический барьер «кишечной» ГАМК (в норме она не проходит через данный барьер).
Слайд 36
Отмечено также:
увеличение плотности ГАМК-эргических рецепторов;
уменьшение плотности рецепторов для возбуждения.
Таким образом, в основе развития печеночной энцефалопатии лежит снижение
возбудимости нейронов (- АТФ↓, активность Nа+/К+ АТФазы↓ → потенциал действия ↓, величина «+» ↓→ вплоть до «-» значений). Нарушаются коммуникационные взаимоотношения между нейронами и нервными центрами. Усилению этого механизма служат:
увеличение концентрации ГАМК и плотности тормозных рецепторов;
снижение плотности рецепторов возбуждения;
образование «ложных» нейротрансмиттеров.