Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Полимеразная цепная реакция- новый метод лабораторной диагностики
Содержание
- 1. Полимеразная цепная реакция- новый метод лабораторной диагностики
- 2. История развития методаАмериканские ученые Джеймс Д. Уотсон,
- 3. Фрэнсис Крик и Дж. Уотсон прогуливаются по кембриджскому двору. На заднем плане - часовня Кингз-колледжа
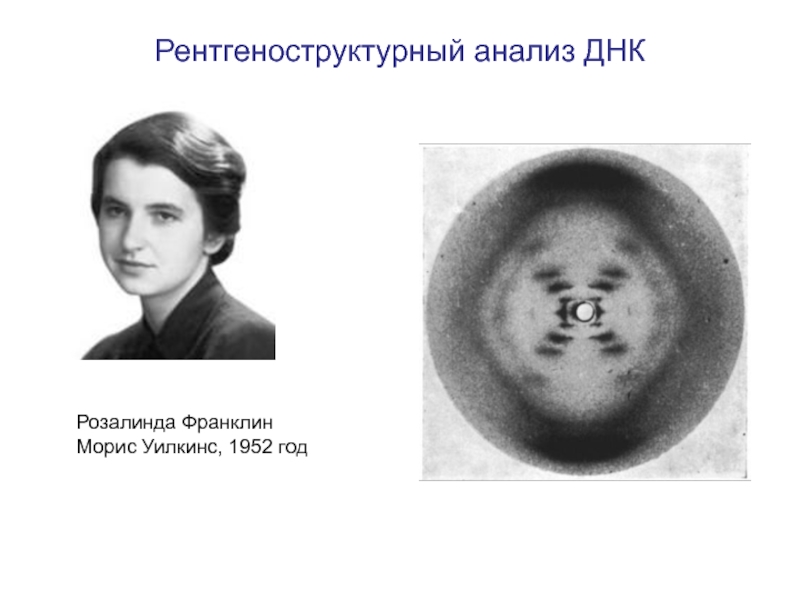
- 4. Рентгеноструктурный анализ ДНКРозалинда ФранклинМорис Уилкинс, 1952 год
- 5. Молекулярная модель ДНКДжеймс УотсонФрэнсис Крик1953 г. – статья в журнале Nature1962 г. – Нобелевская премия
- 6. Все живые клетки на
- 7. Развитие взглядов на наследственностьГиппократ(400 г. до н.э.)
- 8. Генетический код
- 9. Геном человекаОбщая длина молекулы ДНК 1, 5
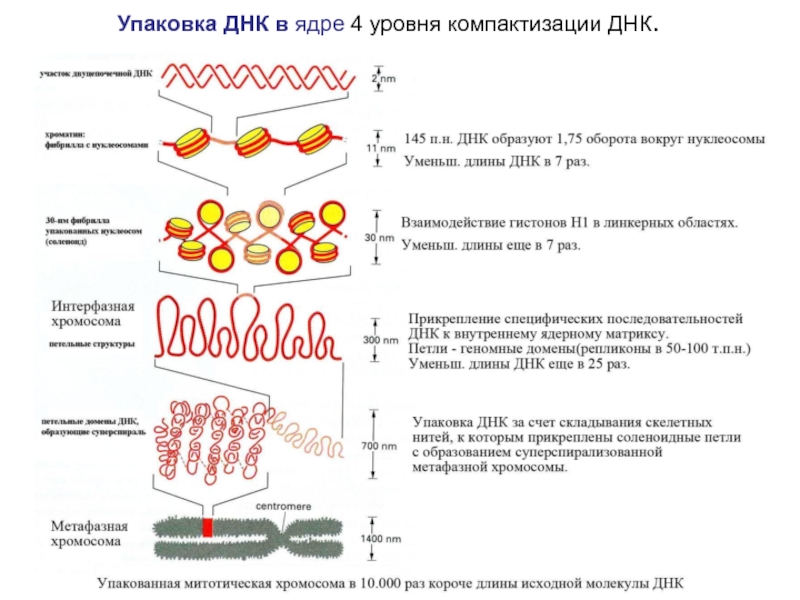
- 10. Упаковка ДНК в ядре 4 уровня компактизации ДНК.
- 11. Мутации – все изменения в последовательности ДНК,
- 12. МутагенезСпонтанный:Ошибки репликации, ошибки репарации,Ошибки рекомбинации,эндогеные метаболитыИонизирующее излучение:Электромагнитные,Рентгеновские,Гамма-,
- 13. Современная молекулярная диагностика –персонализированная медицина
- 14. Применение ПЦРМедицина, система санитарно-эпидемиологического контроля - диагностика
- 15. Генотипирования микроорганизмов:Определения наличия и количестваинфекционного возбудителяТипирование вирусов
- 16. Мультифакториальные заболевания(болезни с наследственной предрасположенностью) — развиваются
- 17. Социально значимые заболевания Согласно Постановлению Правительство
- 18. Социально значимые заболевания Выявление ИППП
- 19. Гемотрансмиссивные инфекции. HIVТак как методом ПЦР определяют
- 20. ПЦР - это ДНК-ТехнологияАлгоритм применения ПЦР (ВПЧ-теста)
- 21. ПЦР - это ДНК-ТехнологияТребование к ВПЧ-тестам для скрининга (2008 г)
- 22. Организация ПЦР-лабораторииТребования к помещениям лаборатории, выполняющей молекулярно-биологические
- 23. Зоны (помещения) ПЦР-лабораторииЛаборатория в соответствии с этапами
- 24. Устройство ПЦР-лаборатории с гибридизационо – флуоресцентный детекциейЗона
- 25. Спасибо за внимание!
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Фрэнсис Крик и Дж. Уотсон прогуливаются по кембриджскому двору. На
заднем плане - часовня Кингз-колледжа
Слайд 5Молекулярная модель ДНК
Джеймс Уотсон
Фрэнсис Крик
1953 г. – статья в журнале
Nature
1962 г. – Нобелевская премия
Слайд 6
Все живые клетки на земле хранят наследственную
информацию в виде двухцепочечной молекулы дезоксирибонуклеиновой кислоты (ДНК)
Наследственность – универсальная способность живых организмов к идентичному самовоспроизведению. Наследственная изменчивость – способность генетического материала претерпевать изменения, наследуемые в потомстве.
Основные генетические процессы:
Репликация
Репарация
Транскрипция
Рекомбинация
Мутагенез
Слайд 7Развитие взглядов на наследственность
Гиппократ(400 г. до н.э.) – Ч.Дарвин (1868):
Теория пангенезиса (прямого наследования):
1865 г. - Г.Мендель: независимое наследование фенотипических
признаков1868г.- Р.Мишер открыл дезоксирибонуклеиновую кислоту
(не связывая ее роли с наследственостью).
1902г. – У.Бэтсон : гомозигота, гетерозигота.
1909г. - В.Иогансен предложил термин “ген”.
1909г. - Т.Морган : анализ сцепленного наследования признаков.
1936г. –Н.В.Тимофеев-Ресовский – оценка размера гена при анализе мутаций,
1944г.- О.Эвери - доказательства генетической роли ДНК при трансформации бактерий
вызываемых ионизирующим излучением (переход от классической к молекулярной генетике)
1949-1951 – правила Э.Чаргаффа- правила, описывающие количественные соотношения между различными типами азотистых оснований в ДНК
1952г. А.Херши и М.Чейз - размножение бактериофагов
1953г.- Дж. Уотсон, Ф.Крик - построение молекулярной модели ДНК на основе рентгеноструктурного анализа ДНК М.Уилкинса, Р.Франклин.
Слайд 8 Генетический код -наследственная информация о всех структурных
и функциональных белках закодирована в виде последовательности нуклеотидов
Слайд 9Геном человека
Общая длина молекулы ДНК 1, 5 – 1,7 м
упакована в ядре диаметром 5 мкм.
Число нуклеотидов 3,17 х 109
Число генов 20 000 - 25 000
Кодирует синтез всех белков организма 1,2% всей ДНК
Идентичность геномов разных индивидуумов составляет 99,0 - 99,9%, Межиндивидуальная вариабельность 0,1 - 10% (полиморфизмы)
Слайд 11
Мутации – все изменения в последовательности ДНК, независимо от их
локализации и влияния на жизнеспособность особи
Мутагенез – процесс возникновения мутаций.
Мутации
– основное патогенетическое звено заболеваний. Используются как маркеры для
уточнения диагноза
определения стадии
мониторинга
выбора стратегии лечения заболевания
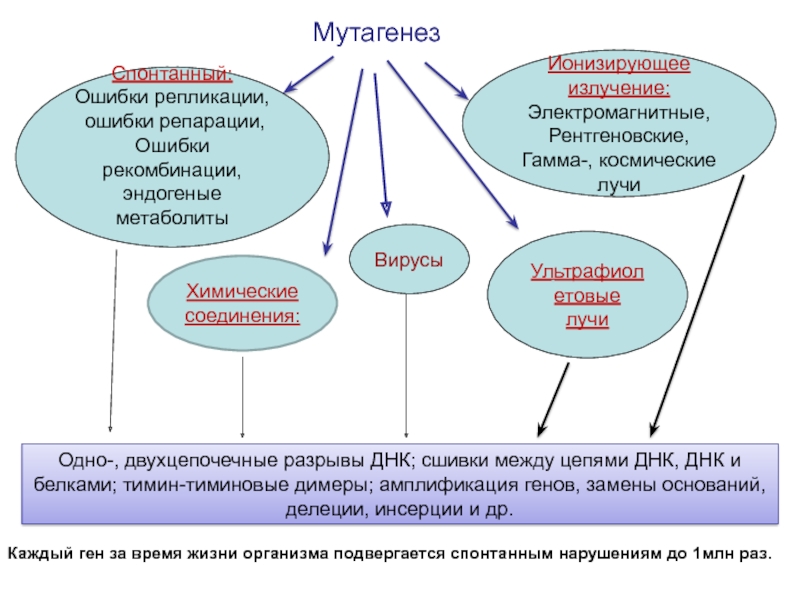
Слайд 12Мутагенез
Спонтанный:
Ошибки репликации,
ошибки репарации,
Ошибки рекомбинации,
эндогеные метаболиты
Ионизирующее излучение:
Электромагнитные,
Рентгеновские,
Гамма-, космические лучи
Ультрафиолетовые
лучи
Химические
соединения:
Одно-, двухцепочечные разрывы ДНК; сшивки между цепями ДНК, ДНК и
белками; тимин-тиминовые димеры; амплификация генов, замены оснований, делеции, инсерции и др.Каждый ген за время жизни организма подвергается спонтанным нарушениям до 1млн раз.
Вирусы
Слайд 14Применение ПЦР
Медицина, система санитарно-эпидемиологического контроля
- диагностика инфекций:
особо опасные и
социально значимые инфекции;
эпидемические инфекции;
гемотрансмиссивные инфекции;
оппортунистические инфекции;
TORCH-инфекции;
исследование биоценозов;
-
диагностика иммунных патологий- генетические исследования наследственных заболеваний
- определение ГМИ пищевых продуктов
Ветеринария и растениеводство
- инфекционные заболевания
- определение видовой принадлежности
Наука
- генная инженерия, микробиология, генетика и др.
Промышленность
- определение биологического загрязнения (санитарный контроль)
Судебная медицина
- идентификация личности
Слайд 15Генотипирования микроорганизмов:
Определения наличия
и количества
инфекционного возбудителя
Типирование вирусов (HPV)
Определение резистентности к
лекарственной терапии
(т.е. выявление чужеродной пациенту ДНК)
Генотипирования человека:
Наследственные заболевания
Онкология, онкогематология
Фармакогенетика
Предрасположенность
к заболеваниюИдентификация личности
(анализ ДНК пациента)
Необходимо различать, что ПЦР используется для
Слайд 16Мультифакториальные заболевания
(болезни с наследственной предрасположенностью) — развиваются в результате взаимодействия
определённых комбинации аллелей разных локусов и специфических воздействий факторов окружающей
среды.известно не менее 1500 генов, относящихся к различным генным сетям МФЗ:
Сердечно-сосудистые заболевания
Остеопороз
Сахарный диабет
Нарушения свертываемости крови
Бронхиальная астма
Ожирение
Нарушение иммунного ответа
Рак молочной железы
Нейродегенеративные заболевания
Слайд 17
Социально значимые заболевания
Согласно Постановлению Правительство Российской Федерации от 1 декабря
2004 г. N 715 «Об утверждении перечня социально значимых заболеваний
и перечня заболеваний, представляющих опасность для окружающих», в соответствии со статьей 41 Основ законодательства Российской Федерации об охране здоровья граждан, перечень социально значимых заболеваний включает:Туберкулез (код по МКБ-10 А 15 - А 19);
Инфекции, передающиеся преимущественно половым путем (А 50 - А 64);
Гепатит В (В 16; В 18.0; В 18.1);
Гепатит С (В 17.1; В 18.2);
Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ) (В 20 - В 24);
Злокачественные новообразования (С 00 - С 97);
Сахарный диабет (Е 10 - Е 14);
Психические расстройства и расстройства поведения (F 00 - F 99);
Болезни, характеризующиеся повышенным кровяным давлением (I 10 - I 13.9).
Слайд 18
Социально значимые заболевания
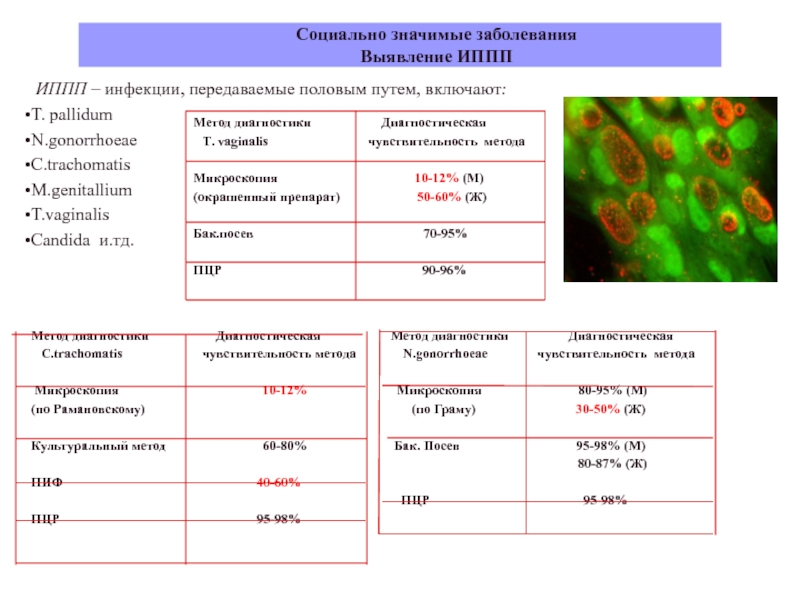
Выявление ИППП
ИППП – инфекции, передаваемые половым путем,
включают:
T. pallidum
N.gоnorrhoeae
C.trachomatis
M.genitallium
T.vaginalis
Candida и.тд.
Метод диагностики
Диагностическая Метод диагностики Диагностическая C.trachomatis чувствительность метода N.gоnorrhoeae чувствительность метода
Микроскопия 10-12% Микроскопия 80-95% (М)
(по Рамановскому) (по Граму) 30-50% (Ж)
Культуральный метод 60-80% Бак. Посев 95-98% (М)
80-87% (Ж)
ПИФ 40-60%
ПЦР 95-98%
ПЦР 95-98%
Метод диагностики Диагностическая
T. vaginalis чувствительность метода
Микроскопия 10-12% (М)
(окрашенный препарат) 50-60% (Ж)
Бак.посев 70-95%
ПЦР 90-96%
Слайд 19Гемотрансмиссивные инфекции. HIV
Так как методом ПЦР определяют не антитела к
продуктам генов ВИЧ, а непосредственно гены, он незаменим при диагностике
ВИЧ-инфекции:В серонегативный период
Исследовании банков крови и препаратов из крови
При неопределенных результатах ИФА
У детей, рожденных ВИЧ-инфицированными матерями (персистенция материнских антител у ребенка может достигать 15 мес.)
При одновременной диагностике множественных инфекций, встречающихся при СПИДе
При дифференциальной диагностике между ВИЧ-1, ВИЧ-2 и другими вирусными заболеваниями,
При испытаниях на животных химиопрепаратов и вакцин против СПИДа.
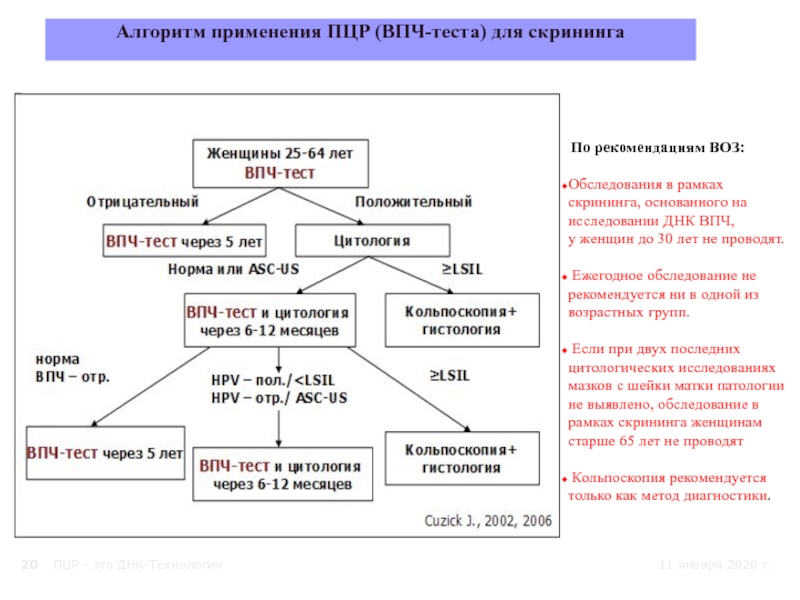
Слайд 20ПЦР - это ДНК-Технология
Алгоритм применения ПЦР (ВПЧ-теста) для скрининга
По
рекомендациям ВОЗ:
Обследования в рамках скрининга, основанного на исследовании ДНК ВПЧ,
у женщин до 30 лет не проводят.
Ежегодное обследование не
рекомендуется ни в одной из
возрастных групп.
Если при двух последних
цитологических исследованиях мазков с шейки матки патологии не выявлено, обследование в рамках скрининга женщинам старше 65 лет не проводят
Кольпоскопия рекомендуется только как метод диагностики.
Слайд 22Организация ПЦР-лаборатории
Требования к помещениям лаборатории, выполняющей молекулярно-биологические диагностические исследования
При
строительстве новых или реконструкции имеющихся помещений лабораторию размещают в отдельно
стоящем здании (изолированной части здания, этажа) с соблюдением требований СП 1.3.1285-03 и (или) СП 1.3.2322-08.При отсутствии возможности размещения помещений лаборатории в виде отдельного блока допускается проведение исследований поступающего материала на базе действующей лаборатории (микробиологической, вирусологической, иммунологической и т.д.) при условии организации в ней самостоятельных или выделенных в составе других функциональных помещений рабочих зон, соответствующих этапам проведения анализа, поточности движения персонала и материалов.
Слайд 23Зоны (помещения) ПЦР-лаборатории
Лаборатория в соответствии с этапами проведения анализа должна
включать следующий набор последовательно расположенных самостоятельных рабочих зон (помещений) или
отдельно выделенных рабочих зон в составе других функциональных помещений, количество которых определяется используемыми МАНК:Рабочая зона 1 - зона приема, регистрации, разбора и первичной обработки материала
Рабочая зона 2 – зона выделения нуклеиновых кислот
Рабочая зона 3 - зона проведения реакции амплификации и учета ее результатов при использовании гибридизационо – флуоресцентного метода детекции
Рабочая зона 4-1 – зона учета результатов реакции амплификации нуклеиновых кислот методом электрофореза и (или) гибридизационно - ферментным методом детекции
Рабочая зона 4-2 – зона учета результатов (детекции) продуктов амплификации нуклеиновых кислот методом секвенирования и (или) на ДНК-чипах
Слайд 24Устройство ПЦР-лаборатории с гибридизационо – флуоресцентный детекцией
Зона приема, регистрации, разбора
и первичной обработки материала (Рабочая зона 1)
Зона выделения нуклеиновых
кислот (Рабочая зона 2)Зона проведения реакции амплификации (Рабочая зона 3)
Для детекции в формате FLASH - ТОЛЬКО КАЧЕСТВЕННЫЙ АНАЛИЗ!
Для детекции в формате real time
– КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ АНАЛИЗЫ!