Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
РАСЧЕТЫ по химическим уравнениям
Содержание
- 1. РАСЧЕТЫ по химическим уравнениям
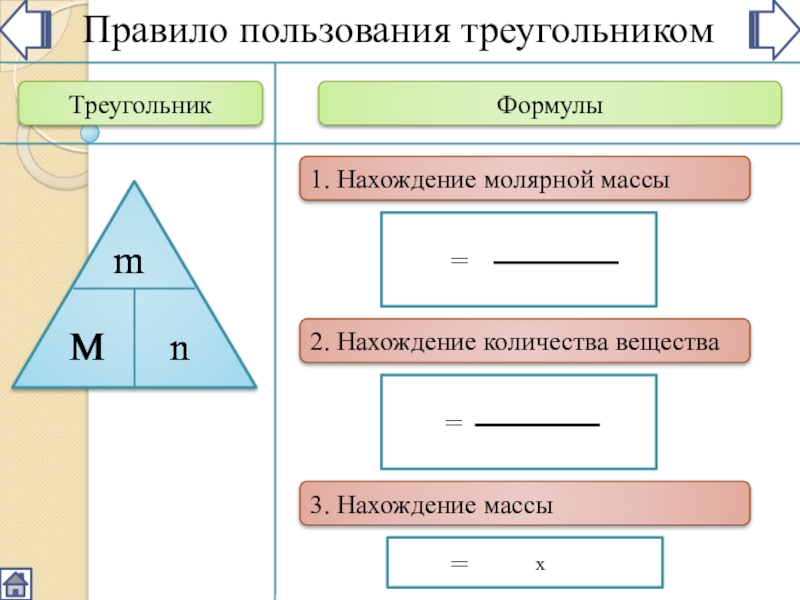
- 2. Треугольник ФормулыMПравило пользования треугольником=1. Нахождение молярной массы mn2. Нахождение количества веществаn=mM3. Нахождение массы хm=Mn
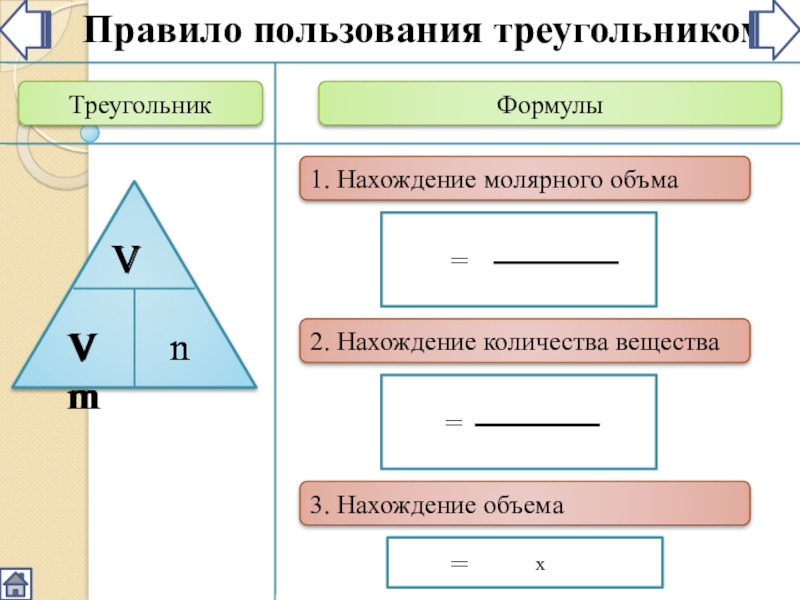
- 3. Треугольник ФормулыVmПравило пользования треугольником=1. Нахождение молярного объма Vn2. Нахождение количества веществаn=VVm3. Нахождение объема хV=Vmn
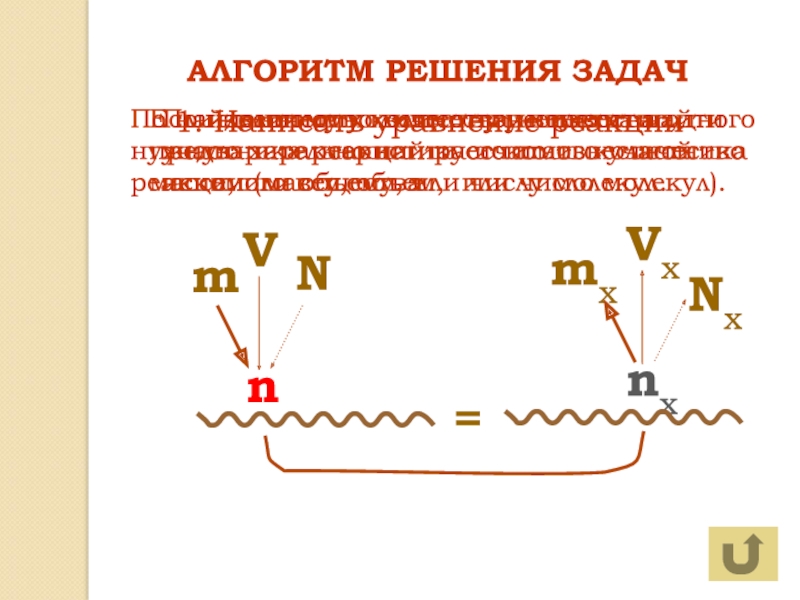
- 4. ?АЛГОРИТМ РЕШЕНИЯ ЗАДАЧNmVnNxmxVxnx1. Написать уравнение реакцииПо известному
- 5. Рассчитайте количество вещества алюминия, который потребуется для
- 6. Дано:n(Al2S3) =2,5 мольn(S) – ?Решение:
- 7. Дано:m(Cu(OH)2)=14,7 гm(CuO) – ?M(Cu(OH)2) = 64+(16+1)·2 =98г/мольM(CuO)
- 8. Дано:m(Zn)=13 гm(ZnCl2) – ?M(Zn) = 65 г/мольM(ZnCl2
- 9. Дано:m(MgO) = 6 гV(O2) – ?M(MgO) =
- 10. Дано:m(Cu)=32 гV(H2) – ?M(Cu) = 64 г/мольVm
- 11. САМОСТОЯТЕЛЬНАЯ РАБОТА:ВАРИАНТ 1: Вычислите массу меди, которая
- 12. ДОМАШНЕЕ ЗАДАНИЕ:Рассчитайте, какая масса кислорода образуется при
- 13. Слайд 13
- 14. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Треугольник
Формулы
M
Правило пользования треугольником
=
1. Нахождение молярной массы
m
n
2. Нахождение количества
вещества
Слайд 3Треугольник
Формулы
Vm
Правило пользования треугольником
=
1. Нахождение молярного объма
V
n
2. Нахождение количества
вещества
n
=
V
Vm
3. Нахождение объема
х
V
=
Vm
n
Слайд 4?
АЛГОРИТМ РЕШЕНИЯ ЗАДАЧ
N
m
V
n
Nx
mx
Vx
nx
1. Написать уравнение реакции
По известному количеству вещества одного
участника реакции рассчитать количество искомого вещества
Если количество вещества неизвестно, предварительно
найти его по известной массе, или объему, или числу молекул.По найденному количеству вещества найти нужную характеристику искомого участника реакции (массу, объем, или число молекул).
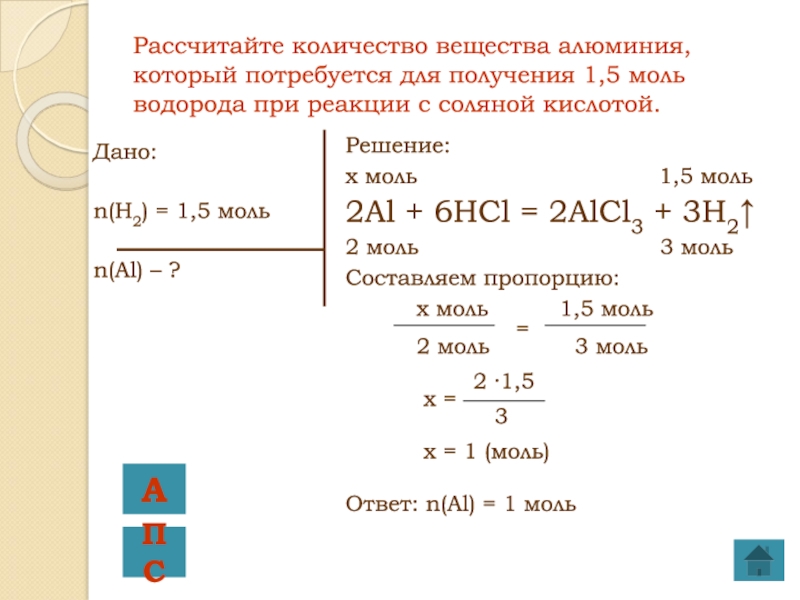
Слайд 5Рассчитайте количество вещества алюминия, который потребуется для получения 1,5 моль водорода
при реакции с соляной кислотой.
Дано:
n(H2) = 1,5 моль
n(Al) – ?
Решение:
x
моль 1,5 моль2Al + 6HCl = 2AlCl3 + 3H2↑
2 моль 3 моль
Составляем пропорцию:
x моль 1,5 моль
=
2 моль 3 моль
2 ·1,5
x =
3
x = 1 (моль)
Ответ: n(Al) = 1 моль
А
ПС
Слайд 6Дано:
n(Al2S3) =2,5 моль
n(S) – ?
Решение:
x моль 2,5 моль
2Al + 3S = Al2S3 3 моль 1 моль
x = n(S) = 3 n(Al2S3) =
= 3·2,5 моль = 7,5 моль
Ответ: n(S) = 7,5 моль
Определите количество вещества серы, необходимое для получения 2,5 моль сульфида алюминия.
ПС
А
Слайд 7Дано:
m(Cu(OH)2)=14,7 г
m(CuO) – ?
M(Cu(OH)2) =
64+(16+1)·2 =
98г/моль
M(CuO) = 64 +16
=
80г/моль
Решение:
14 ,7 г
x мольCu(OH)2 = CuO + H2O
1 моль 1 моль
m(Cu(OH)2)
n(Cu(OH)2) =
M(Cu(OH)2)
14.7 г
n(Cu(OH)2)= = 0,15 моль
98 г/моль
x = n(CuO) = n(Cu(OH)2) = 0, 15 моль
m(CuO) = n(CuO)·M(CuO) =
0,15 моль·80 г/моль = 12 г
Ответ: m(CuO) = 12 г
Вычислите массу оксида меди (II), образующегося при разложении 14,7 г гидроксида меди (II).
ПС
А
0,15 моль
Слайд 8Дано:
m(Zn)=13 г
m(ZnCl2) – ?
M(Zn) = 65 г/моль
M(ZnCl2 =65 +35,5·2 =
136 г/моль
Решение:
0,2 моль
x мольZn + 2HCl = ZnCl2 + H2↑
1 моль 1 моль
m(Zn)
n(Zn) =
M(Zn)
13 г
n(Zn)= = 0,2 моль
65 г/моль
x = n(ZnCl2) = n(Zn) = 0,2 моль
m(ZnCl2) = n(ZnCl2)·M(ZnCl2) =
0,2 моль·136 г/моль = 27,2 г
Ответ: m(ZnCl2) = 27,2 г
Рассчитайте массу соли, которая образуется при взаимодействии 13 г цинка с соляной кислотой.
ПС
А
Слайд 9Дано:
m(MgO) = 6 г
V(O2) – ?
M(MgO) =
24+16 =
40 г/моль
Vm
= 22,4 л/моль
Решение:
0,15 моль
x моль2MgO = 2Mg + O2↑
2 моль 1 моль
m(MgO)
n(MgO) =
M(MgO)
6 г
n(MgO)= = 0,15 моль
40 г/моль
x = n(O2) = ½ n(MgO) = 1/2·0, 15 моль=
0,075 моль
V(O2) = n(O2)·Vm =
0,075 моль·22,4 л/моль = 1,68 л
Ответ: V(O2) = 1,68 л
Какой объем кислорода (н.у.) образуется при разложении 6 г оксида магния.
ПС
А
Слайд 10Дано:
m(Cu)=32 г
V(H2) – ?
M(Cu) = 64 г/моль
Vm = 22,4 л/моль
Решение:
x моль
0,5 мольH2 + CuO = H2O + Cu
1 моль 1 моль
m(Cu)
n(Cu) =
M(Cu)
32 г
n(Cu)= = 0,5 моль
64 г/моль
x = n(H2) = n(Cu) = 0,5 моль
V(H2) = n(H2)·Vm =
0,5 моль·22,4 л/моль = 11,2 л
Ответ: V(H2) = 11,2 л
Рассчитайте, какой объем водорода должен вступить в реакцию с оксидом меди (II), чтобы образовалось 32 г меди.
ПС
А
Слайд 11САМОСТОЯТЕЛЬНАЯ РАБОТА:
ВАРИАНТ 1:
Вычислите массу меди, которая образуется при восстановлении
избытком водорода 4 г оксида меди (II).
CuO + H2 =
Cu + H2OВАРИАНТ 2:
В реакцию с серной кислотой вступило 20 г гидроксида натрия. Рассчитайте массу образовавшейся соли.
2NaOH + H2SO4 = Na2SO4 + 2H2O