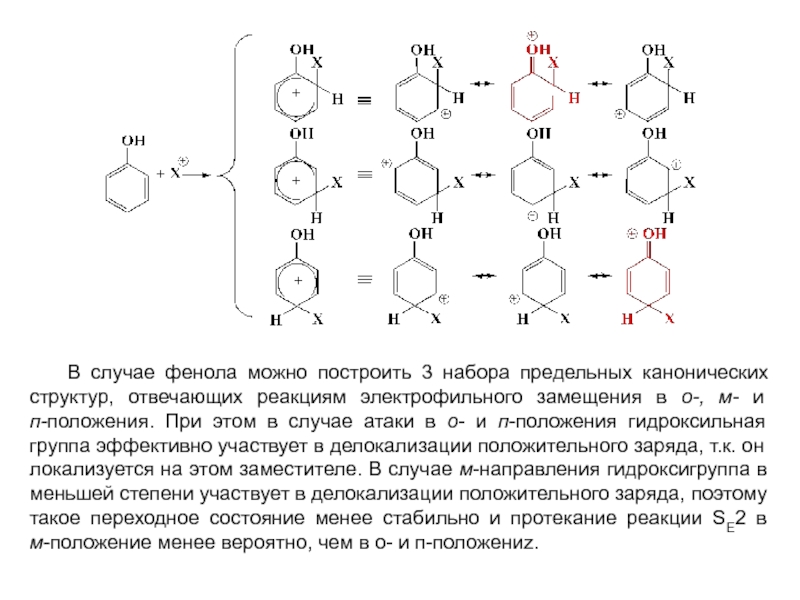
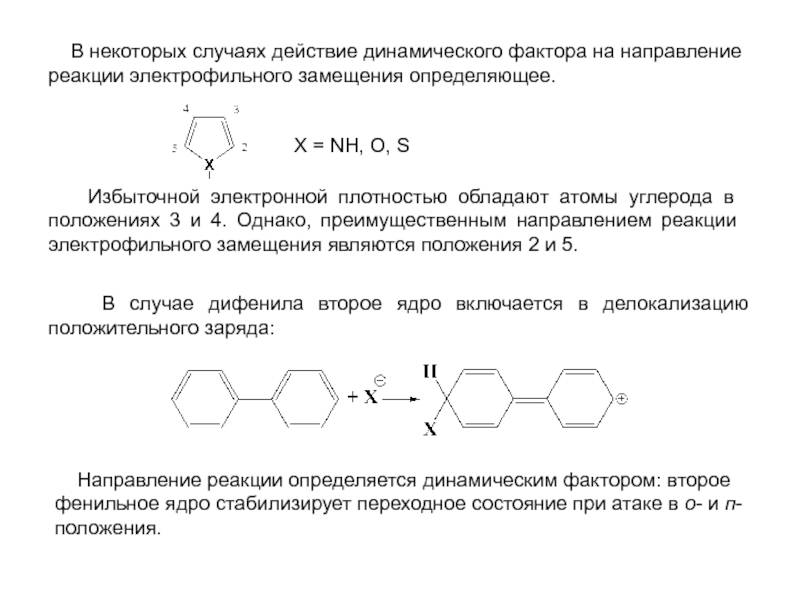
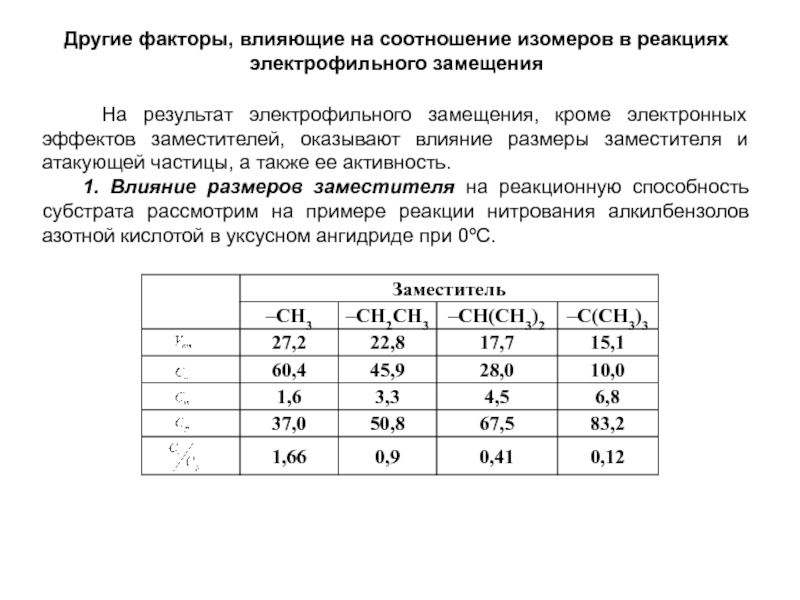
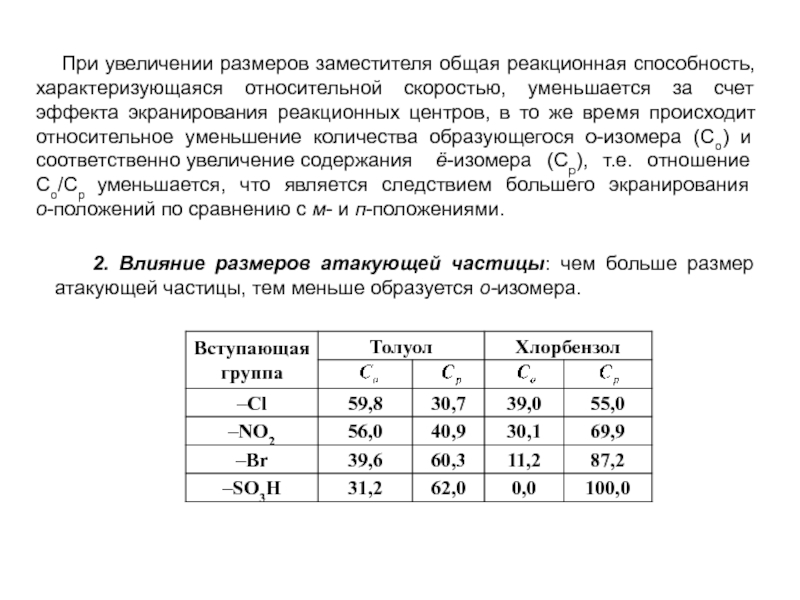
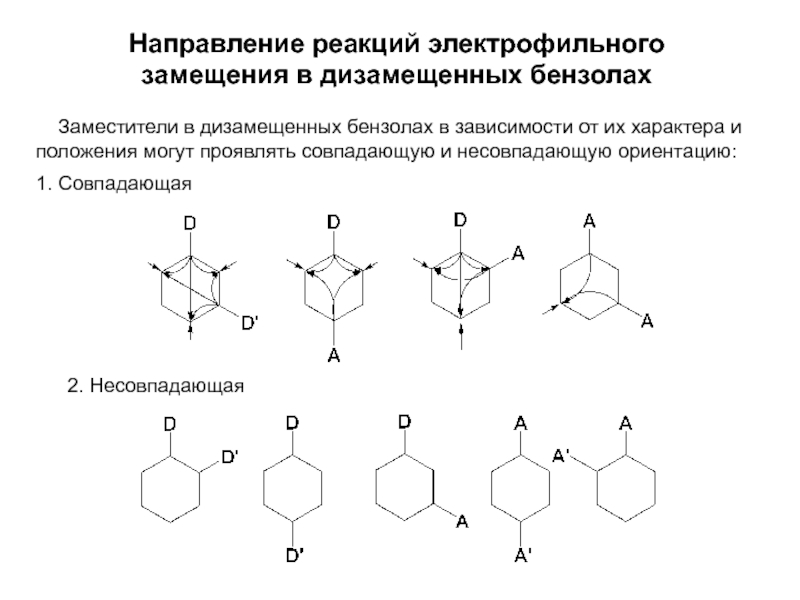
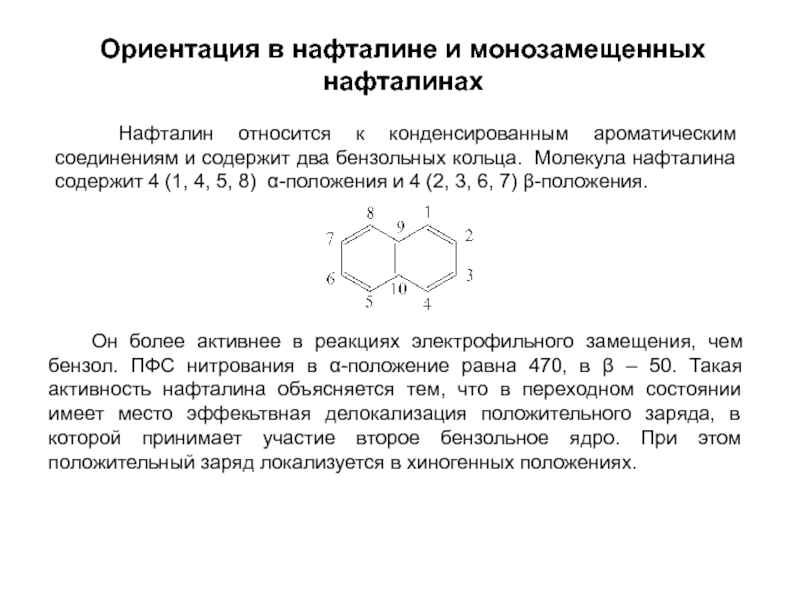
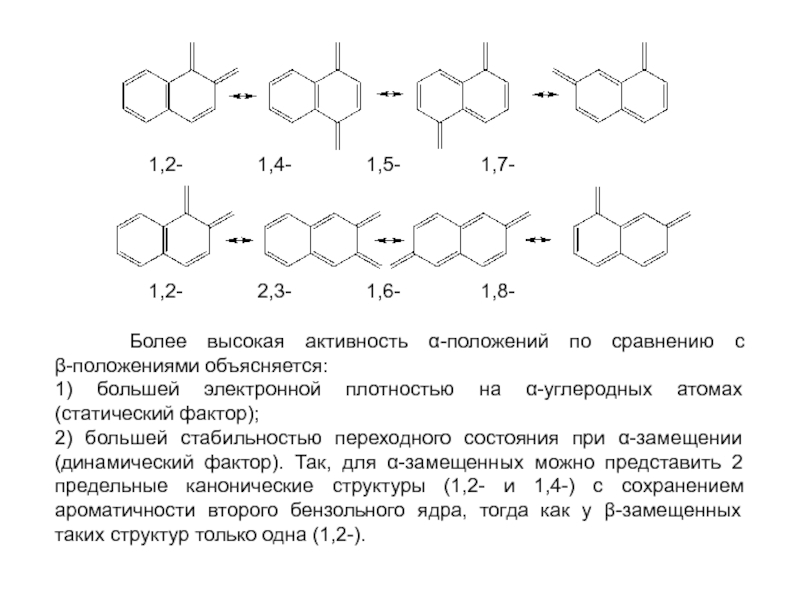
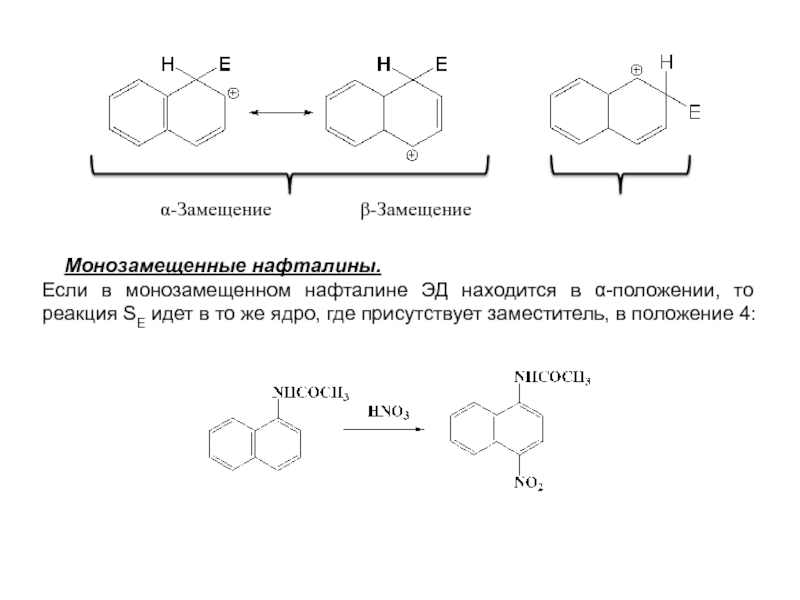
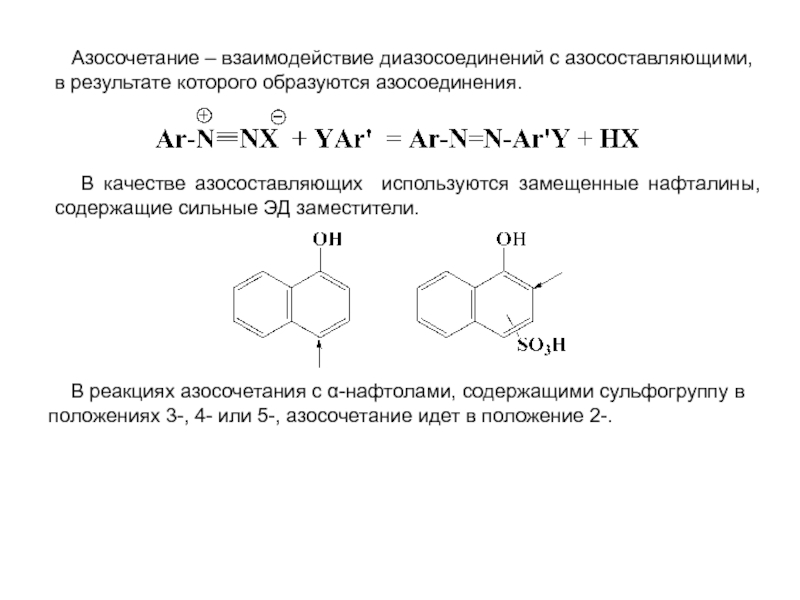
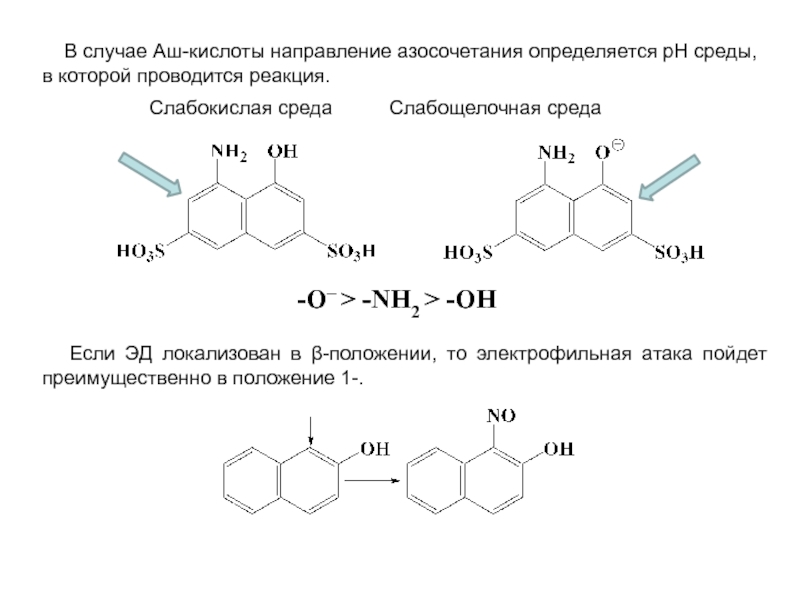
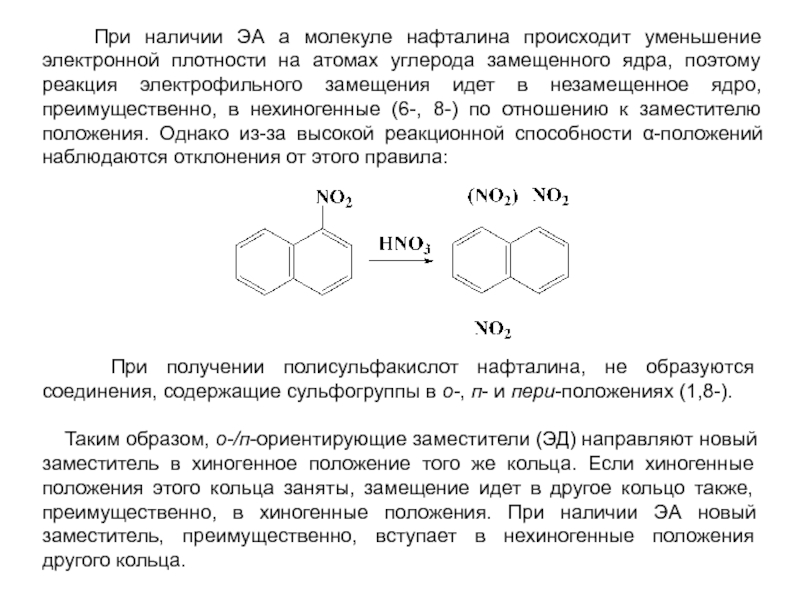
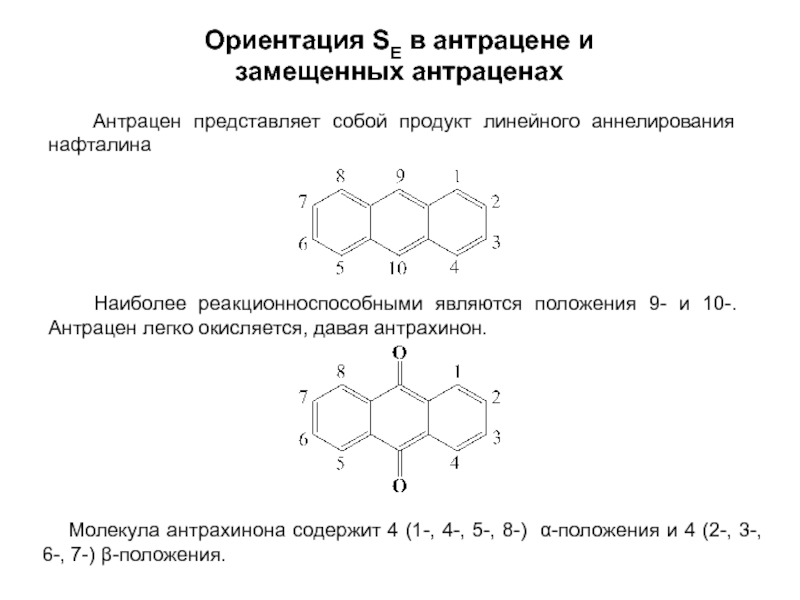
особенно широко используются при переработке ароматического сырья в промежуточные продукты.
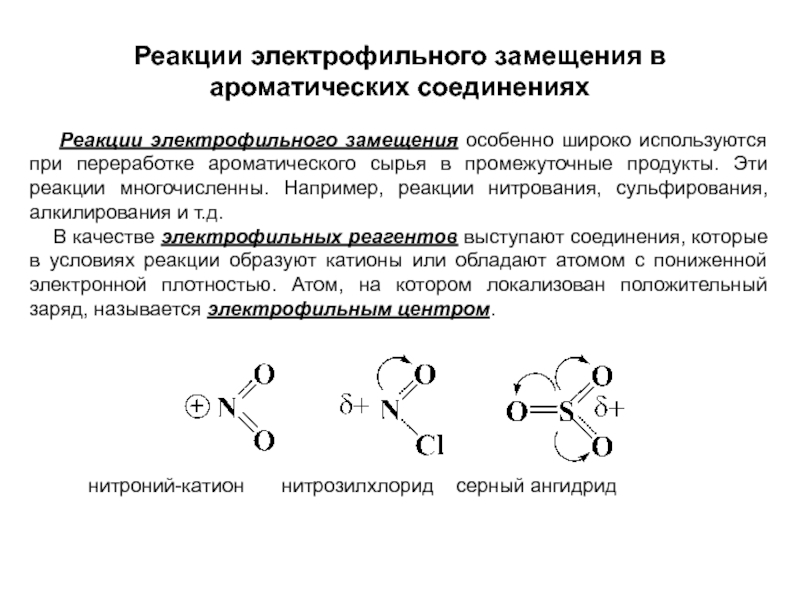
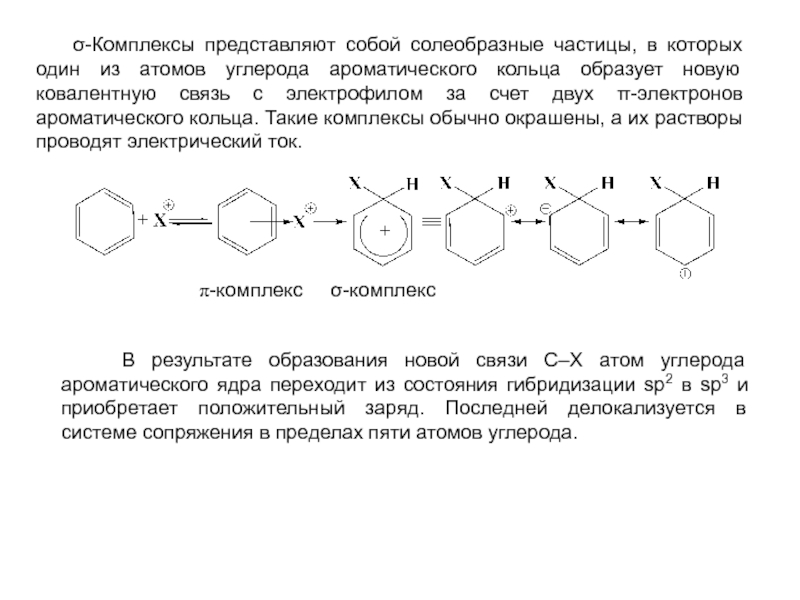
Эти реакции многочисленны. Например, реакции нитрования, сульфирования, алкилирования и т.д.В качестве электрофильных реагентов выступают соединения, которые в условиях реакции образуют катионы или обладают атомом с пониженной электронной плотностью. Атом, на котором локализован положительный заряд, называется электрофильным центром.
нитроний-катион нитрозилхлорид серный ангидрид