Слайд 1РЕГУЛЯЦИЯ И ПАТОЛОГИЯ
БЕЛКОВОГО ОБМЕНА
Слайд 2Белковый обмен
координирует, регулирует и интегрирует процессы обмена веществ в организме.
Общая
скорость синтеза белков до 500 г/сут.
В среднем каждые 3
недели половина белковых компонентов обновляется.
В основе развития патологических состояний в организме лежит нарушение равновесия двух фаз метаболизма: анаболизма и катаболизма.
Слайд 3Гормональная регуляция белкового обмена
Гормоны, влияющие на белковый обмен, делятся на
две группы:
Анаболические гормоны – активируют синтез белка.
Катаболические гормоны – способствуют
распаду белка.
Слайд 4Анаболические гормоны
СТГ (гормон роста) – повышает проницаемость клеточных мембран для
аминокислот, активирует все этапы белкового синтеза, способствует росту костей и
мышц.
Инсулин (гормон сытости) - усиливает поступление аминокислот в клетку, усиливает все этапы синтеза белка, тормозит глюконео-генез из аминокислот (белоксберегающее действие),
Слайд 5Половые гормоны: эстрогены - стимулируют все этапы синтеза белка в
клетках – мишенях (органах репродукции); андрогены – дополнительно и во
всех других тканях, прежде всего в костной и мышечной тканях, ускоряют транспорт нуклеотидов.
Тироксин - в физиологических дозах стимулируют синтез белка в молодом возрасте (ускорение роста), повышает активность ферментов, влияет на дифференцировку клеток.
Слайд 6Катаболические гормоны
Тироксин - в больших дозах усиливает окислительные процессы, в
том числе окисление аминокислот, усиливает распад белков в тканях (активация
протеиназ)
Глюкагон (гормон голода) – активирует распад белка во всех тканях при голодании (способствует глюконеогенезу из аминокислот).
Слайд 7Глюкокортикоиды – ингибируют синтез белков мышечной, костной и лимфоидной тканей
(иммунодепрессорное действие), т.к. активируют глюконеогенез из аминокислот,
(в печени, наоборот,
стимулируют синтез белков, синтез мочевины).
Тормозят транспорт аминокислот в клетку, препятствуют синтезу заменимых аминокислот.
Слайд 8Патология белкового обмена
Врожденная - связана с генетическими дефектами синтеза белка.
Известно
около 2.000 наследственных болезней.
(унаследованы от родителей или результат мутаций при
развитии плода)
Приобретенная – результат нарушения обменных процессов при системной или органной патологии.
Слайд 9Врожденная патология
белкового обмена
Болезни белкового обмена –протеинопатии Нарушается синтез какого
либо белка:
ферментные
неферментные
Неферментные протеинопатии обусловлены синтезом белка неправильной
структуры (страдает функция белка), или выпадением синтеза белка.
Слайд 10Примеры
Нарушение структуры белка:
Гемоглобинозы – синтезируется Нв с аномальной структурой →
анемия, метгемоглобинемия и др.
Болезнь Вильсона–Коновалова – развивается в результате синтеза
аномального церулоплазмина, который не обеспечивает нормальный транспорт меди (слепота, поражение печени).
Аномальные фибриногены – нарушена свертываемость крови.
Слайд 11 Выпадение синтеза белка:
Агаммоглобулинемия – синдром дефицита антител. Неспособность сопротивляться
инфекциям.
Гемофилия А – отсутствие синтеза VIII фактора свертывания крови.
СД II
типа - инсулинрезистентность из-за отсутствия синтеза рецепторных белков.
Слайд 12Ферментативные протеинопатии - ферментопатии
Отсутствие или снижение синтеза
фермента
Нарушается звено метаболизма
А В С
Д
Результатом дефекта могут быть следующие последствия:
Е1
Е2
Е3
блок
накапливаются
уменьшаются
Слайд 131. Накапливающееся вещество оттесняет в клетке все органеллы, нарушается функция
клетки.
Болезни накопления - гликогенозы, липоидозы, мукополисахаридозы.
2. Накапливающееся вещество может быть
токсичным.
фенилпировиноградная олигофрения, гомоцистеинурия.
Слайд 143. Недостаток вещества после блока, необходимого для организма, возникает заболевание:
Кретинизм
- врожденный гипотиреоз,
нарушен синтез тироксина в щитовидной железе.
Альбинизм –
нарушение синтеза меланинов
Слайд 15Приобретенная патология
белкового обмена
При заболевании почек нарушается синтез эритропоэтина (→
почечная анемия), кальцитриола (→ рахит).
Гипоальбуминемия развивается при поражениях печени, почек.
Слайд 16Приобретенная патология
белкового обмена
При лучевых поражениях нарушен синтез иммуноглобулинов →
резко снижается сопротивляемость к инфекциям.
Симптоматический дефицит антител возникает при СПИДе,
стафилококковых инфекциях.
Слайд 17Белковое голодание - недостаток полноценного белка или нехватка белков в
питании. Уменьшается мышечная масса, сопротивляемость к инфекциям (лимфоидная ткань).
Приобретенная патология
белкового обмена
Слайд 18Белковое голодание тяжело протекает у детей:
– болезнь Квашиоркор –«красный
мальчик»: гидрокахексия, депигментация-отек (задержка роста, отеки из-за гипопротеинемии, жировая инфильтрация
печени, диарея, стеаторея, анемия)
Приобретенная патология
белкового обмена
Слайд 19Нарушение переваривания и всасывания белков при инфекциях ЖКТ (холера, дизентерия),
заболеваниях поджелудочной железы, гипо- и авитаминозах.
Гипоксия – дефицит кислорода вызывает
нарушение всех видов обмена.
Биосинтез белка снижается. Это особенно влияет на синтез белков с коротким временем полужизни (факторы свертывания, некоторые гормоны)
Приобретенная патология
белкового обмена
Слайд 21Репликация ДНК
Репликация (удвоение) – синтез дочерней молекулы ДНК на матрице
материнской ДНК.
Процесс идет в ядре клетки
Необходим для деления клетки
(передача наслед-ственной информации в неискаженном виде)
Главный фермент – ДНК–полимераза
Синтез идет в 3 этапа:
инициация (начало синтеза),
элонгация (наращивание цепи),
терминация (завершение).
Слайд 22Ферменты репликации
Хеликаза (ДНК-раскручивающий белок)
SSB-белок (стабилизация, препятствует обратному скручиванию)
Топоизомеразы (релаксация сверхспирализации)
ДНК-полимеразы
(синтез, контроль, репарация, заполнение брешей на отстающей цепи, деградация праймеров)
Праймаза
(ДНК-зависимая РНК-полимераза – синтез праймера)
ДНК-лигаза (соединяющий фермент)
Слайд 23инициация
Образование репликативных вилок в различных участках ДНК
Синтез праймеров – небольших
кусочков РНК (10 – 200 нуклеотидов), функция затравки.
Вслед за праймером
присоединяется ДНК – полимераза и идет удлинение дочерней цепи в направлении 5´→3´
Синтез одной цепи идет непрерывно – лидирующая цепь
элонгация
Слайд 24Синтез второй – отстающей цепи - прерывисто – фрагментами Оказаки
(по 150 - 200 нуклеотидов)
ДНК-полимераза имеет два активных центра:
первый –
распознает нуклеотиды матричной цепи ДНК, второй – отбирает нуклеотиды и связывает их между собой по принципу комплиментарности.
Этап завершается вырезанием праймеров, вместо них достраиваются фрагменты ДНК и все сшивается ДНК-лигазой в единую цепь.
Скорость синтеза около 100 нуклеотидов в секунду
Слайд 25терминация
Наступает, когда исчерпана ДНК матрица (ДНК-полимераза уходит с матрицы)
Лидирующая цепь
реплицируется полностью.
Праймер у 3´-конца отстающей цепи разрушается и не реплицируется.
Теломераза присоединяет теломеры (участки ДНК) для сохранения исходных размеров хромосом.
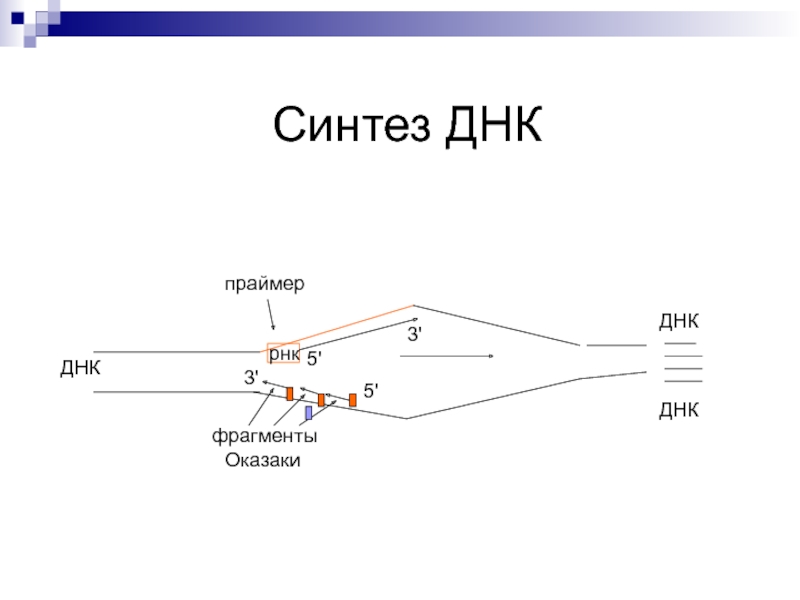
Слайд 26Синтез ДНК
ДНК
праймер
рнк
5'
3'
5'
3'
фрагменты
Оказаки
ДНК
ДНК
Слайд 27МУТАЦИИ
Если ошибка синтеза не устраняется системами репарации, то искажение генетической
программы.
Сохраняющиеся при репликации изменения ДНК – мутации.
Спонтанные (естественные – 10-5
– 10-8 на клетку)
Индуцированные (воздействие различных факторов):
Физических (излучения: УФ, ИК, радиация)
Химические (мутагены)
Биологические (вирусы)
Слайд 28Мутации
точечные и хромосомные
Точечные:
Изменение смысла кодона – замена пар оснований
(Г-Ц на А-Т)
Бессмысленный коддон, не несущий информации (→ обрыв синтеза
белка).
Сдвиг рамки считывания информации – выпадение или вставка нуклеотида (дефектный белок)
Слайд 29Транскрипция – синтез РНК
Переписывание информации
Идет в ядре клетки в 3
этапа.
На одной из нитей ДНК (кодирующей цепи ДНК).
Главный фермент –
ДНК–зависимая РНК– полимераза (транскриптаза)
Инициация – Раскручивание ДНК на определенном участке (транскриптон).
Присоединение фермента к промотору.
Слайд 30Р
Элонгация. Синтез в направлении 5´→3´ по принципу комплементарности (А-У, Г-Ц)
ДНК
О
Структурные
гены
РНК-полимераза
Синтез РНК
Терминация. Завершается при встрече сайта терминации («стоп»-сигнал), синтезируется еще
20-30 нуклеотидов и РНК отделяется от ДНК.
Слайд 31Посттранскрипционное созревание РНК - процессинг
Кепирование – присоединение метилгуанозина
к 5′-концу.
Полиаденилирование – присоединение к 3′- концу ААУААА
Сплайсинг – вырезание
интронов (неинформативных участков) и сшивание экзонов (информативных участков).
Слайд 32Обратная транскрипция
Синтез ДНК на матрице РНК
Фермент – обратная транскриптаза
(ревертаза, РНК-зависимая ДНК-полимераза)
Матрицей для синтеза теломеры является РНК (фермент теломераза).
Ревертаза
есть у РНК-содержащих онкогенных вирусов (ретровирусы) – лейкоза, саркомы, вирусов СПИДа, герпеса.
Слайд 331. Синтез цепи ДНК на матрице РНК
2. Гидролиз матричной ДНК
РНК-азой
3. Синтез на матрице ДНК второй комплиментарной цепи ДНК
и встраивание ДНК в геном клетки хозяина.
При определенных условиях вирусные гены могут быть активированы, что ведет к репликации и размножению вируса или развитию опухоли.
Их особенность – проявление себя через длительный промежуток времени (1 - 10 лет).
Слайд 35Активация аминокислот
Необходимым условием для синтеза белка является наличие не свободных,
а активированный аминокислот.
Активации аминокислот осуществляется с помощью высокоспецифичных ферментов аминоацил–тРНК-синтетаз
(АРСаз) в присутствии АТФ.
Ферменты находят свою аминокислоту, подходящую ей тРНК и сводят их в пару.
Слайд 36 Передача информации о последовательности аминокислот в синтезируемой полипептидной цепи осуществляется
с помощью генетического кода.
Аминокислотный код
(генетический код)
Последовательность трех нуклеотидов,
кодирующая какую
либо аминокислоту.
Слайд 37Свойства кода:
Универсален (для всех организмов)
триплетен – сочетание из четырех по
три дает 64 варианта кодов, 3 из которых бессмысленные
Специфичен (один
триплет кодирует только одну аминокислоту)
Вырожден (множествен) – 18 из 20 аминокислот кодируются более, чем одним триплетами.
Целостный (непрерывный)
Однонаправленный. Имеется точка считывания.
Слайд 38Биосинтез белка
Осуществляется в цитоплазме, на рибосоме.
Рибосома (80S) состоит из
малой (40S) и большой (60S) субъединиц. Имеет два активных центра:
П (пептидильный) и А (аминоцильный).
3 этапа: инициация, элонгация, терминация
Слайд 39инициация
Происходит при участии факторов инициации, ГТФ, Mg2+ .
К малой субъединице
рибосомы присоединяется мРНК
К инициирующему кодону АУГ по принципу комплементарности присоединяется
антикодон тРНК, несущий метионин.
Затем присоединяется большая субъединица рибосомы. Мет-тРНК в П-центре.
Слайд 40элонгация
Циклический процесс
В результате каждого цикла пептидная цепочка удлиняется на одну
аминокислоту
В А-центр рибосомы поступает А-А-тРНК, антикодон которой соответствует кодону мРНК.
Действует
фермент пептидилтрансфераза, происходит перенос АМК из П- в А-центр и формируется пептидная связь.
Затем при участии фермента пептидилтранслоказы осуществляется перемещение мРНК на 1 кодон в направлении 5´→3´.
Слайд 41терминация
Завершается биосинтез когда в рибосому заходит терминирующий (бессмысленный) кодон
Действуют факторы
терминации → диссоциация рибосомы, освобождение пептида.
Процессинг белков
Пептид поступает в аппарат
Гольджи, где идет его химическая модификация (гидроксили-рование, гликирование и т.д.), формирование вторичной, третичной и четвертичной структуры.
Слайд 42 Синтез белка протекает со значительной затратой энергии.
При активации аминокислот: АТФ
до АМФ (две макроэргические связи)
Инициация трансляции: ГТФ.
Элонгация – 2
ГТФ: доставка аминоацил-т-РНК а А-центр рибосомы и процесс транслокации.
Терминация – ГТФ.
Примерная скорость синтеза – 10 - 15 аминокислот в секунду
Слайд 43Регуляция синтеза белка на генетическом уровне
В генах человека закодировано около
300 000 белков, но не все они синтезируются
Одни гены закрыты
– репрессированы, другие открыты – индуцированы
Живая клетка обладает способностью контролировать синтез белков
Слайд 44 Оперон – совокупность генов.
Ген-регулятор – контролирует синтез специфического белка-регулятора (активатора
или репрессора).
Промотор – начальный сайт инициации транскипции.
Ген-оператор, взаимодействует с
белком-регулятором. запускает работу структурных генов.
Структурные гены, участвующие в формировании мРНК.
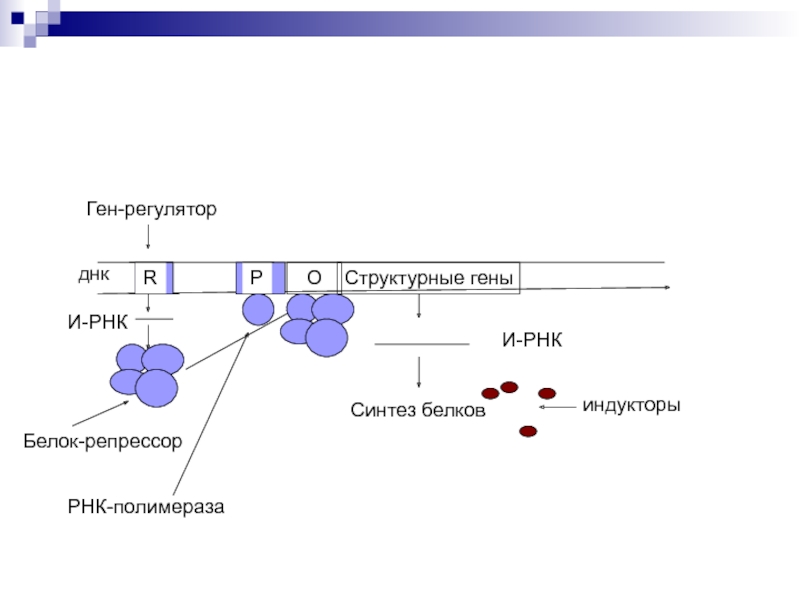
Слайд 45Если белок-регулятор взаимодействует с опера-тором, частично блокирует область промотора, это
препятствует присоединению РНК-полимеразы к промотору (репрессия синтеза).
Если у промотора слабая
способность соединяться с РНК-полимеразой, то присоединение белка-регу-лятора перед промотором способствует присоеди-нению РНК-полимеразы (активация синтеза)
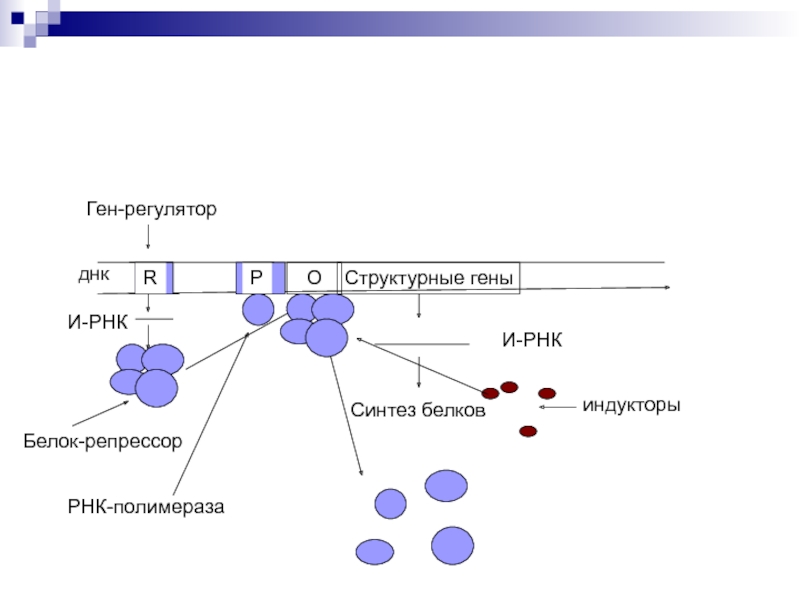
Эффекторы – вещества, взаимодействующие с белками-регуляторами. Индукторы – способ-ствующие запуску транскрипции. Корепрессоры – блокада транскрипции.
Слайд 46Значение этой регуляции
Приспособление организмов к меняющимся условиям окружающей среды
Экономия пластического
материала
Функцию индукторов и корепрессоров выполняют метаболиты, гормоны, лекарства
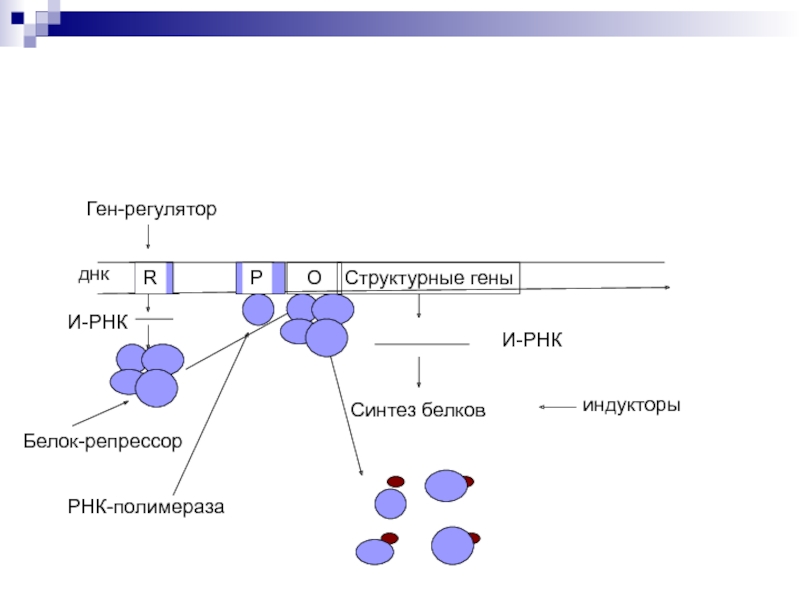
Слайд 47Структурные гены
О
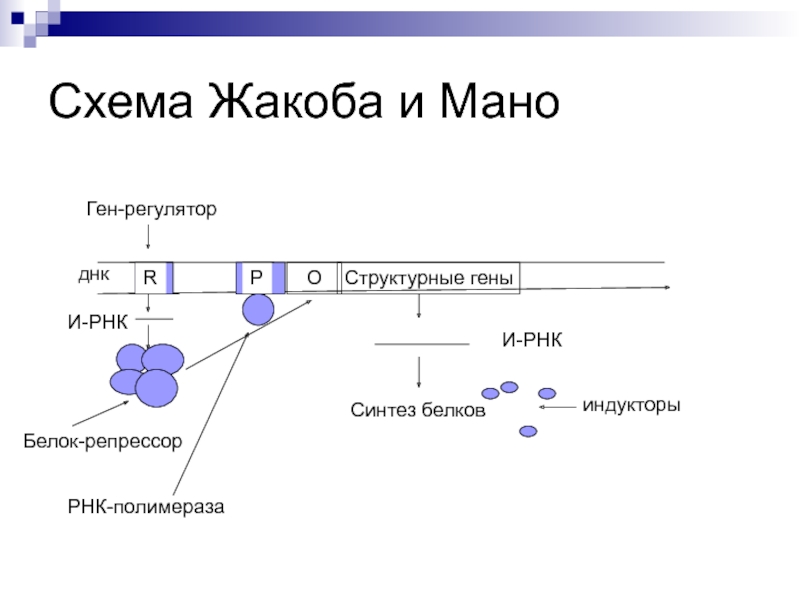
Схема Жакоба и Мано
днк
R
Ген-регулятор
О
Р
И-РНК
Белок-репрессор
РНК-полимераза
И-РНК
Синтез белков
индукторы
Слайд 48Структурные гены
О
днк
R
Ген-регулятор
О
Р
И-РНК
Белок-репрессор
РНК-полимераза
И-РНК
Синтез белков
индукторы
Слайд 49Структурные гены
О
днк
R
Ген-регулятор
О
Р
И-РНК
Белок-репрессор
РНК-полимераза
И-РНК
Синтез белков
индукторы
Слайд 50Структурные гены
О
днк
R
Ген-регулятор
О
Р
И-РНК
Белок-репрессор
РНК-полимераза
И-РНК
Синтез белков
индукторы
Слайд 51Ингибиторы синтеза белка
Многие эффективные антибиотики избирательно взаимодействуют с
белками бактериальных рибосом, ингибируют их синтез белка
Токсины бактерий, растительные яды,
антистатики, противоопухолевые и антивирусные препараты.
Слайд 52Ингибиторы репликации
Антибиотики – актиномицин Д, новобиоцин
Алкилирующие агенты (иприт)
Аналоги азотистых оснований
и нуклеозидов (5-бромурацил, идуксоридин – включается в структуру ДНК вируса
и тормозит его репликацию)
Мутагены – Н3РО4, азотная кислота, химические яды
Слайд 53Ингибиторы транскрипции
Антибиотики – рифампицин (связывается с РНК-полимеразой и препятствует
началу транскрипции)
Аналоги нуклеозидов (цитозин, арабинозид)
Алкалоиды (винкристин, винбластин)
Мутагены – (яд белой
поганки –
α-амонитин)
Слайд 54Ингибиторы трансляции
Антибиотики:
Тетрациклин тормозит связывание с 30S субъединицей рибосомы и блокирует
присоединение аминоацил-т-РНК в А-центр
Стрептомицин ингибирует инициацию трансляции
Эритромицин присоединяется к 50S
субъединице рибосомы и ингибирует транслоказу
Левомицетин присоединяется к 50S субъединице рибосомы и ингибирует пептидилтрансферазу
Дифтерийный токсин – инактивирует 1 из белковых факторов элонгации.